Особенности иммунного ответа при синхронных полинеоплазиях молочной и щитовидной желез по сравнению с солитарным раком щитовидной железы
Автор: Селезнева Т.Д., Кулигин А.В., Попова Т.Н., Зяблое Е.В.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Патологическая физиология
Статья в выпуске: 1 т.17, 2021 года.
Бесплатный доступ
Цель: выявить особенности количественных и качественных изменений гуморального и клеточного звеньев иммунной защиты у пациенток с первично-множественным синхронным раком молочной (ПМСР) и щитовидной желез и солитарным раком щитовидной железы (СРЩЖ). Материал и методы. Произведен сравнительный анализ показателей гуморального и клеточного звеньев иммунной защиты 34 пациенток с ПМСР молочной и щитовидной желез, 36 пациенток с СРЩЖ и 36 женщинами контрольной группы. Результаты. Выявлены достоверные количественные и качественные изменения клеточного и гуморального звеньев иммунитета у пациенток с ПМСР молочной и щитовидной желез по сравнению с соответствующими показателями женщин группы контроля в виде снижения более чем на 30% уровня CD3-, CD16-, сб4-Т-лимфоцитов, всех классов иммуноглобулинов на фоне практически неизмененных показателей С019-В-лимфоцитов. При сравнении показателей иммунитета пациенток с СРЩЖ и группы контроля выявлено снижение примерно на 34% уровня С04-Т-лимфоцитов, на 20% С016-Т-лимфоцитов на фоне отсутствия существенных изменений других изучаемых показателей. Заключение. Выявлены более выраженные изменения нарушений клеточного и гуморального звеньев иммунной защиты у пациенток с ПМСР молочной и щитовидной желез по сравнению с показателями пациенток с СРЩЖ и группой контроля в виде снижения общего количества лимфоцитов, CD3-, CD4-, CD16-Т-лимфоцитов, иммунорегуляторного индекса, а также снижения уровня иммуноглобулинов основных классов.
Солитарный рак щитовидной железы, первично-множественный синхронный рак молочной и щитовидной желез, иммунный ответ
Короткий адрес: https://sciup.org/149134986
IDR: 149134986 | УДК: 616–006.6–031.81
Features of the immune response in synchronous breast and thyroid polyneoplasias in comparison with solitary thyroid cancer
The aim is to identify the features of quantitative and qualitative changes in the humoral and cellular components of the immune defense in patients with primary multiple synchronous breast cancer (PMSC) and thyroid cancer and solitary thyroid cancer (STC). Material and Methods. The indicators of humoral and cellular components of immunity were analyzed in comparison in 34 patients with breast and thyroid multiple primary synchronous cancer, in 36 patients with STC and 36 women of the control group. Results. Significant quantitative and qualitative changes in cellular and humoral immunity in patients with PMSC and thyroid glands in comparison with corresponding indicators of women of the control group in declining more than 30% of the level of CD3-, CD16-, CD4-T-lymphocytes, all classes of immuno-globulins, against virtually unchanged indicators CD19-b cells. When comparing the indicators of immunity in patients with STC and control groups showed a reduction of approximately 34% in CD4-T-lymphocyt.es, 20% CD16-T cells, in the absence of significant changes of the studied parameters. Conclusion. In the course of the study more expressed changes of disorders of cellular and humoral immune protection in patients with PMSC breast and thyroid glands in comparison with the indicators at patients with STC and control group in the form of lower total number of lymphocytes, CD3-T-lymphocytes, CD4-T-lymphocyt.es, CD16-T-lymphocytes, immunoregulatory index, as well as lower level of im-munoglobulins of main classes were identified.
Текст научной статьи Особенности иммунного ответа при синхронных полинеоплазиях молочной и щитовидной желез по сравнению с солитарным раком щитовидной железы
1 Введение. В последние годы отмечается значительный рост заболеваемости злокачественными новообразованиями как солитарного, так и множественного характера [1]. Показатель заболеваемости раком щитовидной железы в Российской Федерации в 2018 г. составил 9,02 на 100 000 населения, в 2011 г. — 6,74 на 100 000 населения. Показатель заболеваемости первично-множественными опухолями в России в 2018 г. составил 37,4 на 100 000 населения (в 2011 г. — 34,1 на 100 000 населения). При этом первично-множественные синхронные опухоли составили 26,7% (в 2011 г. — 34,1%) от общего числа первичномножественных опухолей [2].
Совсем недавно полинеоплазии описывались в литературе как казуистические находки, тогда как в настоящее время они почти ежедневно встречаются в нашей практической деятельности [3].
Определением первично-множественных опухолей принято обозначать независимое возникновение и течение у одного пациента двух и более опухолевых процессов, при этом они могут быть в разных системах и органах. Синхронными злокачественными новообразованиями считают опухоли, выявляемые с интервалом (не более года) после диагностики первой опухоли [3].
В патогенез злокачественных новообразований существенный вклад вносит иммунная система индивидуума. Возникновение и развитие любого опухолевого очага является интерактивным процессом, исход которого находится в зависимости от различных характеристик самой опухолевой ткани и состояния иммунологических механизмов защиты организма пациента, при этом изменения в последних могут касаться только некоторых количественных и качественных показателей [4–6].
Выявление особенностей возникновения и течения ПМСР молочной и щитовидной желез по сравнению с СРЩЖ может влиять на совершенствование методов диагностики и лечения этих заболеваний, а также оптимизировать подходы к профилактике.
Цель — выявить особенности количественных и качественных изменений гуморального и клеточного звеньев иммунной защиты у пациенток с первично-множественным синхронным раком молочной и щитовидной желез и солитарным раком щитовидной железы.
Материал и методы. Произведен ретроспективный анализ иммунологической картины в двух группах пациенток: у 34 пациенток с ПМСР молочной и щитовидной желез (I группа наблюдения) и 36 пациенток с СРЩЖ (II группа наблюдения), получавших лечение в отделении онкологии Дорожной клинической больницы г. Саратова в период с 2005 по 2017 г. В контрольную III группу наблюдения были включены 36 женщин, отобранных методом случайной выборки, сопоставимых по возрасту, влиянию внешней воздействий с пациентками первых двух групп. Количественный и качественный состав иммунитета женщин III группы явился критерием контроля изменений в сравнении с больными исследуемыми формами рака.
Рандомизация групп наблюдения выполнялась в соответствии с TNM-классификацией злокачественных новообразований (8-е издание, 2017 г.), ги-
стологической верификацией диагноза, а также с общепринятыми стандартными методами комплексного клинико-лабораторного обследования. Так, в I группу наблюдения были включены пациентки ПМСР молочной и щитовидной желез. При этом одна из опухолей — узловая форма рака молочной железы без метастазов (T1-2N0M0), по гистологической форме преобладал инвазивный рак у 79,4% (27 пациенток) без признаков специфичности (протоковый). Второе новообразование-опухоль — рак щитовидной железы без метастазов (T1-2N0M0) папиллярный у 55,8% (19 пациенток) или фолликулярный у 44,2% (15 пациенток), при этом каждая из выявленных опухолей у пациенток этой группы не являлись метастазом по отношению к другой и были самостоятельны. Промежуток времени между диагностикой одной и второй опухолей не превышал 12 месяцев.
Во II группу наблюдения были включены пациентки с папиллярным у 58,3% (21 пациентка) или фолликулярным 41,7% (15 пациенток) раком щитовидной железы без метастазов (T1-2N0M0).
Распределение пациенток по возрасту было примерно одинаковым. Бóльшую часть всех групп наблюдения составляли женщины в возрасте 45–65 лет, средний возраст в группе пациенток с ПМСР молочной и щитовидной желез составил 53,8±2,8 года, в группе пациенток с СРЩЖ — 55,4±3,1 года, в группе практически здоровых — 54,7±2,7 года.
Проанализированы показатели периферической крови пациенток до начала лечения в момент поступления в стационар. С помощью моноклональных антител к поверхностным дифференцировоч-ным маркерам лейкоцитов человека (CD3, -4, -8, -19, -16) (производства «Медбиоспектр», Москва) выявляли субпопуляционный состав лимфоцитов определялся методом непрямой иммунофлюоресценции. Определение в сыворотке крови человека количественного уровня иммуноглобулинов основных классов (IgM, G, A) выполнялось методом радиальной иммунодиффузии в геле по методу Манчини. Показатели общего анализа крови (общее число лейкоцитов, процентное содержание лимфоцитов) подсчитывались на гематологическом анализаторе КХ-21 (Япония). Показатели общего анализа крови (общее число лейкоцитов, процентное содержание лимфоцитов) определялись на гематологическом анализаторе КХ-21 (Япония).
Статистическая обработка полученных результатов проводилась с помощью программы Microsoft Excel и программного пакета Statistica 6.0, позволяющих рассчитать среднюю арифметическую величину ( М ), стандартную ошибку средней арифметической ( m ), а также t -критерий Стьюдента. Различия считались значимыми при уровне р <0,05. С целью уточнения нормальности распределения был использован критерий Шапиро — Уилка. Все изучаемые и описываемые в данной работе параметры имели распределение, близкое к нормальному.
Результаты. Во время изучения изменений показателей белой крови в обеих группах наблюдения была выявлена лимфопения, снижение процентного уровня лимфоцитов в лейкоцитарной формуле (табл. 1). В группе пациенток с СРЩЖ содержание лимфоцитов составило 28,2±1,97%, тогда как в группе пациенток с ПМСР молочной и щитовидной желез 21,5±1,72% ( P <0,05 и P <0,01 соответственно по отношению к группе контроля). При этом снижение этого показателя более выражено в группе пациенток с ПМСР молочной и щитовидной желез по срав-
Таблица 1
Изменение показателей клеточного звена иммунитета у пациенток с первично-множественным синхронным раком молочной и щитовидной желез и солитарным раком щитовидной железы
|
Изучаемые показатели |
Контрольная группа |
Первично-множественный синхронный рак молочной и щитовидной желез (I группа наблюдения) |
Солитарный рак щитовидной железы (II группа наблюдения) |
|||||
|
n |
M±m |
N |
M±m |
P |
N |
M±m |
P |
|
|
CD3, % |
36 |
61,7±3,68 |
34 |
47,8±2,18 |
Р <0,01 |
36 |
56,4±2,58 |
Р >0,05 Р 1<0,05 |
|
CD4, % |
40,3±2,85 |
26,1±1,52 |
36 |
33,2±1,71 |
Р <0,05 Р 1<0,01 |
|||
|
CD8, % |
22,1±1,93 |
30,1±1,58 |
36 |
20,1±1,31 |
Р >0,05 Р 1<0,01 |
|||
|
CD4/CD8 |
1,82±0,06 |
0,89±0,05 |
36 |
1,65±0,04 |
Р <0,05 Р 1<0,01 |
|||
|
CD16, % |
17,8±0,66 |
10,6±0,72 |
36 |
14,9±0,68 |
Р <0,01 Р 1<0,01 |
|||
|
Общее число лейкоцитов, *109/л |
6,2±0,34 |
7,1±0,51 |
Р >0,05 |
36 |
6,5±0,37 |
Р >0,05 Р 1>0,05 |
||
|
Содержание лимфоцитов, % |
35,1±2,18 |
21,5±1,72 |
Р <0,01 |
36 |
28,2±1,97 |
Р <0,05 Р 1<0,01 |
||
Примечание: Р — рассчитано по отношению к соответствующим показателям группы контроля; Р 1 — рассчитано по отношению к соответствующим показателям крови у пациенток с ПМСР молочной и щитовидной желез.
нению со пациентками с СРЩЖ ( Р 1<0,01). Развитие лимфопении отмечено на фоне незначительного увеличения уровня общего числа лейкоцитов более выраженное в I группе наблюдения — 7,1±0,51*10 9 /л, однако изменения были статистически незначимы ( Р >0,05) (табл. 1).
Результаты исследования также показали, что узловая форма высокодифференцированного СРЩЖ (II группа) развивается на фоне незначительного снижения общего количества Т-лимфоцитов (56,4±2,58%) и практически неизмененном количестве цитотоксических Т-лимфоцитов (20,1±1,31%), при значительном ( P <0,05) снижении Т-хелперов (33,2±1,71%) (по сравнению с группой контроля), что, в свою очередь, может приводить к снижению иммунорегуляторного индекса 1,65±0,04 (отношением CD4/CD8) (табл. 1, рис. 1).
Нами также выявлено значимое снижения CD3-Т-лимфоцитов (47,8±2,18%) и CD4-T-лимфоцитов (26,1±1,52%) ( Р <0,01 и P <0,01 соответственно) при увеличении CD8-Т-лимфоциты
(30,1±1,58%) ( Р <0,01) при синхронных узловых формах рака молочной и щитовидной желез без метастазов (рис. 1) ( Р <0,01 по сравнению с группой контроля).
Следует отметить, что снижение общего количества CD3-, CD4-T-лимфоцитов, увеличение CD8-Т-лимфоцитов при синхронных узловых формах рака молочной и щитовидной желез без метастазов было выражено в большей степени, чем в группе пациенток с узловой формой высокодифференцированного СРЩЖ ( Р 1<0,01) (рис. 2).
В нашем исследовании при сравнительном наблюдении за больными I группы выявлено, что процентное содержание NK-клеток (CD16-лимфоциты) было значительно снижено и составило 10,6±0,72% по сравнению с группой контроля — 17,8±0,66% ( Р <0,01) и пациентками II группы — 28,25±1,97% ( Р 1<0,01) (табл. 1, рис. 1).
Для определения состояния гуморального звена иммунитета у пациенток изучаемых групп исследова-
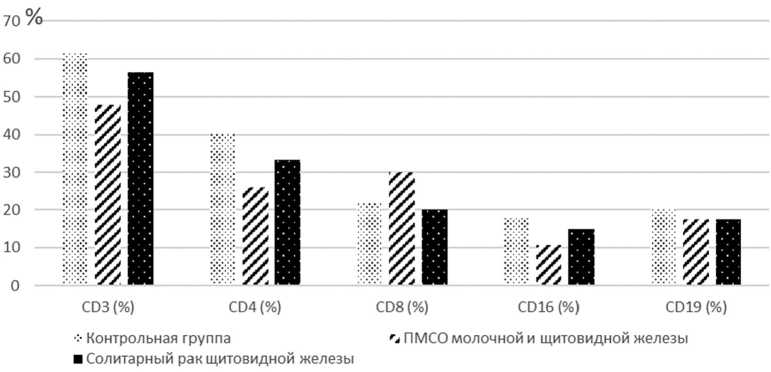
Рис. 1. Изменения показателей основных классов CD-лимфоцитов в исследуемых группах наблюдения
Таблица 2
Изменения показателей основных классов иммуноглобулинов и уровня CD19-лимфоцитов крови у пациенток с первично-множественным синхронным раком молочной и щитовидной желез и солитарным раком щитовидной железы
|
Изучаемые показатели |
Контрольная группа |
Первично-множественный синхронный рак молочной и щитовидной желез (I группа наблюдения) |
Солитарный рак щитовидной железы (II группа наблюдения) |
|||||
|
n |
M±m |
N |
M±m |
P |
N |
M±m |
P |
|
|
igG, г/л |
36 |
15,63±0,412 |
34 |
10,72±0,751 |
Р <0,01 |
36 |
15,27±0,483 |
Р >0,05 Р 1<0,01 |
|
IgA, г/л |
3,24±0,185 |
2,13±0,282 |
2,88±0,212 |
Р >0,05 Р 1<0,05 |
||||
|
IgM, г/л |
1,76±0,074 |
1,13±0,058 |
1,63±0,069 |
Р >0,05 Р 1<0,01 |
||||
|
CD19, % |
20,3±1,53 |
17,4±2,63 |
Р >0,05 |
18,6±1,420 |
Р >0,05 Р 1>0,05 |
|||
Примечание: Р — рассчитано по отношению к соответствующим показателям группы контроля; Р 1 — рассчитано по отношению к соответствующим показателям крови у пациенток с ПМСР молочной и щитовидной желез.
лись уровни иммуноглобулинов (IgG, A, M) и показателей CD19-В-лимфоцитов (табл. 2).
Выявлено незначительное снижение уровня CD19-В-лимфоцитов во всех группах наблюдения (17,4±2,63%, 18,6±1,42% и 20,3±1,53% в I, II группах наблюдения и группе практически здоровых женщин соответственно). Максимальное снижение зафиксировано в группе пациенток с ПМСР молочной и щитовидной желез, однако статистически недостоверное ( Р >0,05; Р 1>0,05) (табл. 2).
Отмечено, что у пациенток I группы уровни всех классов иммуноглобулинов были значительно снижены как по сравнению с группой контроля ( Р <0,05), так и группой пациенток с СРЩЖ ( Р 1<0,05). При этом самые минимальные значения отмечены в уровне IgG и М ( Р <0,01; Р 1<0,05) (рис. 2).
Обсуждение. Как известно, развитие опухолевого процесса — сложный многоступенчатый длительный процесс. Ряд авторов утверждают, что переход стадии инициации (первой стадии канцерогенеза) в стадию промоции происходит в результате нарушения механизмов иммунологической защиты [1, 4, 6, 7]. Наши данные также свидетельствуют в пользу этого утверждения, поскольку при изучении показателей клеточного звена иммунитета как у пациенток с ПМСР молочной и щитовидной желез (I группа наблюдения), так и при СРЩЖ были обнаружены изменения. Выявлены достоверные количественные и качественные изменения клеточного и гуморального звеньев иммунитета у пациенток с ПМСР молочной и щитовидной желез по сравнению с соответствующими показателями женщин группы контроля в виде снижения более чем на 30% уровня CD3-, CD16-, CD4-Т-лимфоцитов, всех классов иммуноглобулинов на фоне практически неизмененных показателей CD19-В-лимфоцитов. При сравнении показателей иммунитета пациенток с СРЩЖ и группы контроля отмечено снижение примерно на 34% уровня cD4-T-лимфоцитов, на 20% CD16-Т-лимфоцитов на фоне отсутствия существенных изменений других изучаемых показателей.
При сравнении данных I и II групп наблюдения установлено, что у пациенток с ПМСР молочной и щитовидной желез обнаружены более выраженные изменения в виде снижения общего количества лимфоцитов, CD4-, CD16-Т-лимфоцитов. В I группе наблюдения развитие описанных изменений происходит на фоне увеличения CD8-Т-лимфоцитов ( Р <0,01), что, в свою очередь, и приводит к выраженному снижению иммунорегуляторного индекса.
Нами выявлено снижение всех классов иммуноглобулинов у пациенток I группы наблюдения значительно более выраженное, чем во II группе наблюдения, по сравнению с таковыми показателями практически здоровых женщин. При этом самые минимальные значения отмечены в уровне IgG и М ( Р <0,01) на фоне практически неизмененного уровня В-лимфоцитов. Последнее может говорить о том,
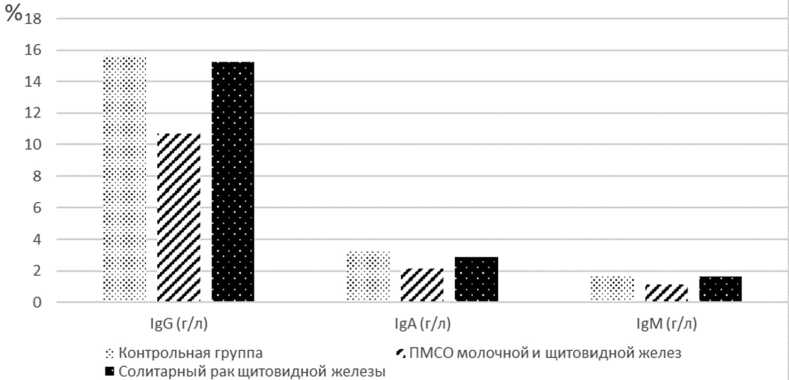
Рис. 2. Изменения показателей основных классов иммуноглобулинов в исследуемых группах наблюдения
что у пациенток с ПМСР молочной и щитовидной желез в процессе подавления продукции IgА, М и G играет роль не столько количественное изменение значений В-лимфоцитов, сколько дефект презентации антигенов, нарушение продукции гуморальных стимуляторов, приводящих к нарушению межклеточного взаимодействия в лимфоидной ткани [4].
Заключение. Анализируя полученные и описанные ранее данные изменения показателей клеточного и гуморального звеньев иммунитета у пациенток с ПМСР молочной и щитовидной желез и СРЩЖ, можно сделать следующие выводы :
-
1. Выявлены общие нарушения клеточного звена иммунологической защиты, более выраженное в I группе наблюдения (у пациенток с ПМСР молочной и щитовидной желез), проявляющиеся снижением общего количества лимфоцитов, CD4-, CD16-Т-лим-фоцитов, иммунорегуляторного индекса.
-
2. Одним из проявлений нарушений противоопухолевого гуморального иммунитета у пациенток с ПМСР молочной и щитовидной желез является значительное снижение уровня иммуноглобулинов основных классов как по сравнению с группой контроля, так и по сравнению с группой пациенток с СРЩЖ.
-
3. Обнаруженные нами изменения показателей иммунологической защиты могут быть применены как дополнительные диагностические и прогностические критерии у больных ПМСР молочной и щитовидной желез, а также учитываться при подборе иммунотерапии.
Список литературы Особенности иммунного ответа при синхронных полинеоплазиях молочной и щитовидной желез по сравнению с солитарным раком щитовидной железы
- Высоцкая И. В., Летягин В. П., Шабанов М.А. и др. Актуальные вопросы канцерогенеза. Клиническая онко-гематология 2019; 12 (1): 101-6.
- Каприна А. Д., Старинский В. В., Петрова Г. В. Злокачественные новообразования в России в 2018 году (заболеваемость и смертность). М.: МНИОИ им. П.А. Герцена филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2019; 250 с.
- Чиссов В. И., Трахтеберг А.Х. Первично-множественные злокачественные опухоли. М.: Медицина, 2000; 360 с.
- Попков B.M., Чеснокова Н.П., Барсуков В.Ю. и др. Канцерогенез, цитокины и иммунитет: патогенетическая взаимосвязь в динамике развития неоплазии. Саратов: Изд-во Сарат гос. мед. ун-та, 2014; 328 с.
- Лыжко H.A. Молекулярно-генетические механизмы инициации, промоции и прогрессии опухолей. Российский биотерапевтический журнал 2017; 16 (4): 7-17.
- Yang S, Gattiononi L, Liu F, et al. In vitro generated anti-tumor T lymphocytes exhibit distinct subsets mimicking in vivo antigen-experienced cells. Cancer Immunol Immunother 2011; 60 (5): 739-49.
- Попков B.M., Чеснокова H. П., Моррисон В. В. и др. Типовые патологические процессы как основа патогенеза болезней различной этиологии. Саратов: Изд-во Сарат. гос. мед. ун-та, 2017; 269 с.


