Особенности экспрессии BDNF в головном мозге крыс при экспериментальном моделировании сахарного диабета I типа
Автор: Шмидт Максим Вячеславович, Смирнов Алексей Владимирович, Тюренков Иван Николаевич, Бакулин Дмитрий Александрович, Великородная Юлия Ивановна, Коломыцев В. В., Гэрюнова Л. В.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 3 т.20, 2023 года.
Бесплатный доступ
Цель исследования. Анализ корреляции между характером и степенью патоморфологических изменений и экспрессией BDNF в различных отделах головного мозга при экспериментальном воспроизведении стрептозотоцининдуцированного сахарного диабета. Экспериментальное исследование проведено на 30 белых беспородных лабораторных крысах в возрасте 12 месяцев. Моделирование стрептозотоцининдуцированного сахарного диабета продолжалось 6 месяцев. Срезы толщиной 5-7 мкм окрашивали тионином по методу Ниссля. Выявление мозгового нейротрофического фактора (BDNF) проводили с помощью иммуногистохимического исследования с использованием первичных антител к белку BDNF. Статистическую обработку данных проводили с использованием пакета программ Statistica 6,0 (StatSoft, USA). Различия между группами оценивали по критерию Манна - Уитни (Mann - Whitney, O-test) и считали статистически значимыми при p
Головной мозг, сахарный диабет, диабетическая энцефалопатия
Короткий адрес: https://sciup.org/142238801
IDR: 142238801 | УДК: 616-005.4:611.813.14:616-092.9
Features of BDNF expression in the rat brain in experimental modeling of type 1 diabetes mellitus
Purpose of the study. Analysis of the correlation between the nature and degree of pathomorphological changes and the expression of BDNF in various parts of the brain during the experimental reproduction of streptozotocin-induced diabetes mellitus. The experimental study was carried out on 30 white outbred laboratory rats aged 12 months. Modeling of streptozotocin-induced diabetes mellitus lasted 6 months. Sections 5-7 pm thick were stained with thionin using the Nissl method. Brain-derived neurotrophic factor (BDNF) was detected by immunohistochemistry using primary antibodies to the BDNF protein. Statistical data processing was carried out using the Statistica 6.0 software package (StatSoft, USA). Differences between groups were assessed using the Mann - Whitney O-test and were considered statistically significant at p
Текст научной статьи Особенности экспрессии BDNF в головном мозге крыс при экспериментальном моделировании сахарного диабета I типа
Funding : the work was carried out with the financial support of the RSF grant No. 21-15-00192.
Сахарный диабет (СД), характеризующийся высокой заболеваемостью и смертностью, является серьезной проблемой здравоохранения во всем мире.
Результирующим действием хронической гипергликемии на организм пациентов является развитие осложнений, сопровождающихся повреждением, дисфункци-
ей и недостаточностью со стороны различных органов: кровеносных сосудов, сердца, почек, органов желудочно-кишечного тракта, а также периферической (ПНС) и центральной нервной системы (ЦНС). В настоящее время любое когнитивное расстройство: тревога, потеря памяти, депрессия, деменция, а также болезнь Альцгеймера, возникшие на фоне СД, при отсутствии других предрасполагающих факторов, рассматривается как диабетическая энцефалопатия (ДЭ). Гипергликемия провоцирует ряд механизмов, которые, как считается, лежат в основе ДЭ, включая апоптоз нейронов, окислительный стресс, нейровоспаление и измененный нейрогенез, гипер-лептинемию, повышение уровня глюкокортикоидов, митохондриальую дисфункцию и т. д. [1, 2]
Нейротрофический фактор головного мозга (BDNF) представляет собой белок, участвующий в регуляции нескольких процессов, включая нейропластичность, нейровоспаление, нейрогенез и дифференцировку нейронов, и связан с рядом неврологических и психиатрических расстройств [3–5]. Обнаружен низкий уровень BDNF и развитие когнитивного дефицита при СД. Предполагается, что снижение уровня BDNF может нарушать метаболизм глюкозы и способствовать проггрессированию СД и его осложнений [4].
Показано, что когнитивный дефицит у мышей при СД снижается при лечении производными адамантана, что приводит к возрастанию экспрессии GLP-1-глюкагоноподобного пептида, а также генов BDNF, Cav1 в головном мозге и центральной блокаде провоспалительного синтеза цитокинов [6].
Кроме того, до настоящего времени, остаются малоизученным вопрос об особенностях иммуногистохимической экспрессии BDNF в различных отделах головного мозга при диабетической энцефалопатии и сопряженности данной экспрессии с характером и степенью нейродегенеративных изменений.
ЦЕЛЬ РАБОТЫ
Анализ корреляции между характером и степенью патоморфологических изменений и экспрессией BDNF в различных отделах головного мозга при экспериментальном воспроизведении стрептозотоци-ниндуцированного СД.
МЕТОДИКА ИССЛЕДОВАНИЯ
Экспериментальное исследование проведено на 30 белых беспородных лабораторных крысах-самках в возрасте 12 месяцев. Моделирование стрептозотоци-ниндуцированного СД длительностью 6 месяцев проводили по ранее описанной методике [7]. В качестве позитивного контроля использовали крыс без СД (интактных) той же партии животных. Забор тканей головного мозга проводили у наркотизированных (хлоралгидрат, 400 мг/кг, внутрибрюшинно) животных.
Материал фиксировали в 10%-м нейтральном формалине, с дальнейшим обезвоживанием в бата- рее спиртов и изготовлением парафиновых блоков. Срезы толщиной 5–7 мкм окрашивали тионином по методу Ниссля. Исследовали признаки повреждения в высокочувствительных к различным повреждающим факторам популяциях клеток ганглионарного слоя коры и пирамидных нейронов гиппокампа (поля СА1, СА3).
Выявление мозгового нейротрофического фактора (BDNF) проводили с помощью иммуногистохимического исследования с использованием первичных антител к белку BDNF (нейротрофический фактор мозга; англ. brain-derived neurotrophic factor) в соответствии с инструкциями производителя (разведение 1 : 100) (Affinity Biosciences, China) и визуализирующей полимерной системы детекции Гистофайн – N-Histofine® Simple Stain MAX PO (MULTI) (Nichirei Nichirei Biosciences INC., Japan). Срезы докрашивали гематоксилином. Интенсивность экспрессии BDNF на срезах оценивали с помощью программы анализа изображений ImageJ 1.54d. Определяли относительную площадь, занимаемую иммунопози-тивным материалом в поле зрения микроскопа. Фотодокументирование осуществляли цифровой фотокамерой Olympus (Япония). Статистическую обработку данных проводили с использованием пакета программ Statistica 6,0 (StatSoft, USA). Различия между группами оценивали по критерию Манна – Уитни (Mann – Whitney, U -test) и считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
В серии экспериментов по моделированию стреп-тозотоцининдуцированного СД структурные изменения носили неоднородный характер в различных структурах головного мозга и значительно варьировали от животного к животному. В гиппокампе среди нейронов пирамидного слоя СА1 поля у крыс с экспериментальным СД обнаружены единичные гиперхромные клетки (табл. 1).
В СА3 гиппокампа визуализировалось значительное количество сморщенных нейронов с гиперх-роматозом цитоплазмы перикарионов.
Обнаруживались также единичные сморщенные нейроны с резко выраженной базофилией цитоплазмы перикарионов и пикнотичным ядром. При морфометрическом анализе отмечена тенденция к увеличению количества поврежденных нейронов. Относительная плотность гиперхромных нейронов с дистрофическими изменениями в группе животных с экспериментальным СД составляла (10,19 ± 4,09) %, в группе контрольных крыс данный показатель составил (2,38 ± 0,75) % (при p > 0,05).
Из всех функциональных отделов церебральной коры патоморфологические изменения наблюдалось, в основном, в моторных, соматосенсорных и аудиторных областях коры. Обращает на себя внимание тот факт, что дистрофический процесс затрагивал преимущественно крупные клетки ганглионарного слоя. Преобладали гиперхромные изменения, характеризующиеся уменьшением объема и деформацией клеточных тел. Отмечалось усиление базофилии цитоплазмы, при этом глыбки базофильного материала локализовались перинуклеарно или по периферии перикариона.
Ядра также деформировались и уменьшались в объеме. Часть клеток характеризовались выраженной гиперхромией и гомогенизацией цитоплазмы с невозможностью визуализации ядерного материала. В некоторых нейронах данные изменения сочетались с появлением внутрицитоплазматических вакуолей.
По данным морфометрического исследования, достоверное увеличение поврежденных нейронов фиксировалось во всех исследуемых отделах неокор-текса, однако наиболее выраженные дистрофические изменения фиксировались в моторных и соматосенсорных отделах неокортекса (см. табл.).
Относительная численная плотность поврежденных нейронов в различных отделах головного мозга ( M ± m ) %
|
Структуры головного мозга |
Степень патоморфологических изменений нейронов |
Интакт |
СД |
|
CA1 поле гиппокампа |
НН |
96,42 ± 0,63 |
96,48 ± 0,48 |
|
СН |
3,25 ± 0,39 |
2,98 ± 0,40 |
|
|
ГН |
0,32 ± 0,32 |
0,55 ± 0,37 |
|
|
CA3 поле гиппокампа |
НН |
97,62 ± 0,75 |
89,81 ± 4,09 |
|
СН |
1,99 ± 0,57 |
2,54 ± 0,25 |
|
|
ГН |
0,39 ± 0,39 |
7,65 ± 4,05 |
|
|
Моторная кора |
НН |
98,14 ± 0,63 |
85,16 ± 2,35 * |
|
СН |
1,59 ± 0,52 |
6,78 ± 2,26 * |
|
|
ГН |
0,28 ± 0,28 |
8,06 ± 2,01 * |
|
|
Соматосенсорная кора |
НН |
97,65 ± 0,69 |
68,10 ± 4,47 * |
|
СН |
2,11 ± 0,64 |
7,20 ± 1,97 * |
|
|
ГН |
0,25 ± 0,25 |
24,70 ± 3,86 * |
|
|
Аудиторная кора |
НН |
97,70 ± 0,85 |
89,47 ± 1,36 * |
|
СН |
2,01 ± 0,78 |
5,83 ± 4,24 * |
|
|
ГН |
0,29 ± 0,29 |
4,70 ± 1,24 * |
Примечания: * - показатели статистически значимо отличаются от группы Интакт при р < 0,05; Критерий Манна - Уитни. Степень поражения нейронов [Чубинидзе А. И., 1972]: нейроны нормальные, неизмененные (НН); слабоизменен-ные нейроны (СН) с сохранением ядра, но со структурными или тинкториальными нарушениями компонентов цитоплазмы (набухание, гиперхроматоз, хроматолиз, центральная тинкториальная ацидофилия); грубо измененные нейроны (ГН) -выраженное сморщивание, «тяжелое изменение», гомогенизирующее изменение нейронов, клетки-тени.
У интактных животных нейротрофический фактор выявлялся преимущественно в цитоплазме нейронов и клеток глии, а также эндотелии средних и крупных сосудов. Иммунопозитивное окрашивание носило неоднородный характер: преобладали клетки с умеренной экспрессией белка в цитоплазме, однако, в единичных случаях обнаруживались интенсивно окрашенные клетки (рис. 1).
У экспериментальных животных со стрептозото-цининдуцированном СД иммуногостохимическое исследование продемонстрировало достоверное снижение относительной площади иммунопозитивного материала как в полях гиппокампа, так и различных функциональных отделах церебральной коры (рис. 2).
В СА1 поле гиппокампа фиксировалось преимущественно уменьшение концентрации BDNF в цитоплазме клеток без значимых признаков повреждения нейронов.
По сравнению с интактными крысами увеличивалось количество слабо позитивных и BDNF-негативных нейронов. В СА3 поле и исследуемых отделах неокортекса сохранялась данная тенденция, но дополнительно отмечалось выраженное снижение экс- прессии нейротрофического фактора в клетках с признаками повреждения различной степени выраженности (рис. 1).
Таким образом, результаты проведенной нами работы позволили выявить сопряженность снижения уровня экспрессии BDNF cо степенью нейродегене-ративных изменений в коре головного мозга крыс при экспериментальном моделировании СД I типа.
Стоит отметить тот факт, что при экспериментальной диабетической энцефалопатии, экспрессия нейротрофического фактора начинала снижаться даже в отсутствие видимых патоморфологических изменений в нейронах и в клетках глии, что наблюдалось нами в СА1 поле гиппокампа. При этом, дефицит нейротрофина продолжал нарастать по мере развития дистрофических изменений, за счет резкого снижения экспрессии BDNF в цитоплазме поврежденных клеток (СА3 поле гиппокампа, церебральная кора), что позволяет рассматривать развитие когнитивных нарушений и признаков атрофических и обратимых изменений в нейронах коры головного мозга при СД в контексте снижения нейропротекторного влияния BDNF [8, 9].
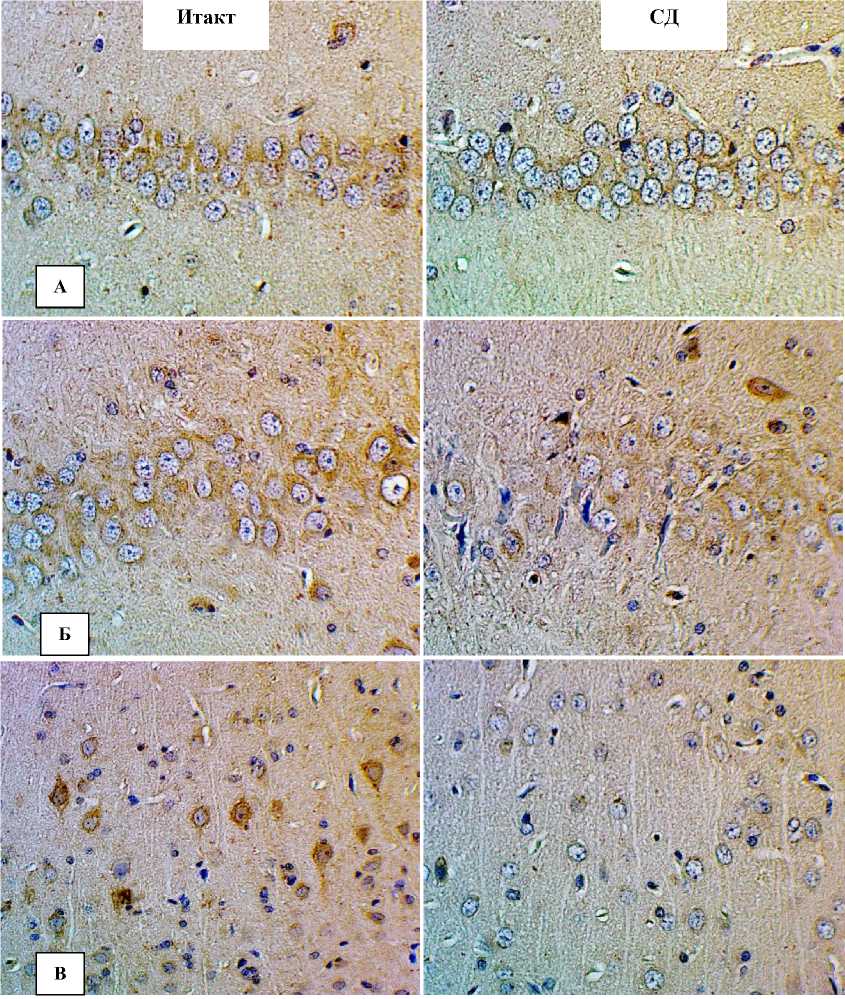
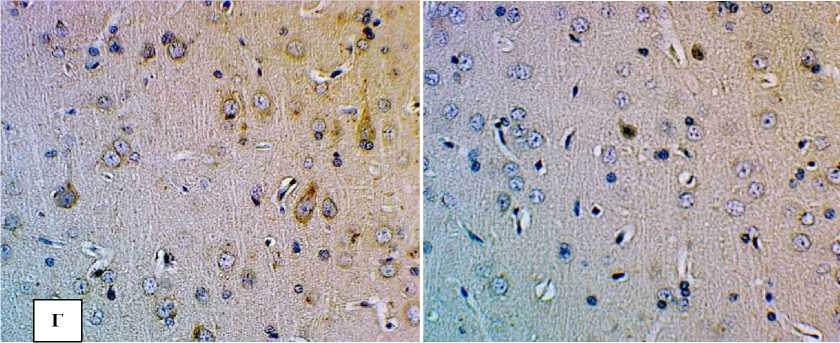
Рис. 1. Снижение экспрессии BDNF в структурах головного мозга при экспериментальной диабетической энцефалопатии: А – СА1 поле гиппокмпа; Б – СА3 поле гиппокмпа; В – Моторная кора. Г – Аудиторная кора. Иммуногистохимическое исследование, антитела против BDNF, докраска гематоксилином. Увеличение x400.
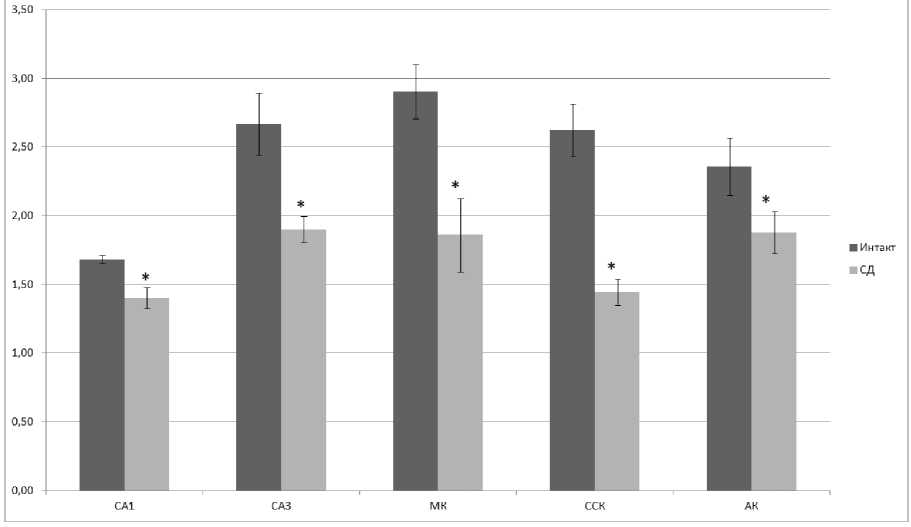
Рис. 2. Относительная площадь экспрессии BDNF в различных функциональных отделах головного мозга при моделировании СД M ± m %. СА1- СА1 поле гиппокампа; СА3- СА3 поле гиппокампа; МК – моторная кора; ССК – соматосенсорная кора;
АК – аудиторная кора
Примечание. * – показатели статистически значимо отличаются от группы интакт при р < 0,05; Критерий Манна – Уитни.
Кроме того, данное исследование свидетельствует о том, что иммуногистохимическое определение экспрессии BDNF в структурах головного мозга является чрезвычайно чувствительным методом, выявляющим морфофункциональные изменения нейронов и клеток глии на самых ранних стадиях ДЭ.
ЗАКЛЮЧЕНИЕ
Таким образом, морфологические изменения в головном мозге при экспериментальном моделировании диабетической энцефалопатии характеризуются снижением цитоплазматической экспрессии белка BDNF в моторных, соматосенсорных, аудиторных областях коры головного мозга и в СА1, СА3 полях гиппокампа в нейронах с признаками обратимых изменений, а также в нейронах без значимых патоморфологиче-ских признаков повреждения, что, по-видимому, способствует снижению устойчивости нейронов неокортек-са и архикортекса к повреждению при СД.
Нейропротективное влияние BDNF может быть связано с его противовоспалительным, регенераторным, а также антиапоптотическим свойствами [3, 10, 11], делает актуальным поиск путей сохранения и/или стимуляции продукции BDNF для патогенетически обоснованной нейропротекции при СД и его осложнениях.
Список литературы Особенности экспрессии BDNF в головном мозге крыс при экспериментальном моделировании сахарного диабета I типа
- Смирнов А. В., Бисинбекова А. И., Файбисович Т. И. Морфофункциональные изменения головного мозга при сахарном диабете. Вестник Волгоградского государственного медицинского университета. 2022;19(3):3–8.
- Wang C., Li J, Zhao S, Huang L. Diabetic encephalopathy causes the imbalance of neural activities between hippocampal glu-tamatergic neurons and GABAergic neurons in mice. Brain Res. 2020;1742:146863. doi:10.1016/j.brainres. 2020.146863
- Аврущенко М. Ш., Острова И. В. Постреанимацион-ные изменения экспрессии мозгового нейротрофического фактора (BDNF): взаимосвязь с процессом гибели нейронов. Общая реаниматология. 2017;13(4):6–21.
- Moosaie F., Mohammadi S., Saghazadeh A. et al. Brain-derived neurotrophic factor in diabetes mellitus: A systematic review and meta-analysis. PLoS ONE 2023; 18(2):e0268816. https://doi.org/10.1371/journal.pone.0268816.
- Magdalena M., Morici J. F., Zanoni M. B. et al. Brain-Derived Neurotrophic Factor: A Key Molecule for Memory in the Healthy and the Pathological Brain. Frontiers in Cellular Neuro-science. 2019;13:363.
- Piątkowska-Chmiel I., Gawrońska-Grzywacz M., Popiołek Ł. et al. The novel adamantane derivatives as poten-tial mediators of inflammation and neural plasticity in diabetes mice with cognitive impairment. Sci Rep. 2022;12(1):6708.
- Тюренков И. Н., Смирнов А. В., Бакулин Д. А. и др. Морфологические особенности миокарда при экспериментальном сахарном диабете и его фармакологической коррекции мефаргином. Волгоградский научно-медицинский журнал. 2022;4:25–29.
- Selvarajah D., Wilkinson I. D., Fang F. et al. Structural and Functional Abnormalities of the Primary Somatosensory Cortex in Diabetic Peripheral Neuropathy: A Multimodal MRI. Tesfaye Diabetes. 2019;68(4):796–806. doi: 10.2337/db18-0509.
- Tyurenkov I. N., Smirnov A. V., Mednikov D. S. et al. Functional and morphological changes in the pyramidal layer of the hippocampus in rats with encephalopathy induced by prolonged exposure to gravitational overloading. Neuroscience and Behavioral Physiology. 2020;50(4):479–484.
- Liu P., Li H., Wang Y. et al. Harmine Ameliorates Cognitive Impairment by Inhibiting NLRP3 Inflammasome Activation and Enhancing the BDNF/TrkB Signaling Pathway in STZ-Induced Diabet-ic Rats. Frontiers in Pharmacology. 2020;11:535.
- Rozanska O., Uruska A., Zozulinska-Ziolkiewicz D. Brain-Derived Neurotrophic Factor and Diabetes. Int. J. Mol. Sci. 2020;21:841.


