Особенности экспрессии глиального фибриллярного кислого белка в гиппокампе у крыс зрелого возраста при моделировании сахарного диабета первого типа и фармакологической коррекции
Автор: Смирнов А.В., Тюренков И.Н., Пустынников В.Э., Великородная Ю.И., Петров А.Д.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 1 т.23, 2026 года.
Бесплатный доступ
Исследование экспрессии глиального фибриллярного кислого белка (ГФКБ, GFAP), ключевого маркера функционального состояния астроцитов при моделировании сахарного диабета (СД), является актуальным в связи со значительной частотой встречаемости диабетической энцефалопатии у пациентов пожилого возраста с СД и ограниченностью данных о патогенетических подходах к ее терапии. Материалы и методы. На модели СД 1-го типа, индуцированного стрептозотоцином, у 50 крыс линии Wistar (возраст 12 месяцев) через 6 месяцев стойкой гипергликемии изучали эффекты 30-дневного курса аминалона (1000 мг/кг/сут.), сукцикарда (50 мг/кг/сут.) и мефаргина (20 мг/кг/сут.). Экспрессию GFAP в гиппокампе оценивали иммуногистохимически с последующей морфометрией в программе ImageJ и статистическим анализом по критерию ANOVA. Результаты и обсуждение. В группе нелеченных животных с СД зафиксирована достоверное уменьшение относительной площади экспрессия GFAP в астроцитах гиппокампа относительно интактного контроля. При терапии аминалоном было зафиксирована большая площадь ИРМ в нейронах гиппокампа, чем у животных с СД. На фоне приема сукцикарда у животных также наблюдалась большая площадь ИРМ в нейронах гиппокампа по сравнению с животными с СД без лечения. У животных с СД, получавших мефаргин, была отмечена тенденция к повышению ИРМ по сравнению с материалом животных без лечения. Заключение. Экспериментальный СД приводит к снижению экспрессии GFAP в гиппокампе, что указывает на нарушение астроцитарного гомеостаза и на участие клеток глии в реализации процессов нейровоспаления при диабетической энцефалопатии. ГАМК и ее производные воздействуют на астроциты и способствуют восстановлению уровня экспрессия GFAP. Полученные результаты обосновывают перспективность дальнейшего изучения производных ГАМК в качестве средств нейропротекции при когнитивных нарушениях диабетического генеза.
Сахарный диабет, GFAP, гиппокамп, ГАМК, аминалон, сукцикард, мефаргин
Короткий адрес: https://sciup.org/142247591
IDR: 142247591 | УДК: 616-091.0 | DOI: 10.19163/2658-4514-2026-23-1-47-53
Features of GFAP expression in hippocampus of mature rats during modeling of type 1 diabetes mellitus and pharmacological correction
Investigation of the expression of glial fibrillary acidic protein (GFAP), a key marker of the functional state of astrocytes, in experimental modeling of diabetes mellitus (DM) is relevant due to the high incidence of diabetic encephalopathy in elderly patients with DM and the limited data on pathogenetic approaches to its therapy. Materials and methods: Using a model of type 1 DM induced by streptozotocin in 50 Wistar rats (aged 12 months), the effects of a 30-day course of aminalon (1000 mg/kg/day), succicard (50 mg/kg/day), and mefargin (20 mg/kg/day) were studied after 6 months of persistent hyperglycemia. GFAP expression in the hippocampus was assessed immunohistochemically followed by morphometry in ImageJ software and statistical analysis using ANOVA. Results and discussion: In the group of untreated diabetic animals, a significant decrease in the relative area of GFAP expression in hippocampal astrocytes was recorded compared to the intact control. Treatment with aminalon resulted in a larger area of immunoreactive material (IRM) in hippocampal neurons compared to diabetic animals. Animals receiving succicard also showed a larger area of IRM in hippocampal neurons compared to untreated diabetic animals. In diabetic animals treated with mefargin, a trend toward increased IRM was noted compared to material from untreated animals. Conclusion: Experimental DM leads to decreased GFAP expression in the hippocampus, indicating impaired astrocytic homeostasis and the involvement of glial cells in mechanisms of neuroinflammation in diabetic encephalopathy. GABA and its derivatives exert effects on astrocytes and promote the restoration of GFAP expression levels. The obtained results substantiate the promise of further investigation of GABA derivatives as agents for neuroprotection in cognitive disorders of diabetic origin.
Текст научной статьи Особенности экспрессии глиального фибриллярного кислого белка в гиппокампе у крыс зрелого возраста при моделировании сахарного диабета первого типа и фармакологической коррекции
doi:
ORIGINAL ARTICLE doi:
Financing. This work was supported by the Russian Science Foundation (grant number 24-25-00247).
Диабетическая энцефалопатия (ДЭ) представляет собой одно из тяжелых осложнений сахарного диабета, характеризующихся прогрессирующими структурными и функциональными нарушениями в центральной нервной системе (ЦНС). В основе патогенеза ДЭ лежит комплекс метаболических расстройств, включающих хроническую гипергликемию, окислительный стресс, нитрозативный стресс, нейровоспаление, микро- и макроангиопатии, приводящие к дисфункции и гибели нейронов [1]. При этом глиальные клетки играют основную роль в поддержании гомеостаза в головном мозге [2].
Одним из маркеров состояния астроцитов является белок GFAP (глиальный фибриллярный кислый белок), который входит в состав промежуточных филаментов этих клеток. В норме GFAP экспрессируется в астроцитах, где он выполняет структурную функцию, обеспечивая механическую поддержку и участвуя в поддержании формы клеток и их отростков [3]. Помимо этого, GFAP участвует в процессах репарации, синаптической пластичности и активации астроцитов при воспалении [4].
Уровень GFAP неоднозначен при различных патологических состояниях. При сахарном диабете (СД), в условиях хронического метаболического стресса, изначально наблюдается повышение уровня GFAP, вследствие перехода астроцитов в состояние реактивного астроглиоза. При длительном течении СД компенсаторные механизмы астроцитов истощаются, что отражает функциональные нарушения, а позднее – гибель нейронов, глиальных клеток, в т. ч. астроцитов (но астроциты могут делиться), тем самым снижая уровень GFAP в головном мозге [5]. При физиологическом старении происхо- дит глиоз, характеризующийся увеличением уровня GFAP, что является компенсаторной реакцией на накопление возрастных повреждений [6, 7]. Сочетание старения и сахарного диабета способствует развитию более выраженных когнититвных нарушений [8].
Учитывая развитие нейровоспаления у стареющих животных с СД, сопровождающегося повышением уровня IL6 в коре головного мозга [9], изучение состояния глиальных клеток является актуальным.
В поиске стратегий фармакологической коррекции диабет-индуцированных повреждений ЦНС значительный интерес представляет γ-аминомасляная кислота (ГАМК).
Введение ГАМК или ее агонистов может способствовать восстановлению нормального состояния ЦНС за счет подавления нейровоспаления и снижения окислительного стресса [7]. Важным механизмом является способность ГАМК поддерживать активность астроцитов, нормализуя экспрессию GFAP, тем самым способствуя репарации глиальной сети [10].
Актуальным направлением фармакологической коррекции неврологических нарушений является поиск среди соединений на основе ГАМК, таких как аминалон, сукцикард и мефаргин. В связи с этим иммуногистохимический анализ экспрессии белка GFAP в головном мозге крыс при экспериментальной диабетической энцефалопатии на фоне старения и ее коррекции производными ГАМК представляется актуальным.
ЦЕЛЬ РАБОТЫ
Охарактеризовать уровень экспрессии глиального фибриллярного кислого белка (GFAP) в гиппокампе стареющих крыс при моделирова- нии сахарного диабета и его фармакологической коррекции ГАМК и ее производными.
МЕТОДИКА ИССЛЕДОВАНИЯ
Исследование выполнено на 50 беспородных крысах-самцах линии Wistar в возрасте 12 месяцев (масса тела 280–320 г). Содержание животных осуществляли в стандартных условиях вивария: температура (22 ± 2) °C, влажность (55 ± 10) %, 12-часовой цикл «свет – темнота» со свободным доступом к воде и стандартному гранулированному корму. Все процедуры проводили в соответствии с международными биоэтическими принципами и были одобрены локальным этическим комитетом (протокол № 2022/116 от 04.03.2022).
Моделирование сахарного диабета 1-го типа проводили на фоне 14-часовой пищевой депривации посредством однократного внутрибрюшинного введения стрептозотоцина (STZ) в дозе 60 мг/кг (производитель: SRL, Индия). Уровень гликемии контролировали через 72 часа после инъекции STZ, а в дальнейшем – ежемесячно на протяжении 6 месяцев с использованием глюкометра Contour TS.
Критерием включения животных в эксперимент была стабильная гипергликемия в интервале от 10 до 18 ммоль/л, сохранявшаяся в течение полугодового периода.
Через полгода после верификации диабета животные были рандомизированы на пять групп по 7 особей: группа Интакт – интактные особи без диабета; группа СД – крысы с сахарным диабетом, не получавшие лечение; группа СД + аминалон – животные с диабетом, получавшие аминалон в дозе 1000 мг/кг/сут.; группа СД + сукцикард – животные с диабетом, получавшие сукцикард в дозе 50 мг/кг/сут.; группа СД + мефаргин – животные с диабетом, получавшие мефаргин в дозе 20 мг/кг/сут. Препараты вводили ежедневно внутрижелудочно в течение 30 дней.
После окончания курса терапии животных подвергали наркотизации внутрибрюшинным введением хлоралгидрата (400 мг/кг) с последующей транскардиальной перфузией 10%-м нейтральным забуференным формалином для фиксации головного мозга. Гистологическую обработку проводили по стандартным протоколам с изготовлением парафиновых срезов толщиной 4–5 мкм. Для детекции GFAP проводили иммуногистохимическое окрашивание с использова- нием поликлональных антител (Cloud-Clone Corp., рабочий титр 1 : 100). Визуализацию проводили с применением полимерной системы LSAB и хромогена DAB (DAKO, Дания). Специфичность иммуногистохимической реакции контролировали на срезах, инкубированных без добавления первичных антител.
Морфометрический анализ экспрессии иммунореактивного материала (ИРМ) при использовании первичных антител против GFAP в гиппокампе выполняли с использованием программного обеспечения ImageJ 1.54d (NIH, США), рассчитывали относительную площадь ИРМ [11].
Статистическую обработку данных осуществляли в программе Prism 10 (GraphPad Software, США). Нормальность распределения оценивали тестом Шапиро – Уилка. Для анализа межгрупповых различий применяли однофакторный дисперсионный анализ (ANOVA) с последующим пост-тестом Тьюки параметрического распределения или непараметрический критерий Крускала – Уоллиса с коррекцией Данна.
Различия считали статистически значимыми при уровне p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯИ ИХ ОБСУЖДЕНИЕ
При скрининговом анализе различных отделов головного мозга стареющих крыс при СД наиболее выраженные изменения экспрессии GFAP были обнаружены в гиппокампе.
При иммуногистохимическом анализе была выявлена интенсивная экспрессия GFAP в цитоплазме тел и отростков астроцитов в гиппокампе 19-месячных интактных крыс, не страдающих сахарным диабетом. Иммунопозитив-ные астроциты более плотно располагались в молекулярном и краевом слоях. При морфометрическом анализе относительная площадь ИРМ GFAP в гиппокампе у животных без СД составила (18,26 ± 0,69) %.
У крыс с экспериментальным сахарным диабетом, не получавших лечение, в гиппокампе выявлена меньшая относительная площадь экспрессии GFAP, при этом меньше всего астроцитов обнаружено в пирамидном слое.
Количественный анализ показал достоверное уменьшение иммунореактивности в СА1, СА2, СА3, более выражено в области СА1 до (7,61 ± 0,23) % по сравнению с интактными животными (p < 0,0001). Морфологические изменения свидетельствуют о развитии дисфункции нейронального метаболизма в условиях диабетической нейродегенерации.
На фоне фармакологической коррекции было выявлено различие в степени восстановления уровня GFAP. У животных с СД, получавших сукцикард, уровень экспрессии в гиппокампе [(9,25 ± 0,18) %] достоверно превышал показатели группы СД без лечения (p < 0,001), что свидетельствует о влиянии исследуемого препарата на астроциты, экспрессирующие GFAP в условиях диабетической энцефалопатии. В группе животных с СД, получавших аминалон, относительная площадь ИРМ в гиппокампе была ниже [(9,78 ± 0,19) %], чем при применении сукцикарда, но также статистически отличалась от группы СД (p < 0,05). Подобные изменения указывают на менее выраженное влияние сук-цикарда на астроцитарную глию.
У животных, получавших мефаргин, уровень экспрессии GFAP в гиппокампе составил (7,87 ± 0,28) %, что сопоставимо с показателями группы СД без лечения и было ниже, чем в группах СД с фармакокоррекцией аминалоном и сукцикардом (рис. 1,2).
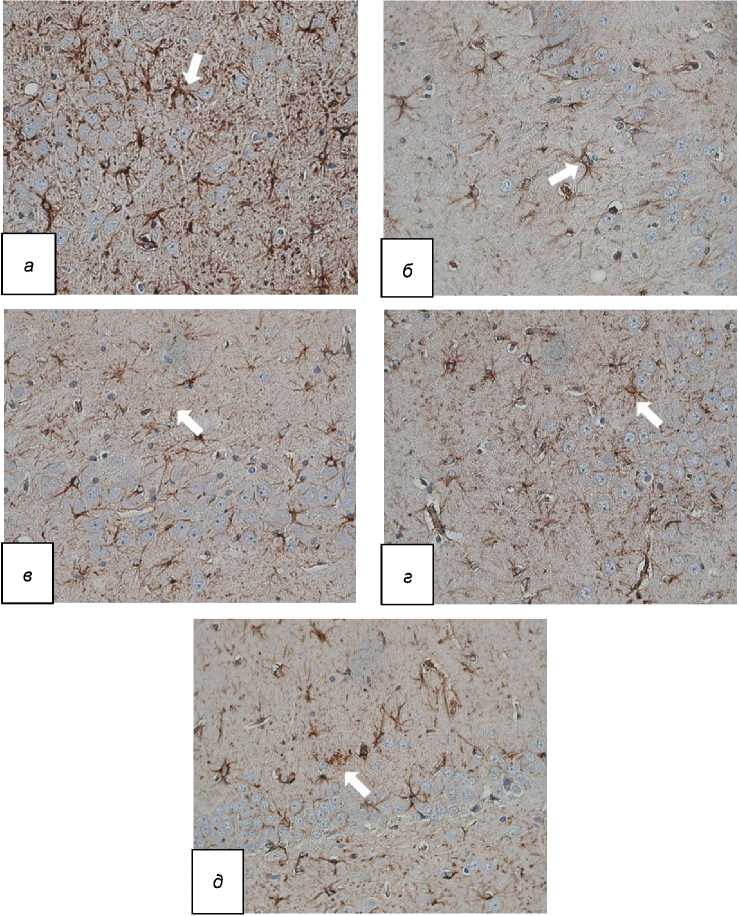
Рис. 1. Изменение экспрессии GFAP в цитоплазме астроцитов гиппокампа старых крыс при экспериментальном сахарном диабете:
а – группа интактных животных (крысы без СД); б – группа животных с сахарным диабетом (СД); в – группа животных с сахарным диабетом и фармакокоррекцией аминалоном (СД + аминалон); г – группа животных с сахарным диабетом и фармакокоррекцией сукцикардом (СД + сукцикард); д – группа животных с сахарным диабетом и фармакокоррекцией мефаргином (СД + мефаргин). Иммуногистохимическое исследование, антитела против GFAP, докраска гематоксилином.
Увеличение ×400. Белые стрелки – экспрессия ИРМ
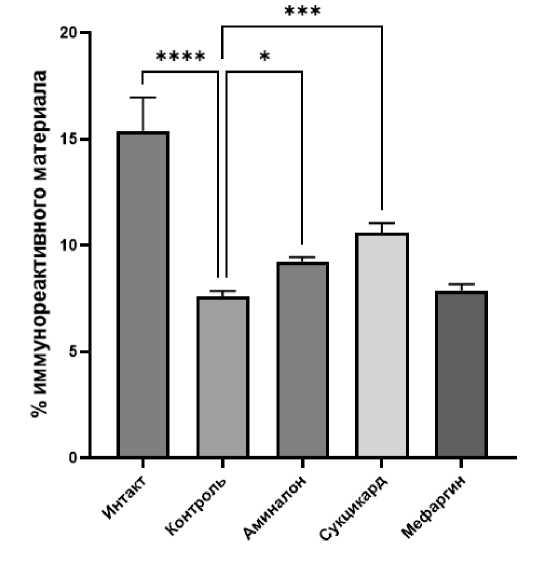
Рис. 2. Удельная площадь экспрессии иммунореактивного материала в гиппокампе:
**** - различия между группами статистически значимы (Anova-Тест), p < 0,0001; *** - различия между группами статистически значимы (Anova-Тест), p < 0,001; ** - различия между группами статистически значимы (Anova-Тест), p < 0,005; * - различия между группами статистически значимы (Anova-Тест), p < 0,05
Полученные данные демонстрируют влияние физиологического старения и сахарного диабета на экспрессию белка GFAP в астроцитах гиппокампа. Выявленное значительное подавление экспрессии GFAP при экспериментальном диабете 1-го типа развивается на фоне возрастных изменений астроцитарной глии [12], что свидетельствует о патогенном воздействии ряда патогенетических факторов. При этом уровень GFAP отражает взаимодействие компенсаторных и патологических процессов, формирование реактивного, возможно заместительного астроглиоза с изменением экспрессии GFAP, как белка промежуточных филаментов цитоскелета астроцитов, уровень которого снижался в гиппокампе при СД у стареющих животных, что приводит к истощению компенсаторных механизмов и к более раннему развитию диабетической энцефалопатии.
Полученные нами данные согласуются с современными представлениями о GFAP как маркере функционального состояния астроцитов [13]. Изменение экспрессии этого белка отражает такие патологические процессы, как утрата структурной опоры для нейронов и развитие нейровоспаления [14], а также приводит к нарушению функций гематоэнцефалического барьера и снижению защитных резервов ЦНС. В совокупности это тормозит восстановление нервной ткани и обуславливает возникновение когнитивного дефицита [10].
По нашим данным, фармакологическая коррекция производными ГАМК, в частности ами-налоном и сукцикардом, способствовала восстановлению уровня GFAP в гиппокампе, что свидетельствует о способности исследуемых веществ поддерживать активность и защитные функции астроцитов в условиях диабетической энцефалопатии. Эффект объясняется восполнением энергетического метаболизма через вовлечение ГАМК-шунта и цикла Кребса [15], что подтверждает связь между ГАМК-ергической передачей и регуляцией экспрессии GFAP.
Актуальным направлением является дальнейшее изучение сигнальных путей, связывающих ГАМК-ергическую нейротрансмиссию с функциональным состоянием астроцитов и экспрессией GFAP. Учитывая роль астроцитарной дисфункции в патогенезе диабетической энцефалопатии [5], полученные данные уточняют механизмы изменения астроглии при СД и способствуют дальнейшему изучению производных ГАМК как потенциальных нейропротективных агентов, направленных на сохранение глиального гомеостаза при диабет-ассоциированных когнитивных нарушениях.
ЗАКЛЮЧЕНИЕ
Экспериментальный СД приводит к снижению экспрессии GFAP в гиппокампе, что указывает на нарушение астроцитарного гомеостаза, и участие клеток глии в реализации процессов нейровоспаления при диабетической энцефалопатии. ГАМК и ее производные оказывают воздействие на астроциты и способствуют восстановлению уровня экспрессия GFAP. Полученные результаты обосновывают перспективность дальнейшего изучения производных ГАМК в качестве средств нейропротекции при когнитивных нарушениях диабетического генеза.


