Особенности каталитической трансформации метанола в углеводороды в условиях микроструктурированных потоков
Автор: Бровко Роман Викторович, Мушинский Лев Сергеевич, Долуда Валентин Юрьевич
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Химические науки
Статья в выпуске: 1 т.8, 2022 года.
Бесплатный доступ
Трансформация метанола в углеводороды - сложная каталитическая реакция, сопровождающаяся образованием широко перечня углеводородов и протекающая на поверхности кислотных центров различных цеолитов. При этом наиболее часто используемый в качестве катализатора цеолит H-ZSM-5 представляет из себя высокодисперсный материал с диаметром кристаллов 1-20 мкм, что затрудняет его непосредственное использование в реакторах с закрепленным слоем катализатора в связи с высоким гидравлическим сопротивлением каталитического слоя. Традиционно в промышленности подобный вопрос решается применением сложных реакторных систем с псевдоожиженным слоем, что является обоснованным в крупнотоннажном производстве. В установках малой и средних мощностей использование систем с псевдоожиженным слоем является экономически не обоснованным. Одним из возможных решений этой проблемы является использование монолитного катализатора с нанесенным слоем цеолита H-ZSM-5. В настоящей статье приводится исследование каталитической активности цеолитсодержащего микроструктурированного монолита в реакции трансформации метанола в углеводороды. Синтез монолита производился методом прессования цеолитсодержащей массы с последующей сушкой, кальцинированием и вторичным ростом цеолита на поверхности монолита. Были синтезированы образцы монолита со средним диаметром каналов 0,5, 1,0, 1,5, 2,0 мм. Образцы микроструктурированного катализатора были протестированы при варьировании температуры от 250 до 450 °C и при варьировании удельной скорости подачи метанола от 0,65 до 2,3 кг (MeOH)/(кг (Кат)ч). Для чего монолитный катализатор помещался в установки для тестирования микроструктурированных катализаторов состоящую из насоса, термоконтроллера, каталитического реактора, конденсатора, делительной воронки и хроматографа. Варьирование условий показало, что для преимущественного получения газообразных углеводородов С1-С4 целесообразно проводить реакцию в следующих условиях: средний диаметр каналов катализатора 2 мм, температура проведения реакции 350 °C, скорость подачи метанола 1,65 кг (MeOH)/(кг (Кат)ч). Для преимущественного образования жидких углеводородов фракции С5-С8 целесообразно проведение процесса трансформации метанола в углеводороды в следующих условиях: средний диаметр каналов катализатора 1 мм, температура проведения реакции 350 °C, скорость подачи метанола 0,65 кг (MeOH)/(кг(Кат)ч). Для преимущественного образования жидких углеводородов фракции С9-С12 целесообразно проведение процесса трансформации метанола в углеводороды в следующих условиях: средний диаметр каналов катализатора 0,5 мм, температура проведения реакции 350 °С, скорость подачи метанола 0,65 кг (MeOH)/(кг (Кат)ч).
Метанол, микрореактор, трансформация, катализатор, цеолит
Короткий адрес: https://sciup.org/14121637
IDR: 14121637 | УДК: 544.47 | DOI: 10.33619/2414-2948/74/02
Catalytic methanol to hydrocarbons transformation particularities in case of micro structured flows application
The methanol into hydrocarbons transformation is a complex catalytic reaction accompanied by the formation of a wide range of hydrocarbons and proceeding on the surface of acid sites of various zeolites. Zeolite H-ZSM-5 considered to be most often used catalyst for this process. H-ZSM-5 is a highly dispersed material with a crystal diameter of 1-20 microns, which complicates its direct use in reactors with a fixed catalyst bed due to the high hydraulic pressure drop of the catalytic bed. Traditionally in industry, this issue is solved by using complex reactor systems with a fluidized bed, which is justified for large-scale production. In small and medium-size plants, the use of fluidized bed systems is not economically feasible. One of the possible solutions to this problem is the use of a monolithic catalyst with a supported layer of H-ZSM-5 zeolite. This article presents a study of the catalytic activity of a zeolite-containing microstructured monolith in methanol into hydrocarbons transformation. The monolith was synthesized by pressing a zeolite-containing mass followed by drying, calcining, and secondary growth of the zeolite on the monolith surface. A sample of a monolith with an average channel diameter of 0.5, 1.0, 1.5, 2.0 mm were synthesized this way. Samples of the microstructured catalyst were tested at varying temperatures from 250 to 450 °C and at varying the specific methanol feed rate from 0.65 to 2.3 kg (MeOH)/(kg (Cat) h). For this purpose, the monolithic catalyst was placed in a reactor for testing microstructured catalysts, which consisted of a pump, a temperature controller, a catalytic reactor, a condenser, a separating funnel, and a chromatograph. Varying the conditions showed that for the preferential production of gaseous C1-C4 hydrocarbons, it is advisable to carry out the reaction under the following conditions: the average diameter of the catalyst channels is 2 mm, the reaction temperature is 350 °C, the methanol feed rate is 1.65 kg (MeOH)/(kg (Cat) h). For the predominant formation of liquid hydrocarbons of the C5-C8 fraction, it is advisable to carry out the transformation of methanol into hydrocarbons under the following conditions: the average diameter of the catalyst channels is 1 mm, the reaction temperature is 350 °C, the methanol feed rate is 0.65 kg (MeOH) / (kg (Cat) h). For the predominant formation of liquid hydrocarbons of the C9-C12 fraction, it is advisable to carry out the transformation of methanol into hydrocarbons under the following conditions: the average diameter of the catalyst channels is 0.5 mm, the reaction temperature is 350 °C, and the methanol feed rate is 0.65 kg (MeOH) / (kg (Cat) h).
Текст научной статьи Особенности каталитической трансформации метанола в углеводороды в условиях микроструктурированных потоков
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 544.47
Использование микро структурированных реакторов является одним из возможных вариантов интенсификации химико-технологических процессов [1–2]. По сравнению с обычными реакторами микроструктурированные реактора обладают рядом преимуществ, таких как улучшенный тепло- и массообмен как следствие увеличенного отношения площади поверхности к объему [3–4]. Кроме этого, возможен более точный контроль температуры реакционного потока, что позволяет эффективно регулировать образование конкретных продуктов реакции [5]. Возможность проведения гетерогенных каталитических процессов в условиях микрореакторов была успешно продемонстрированы для различных химико-технологических процессов [6–7], как в уплотненном слое, в виде тонких пленок, покрывающих стенки микрореактора, либо монолитные микрореакторы. Однако, несмотря на существенные преимущества [2], микрореакторные технологии еще не нашли широкого распространения, что может быть вызвано как теоретическими, так и практическими сложностями их использования. Каталитическая трансформация метанола в углеводороды может рассматриваться в качестве одного из возможных способов получения синтетических углеводородов, в том числе из возобновляемого сырья [8–10]. При этом, широкий спектр получаемых углеводородов, позволяет использовать их как в качестве топлива, так и в качестве сырья для производства полимеров, фармацевтических препаратов, красителей и т. п. Традиционно используемые технические решения в этой области, включают применение крупнотоннажных реакторов с псевдоожиженным слоем, характеризующихся невысокой конверсией исходного сырья, однако позволяющих осуществлять одновременную регенерацию катализатора [5–8]. Одним из возможных путей увеличения конверсии исходных реагентов является использование микроструктуриованных реакторов с монолитным катализатором, при этом регенерация катализатора может производиться последовательно при использовании нескольких реакторных сборок. Кроме этого, использование микроструктурированных монолитных катализаторов позволяет создавать установки средней и малой мощностей для производства синтетических углеводородов. В статье приводятся результаты тестирования монолитных катализаторов с активным слоем цеолита H-ZSM-5 с разным диаметром каналов.
Материал и методы исследования
Для синтеза монолитной подложки производилось влажное прессование смеси 80% оксида алюминия с 10% каолина и 10% цеолита H-ZSM-5 в щелочной среде, формы с микроканалами выдерживались под давлением в течение четырех часов, после чего монолит диаметром 10 мм, длинной 50 мм и диаметрами внутренних каналов от 0,5, 1,0, 1,5, 2,0 мм высушивался при температуре 105 °С, и кальцинировался в муфельной печи при температуре 600 °С в течение четырех часов. Затем монолит обрабатывался 5 масс. % раствором гидроксида тетрапропиламмония и помещается в гель состоящий из 30 масс.% коллоидного раствора оксида кремния, 3 масс. % оксида алюминия 15 масс% гидроксида натрия и 52 мас. % дистиллированной воды. Средняя масса получаемого монолита составляла составила 7,2 г. Монолит помещался в автоклав и догревался до 140 °С и выдерживался при этой температуре в течение 48 часов, после чего высушивался при 105 °С, и кальцинировался в муфельной печи при температуре 600 °С в течение 4 часов. После чего каталитический монолит помещался в установку представленную на Рисунке 1.
Метанол с расходом 0,1–0,3 мл/мин подавался из емкости (2) насосом (1) в реактор (4) догретый до 250–470 °С, после чего реакционная смесь направлялась в холодильник (5), после чего проходило разделение жидкой и газовых фракций в сепараторе 6. Газовая фракция направлялась в хроматограф для анализа, а жидкая фракция отбиралась в виалы с установленной периодичностью. Анализ газовых и жидких фракций проводился в соответствие с ГОСТ Р 54484-2011 и ГОСТ 32507-2013.
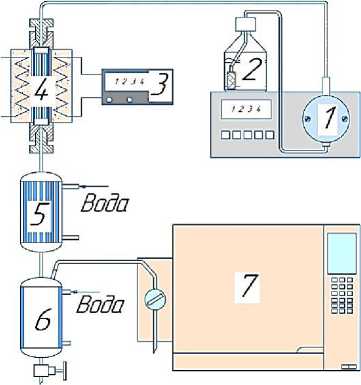
Рисунок 1. Установка для тестирования микроструктурированных катализаторов в реакции трансформации метанола в углеводороды (1 — насос, 2 — емкость для метанола, 3 — термоконтроллер 4 — каталитический реактор, 5 — конденсатор, 6 — делительная воронка, 7 — хроматограф)
Результаты и обсуждение
Изучение влияния температуры на протекание реакции трансформации метанола с образованием углеводородов для монолитного цеолитсодержащего катализатора со средним диаметром канала равным одному миллиметру представлено на Рисунке 2. Увеличение температуры от 250 °С до 350 °С способствует значительному увеличению скорости трансформации метанола с 0,14 до 0,23 кг (МеОН)/(кг (Кат)ч), при этом дальнейшее увеличение температуры до 450 °С способствует лишь небольшому увеличению скорости трансформации метанола в углеводороды до 0,24 кг (МеОН)/(кг (Кат)ч).
x-^v 1,8
го 1,6
'' 1,4
T о 1,2
Ф
"lS* 1,0
—
0,8

a)
• t=2500C
0 ° t=3000C
’ t=3500C
. л t=4000C
’ ■ t=4500C
20 30 40
Время, ч
Углеводороды
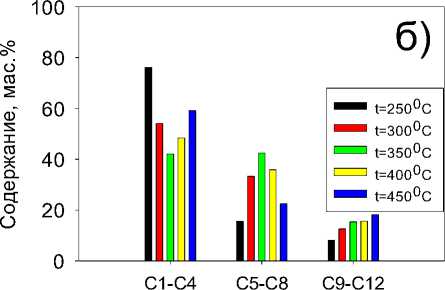
Рисунок 2. Кривые а) скорости конверсии метанола от времени, б) диаграмма состава получаемых углеводородов. (Скорость подачи метанола 0,25 мл/мин, масса монолита 7,5 г, температура реакционной среды 250–450 °С, средний диаметр каналов используемого монолита 1 мм)
Однако, при этом также наблюдается существенное изменение состава образующихся углеводородов. Так увеличение реакционной температуры от 250 °С до 350 °С способствует уменьшению долу фракции газообразных углеводородов с числом углеродных атомов С 1 -С 4 с 76 мас. % до 42 мас. %, количество жидких углеводородов фракции С 5 -С 8 увеличивается с 16 мас. % и достигает 43 мас. %, количество тяжелых углеводородов с числом углеродных атомов С 9 -С 12 увеличивается с 8 мас. % до 15,4 мас.%. Это свидетельствует о сдвиге цепочки реакций в сторону формирования тяжелых углеводородов. Дальнейшее увеличение температуры трансформации метанола в углеводороды до 450 °С приводит к увеличению количества образующихся газообразных углеводородов с числом углеродных атомов С 1 -С 4 до 59 мас. %, количество же жидких углеводородов с числом углеродных атомов С 5 -С 8 несколько уменьшается до 23 мас. %, а количество тяжелых углеводородов с числом углеродных атомов С 9 -С 12 увеличивается до 18 мас. %. Что свидетельствует о существенном вкладе вторичных процессов деструкции жидких углеводородов в газообразные углеводороды.
Исследование влияния количества подаваемого метанола на скорость его трансформации и состав углеводородной фракции представлено на рисунке 3. Увеличение начальной скорости подачи метанола с 0,65 до 1,97 кг (МеОН)/(кг (Кат)ч) способствует значительному увеличению скорости трансформации метанола с 0,63 до 1,78 кг (МеОН)/(кг (Кат)ч), при этом дальнейшее увеличение начальной скорости подачи метанола до 2,3 кг (МеОН)/(кг (Кат)ч) способствует лишь небольшому увеличению скорости трансформации метанола в углеводороды до 1,9 кг (МеОН)/(кг (Кат)ч).
.-—**. 2,0
аз
Si 1,6
1,4
1,2
1,0
0,8
0,6


a)
W =0.65 (кг(MeOH)/(кг(Кат)ч)
W =1 (кг(MeOH)/(кг(Кат)ч)
W =1.65(кг(MeOH)/(кг(Кат)ч)
W =1.97(кг(MeOH)/(кг(Кат)ч)
W =2.3(кг(MeOH)/(кг(Кат)ч)
0 10 20 30 40
Углеводороды
Время, ч
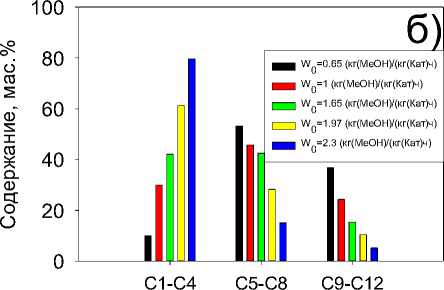
Рисунок 3. Кривые а) скорости конверсии метанола от времени, б) диаграмма состава получаемых углеводородов при варьировании начальной скорости подачи метанола. (Скорость подачи метанола 0,10–0,35 мл/мин, масса монолита 7,5 г, температура реакционной среды 350 °С, средний диаметр каналов используемого монолита 1 мм)
При этом также наблюдается существенное изменение состава образующихся углеводородов. Так увеличение начальной скорости подачи метанола с 0,65 до 1,97 кг (МеОН)/(кг (Кат)ч) способствует увеличению доли газообразных углеводородов с числом углеродных атомов С 1 -С 4 с 10 мас. % до 80 мас. %, количество жидких углеводородов фракции С 5 -С 8 уменьшилось с 53 мас. % до 15 мас. %, количество тяжелых углеводородов с числом углеродных атомов С 9 -С 12 также уменьшилось с 36 мас. % до 5 мас. %. Это свидетельствует о сдвиге цепочки реакций в сторону формирования легких углеводородов.
Бюллетень науки и практики / Bulletin of Science and Practice
Исследование влияния среднего диаметра каналов полученного монолитного цеолитсодержащего катализатора на скорость трансформации метанола и состав углеводородной фракции представлено на рисунке 4. Увеличение диаметра канала с 0,5 мм до 2,0 мм способствует уменьшению скорости трансформации метанола с 1,62 до 1,10 кг (МеОН)/(кг (Кат)ч).
1,6
1,4
1,2
1,0

a)
-
• dср=0.5 мм
о dср=1 мм
-
▼ dср=1.5 мм
-
△ dср=2 мм
10 20 30 40
Углеводороды
Время, ч
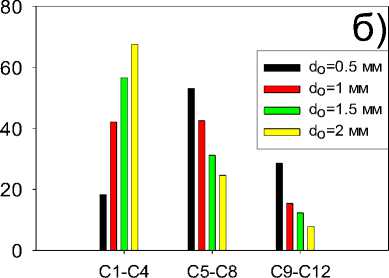
Рисунок 4. Кривые а) скорости конверсии метанола от времени, б) диаграмма состава получаемых углеводородов при варьировании среднего диаметра каналов монолита. (Скорость подачи метанола 0,25 мл/мин, масса монолита 7,5 г, температура реакционной среды 350 °С, средний диаметр каналов используемого монолита 0,5–2,0 мм)
При этом также наблюдается изменение состава образующихся углеводородов. Так увеличение начальной среднего диаметра каналов с 0,5 до 2,0 мм способствует увеличению доли газообразных углеводородов с числом углеродных атомов С 1 -С 4 с 18 мас. % до 68 мас. %, количество жидких углеводородов фракции С 5 -С 8 уменьшилось с 53 мас. % до 25 мас. %, количество тяжелых углеводородов с числом углеродных атомов С 9 -С 12 также уменьшилось с 29 мас. % до 8 мас. %. Что также свидетельствует о сдвиге цепочки реакций в сторону формирования легких углеводородов.
Заключение
Варьирование условий реакции трансформации метанола в углеводороды с использованием цеолитсодержащего монолитного катализатора показало, что для преимущественного получения газообразных углеводородов С 1 -С 4 целесообразно проводить реакцию в следующих условиях: средний диаметр каналов катализатора 2 мм, температура проведения реакции 350 °С, скорость подачи метанола 1,65 кг (МеОН)/(кг (Кат)ч). Для преимущественного образования жидких углеводородов фракции С 5 -С 8 целесообразно проведение процесса трансформации метанола в углеводороды в следующих условиях: средний диаметр каналов катализатора 1 мм, температура проведения реакции 350 °С, скорость подачи метанола 0,65 кг (МеОН)/(кг (Кат)ч). Для преимущественного образования жидких углеводородов фракции С 9 -С 12 целесообразно проведение процесса трансформации метанола в углеводороды в следующих условиях: средний диаметр каналов катализатора 0,5 мм, температура проведения реакции 350 °С, скорость подачи метанола 0,65 кг (МеОН)/(кг (Кат)ч).
Исследование выполнено в рамках проекта МД-903.2021.4 совета по грантам Президента РФ.
Список литературы Особенности каталитической трансформации метанола в углеводороды в условиях микроструктурированных потоков
- Renken A., Kiwi-Minsker L. Microstructured catalytic reactors // Advances in catalysis. 2010. V. 53. P. 47-122. https://doi.org/10.1016/S0360-0564(10)53002-5
- Hartman R. L., McMullen J. P., Jensen K. F. Deciding whether to go with the flow: evaluating the merits of flow reactors for synthesis // Angewandte Chemie International Edition. 2011. V. 50. №33. P. 7502-7519. https://doi.org/10.1002/anie.201004637
- Kockmann N. Modular equipment for chemical process development and small-scale production in multipurpose plants // ChemBioEng Reviews. 2016. V. 3. №1. P. 5-15. https://doi.org/10.1002/cben.201500025
- Wörz O., Jäckel K. P., Richter T., Wolf A. Microreactors-a new efficient tool for reactor development // Chemical engineering & technology. 2001. V. 24. №2. P. 138-142. https://doi.org/10.1002/1521-4125(200102)24:23.0.CO;2-C
- Laue S., Haverkamp V., Mleczko L. Experience with scale-up of low-temperature organometallic reactions in continuous flow // Organic Process Research & Development. 2016. V. 20. №2. P. 480-486. https://doi.org/10.1021/acs.oprd.5b00183
- Frost C. G., Mutton L. Heterogeneous catalytic synthesis using microreactor technology // Green Chemistry. 2010. V. 12. №10. P. 1687-1703. https://doi.org/10.1039/C0GC00133C
- Munirathinam R., Huskens J., Verboom W. Supported catalysis in continuous-flow microreactors // Advanced synthesis & catalysis. 2015. V. 357. №6. P. 1093-1123. https://doi.org/10.1002/adsc.201401081
- Ji Y., Birmingham J., Deimund M. A., Brand S. K., Davis M. E. Steam-dealuminated, OSDA-free RHO and KFI-type zeolites as catalysts for the methanol-to-olefins reaction // Microporous and Mesoporous Materials. 2016. V. 232. P. 126-137. https://doi.org/10.1016/j.micromeso.2016.06.012
- Froment G. F., Dehertog W. J. H., Marchi A. J. Zeolite catalysis in the conversion of methanol into olefins. 2020. https://doi.org/10.1039/9781847553218-00001
- Schipper P. H., Krambeck F. J. A reactor design simulation with reversible and irreversible catalyst deactivation // Chemical engineering science. 1986. V. 41. №4. P. 1013-1019. https://doi.org/10.1016/0009-2509(86)87187-1


