Особенности кровообращения в своде вертлужной впадины при дисплазии тазобедренного сустава собак (экспериментальное исследование)
Автор: Бунов Вячеслав Сергеевич, Кононович Наталья Андреевна
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 1, 2014 года.
Бесплатный доступ
Цель. Изучение кровообращения вертлужной впадины и параоссальных тканей в области тазобедренного сустава у растущих собак. Материалы и методы. С помощью реографии у щенков в возрасте от 6 до 11 месяцев произведены исследования гемодинамики в костной части свода вертлужной впадины и параоссальных мягких тканях. Результаты. При отсутствии различий в величине притока крови выявлено снижение амплитудных параметров пульсового кровотока в участках исследований и уменьшение объёмной скорости кровотока в костной части свода вертлужной впадины. Заключение. На основании полученных данных установлено, что дисплазия вертлужной впадины сопровождается врождённой аномалией сосудистого русла.
Вертлужная впадина, дисплазия, кровообращение, гемодинамика, реография, пульсовой кровоток, объемная скорость кровотока, аномалия сосудистого русла
Короткий адрес: https://sciup.org/142121726
IDR: 142121726 | УДК: 612.13:616.718.16:
Circulation features in the acetabular vault area for dysplasia of the canine hip (an experimental study)
Purpose. To study the circulation of acetabulum and paraosseous tissues in the hip area of growing dogs. Materials and Methods. Hemodynamics investigated in the bone part of acetabular vault, as well as in paraosseous soft tissues of puppies at the age of 6-11 months using rheography. Results. The reduction of the amplitude parameters of pulse blood flow observed in the parts investigated, as well as the decrease of volumetric circulation rate in acetabular bone part in case of the absence of the differences in the value of blood inflow. Conclusion. Based on the findings acetabular dysplasia established to be accompanied by congenital anomaly of the vascular bed.
Текст научной статьи Особенности кровообращения в своде вертлужной впадины при дисплазии тазобедренного сустава собак (экспериментальное исследование)
Известно, что наследуется предрасположенность к дисплазии суставов, а её проявления нарастают в онтогенезе [1]. У щенков дисплазия тазобедренного сустава начинает проявляться замедлением развития ядер окостенения, в частности, свода вертлужной впадины [2]. Так как остеогенез нуждается в своевременном обеспе- чении энергетическими и пластическими материалами [3], появилось предположение, что причиной его недостаточной активности служат нарушения кровообращения, и для выявления особенностей гемодинамики в своде вертлужной впадины при дисплазии тазобедренного сустава были проведены исследования на собаках.
МАТЕРИАЛ И МЕТОДЫ
Исследования проведены на щенках в возрасте от 6 до 11 месяцев с учетом требований Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей [4]. Инвазии осуществляли стерильными инструментами в условиях операционной во время наркотического сна животных. После пробуждения функция тазобедренных суставов была сохранена.
Контрольную группу составили исследования 48 вертлужных впадин 24 щенков беспородных собак, не имеющих патологии. Опытную группу – 4 вертлужных впадины 2 щенков – метисов овчарки, у которых двусторонняя дисплазия тазобедренных суставов к 10 месяцам достигла степени D [5].
Наркотизированное животное фиксировали на животе, с области таза удаляли волосяной покров. Снаружи в переднюю и заднюю часть свода вертлужной впадины на глубину 3 мм вводили иглы для переливания крови диаметром 2,0 мм. Расстояние между иглами составляло 5 см (рис. 1). Отступив кнутри 0,5 см от введенных в кость игл в мягкие ткани до кости (под надкостницу) вводили иглы для внутримышечных инъекций. Все иглы заполняли физиологическим раствором.
Рис. 1. Очаговые повреждения свода вертлужной впадины после введения электродов
Исследования гемодинамики проводили с помощью биполярной реографии: регистрировали изменения зондирующего электрического тока, возникающие вследствие пульсовых колебаний кровенаполнения в межэлектродном пространстве. Для получения рео-грамм использовали полианализатор-РГПА-6/12 «РЕ-АН-ПОЛИ» (МЕДИКОМ-МТД, Россия, г. Таганрог), использовали частоту зондирующего тока 47 кГц, калибровочный сигнал 0,1 Ом амплитудой Ак = 1 см. Одновременно регистрировали ЭКГ, реограммы кости и мягких тканей и их первые производные. Полианализатор обеспечивал регистрацию и вычисления параметров, из которых выбирали следующие [6]:
-
1) RR, с – продолжительность пульсовой волны на ЭКГ;
-
2) БИ, Ом – импеданс, электрический эквивалент кровенаполнения межэлектрод-ного пространства;
-
3) ВРПВ, м/сек. – время распространения пульсовой волны от зубца Q ЭКГ до начала пульсовой волны в межэлектродном пространстве. Характеризует плотность стенок артерий, обеспечивающих приток крови к зоне исследования;
-
4) ВМСК, м/сек. – время максимального систолического кровенаполнения (продолжительность анакро-ты). Меняется при затруднениях и улучшении кровотока в межэлектродном пространстве;
-
5) ВБКН, м/сек. – время быстрого кровенаполнения, характеризует эластичность крупных артерий межэлектродного пространства;
-
6) ЧСС – частота сердечных сокращений, ед./мин.: ЧСС=60/RR, где 60 – количество секунд в минуте;
-
7) ПМУ – показатель модуля упругости стенок артерий межэлектродного пространства (%): ПМУ=(ВМСН/RR)×100;
-
8) ПЭС – показатель эластичности стенок артерий среднего калибра межэлектрод-ного пространства (%): ПЭС=(ВМКН/ВБКН)×100 %, где ВМКН, м/сек. – время медленного кровенаполнения (RR-ВБКН);
-
9) ДКИ, % – дикротический индекс, показатель тонуса артерий мелкого калибра: ДКИ=(Аi/Ри)×100 %, где Аi – амплитуда инцизуры, Ом;
-
10) ППСС, % – показатель тонуса резистивных сосудов, периферического сосудистого сопротивления: ППСС=(АСФВК/Ри)×100 %, где АСФВК – амплитуда систолической фазы венозной компоненты;
-
11) ДСИ-10 %, % – диастолический индекс, показатель венозного оттока: ДСИ-10 % = (Аd/ Ри)×100 %, где Аd – амплитуда диастолической волны, Ом;
-
12) АБКН, Ом – амплитуда быстрого кровенаполнения: АБКН=(ААК×к)/Ак, где ААК – эквивалент пульсового кровенаполнения при окончании периода быстрого кровенаполнения, мм; к – калибровка, Ом; Ак – амплитуда калибровки, мм;
-
13) РИ, Ом – реографический индекс, эквивалент пульсового кровенаполнения межэлектродного пространства в момент равенства притока и оттока крови: РИ=(АРГ×к)/Ак, где АРГ – максимальная амплитуда реограмм, мм;
-
14) Vq100, мл/мин/100 см3 ткани – расчётный эквивалент объёмной скорости кровотока в 100 см3 ткани межэлектродного пространства за одну минуту: Vq100=6000×tg а×Тизг.×К/RR×БИ×Ак, где 6000 – коэффициент; tg a (угол наклона анакроты) = АБКН/ВБКН, мм/с: Тизг, сек. (период изгнания) = 0,109×(RR+0,159); К – калибровка в Ом; Ак – амплитуда калибровки в мм;
-
15) ВКЖ, мл – эквивалент количества внеклеточной жидкости в межэлектродном пространстве: ВКЖ=(L2×0,095/БИ)×1000, где L, см – расстояние между электродами.
Из полученных данных составляли невзвешенные вариационные ряды. Анализ проводили с помощью программ Excel 7,0 и «Аттестат» [7]. Определяли средние и их ошибку. Для оценки различий между средними использовали парный критерий t-Стьюдента. Сравнивали параметры гемодинамики у животных с дисплазией и без дисплазии вертлужной впадины.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
У щенков без дисплазии тазобедренного сустава рео-граммы костной части свода вертлужной впадины (РВГк) и мягких тканей (РВГм) имели обычную конфигурацию (рис. 2, а, б). При дисплазии тазобедренного сустава ре-ограммы костной части вертлужной впадины и мягких тканей отличались низкой амплитудой (рис. 2, в, г).
На основании ВРПВ плотность стенок артерий, обеспечивающих приток крови к своду вертлужной впадины, у щенков с дисплазией тазобедренного сустава и без неё достоверных различий не имела (табл. 1). В своде вертлужной впадины продолжительность пульсовой волны (RR), продолжительность анакроты (ВМСН), а также упругость стенок артерий (ПМУ) достоверных различий не имели.
При дисплазии тазобедренного сустава в своде вертлужной впадины эла-стичность стенок артерий среднего калибра (ПЭС), тонус стенок артерий мелкого калибра (ДКИ) и резестивных сосудов (ППСС) были ниже, чем у щенков без патологии. Время быстрого (ВБКН) и максимального пульсового кровенаполнения (ВМКН) достоверно не отличались от таковых у животных без патологии, а амплитуда быстрого (АБКН) и максимального пульсового кровенаполнения (Ри) была меньше и составляла 21 и 37 % соответственно. Объёмная скорость кровотока составляла 55 %, показатель венозного оттока (ДСИ – 10 %) был в 5 раз меньше, а кровенаполнение и содержание внеклеточной жидкости были на 38 и 66 % больше соответственно.
На основании ВРПВ плотность стенок артерий, обеспечивающих приток крови к мягким тканям над костной частью свода вертлужной впадины, у щенков с дисплазией тазобедренного сустава и без неё достоверных различий не имела (табл. 2). В мягких тканях продолжительность пульсовой волны (RR), анакроты (ВМСН), упругость стенок артерий (ПМУ), эластичность стенок артерий среднего калибра (ПЭС), тонус стенок артерий мелкого калибра (ДКИ) и резестивных сосудов (ППСС) достоверно не отличались как у щенков при наличии, так и при отсутствии патологии.
При дисплазии тазобедренного сустава время быстрого (ВБКН) и максимального пульсового кровенаполнения (ВМКН) достоверно не отличались от таковых у щенков без патологии, а амплитуда быстрого (АБКН) и максимального пульсового кровенаполнения (Ри) были меньше, составляли 45 % и 42 % соответственно. Объёмная скорость кровотока и показатель венозного оттока (ДСИ-10%) у щенков с дисплазией тазобедренного сустава и без неё достоверных различий не имели. Кровенаполнение и содержание внеклеточной жидкости при дисплазии тазобедренного сустава были больше на 37 % и 48 % соответственно.
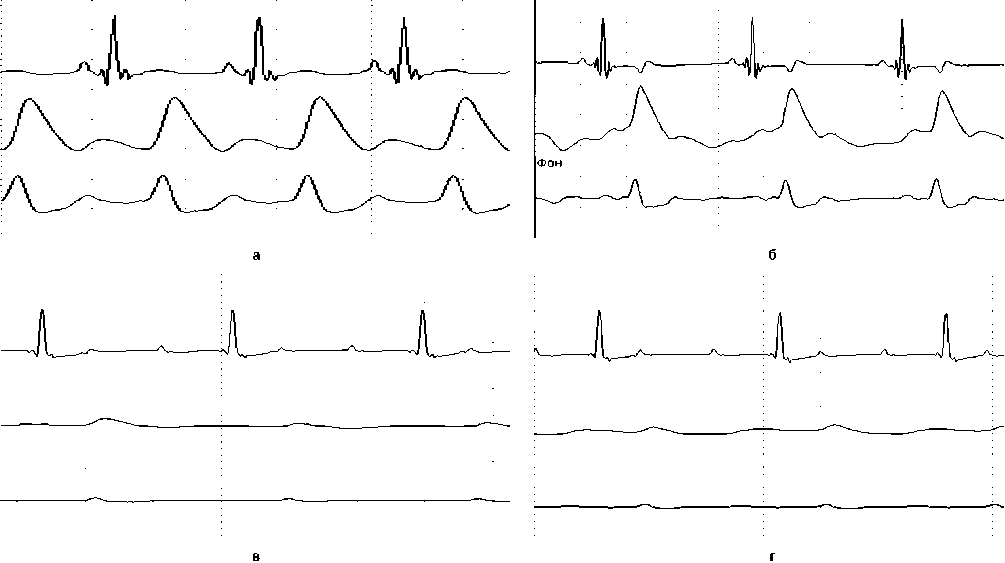
Рис. 2. Реограммы костной части свода вертлужной впадины (а) и мягких тканей над ней (б) при отсутствии патологии. Снижение амплитуды пульсовой волны в костной части свода вертлужной впадины (в) и мягких тканях (г) при дисплазии тазобедренного сустава
Таблица 1
|
№ |
Параметры |
Контроль |
Опыт |
% |
p< |
|
1 |
ВRПВ, сек. |
0,137±0,003 |
0,159±0,013 |
116 |
– |
|
2 |
ПМУ, % |
13,60±0,600 |
11,50±1,400 |
84 |
– |
|
3 |
ПЭС, % |
90,38±2,670 |
85,50±2,400 |
95 |
– |
|
4 |
ДКИ, % |
-10,33±3,640 |
-39,75±8,760 |
385 |
0,01 |
|
5 |
ППСС, % |
16,27±6,430 |
-11,75±7,990 |
-172 |
0,01 |
|
6 |
ДСИ-10 %,% |
5,940±3,300 |
-27,00±5,840 |
554 |
0,001 |
|
7 |
RR, сек. |
0,714±0,028 |
0,796±0,085 |
111 |
– |
|
8 |
ЧСС, ед. |
90,80±3,800 |
78,20±8,900 |
86 |
– |
|
9 |
БИ, Ом |
92,40±3,000 |
57,40±6,400 |
62 |
0,001 |
|
10 |
ВКЖ, мл |
25,80±1,200 |
42,80±4,600 |
166 |
0,001 |
|
11 |
АБКН, Ом |
0,012±0,003 |
0,003±0,001 |
21 |
0,01 |
|
12 |
ВБКН, сек. |
0,051±0,001 |
0,048±0,002 |
94 |
– |
|
13 |
РИ, ед. |
0,019±0,002 |
0,007±0,001 |
37 |
0,05 |
|
14 |
ВМСН, сек. |
0,090±0,002 |
0,088±0,002 |
98 |
– |
|
15 |
Vq100, см3/в 100 см3 |
0,455±0,088 |
0,249±0,032 |
55 |
0,05 |
Параметры гемодинамики в костной части свода вертлужной впадины
Таблица 2
Параметры гемодинамики в мягких тканях над сводом вертлужной впадины
|
№ |
Параметры |
Контроль |
Опыт |
% |
p< |
|
1 |
ВRПВ-R, сек. |
0,137±0,003 |
0,152±0,009 |
111 |
– |
|
2 |
ПМУ, % |
12,50±0,700 |
12,80±2,000 |
102 |
– |
|
3 |
ПЭС, % |
80,65±3,270 |
82,25±4,620 |
– |
|
|
4 |
ДКИ, % |
-30,34±5,170 |
-69,00±25,04 |
– |
|
|
5 |
ППСС, % |
-4,720±5,000 |
-21,75±20,88 |
– |
|
|
6 |
ДСИ-10 %, % |
-7,220±4,570 |
-26,50±11,54 |
– |
|
|
7 |
БИ, Ом |
121,2±5,200 |
76,10±2,500 |
63 |
0,001 |
|
8 |
ВКЖ, мл |
21,10±0,800 |
31,30±1,000 |
148 |
0,001 |
|
9 |
АБКН, Ом |
0,011±0,002 |
0,005±0,001 |
45 |
0,05 |
|
10 |
ВБКН, сек. |
0,050±0,001 |
0,055±0,004 |
110 |
– |
|
11 |
РИ, ед. |
0,024±0,003 |
0,010±0,002 |
42 |
0,001 |
|
12 |
ВМСН, сек. |
0,085±0,003 |
0,098±0,008 |
115 |
– |
|
13 |
Vq100, см3/в 100 см3 |
0,288±0,026 |
0,249±0,039 |
86 |
– |
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
У щенков с дисплазией тазобедренного сустава плотность стенок артерий, обеспечивающих приток крови к костной части свода вертлужной впадины и мягким тканям над ним, а также упругость стенок крупных артерий межэлектродного пространства достоверно не отличались от таковых у щенков, не имеющих патологии. Продолжительность и временные параметры пульсовой волны достоверных отличий тоже не имели. Следовательно, пульсовой приток крови по магистральным артериям к костной части свода вертлужной впадины и мягким тканям над ним у животных с дисплазией тазобедренного сустава достоверно не отличался от такового у животных без патологии.
У щенков с дисплазией тазобедренного сустава в костной части свода вертлужной впадины эластичность и тонус стенок артерий среднего и мелкого калибра, а также резестивных сосудов были ниже, чем у щенков без патологии. Известно, что резестивные сосуды определяют количество функционирующих капилляров и давление крови в артериальном отделе капилляра, от чего зависят фильтрация жидкости из крови в интерстициальные пространства и поперечное сечение (кровенаполнение) капилляров [6]. Следовательно, причиной увеличения кровенаполнения и содержания внеклеточной жидкости в костной части свода вертлужной впадины у щенков с дисплазией вертлужной впадины был низкий тонус стенок артерий среднего и мелкого калибра, а также резестивных сосудов.
В условиях недостоверных различий между притоком крови по магистральным артериям относительно низкий тонус стенок артерий среднего и мелкого калибра, а также резестивных сосудов, у щенков с дисплазией тазобедренного сустава должен создать условия для местного (регионального) усиления кровообращения. Однако в костной части свода вертлужной впадины регистрировали относительно низкие амплитудные характеристики пульсовой волны и уменьшение объёмной скорости кровотока. Недостаточность артериального притока подтверждало регистрируемое уменьшение венозного оттока. Из этого следует, что микроциркулятор-ное русло костной части свода вертлужной впадины не получало приток крови от магистральной артерии под достаточным артериальным давлением крови: микро-циркуляторное русло костной части свода вертлужной впадины не было связано с магистральной артерией сосудом, имеющим достаточно большое поперечное сечение. Вероятно, причиной недостаточности кровообращения в костной части свода вертлужной впадины была врождённая аномалия сосудистого русла – отсутствие ветви магистральной артерии с относительно большим поперечным сечением, обеспечивающей приток крови к микроциркуляторному руслу свода вертлужной впадины под достаточно высоким давлением.
В параоссальных мягких тканях над костной частью свода вертлужной впадины также выявлено уменьшение амплитудных параметров пульсовой волны, увеличение кровенаполнения и содержания внеклеточной жидкости. Вероятно, причиной недостаточности артериального притока было врождённое отсутствие той же ветви магистральной артерии.
ЗАКЛЮЧЕНИЕ
У щенков с дисплазией тазобедренного сустава и без неё приток крови по магистральным артериям к своду вертлужной впадины и мягким тканям над ним достоверных различий не имеет. В костной части свода вертлужной впадины выявлено снижение амплитудных параметров пульсовой волны и уменьшение объёмной скорости кровотока, в мягких тканях над сводом вертлужной впадины – снижение амплитудных пара- метров пульсовой волны. Вероятно, причиной уменьшения амплитудных параметров пульсовой волны у щенков с дисплазией тазобедренного сустава служила врождённая аномалия сосудистого русла: отсутствие ветви магистральной артерии с относительно большим поперечным сечением, обеспечивающей под относительно высоким давлением приток крови к костной части вертлужной впадины и мягким тканям над ней.


