Особенности лечения и профилактики послеоперационного пареза кишки и кишечной непроходимости при проведении робот-ассистированной простатэктомии
Автор: Кряжева К.А., Иванов М.В., Ковачич А.С., Васильев А.О., Ширяев А.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Общие вопросы
Статья в выпуске: 1 (71), 2020 года.
Бесплатный доступ
Кишечная непроходимость (илеус) - одно из наиболее грозных патологических состояний, встречающихся как в абдоминальной хирургии, так и в других областях медицины при ряде заболеваний. Внедрение методики робот-ассистированной радикальной простатэктомии (РАРПЭ) позволяет существенно снизить риск развития осложнений, но не исключить полностью. С учетом возникновения данного осложнения и его непосредственного влияния на состояние пациента, следует заострить внимание на профилактических и лечебных мероприятиях, способствующих снижению и более скорому разрешению послеоперационного пареза. Для этого необходимо учитывать патогенетические факторы, способствующие возникновению илеуса, и с учетом их выстраивать план лечения и профилактических мероприятий.
Послеоперационные осложнения, лапароскопические и робот-ассистированные методы лечения, кишечная непроходимость, профилактика
Короткий адрес: https://sciup.org/142224470
IDR: 142224470 | УДК: 616-06, | DOI: 10.17238/issn2072-3180.2020.1.33-42
Features of treatment and prevention of postoperative intestinal paresis and intestinal obstruction during robot-assisted prostatectomy
Intestinal obstruction (ileus) is one of the most formidable pathological conditions encountered both in abdominal surgery and in other areas of medicine in a number of diseases. The introduction of the technique of robot-assisted radical prostatectomy (RARP) can signifi antly reduce the risk of complications, but not completely exclude it. Given the occurrence of this complication and its direct effect on the patient’s condition, attention should be paid to preventive and therapeutic measures that contribute to the reduction and faster resolution of postoperative paresis. For this, it is necessary to take into account pathogenetic factors that contribute to the appearance of ileus and, taking them into account, build a treatment plan and preventive measures.
Текст научной статьи Особенности лечения и профилактики послеоперационного пареза кишки и кишечной непроходимости при проведении робот-ассистированной простатэктомии
Рак предстательной железы (РПЖ) - злокачественное новообразование предстательной железы. Это самый распространенный вид рака, входящий в «первую тройку» по онкологической смертности у мужчин [1]. Мировыми лидерами по показателям заболеваемости РПЖ являются США (200 000 новых случаев ежегодно), Канада и некоторые страны Европы. В России также отмечается неуклонный рост заболеваемости РПЖ. Каждый год обнаруживается более 35 000 новых случаев рака простаты, что составляет около 9% от всех злокачественных образований, выявленных у мужчин в течение года. Согласно имеющимся данным, прирост заболеваемости с 2008 по 2018 гг. составил более 95%, а за последние 10 лет количество больных с впервые выявленным диагнозом рака простаты на 100 000 населения возросло на 300% [2] .
Наиболее оптимальным методом радикального лечения на сегодняшний день является радикальная простатэктомия. Эта операция подразумевает полное удаление предстательной железы, с проходящей через нее частью мочеиспускательного канала.
Внедрение методики робот-ассистированной радикальной простатэктомии (РАРП) позволило существенно снизить риск числа послеоперационных осложнений. Тем не менее, как и после любого хирургического вмешательства, по-прежнему существует ряд функциональных изменений, значительно снижающих качество жизни пациента и влияющих как на время восстановления в послеоперационном периоде, так и на исход основного заболевания. Одним из таких редких, но грозных осложнений является послеоперационной парез желудочно-кишечного тракта (ЖКТ) и кишечная непроходимость, требующие особого внимания.
С учетом возникновения данного осложнения и его непосредственного влияния на состояние пациента, следует заострить внимание на осуществлении профилактических и лечебных мероприятиях, способствующих снижению и более скорому разрешению послеоперационного пареза. Для того чтобы построить грамотную концепцию лечебно-профилактических мер следует подробно рассмотреть особенности проведения робот-ассистированной радикальной простатэктомии, анестезиологического обеспечения данной операции и особенности патофизиологических процессов, возникающих как следствие конкретного хирургического вмешательства.
С учетом современных тенденций хирургическая помощь должна отвечать определенным стандартам. Которые заключаются не только в высококвалифицированном лечении конкретного заболевания, но и в обеспечении высокого качества жизни пациента, характеризующейся минимизацией осложнений в послеоперационном периоде. Объективно, это значительно сокращает время пребывания пациентов в стационаре, тем самым, снижая вероятность возникновения внутрибольничных инфекций, декомпенсации имеющихся хронических заболеваний и, как следствие, сокращение числа летальных исходов. С учетом выше сказанного, можно судить о высокой степени актуальности поиска решения проблемы послеоперационного пареза и кишечной непроходимости.
Патофизиология
Основным звеном, влияющим на возникновение послеоперационного пареза ЖКТ (илеус), считается повышенная активность симпатической нервной системы, в ответ на травматизацию брюшины и тканей. За счет этого происходит усиленный выброс катехоламинов в кровеносное русло, действие которых ассоциировано с ингибированной моторикой ЖКТ. Появление спазма и снижение моторики будет возникать вследствие возбуждающего действия катехоламинов на клетки гладкой мускулатуры и констриктирующего действия на сосуды ЖКТ [3-5]. В связи с повышенной концентрацией ацетилхолина, в клетке происходит изменение ионного баланса, усиливается поток ионов натрия внутрь клетки, вызывая деполяризацию и потенциал действия в клеточной мембране. Ионы кальция в избытке поступают внутрь мышечной клетки, вызывая сокращение миофибрилл [6, 7]. Активация калликреин-кинино-вой системы с гиперсекрецией гистамина, протеолитических ферментов и брадикинина также способствует возникновению послеоперационного пареза. Данные биологически активные вещества вызывают спазм гладкой мускулатуры, расширение просвета капилляров с увеличением их проницаемости и формированием отека прилежащих тканей. В свою очередь происходит возбуждение мозгового вещества надпочечников с выделением адреналина (катехоламин) [8]. Снижение активности серотонина и мотилина, оказывает угнетающее действие на моторику ЖКТ, поскольку в норме эти гормоны участвуют в формировании мигрирующего миоэлектрического комплекса и регуляции периферического кровообращения. Мотилин содержится в эндокринных клетках тонкой кишки. В области кишечных крипт эпителий включает в себя энтерохромаффинные клетки, содержащие серотонин. Определенное количество серотонина также находится в нейронах тонкой кишки и обеспечивает нейрональную связь между мышечными клетками. В основе нарушения перистальтики ЖКТ лежит снижение взаимодействия серотонина с серотонинэргическими рецепторами гладкой мускулатуры с последующим ухудшением микроциркуляции и, как следствие, формированием гипоксии. С учетом патологического состояния организма происходит увеличение содержания лигандов, которые имеют сродство с серотониновыми рецепторами и делятся на агонисты и антагонисты. Происходит конкурентное взаимодействие лигандов и серотонина с рецепторным аппаратом тонкой кишки. Лиганды оказывают паралитическое и спастическое действие на гладкую мускулатуру кишки, возникают различные метаболические и электролитные нарушения [9-12]. Нарушение регуляции выделения холицистокинина из проксимального отдела тонкой кишки, секретина из S-клеток двенадцатиперстной кишки и глюкагоноподоброго пептида, выделяющегося из клеток слизистой оболочки толстой и подвздошной кишок, подавляет двигательную активность всех отделов ЖКТ. Это происходит за счёт смещения баланса и изменения количества данных гормонов, поскольку их активность осуществляется за счёт взаимодействия друг с другом [13].
При оперативном вмешательстве происходит мощный выброс эндогенных опиоидов в ответ на повреждение брюшины, и поступление их извне при проведении анальгезии. Механизм действия опиоидов основан на угнетении чувствительности ноцицептивных центров в таламусе, которые проводят болевою импульсацию к коре полушарий. Происходит связывание μ-агонистов и δ-агонистов с опиоидными рецепторами, активация клеток-мишений и формирование ответной реакции. Опиоиды подавляют моторику ЖКТ и препятствуют ее восстановлению, воздействуя на гладкую мускулатуру через энтеральную нервную систему. Они снижают интенсивность пропульсивной волны в толстой кишке, одновременно увеличивая амплитуду сокращений и мышечный тонус в вышележащих отделах. Происходит формирование жесткого стула, за счет задержки транзита стула по толстой кишке и повышенного всасывания воды из просвета кишки [14-19]. При связывании опиоидов с μ-рецепторами так же может отмечаться угнетение дыхания и увеличение активности блуждающего нерва, в то время как взаимодействие с дельта-рецепторами обеспечивает анальгезию. Стоит отметить, что по статистике в лечебных учреждениях чаще применяют дженерики опиоидов. Данные лекарственные средства содержат активное химическое вещество, идентичное запатентованному препарату. Но количество и состав примесей, а также степень активности содержащихся ингредиентов могут отличаться от оригинального продукта и повлечь за собой осложнения после их применения. По-видимому, именно этот факт играет ключевую роль в ухудшении состояния пациентов в послеоперационном периоде, в усугублении и увеличении количества осложнений. Хирургические манипуляции сопровождаются травматизацией тканей и в особенности брюшины, это способствует формированию воспалительной реакции с высвобождением интерлейкинов 1 и 6, цитокинов, простоглан-динов, оксида азота. Непосредственно оксид азота взаимодействует с белками и фосфолипидами митохондрий мышечной клетки, вызывая их окисление и нитрозилирование, тем самым, угнетая функцию самой клетки [20-22]. Роль вазоактивного интестинального пептида, субстанции Р и кальцитонин ген-связанного пептида в формировании послеоперационного пареза ЖКТ доказана экспериментально. При применении антагонистов рецепторов аффинных к данным медиаторам, усиливается кишечная перистальтика [23, 24].
Одной из самых частых причин возникновения послеоперационной кишечной непроходимости, следует отнести возможность нанесения интраоперационной травмы кишки. Вследствие повреждения осуществляется ответная реакция со стороны симпатической нервной системы, которая характеризуется гормональной и медиаторной активацией в ответ на раздражение рецепторов ЖКТ [5, 25].
Отягощенный соматический статус пациента, подразумевающий, например, такое заболевание как сахарный диабет, может способствовать возникновению пареза и кишечной непроходимости через сформированную сосудистую патологию. Как упоминалось ранее, в ходе хирургического вмешательства происходит нарушение адекватного кровоснабжения и микроциркуляции всех отделов ЖКТ с развитием циркуляторной гипоксии, метаболических нарушений в клетках и, как следствие, неспособности их к сократительной функции. Макроангиопатия при сахарном диабете, характеризующаяся прогрессирующим поражением артериол, венул и капилляров, сужением просвета и нарушением сократительной функции сосудов, усугубляет и препятствует компенсации сформировавшихся гипоксических нарушений в пищеварительном тракте [26, 27].
При проведении робот-ассистированной простатэктомии осуществляют создание оперативного пространства, путем наложения карбоксиперитонеума и придание пациенту литотомической позиции в положения Тределенбурга с углом наклона не менее 35° (Рис. 1).
В связи с особенностями выполнения данных манипуляций, их потенцирующие действие, заключается в: снижении скорости кровотока в церебральных сосудах [28]; нарушении оттока крови из вен головы с повышением внутричерепного давления; снижении венозного возврата к нижним конечностям из-за распределения крови во внутренних органах с учетом наклона тела пациента; в возрастании периферического сосудистого сопротивления; увеличении внутригрудного давления, вследствие смещения органов брюшной полости в краниальную сторону. Все эти изменения способствуют формированию гемодинамических и гипоксических нарушений, которые в свою очередь являются причиной расстройства нормальной моторики, кровоснабжения и иннервации пищеварительной трубки с возникновением послеоперационного пареза (Рис. 2,3).
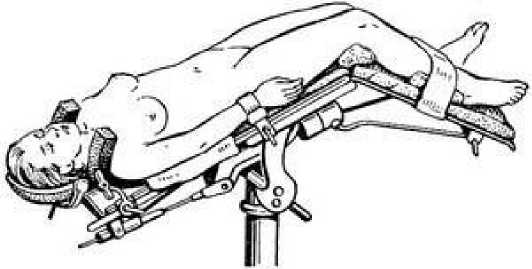
Рис. 1 Положение Тренделенбурга с углом наклона не менее 35°
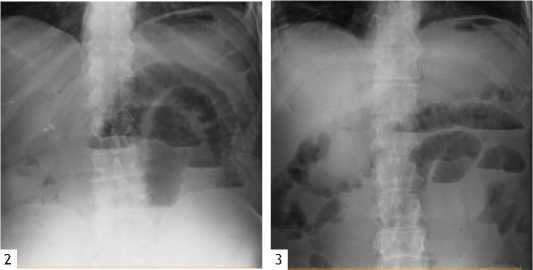
Рис.2, 3 Обзорная рентгенограмма брюшной полости через 20 часов после операции
Меры профилактики и лечение илеуса
Послеоперационный парез ЖКТ - это многофакторная патология, которая требует мультимодального подхода к лечению, проведения профилактических мероприятий в предоперационном периоде и в ходе самого хирургического вмешательства (Рис. 4,5). Основным патогенетическим фактором возникновения пареза является применение системных опиатов [29]. Поэтому стоит рассмотреть методы для снижения их дозировки при проведении аналгезии перед оперативным вмешательством, и в послеоперационном периоде для обезболивания.
Проведение эпидуральной анестезии используется как дополнение к наркозу для местного введения анестетиков. В сравнении с системными опиоидами, эпидуральная анестезия показывает более положительные результаты в отношении времени разрешения илеуса [19, 30, 31]. Постановка эпидурального катетера именно на уровне грудного отдела Th 10-11, способна обеспечить достаточное снижение негативной импульсации от оперативной зоны и активности тормозных спинальных рефлексов спинного мозга, тем самым уменьшить риск возникновения тяжелого пареза и его продолжительность [12, 32]. Преимущество использования эпидуральной анестезии заключается в возможности снизить потребность в опиоидных анальгетиках в послеоперационном периоде.
Нестероидные противовоспалительные средства (НПВС) и анилиды (парацетамол) снижают продолжительность илеуса за счет своего противовоспалительного и обезболивающего действий. Обезболивание, по всей видимости, является одним из важнейших эффектов от применения НПВС, так как позволяет снизить потребность в использовании опиатов и соответственно, уменьшить риск возникновения побочных действий [12, 33]. На сегодняшний день предпочтение отдают селективным ингибиторам ЦОГ-2, которые, в отличие от остальных НПВС, в меньшей степени способствует развитию кровотечений из ЖКТ. Антиноцицептивная система представлена пятью типами опиоидных рецепторов: m (mu), k (kappa), s (sigma), d (delta), e (epsilon). Каждый в свою очередь подразделяется на подтипы, имеющие различную органо- и ткане- специфичную локализацию. К наиболее изученным, с точки зрения физиологических эффектов активации, относят m (mu), k (kappa), d (delta) опиоидные рецепторы. Антагонисты опиоидных рецепторов применяются для купирования побочных действий эндогенных и экзогенных опиоидов, в том числе таких, как кишечный парез. Действие их заключается в блокаде соответствующих рецепторов, и в зависимости от того, с каким типом рецепторов соединяется антагонист, возникает торможение определенных реакций органов и тканей мишеней в ответ. Для лечения опиоидной дисфункции кишечника целесообразно применение антагонистов именно мю-опиоидных рецепторов, таких как налаксон и его аналоги [34].
Алвимопан селективный антагонист мю-рецепторов, был разработан для лечения послеоперационной непроходимости и илеуса [35]. Этот препарат является достаточно безопасным, с терапевтической точки зрения, так как почти не всасывается в ЖКТ. Способствует подавлению рвоты и улучшает моторику кишечника без подавления обезболивающего эффекта опиатов [36, 37]. Из энтеральных клеток выделяются нейропептиды, называемые энкефалинами. Было обнаружено, что применение данных веществ оказывает влияние на моторику желудочнокишечного тракта [37].
Нарушение моторики ЖКТ в послеоперационном периоде будет возникать в любом случае, в той или иной степени. Поэтому, использование препаратов, способствующих улучшению работы пищеварительного тракта, является важной частью мультимодального подхода в лечении и профилактики илеуса. Неостигмин является антихолинэстеразным средством. Механизм его действия заключается в обратимом ингибировании ацетилхолинэстеразы, накоплением повышенного количества ацетилхолина в синаптической щели и, как следствие, ускорение прохождения нервного импульса с активацией парасимпатической нервной системы. Происходит увеличение сократительной способности тонкой и толстой кишок со снижением пареза [38].
Метоклопрамид относится к фармакологической группе противорвотных средств, обладает противорвотным, противо-икотным и прокинетическим действиями. Препарат является антагонистом дофаминовых и серотониновых рецепторов. Стимулирует и нормализует моторную активность верхних отделов
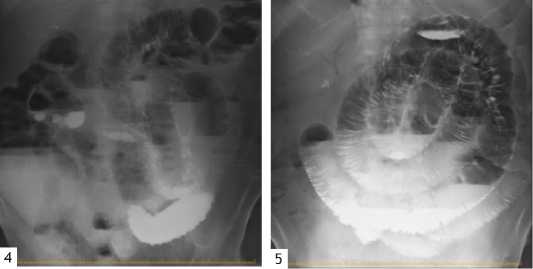
Рис. 4,5 Пассаж бариевой взвеси по тонкому кишечнику. Через 72 часа после операции
ЖКТ, уменьшает спазм сфинктеров и способствует лучшему отделению желчи из желчного пузыря [39]. Домперидон - про-кинетик, блокатор дофаминовых рецепторов и хеморецепторов рвотного центра. Препятствует ингибирующему действию дофамина на перистальтику ЖКТ, тем самым, повышая моторику, тонус и продолжительность сократительной активности верхних отделов пищеварительной трубки [40]. Цизаприд – препарат, относящийся к серотонинергическим средствам. Усиливает выброс ацетилхолина из нейронов миоэнтерального сплетения, повышая чувствительность м-холинорецепторов гладкомышечной ткани ЖКТ. Обладает стимулирующим моторику и тонус, слабительным и антирегургитантным фармакологическими действиеми, за счет этого происходит ускорение прохождения пищевого комка по пищеварительному тракту. Стоит отметить, что при пероральном введении данного лекарственного средства, эффект основного действия гораздо выше, чем при ректальном. Побочным же, будет являться удлинение интервала Q-T, что может привести в дальнейшем к внезапной смерти пациента [38, 39, 11]. Эритромицин - антибиотик который относится к фармакологической группе макролидов, является агонистом мотилина и обладает прокинетической активностью [41]. За счет этого происходит стимуляция мигрирующего моторного комплекса (ММК) в кишечном тракте и более скорое опорожнение желудка, даже после рассечения ветвей блуждающего нерва. С учетом соответствующих характеристик, данный лекарственный препарат можно использовать для лечения пареза кишки. Но, принимая во внимание осложнения, возникающие при долгом приеме данного антибиотика и других макролидов, внедрить его в широкую медицинскую практику как прокинетический препарат, вряд ли станет возможным [40]. Препарат с прокенетическим эффектом, который можно рассматривать как один из основных для лечения пареза – это итоприда гидрохлорид (ганатон). Он обладает двойным действием, являясь антагонистом дофаминовых рецепторов и игибитором ацетилхолинэстеразы, имеет наименьшее количество побочных действий [40, 42]. С учетом особенностей механизма работы данного лекарственного средства, происходит улучшение моторики, более скорое опорожнение желудка при застойных явлениях и подавление рвоты. При проведении крупных рандомизированных плацебо-контролируемых исследований была доказана высокая эффективность итоприда гидрохлорида в лечении функциональных расстройств и диспепсии ЖКТ [43, 44].
В лечение илеуса в послеоперационном периоде робот-ассистированной простатэктомии требуется не только достижение улучшения моторики кишки, но и обезболивающий, спазмолитический эффекты. Применение агонистов опиоидных рецепторов способствует достижению соответствующих положительных клинических эффектов.
Тремибутин является представителем агонистов периферических опиоидных рецепторов, препятствующим прохождению нервного импульса от механических и ноцицептивных рецепторов энтеральной нервной системы в чувствительные нейроны спинного мозга.
Данный препарат показал высокую эффективность в лечении послеоперационного пареза [45, 46]. Так же, на основании исследований, было выявлено преимущество тремибутина, в сравнении с другими спазмолитиками и прокинетиками при лечении функциональных расстройств ЖКТ [47, 48]. Федо-тозин агонист преимущественно каппа-рецепторов. Его обезболивающий эффект обусловлен воздействием на синапсы вегетативных нервных волокон. Путем эксперементальных исследований было доказано обезболивающее действие фе-дотозина с повышением порога болевого восприятия, а также значительное улучшение работы кишечника [49, 50].
На сегодняшний день, роль оксида азота в формировании послеоперационного пареза доказана и изучена. NO-восприимчивые клетки расположены в нижних отделах ЖКТ. При взаимодействии рецепторов с оксидом азота, происходит активация гуанилатциклазы с увеличением синтеза G-протеинкиназы, активация K-каналов с угнетением Ca-каналов. За счёт этого происходит снижение чувствительности гладкомышечных клеток кишечника к кальциевым ионам и их последующая релаксация, снижение тонуса [51]. Если рассматривать оксид азота как звено патогенеза илеуса, то применение ингибиторов NO и гуанилатциклазы можно считать актуальным и правильным решением. На данный момент существует достаточно много соединений, обладающими ингибирующими свойствами, но они недостаточно действенны. Препарат бруне-омицин и его производные, оказывают существенный эффект на снижение активности NO-зависимой гуанилатциклазы, на данный момент, их можно назвать самими действенными средствами в своей группе [52]. Разрабатываются новые методы лечения послеоперационного пареза ЖКТ, пока что не прошедшие крупных рандомизированных исследований, такие как антагонисты вазоактивного интестинального полипептида (ВИП) [10]. ВИП содержится в большом количестве в пищеварительном тракте и поджелудочной железе. Данный нейропептидный гормон оказывает релаксирующее действие на гладкомышечные клетки кровеносных сосудов, повышает секрецию ферментов поджелудочной железы (бикарбонаты), пепсиногена, угнетает секрецию соляной кислоты [53]. Препарат тримебутин обеспечивает снижение количества ВИП и повышение тонуса мускулатуры кишечного тракта.
Субстанция Р – нейропептид, представитель тахикининов, как и нейрокинины А,В, которые находятся в энтерохромаффи-ноподобных клетках и нейронах желудочно-кишечного тракта. В норме данный нейропептид стимулирует моторику кишечника и секрецию ферментов поджелудочной железы. Обладает сосудорасширяющим действием, увеличивает проницаемость сосудистой стенки и обеспечивает секрецию медиаторов воспаления. Также обеспечивает передачу болевой импульсации от ноцицептивных рецепторов в центральную нервную систему. При оперативном вмешательстве происходит травматизация тканей с активацией ноцицептивной системы и увеличением секреции тахикининов, проводящих болевой импульс в высшие отделы нервной регуляции. Увеличивается выброс катехоламинов, являющихся патогенетическими звеньями в формировании послеоперационного пареза. Препараты группы бензотиофенов достаточно новые лекарственные средства, применяющиеся в качестве антагонистов тахикининовых рецепторов [54]. Тем самым, прерывается каскад ферментативных реакций, участвующих в возникновении пареза и кишечной непроходимости. Формирование илеуса происходит за счет изменения заряда мембраны клеток кишечника, нарушения прохождения нервного импульса, и соответственно, сбой в работе ионных насосов. Смещение водно-электралитного баланса нуждается в коррекции, что поспособствует восстановлению исходного заряда мембраны энтероцитов, а значит, и снижение риска возникновения осложнений, связанных с метаболизмом различных ионов, воды и микроэлементов. Например, при нарушении работы кишечника, одним из самых грозных осложнений является гипокалиемия. Смещение баланса этого иона усугубляет патологическое состояние ЖКТ и оказывает негативное влияние на другие органы и системы.
Одним из эффективных методов профилактики и лечения послеоперационного пареза можно считать проведение энтеросорбции. Оно заключается в выведении специальными препаратами (энтеросорбентами) различных токсических веществ. За счет этого, снижается риск интоксикационных осложнений, поддерживается нормальное состояние микро-биоциноза кишечника, а соответственно и его метаболическая и моторная активность.
Следует индивидуализировано подходить к установке назогастрального зонда пациентам. Поскольку он способствует возникновению инфекционных осложнений на дыхательную систему – ателектаз, пневмония. В дальнейшем, возможна генерализация инфекции, ведущей к ухудшению работы ЖКТ и усугублению пареза [55].
Актуально применение метода проведения раннего энтерального питания. Это обеспечивает повышение сократительной функции ЖКТ и разрешению илеуса, улучшению работы иммунной системы и более скорое восстановление ресурсов организма после хирургического вмешательства [56-57]. Такие методы, как мнимое вскармливание и стимуляция блуждающего нерва, пока что невозможно применить в широкой медицинской практике, поскольку они не прошли крупных рандомизированных исследований. Но, предположительно, эти методы способны участвовать в разрешение послеоперационного пареза, и являются достаточно безопасными, чтобы оказывать системный положительный эффект на организм пациента [12].
Вывод
Для того чтобы снизить риск возникновения таких тяжелых осложнений как парез и кишечная непроходимость в послеоперационном периоде робот-ассистированной радикальной простатэкномии, следует применить индивидуализированный и мультимодальный подход в лечении и профилактики. Необходимо учитывать патогенетические факторы, способствующие возникновению илеуса, и с учетом их выстраивать план лечения и профилактических мероприятий. Следует обратить внимание на некоторые новые разработанные препараты и манипуляции, которые впоследствии смогли бы применяться в широкой медицинской практике. А также, не стоит забывать о классических методах, многократно доказавших свою эффективность в разрешении пареза желудочно-кишечного тракта.
26(4). С. 14–23.
Features of cerebral hemodynamics during endovascular surgery on the pelvic organs in patients with various autonomic activities. Endoscopic Surgery , 2002, 6, pp. 27-30 (In Russ.)
(In Russ.)
Список литературы Особенности лечения и профилактики послеоперационного пареза кишки и кишечной непроходимости при проведении робот-ассистированной простатэктомии
- Torre L.A., Bray F., Siegel R.L., Ferlay J., Lortet-Tieulent J., Jemal A. Global cancer statistics, 2012. CA Cancer J Clin, 2015, 65, p. 87-108.
- Пушкарь Д.Ю., Раснер П.И., Куприянов Ю.А., Мальцев Е.Г., Гуров Е.Ю., Умяров М.С., Сидоренков А.В. Рак предстательной железы // Российский медицинский журнал. 2014. 17(5). С. 1-3.
- Livingston E.N., Passaro E.P. Postoperativeileus. Dig Dis Sci. 1990, 35(1), p. 121-132.
- Smith J., Kelly K.A., Weinshilboum R.M. Pathophysiology of postoperative ileus. ArchSurg, 1977, 112, pp. 203-209.
- Васильев А.О., Ширяев А.А., Говоров А.В., Колонтарев К.Б., Раснер П.И., Дьяков В.В., Семенякин И.В., Пушкарь Д.Ю. Кишечная непроходимость в раннем послеоперационном периоде после робот-ассистированной радикальной простатэктомии // Журнал им. Н.И. Пирогова. 2018. 4. С. 90-93.
- Kronberg U., Kiran R.P., Soliman M. Setal. A characterization of factors determining postoperative ileus after laparoscopic colectomy enables the generation of a novel predictive score. Ann Surg, 2011, pp. 253-278.
- Prasad M., Matthews J.B. Deflating postoperative ileus. Gastroenterology, 1999, 117(2), pp. 489-492.
- Савчук Б.Д. Гнойный перитонит. Библиотека практического врача. М.: Медицина, 1979. 192 с.
- Wade P.R., Tamir H., Kirchgessner A.L. Analysis of the role of 5-HT in the enteric nervous system using anti-idiotypic antibodies to 5-HT receptors. AmJPhysiol, 1994, 266, p. 403-416.
- Симоненков А.П., Федоров В.Д. Профилактика и лечение серотониновой недостаточности у хирургических больных // Хирургия. 2003. 3. С. 76-80.
- Симоненков А.П., Федоров В.Д., Клюжев В.М. Применение серотонина адипината для восстановления нарушенной функции гладкой мускулатуры у хирургических и терапевтических больных // Вестник интенсивной терапии. 2005. 1. С. 53-57.
- Brian Behm and Neil Stollman. Postoperative Ileus: Etiologies and Interventions. Clinical Gastroenterology and Hepatology, 2003, 1(2), pp. 71-80.
- Петров В.П., Ерюхин И.А. Кишечная непроходимость. М: Медицина, 1999. 285 с.
- Биряльцев В.Н., Бердников А.В., Филиппов В.А., Велиев Н.А. Электрогастро энтерография в хирургической гастроэнтерологии // Казанский медицинский журнал. 2002. 83(2). С. 94-96.
- Adrian T.E., Ferri G.L., Bacarese-Hamilton A.J. Human distribution and release of a putative new gut hormone, peptide YY. Gastroenterology. 1985, 89(5), pp. 1070-1077.
- Espat N.J., Cheng G., Kelley M.C. Vasoactive intestinal peptide and substance P receptor antagonists improve postoperative ileus. J Surg Res. 1995, 58(6), pp. 719-723.
- Yukioka H., Bogod D.G., Rosen M. Recovery of bowel motility after surgery. Br J Anaesth. 1987, 59, pp. 581-584.
- Zagon I.S., Wu Y., McLaughlin P.J. Opioid growth factor is present in human and mouse gastrointestinal tract and inhibits DNA synthesis manner. Am. J. Physiol. 1997, 272, pp. 1094-1104.
- Е.А. Хомяков, Е.Г. Рыбаков. Послеоперационный парез желудочно-кишечного тракта. Хирургия // Журнал им. Н.И. Пирогова. 2017. 3. С. 76-85
- D. Brealey. Association between mitochondrial dysfunction and severity and outcome of septic shock. Lancet. 2002, 360, pp. 219-223.
- A. Ushmorov Nitric Oxide-Induced Apoptosis in Human Leukemic Lines Requires Mitochondrial Lipid Degradation and Cytochrome C Release. Blood, 1999, 93, pp. 2342-2352.
- В.А. Косинец. Синдром энтеральной недостаточности: патогенез,современные принципы диагностики и лечения // Новости хирургии. 2008. 16(2). С. 130-138.
- Espat NJ, Cheng G, Kelley MC, Vogel SB, Sninsky CA, Hocking MP. Vasoactive intestinal peptide and substance P receptor antagonists improve postoperative ileus. J Surg Res, 1995, 58, pp. 719 -723.
- Kalff J.C., Schraut W.H., Billiar T.R., Simmons R.L., Bauer A.J. Role of inducible nitric oxide synthase in postoperative intestinal smooth muscle dysfunction in rodents. Gastroenterology, 2000, 118, pp. 316 -327
- Moss G., Regal M.E., Lichtig L. Reducing postoperative pain, narcotics, and length of hospitalization. Surgery, 1986, 99, pp. 206-210.
- Holte K., Kehlet H. Postoperative ileus: a preventable event. Br. J. Surg, 2000, 87, pp. 1480-1493.
- Каминский В.В. Методы профилактики парезов кишечника в оперативной гинекологии / В.В. Каминский, А.М. Дубов, Р.А. Ткаченко // Таврический медико-биологический вестник. 2011. 14. 3. 2(55). С. 264-266.
- Каиров Г.Т., Балановский А.П., Чернов Ю.Н., Свирко С.В., Удут В.В. Особенности церебральной гемодинамики при эндовидеохирургических вмешательствах на органах малого таза у больных с различным вегетативным обеспечением деятельности // Эндоскопическая хирургия. 2002. 6. С. 27-30.
- Фомин В.С., Заяратьянц Г.О., Яковенко В.Н. Способ консервативной комплексной коррекции динамической кишечной непроходимости. Патент RU 2655788, Номер заявки: 2018100817; 2018.
- Казаков А.С., Колонтарев К.Б., Пушкарь Д.Ю., Пасечник И.Н. Анестезиологическое обеспечение робот-ассистированной радикальной простатэктомии // Хирургия. Журнал им. Н.И. Пирогова. 2015. 2. С. 56-62.
- Fotiadis R.J., Badvie S., Weston M.D., Allen-Mersh T.G. Epidural analgesia in gastrointestinal surgery. Br J Surg, 2004, 91(7), pp. 828-841.
- Wallin G.,Cassuto J., Hogstrom S., Rimback G., Faxen A., Tollesson P.O. Failure of epidural anesthesia to prevent postoperative paralytic ileus. Anesthesiology, 1986, 65, pp. 292-297.
- Cheng G, Cassissi C, Drexler PG, Vogel SB, Sninsky CA, Hocking MP. Salsalate, morphine, and postoperative ileus. Am J Surg, 1996, 171, pp. 85-88.
- Hodgson P.S., Liu S.S., Carpenter R.L. ADL 8-2698 prevents morphine inhibition of GI transit. Clin Pharmacol Th rapeut, 2000, 67, p. 93.
- Vassallo M., Camilleri M., Phillips S.F. et al. Transit through the proximal colon influences stool weight in the irritable bowel syndrome. Gastroenterology, 1992, 102, pp. 102-108.
- Garnett W., Kelleher D.L., Hickmott.F et al. Alvimopan (ALV) shortens whole bowel transit time in adults with chronic constipation (CC). Gastroenterology, 2004, 126, p. 643.
- Курзанов А.Н. Лиганды опиоидных рецепторов в ракурсе клинической гастроэнтерологии // Современные проблемы науки и образования. 2011. 6. С. 4-199.
- Aitkenhead A.R. Anaesthesia and bowel surgery. Br J Anaesth. 1984, 56, pp. 95-101.
- USP DI. Drug information for the health care provider. Englewood, CO: Micromedex, 2001.
- Тарасова Л.В., Трухан Д.И. Выбор эффективного ибезопасного прокинетика: в фокусе внимания итоприда гидрохлорид // Acta Medica Eurasica. 2015. 4. С. 29-40.
- Peeters T., Matthijs G., Depoortere I., Cachet T., Hoogmartens J., Vantrappen G. Erythromycin as a motilin receptor agonist. Am J Physiol, 1989, 257, pp. 470-474.
- Holtmann G. Understanding functional dyspepsia and its treatment with itopride. Medical Tribune, 2006, 11, pp. 1-15.
- Trukhan D.I., Tarasova L.V., Grishechkina I.A. Prokinetics: focus on itopride hydrochloride. Ros. Med. Vesti, 2013, 3, pp. 29-40.
- Qi Z. Recent Data of Itopride in the Treatment of Functional Dyspepsia in Chinese Patients. Ganaton Regional Advisory Board Meeting Thailand. 2010, 3, pp. 1-8.
- Inoue K., Kobatake K., Haruma K. et al. Gastric emptying in elderly patients with cerebral vascular diseases and the effect of trimebutine. Nihon Ronen IgakkaiZasshi, 1993, 30 (1), pp. 41-45.
- Тропская Н.С. Механизмы послеоперационных нарушений моторно-эвакуаторной функции желудка и тонкой кишки и их фармакологическая коррекция: автореф. дис. докт. биол. наук. М., 2009.
- Ивашкин В.Т., Полуэктова Е.А., Рейхарт Д.В. Эффективность наиболее часто назначаемых групп препаратов у пациентов с функциональными расстройствами желудочно-кишечного тракта - синдромом функциональной диспепсии и синдромом раздраженного кишечника(результатынаблюдательногоисследования)//Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2016.
- Фомин В.С., Зайратьянц Г.О., Яковенко В.Н. Способ консервативной комплексной коррекции динамической кишечной непроходимости // Фарматека. 2018. 7(360). С. 97-101.
- Corazziari E. Role of opioid ligands in the irritable bowel syndrome. J GastroenterolHepatol, 2004, 19(7), pp. 744-9.
- De Winter B.Y., Boeckxstaens G.E., De Man J.G., Moreels T.G., Herman A.G., Pelckmans P.A. Effects of mu- and kappa-opioid receptors on postoperative ileus in rats. Eur J Pharmacol, 1997, 339, pp. 63- 67.
- Fritz E., Hammer J., Schmidt B. et al. Stimulation of the nitric oxideguanosine 3,5 -cyclic monophosphate pathway by sildenafil: effect on rectal muscle tone, distensibility and perception in health and in irritable bowel syndrome. Am. J. Gastroenterol, 2003, Vol. 98, pp. 2253 - 2260.
- Пятакова Н.В. Хропов Ю.В., Бусыгина О.Г., Северина И.С., Преображенская М.Н. Ингибитор NO-зависимой активации растворимой формы гуанилатциклазы. Патент RU 2 188 865C1, дата подачи заявки: 2001.01.16
- Галейся Е.Н.', Лычкова А.Э. Нервная регуляция толстой кишки // Экспериментальная клиническая гастроэнтерология. 2013. 8. С. 54-60.
- Bruce Donald Gitter, William Henry Walker Lann. Use of non-peptide tachykinin receptor antagonists. Patent WO 1995017382, Publication Date 29.06.1995
- Sagar P.M., Kruegener G., Macfi J. Nasogastric intubation and elective abdominal surgery. Br J Surg, 1992, 79, pp. 1127-1131.
- Carr C.S., Ling K.D.E., Boulos P., Singer M. Randomised trial of safety and effi acy of immediate postoperative enteral feeding in patients undergoing gastrointestinal resection. BMJ 1996, 312, pp. 869 - 871.
- Watters J.M., Kirkpatrick S.M., Norris S.B., Shamji F.M., Wells G.A. Immediate postoperative enteral feeding results in impaired respiratory mechanics and decreased mobility. Ann Surg, 1997, 226, pp. 369 -380.


