Особенности локализации обработки протеазы Arg-X в супраструктурах интерфазного хроматина в условиях остановки клеточного цикла бутиратом натрия при индукции роста морфогенеза зрелых эмбрионов зимней и яровой пшеницы
Автор: Иванов Р.С., Иванова Е.А., Вафина Г.Г.
Журнал: Журнал стресс-физиологии и биохимии @jspb
Статья в выпуске: 3 т.12, 2016 года.
Бесплатный доступ
2132/5000 Основным свойством многих организмов является способность чувствовать, оценивать направление действия сигнала и реагировать на условия окружающей среды. Известно, что хроматин играет важную роль в организации регуляции активности генов. Однако наше понимание того, как состояние организации супраструкции хроматина и его белков реагирует не только на изменения окружающей среды, но и на развитие конкретных сигналов, остается в значительной степени неясным. В ходе этой работы мы проанализировали результат различных способов модификации хроматина: регуляторную обработку Arg-X протеазой и ингибирование деацетилирования белка бутиратом натрия. Бутират натрия вызывает остановку клеточного цикла в фазе G0 / G1 и способствует длительности транскрипционной активности хроматина. Эксперименты по молекулярно-генетическому состоянию хроматиновой матрицы проводились при индукции морфогенеза роста в физиологический период поглощения активной воды зрелых семян и зародышей пшеницы, которые целенаправленно трансформировались и формировались в различных условиях окружающей среды. Во время целенаправленной, долговременной трансформации яровой пшеницы Артемовка в озимую пшеницу Мироновская 808, а последняя из них снова в Мироновскую яровую пшеницу при остановке клеточного цикла в фазе G0 / G1, в основном происходит активная обработка Arg-X протеазой при уровень негистонных белков и гистоны линкеров хроматина супраструктур. Мы предполагаем, что регуляторная протеолитическая обработка и продление ацетилирования белков может быть взаимосвязана в регуляции конформационных переходов хроматина на разных уровнях его организации: как супраструктуры, так и на более глубоком протеомном уровне негистонных и гистоновых блоков и имеют свои особенности в период активации транскрипции. Мы надеемся, что особенности изучения мест регулятивного протеолиза в условиях ингибирования деацетилирования в весенних и зимних формах пшеницы могут дать новую возможность для понимания эпигенетического кода растений с целью повышения урожайности и качества сельскохозяйственных культур.
Короткий адрес: https://sciup.org/14323996
IDR: 14323996
Features of localization of Arg-X protease-processing in the suprastructures of interphase chromatin under conditions of cell cycle arrest by sodium butyrate, upon induction of growth morphogenesis of mature embryos of winter and spring wheat
A fundamental property of many organisms is the ability to feel, to assess direction of the signal action and respond to the environmental conditions. It is known that chromatin plays a major role in organizing the regulation of gene activity. However, our understanding of how state of the suprastructure organization of chromatin and its proteins reacts not only to changes in the environment, but also on the development of specific signals remains largely unclear. In the course of this work, we have analyzed the result of the various ways of chromatin modifications: the regulatory Arg-X protease-processing and inhibition of protein deacetylation with sodium butyrate. Sodium butyrate causes cell cycle arrest in the G0/G1 phase, and promotes of duration of the transcriptional activity of chromatin. Experiments on molecular-genetic state of the chromatin matrix were carried out at the induction of growth morphogenesis in the physiological period of active water absorption of mature seeds and wheat germs, which were purposefully transformed and formed in different environmental conditions. During focused, long-term transforming of spring wheat Artemovka into winter wheat Mironovskaya 808 and the last of them again into Mironovskaya Spring wheat while stopping of the cell cycle in the G0/G1 phase, mainly occurs the active Arg-X protease-processing at the level of non-histone proteins, and linker histones of suprastructures chromatin. We assume that the regulatory proteolytic processing and prolongation of acetylation of proteins can be interconnected in the regulation of conformational transitions of chromatin at the different levels of its organization: both suprastructures and at the more profound proteomic level of non-histone and histone blocks, and have its peculiarities during the period of transcriptional activation. We hope that the study peculiarities of locations of regulatory proteolysis in the conditions of inhibition of deacetylation in spring and winter forms of wheat can give a new possibility for understanding the epigenetic code of plants in order to increase crop yields and quality.
Текст научной статьи Особенности локализации обработки протеазы Arg-X в супраструктурах интерфазного хроматина в условиях остановки клеточного цикла бутиратом натрия при индукции роста морфогенеза зрелых эмбрионов зимней и яровой пшеницы
Как известно, фундаментальным свойством многих организмов является способность чувствовать, оценивать направление действия сигнала, реагируя на экологические условия окружающей среды. Классическим примером является яровизация пшеницы, где важнейшая роль принадлежит, как считают ученые (Angel, 2015) регуляции транскрипционной активности генов. Однако понимание того, как состояние хроматина изменятся в ответ на действие сигналов изменяющейся окружающей среды, способствуя адаптации развития растений и эпигенетическому сохранению в течение многих клеточных делений, остается во многом неясным (Berry, Dean, 2015). В зависимости от условий окружающей среды, хроматин способен к выбору части информации, которая затем реализуется в признаки, а так же приводит к изменению онтогенетической подпрограммы развития растений. Эти подпрограммы представляют собой строго упорядоченную во времени и пространстве скоординированную экспрессию сотен и тысяч генов (Lutova, 2010). Многократная пространственновременная реорганизация хроматина происходит при сохранении доступности определенных участков ДНК для регуляторных факторов и ферментов транскрипции в ходе выполнения морфогенетических подпрограмм развития (Razin, 2006). Хроматин может быть модифицирован множеством способов (Ivanova, Giljazetdinov, Ahmetov, 1975; Ivanova, 1977). В совокупности эти механизмы создают набор взаимосвязанных метаболических путей, которые все вместе вызывают изменения гетерополимерной матрицы хроматина. Одной из этих модификаций, которые остаются во многом недостаточно изученными, является регуляторный протеолиз (Ivanova, Davletova, 1986, Vossaert et al. 2014). Начиная с первых работ проведенных десятилетия назад, протеолиз был обнаружен в широком спектре эукариотических организмов (Dhaenens et al. 2014). В настоящее время протеолиз рассматривается как новый вид необратимых посттрансляционных модификаций (Ivanova, Vafina, 1998; Purohit et al., 2012; Panda et al. 2013; Azad, Tomar 2014). Это приводит к изменению парадигмы от концепции протеаз как белок-разрушающих ферментов, к протеазам как реконструкторам ключевых сигнальных молекул (Turk et al., 2012; Ivanova, Vafina, Ivanov, 2014).
Проведение исследований протеаз заметно увеличилось в последнее десятилетие, главным образом в результате очень быстрого развития новых технологий. Однако основные работы по исследованию протеолиза белков клеточного ядра в настоящее время активно проводятся только на модельных объектах животного происхождения. Работы по исследованию протеазо-процессинга на уровне супраструктурной организации интерфазного клеточного ядра и его транскрипционной активности у растений, в особенности в связи с процессами формирования озимых и яровых форм, в частности у пшеницы, в данный момент являются уникальными как в отечественной, так и в зарубежной науке (Ivanov et al. 2015; Ivanova et al. 2015 a, b, c). Новизна наших данных заключается в том, что мы на модельной системе ярового и выведенного из него озимого сорта, при инициации ростового морфогенеза зрелых зародышей пшеницы, рассмотрели проявление активности Арг-Х протеолитического процессинга на уровне отдельных супраструктур хроматина и входящих в их состав негистоновых и гистоновых белков. В ранее опубликованной работе (Ivanova et al., 2015 a) приведены данные по состоянию конформационных изменений молекулярногенетической основы морфогенеза супраструктур хроматина зрелых зародышей пшениц в период активного семенами водопоглощения.
Целью данной работы был анализ локализации активности Арг-Х протеазо-процессинга в условиях ингибирования деацетилирования негистоновых и гистоновых белков супраструктур клеточных ядер: нуклеоплазмы, хроматина, ядерного матрикса; в период остановки клеточного цикла в фазе G 0 / G 1 ; при биологическом покое, инициации активного водопоглощения; и влиянии этого процесса на организацию надмолекулярного ростового морфогенеза при индукции вегетативной фазы зрелых зародышей яровой и озимой пшениц.
MATERIALS AND METHODS
Подробное описание сортов Артемовки (яровой), выведенной из нее Мироновской 808 (озимой) и выведенной из последней Мироновской Яровой представлено в работе (Ivanov et al., 2015). Состояние воздушно-сухого семени и зародыша (находящиеся в состоянии биологического покоя), мы условно приняли за 0ч. Из воздушно-сухих семян (0ч), набухающих под водой («контроль») в течение 3ч, а далее высеянных для прорастания (6ч) («контроль») отделяли от эндосперма зародыши (рис.1-3: «контроль»), из которых выделяли клеточные ядра, их надмолекулярные супраструктуры: нуклеоплазму (Нп) – “лабильный хроматин” (Konarev, 2001), хроматин непрочно- (Хр-I) и прочно- (Хр-II) связанный с ядерным матриксом (ЯМ) и собственно ЯМ (рис. 1,2: супраструктуры), а также негистоновые (НГБ) и гистоновые (НI - линкерный, Н2А+Н2В, Н3+Н4: коровые) белки (рис. 1, 3: НГБ, гистоны) по способу подробно описанному в работах (Ivanova, 1972; Ivanova, Vafina, 1992; Ivanova, Vafina, 2011). Для замачивания семян и прорастания зародышей в условиях ингибирования деацетилирования белков (рис. 1-3: «опыт») был использован бутират натрия (Ivanova, Vafina, 2010). Активность Арг-Х протеолиза в супраструктурах клеточных ядер и выделенных из них НГБ и гистонов, оценивали по расщеплению Арг-Х связей в аргинин-обогащенном белке – протамине-Salmine-A-I («Merk»).
RESULTS
В данной работе наша задача заключалась в том, чтобы выявить в надмолекулярных структурах клеточного ядра зоны проявления активности Арг-Х протеазо-процессинга при условиях ингибирования деацетилирования белков – «опыт», в индуцированных к росту зрелых зародышей пшениц, сформировавшихся в разных условиях окружающей среды (рис. 1-3). Для более наглядного восприятия экспериментальных данных (рис. 1) представлено их схематическое изображение (рис. 2-3). В графическом представлении экспериментальных данных (рис. 1) показатели: 0-5 нмоль аргинина / (с ∙ мг белка) для супраструктур (рис.1: супраструктуры) и 0-2∙10-3 нмоль аргинина / (с ∙ мг белка) для негистонов (НГБ) и гистонов (рис.1: НГБ, гистоны) были условно приняты за «фоновую активность», которая отделена горизонтальной линией на каждом графике. Это было сделано с целью выделить наиболее яркие показатели «опытного» эксперимента. Поэтому в схемах (рис. 2, 3) представлены только «качественные» данные, которые были выше фона. Насчет «качественных» показателей уместно привести слова Резерфорда: «качественное соответствие теории и эксперимента – не что иное, как огрубленное количественное» (Tom, 2002, p.9).
АРТЕМОВКА (яровая) - исходный сорт пшеницы, для выведения Мироновской 808.
Активность Арг-Х протеазо-процессинга, в условиях «опыта», при воздействии бутирата натрия, сразу переключается на супраструктуры ядерного матрикса (рис. 1, 2: супраструктуры - «Артемовка-опыт»; ЯМ: 3ч, 6ч). Что касается следующего этапа эксперимента по определению локализации активности Арг-Х протеазо-процессинга в негистоновых и гистоновых блоках супраструктур клеточных ядер, проведенного в условиях влияния бутирата натрия на индукцию многоуровневого ростового морфогенеза зрелых зародышей пшеницы, то эти данные представлены на рисунке 1 и рисунке-схеме 3. В условиях ингибирования деацетилирования белков, блоки НГБ и гистонов не проявляют Арг-Х протеазо-процессинга (рис. 1, 3: «Артемовка: НГБ и гистоны» - «опыт»; 3ч, 6ч).
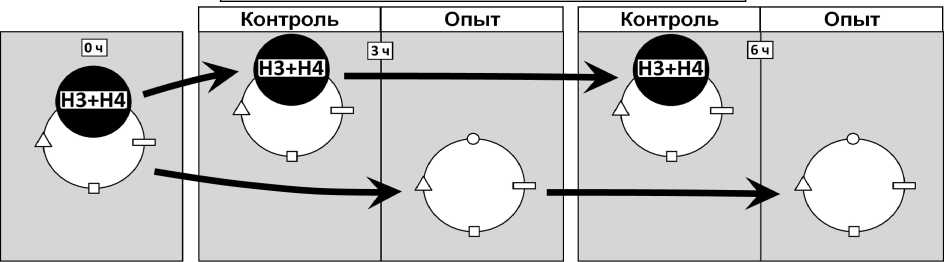
МИРОНОВСКАЯ 808 (озимая). В условиях процесса водопоглощения (3ч, 6ч) в присутствии бутирата натрия (рис. 1, 2: супраструктуры - «озимая-опыт»; Хр-I: 3ч, 6ч) Арг-Х протеазо-активность проявляется только в период метаболизма воды в семени (6ч) в супраструктурах Хр-I (рис. 1, 2: супраструктуры - «озимая-опыт»; Хр-I: 6ч). В условиях проращивания в среде бутирата натрия семян озимой пшеницы - Мироновской 808 (рис. 1, 3: «озимая-опыт»; 3ч), при активном водопоглощении семенами, в клеточных ядрах зародышей (3ч) происходит активация Арг-Х протеазо-процессинга на уровне коровых гистонов H3+H4 хроматина прочносвязанного с ЯМ и самого ЯМ (рис. 1, 3: «озимая-опыт»; Хр-I: НГБ; Xp-II: Н3+Н4; ЯМ: HI, Н3+Н4; 3ч). В период физиологических особенностей метаболизма воды в семени (6ч) (рис. 1, 3: «озимая-опыт»; 6ч) на уровне супраструктур Хр-I дополнительно включается Арг-Х протеазо-процессинг линкерного гистона HI, при одновременном протеазо-процессинге гистона HI и коровых белков Н2А+Н2В в супраструктурах Хр-II (рис. 1, 3: «озимая-опыт»; Хр-I: НГБ, HI; Хр-II: HI, Н2А+Н2В; 6ч). На уровне ЯМ (6ч) Арг-Х протеазо-процессинг активно проявляется в коровых белках Н2А+Н2В при следовых количествах Н3+Н4 (рис. 1, 3: «озимая-опыт»; ЯМ: HI, Н2А+Н2В, Н3+Н4; 6ч).
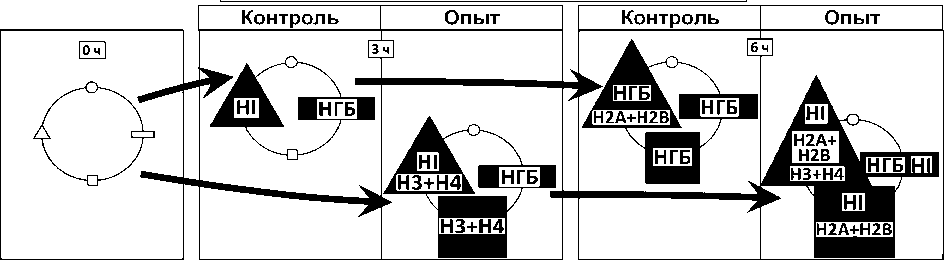
МИРОНОВСКАЯ ЯРОВАЯ выведенная из Мироновской 808 . На воздействие бутирата натрия, супраструктуры клеточных ядер не проявили Арг-Х протеазо-активности выше фоновой (рис. 1, 2: супраструктуры-«Мироновская Яровая- опыт»: 0ч, 3ч, 6ч). При проращивании семян Мироновской Яровой, в условиях бутирата натрия, в клеточных ядрах зрелых зародышей происходит сохранение Арг-Х протеазо-процессинга на уровне НГБ в Хр-II (рис. 1, 3: «Мироновская Яровая-опыт»; Хр-II: НГБ; 0ч, 3ч, 6ч) и пролонгирование активности на уровне НГБ
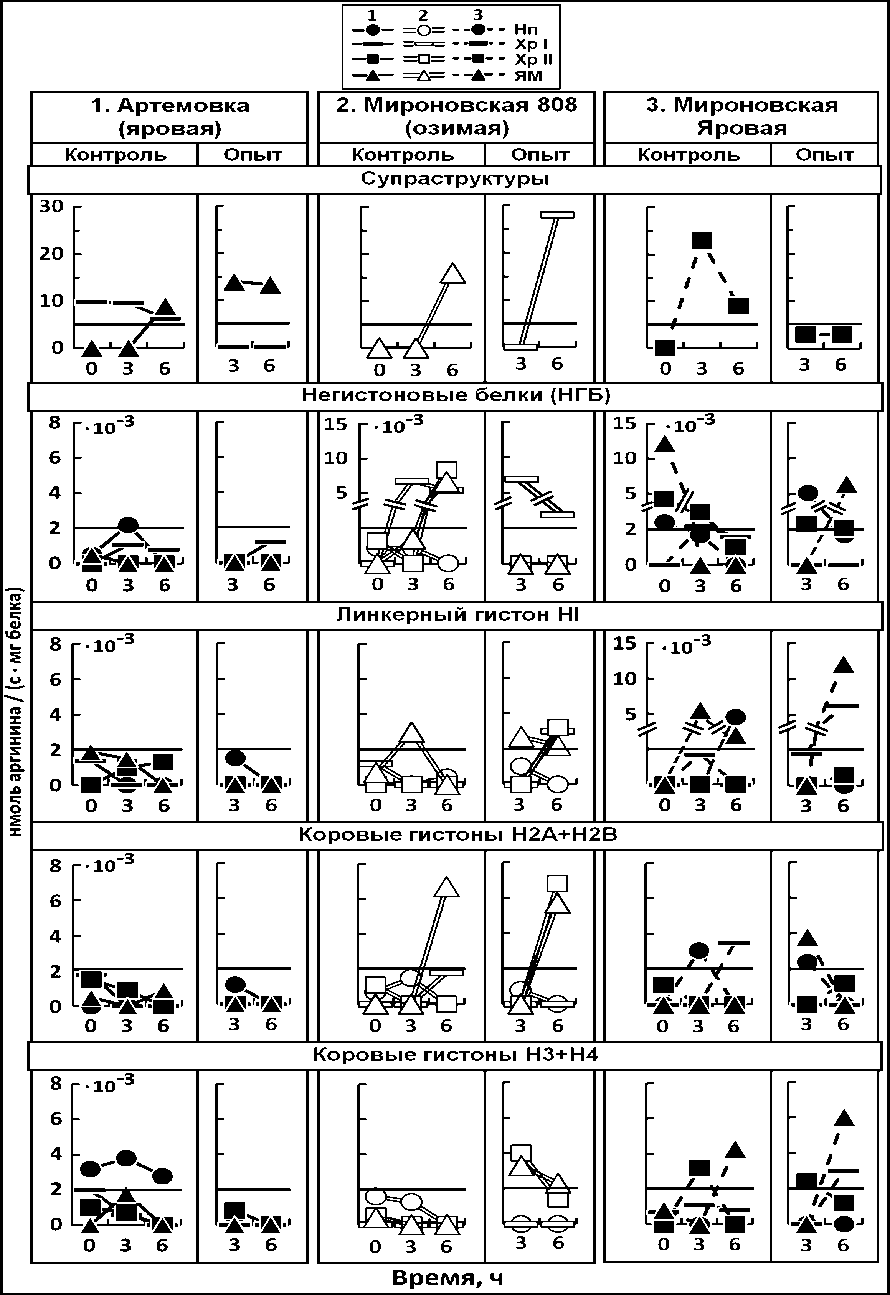
Figure 1. Активность Арг-Х протеолиза в нормальных условиях прорастания (Контроль) и в условиях влияния ингибирования деацетилирования белков (Опыт) в супраструктурах и выделенных из них блоков негистоновых и гистоновых белков зародышей пшениц сортов: Артёмовка (яровая) (1), выведенная из неё Мироновская 808 (озимая) (2) и выведенная из последней Мироновская яровая (3). Супраструктуры: Нп – нуклеоплазма (лабильный хроматин), Хр-I – хроматин непрочносвязанный с ЯМ, Хр-II - хроматин прочносвязанный с ЯМ, ЯМ – ядерный матрикс.
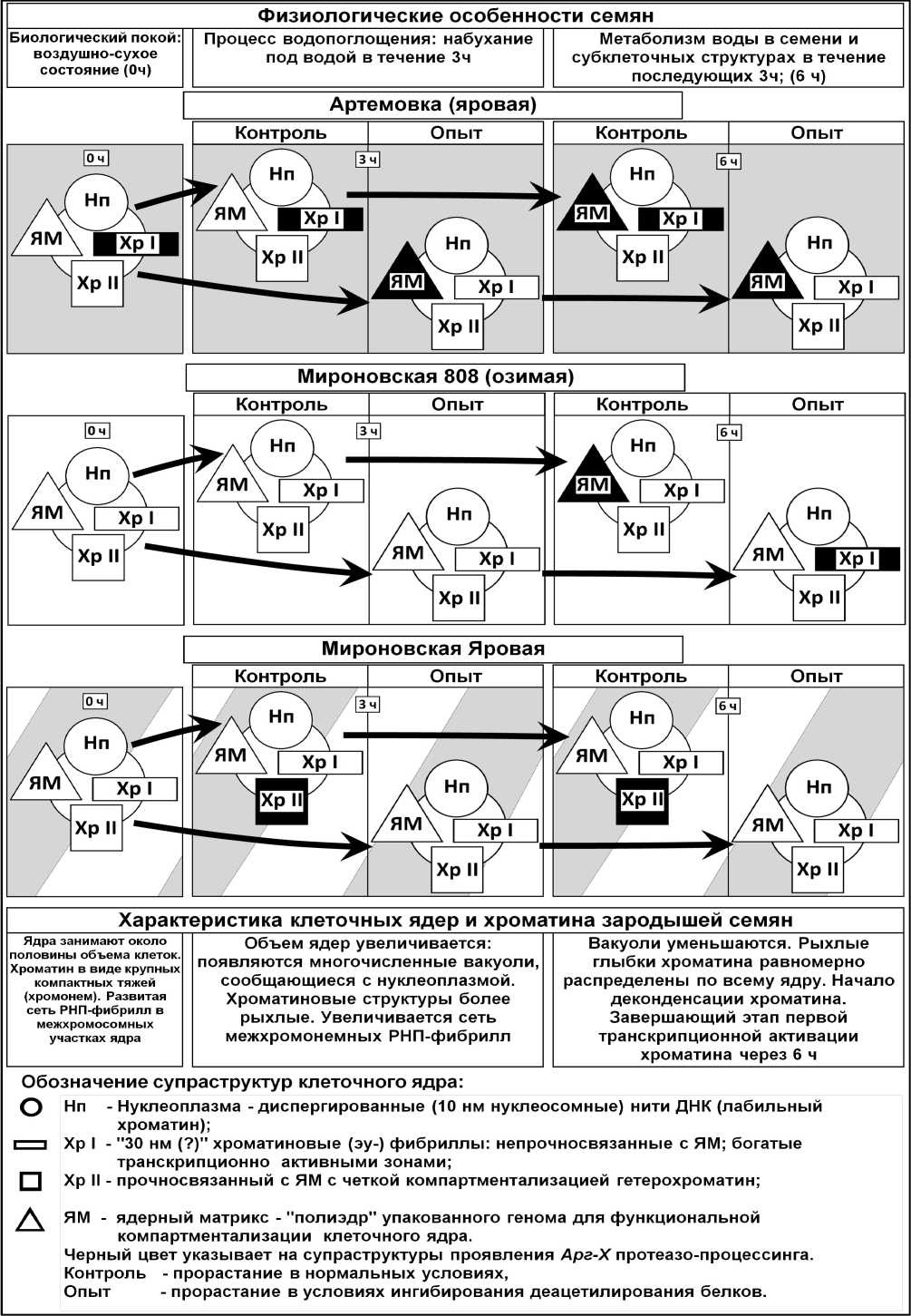
Figure 2. Схема распространения Арг-Х протеолитической системы на поверхности супраструктур интерфазных клеточных ядер зрелых зародышей пшениц.
|
Физиологические особенности семян |
||||
|
Биологический покой: воздушно-сухое состояние (0ч) |
Процесс водопоглощения: набухание под водой в течение Зч |
Метаболизм воды в семени и субклеточных структурах в течение последующих Зч; (6 ч) |
||
Артемовна (яровая)
Мироновская 808 (озимая)
Мироновская Яровая
Ядра занимают около половины объема клеток. Хроматин в виде крупных компактных тяжей (хромонем).
Развитая сеть РН Fl-фибрилл в межхромосомных участках ядра
Характеристика клеточных ядер и хроматина зародышей семян
Объем ядер увеличивается: появляются многочисленные вакуоли, сообщающиеся с нуклеоплазмой. Хроматиновые структуры более рыхлые. Увеличивается сеть межхромонемных РНП-фибрилл
Вакуоли уменьшаются. Рыхлые глыбки хроматина равномерно распределены по всему ядру. Начало деконденсации хроматина. Завершающий этап первой транскрипционной активации хроматина через 6 ч
Обозначение супраструктур клеточного ядра:
о
Нп - Нуклеоплазма - диспергированные (10 нм нуклеосомные) нити ДНК (лабильный хроматин);
Хр I - "30 нм (?)" хроматиновые (эу-) фибриллы: непрочносвязанные с ЯМ; богатые транскрипционно активными зонами;
Хр II - прочносвязанный с ЯМ с четкой компартментализацией гетерохроматин;
ЯМ - ядерный матрикс - "полиэдр" упакованного генома для функциональной компартментализации клеточного ядра.
Черный цвет указывает на супраструктуры проявления Арг-Х протеазо-процессинга. Контроль - прорастание в нормальных условиях,
Опыт - прорастание в условиях ингибирования деацетилирования белков.
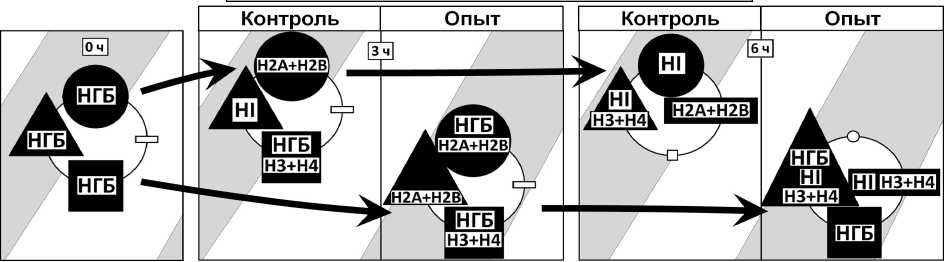
Figure 3. Схема распространения Арг-Х протеолитической системы в негистоновых и гистоновых блоках супраструктур интерфазных клеточных ядер зрелых зародышей пшениц. НГБ – негистоновые белки; HI – линкерный гистон; коровые гистоны: H2A+H2B – умеренно лизин богатые, H3+H4 – аргинин богатые.
лабильного хроматина (3ч) и ЯМ (6ч) (рис. 1, 3: «Мироновская Яровая - опыт»; Нп: НГБ, 3ч; ЯМ: НГБ, 6ч), кроме того, период водопоглощения (3ч) сопровождается включением в протеазо-процессинг коровых гистонов Н2А+Н2В лабильного хроматина (Нп), ЯМ и коровых гистонов Н3+Н4 в Хр-II (рис. 1, 3: «Мироновская Яровая - опыт»; Нп: НГБ, Н2А+Н2В; Хр-II: НГБ, Н3+Н4; ЯМ: Н2А+Н2В; 3ч). В период метаболизма воды в семени (6ч) переключение протеазо-процессинга в негистоновых и гистоновых компонентах супраструктур происходит следующим образом: (рис. 1, 3: «Мироновская Яровая-опыт»; Хр-I: НI, Н3+Н4; Хр-II: НГБ; ЯМ: НГБ, НI, Н3+Н4; (6ч).
DISCUSSION
В предыдущих работах (Ivanova et al., 2015 a, b, c) дана подробная характеристика физиологических и молекулярно-генетических особенностей зрелых зародышей пшениц, сформировавшихся в условиях экологического стресса, а также представлен анализ экранируемости морфогенетических интерфазных супраструктур хроматиновой матрицы в процессе метаболизма инициации водопоглощения. Анализ проделанной работы позволил предположить, что в условиях многолетней адаптации к холодовому шоку у пшеницы на уровне супраструктур хроматина, главным образом ЯМ (упакованный в ядерный матрикс геном (Razin et al., 2014), происходит тотальная экранируемость поверхностных аргинин-Х сайтов к регуляторному протеазо-процессингу (Ivanova et al., 2015 a).
Весь представленный блок информации о фазах физиологии водопоглощения семенами, о состоянии гетерополимерных супраструктур хроматиновой матрицы, о лабораторно-долголетнем отборе и динамики выращивания и «перевода» яровой пшеницы в озимую, последнюю вновь в яровую; о состоянии поверхностных супраструктур хроматиновой матрицы и их белков к Арг-Х протеазо-процессингу, как механизму быстрого реагирования на окружающие условия среды приводит пока к «огрубленному» предположению, что основная роль, во всей выше изложенной динамики молекулярно-генетического морфогенеза, периода остановки клеточного цикла в фазе G0 / G1, принадлежит НГБ и НI. Именно в НГБ находятся блоки регуляторных белков и шапероны, участвующие в нуклеосомной организации хроматина (Ellis, 1990) и способствующие взаимодействию с коровыми гистонами (Bondarenko et al., 2015). Что касается НI (линкерный гистон, не входящий в состав нуклеосомного ядра), то это один из основных структурных белков хроматина, известен давно. Считают, что НI участвует в организации хроматиновых структур высшего порядка, в частности 30-нм фибриллы. Наиболее вероятным местом локализации этого белка является область в районе оси симметрии нуклеосомы, которая расположена рядом с участками входа и выхода ДНК с нуклеосомной частицы. Ключевая роль при связывании НI с нуклеосомой принадлежит не точной последовательности аминокислот в его фрагментах, а скорее всего характеру боковых цепей, их размеру, заряду и гидрофобности (Ljubitelev et al., 2016). Доказано, что при потере одного из вариантов линкерного гистона остальные способны его замещать без заметных физиологических изменений (Ljubitelev et al., 2016). Кроме того, глобулярный домен линкерных гистонов имеет структуру типа «спираль с крылом», включающую в себя мотив «спираль— поворот—спираль». Укладка «спираль с крылом» распространена среди белков, взаимодействующих с ДНК. Почти вся поверхность глобул линкерных гистонов заряжена положительно в отличие от большинства других белков с укладкой «спираль с крылом», обладающих дипольным моментом. При этом негистоновые белки с такой укладкой имеют только один сайт связывания с ДНК, тогда как на глобулах линкерных гистонов таких сайтов не менее двух, хотя их точное положение до настоящего момента не определено. Все предложенные модели положения линкерного гистона на нуклеосоме также предполагают наличие, по меньшей мере, двух контактов с ДНК (Ljubitelev et al., 2016). Ранние данные по соотношению содержания K/R в НГБ и НI соответственно составляло 2,2; 11,2 (Ivanova, 1977; Ivanova, Ahmetov, 1987). То есть, НГБ имеют значительно больше возможностей для Арг-Х протеазо-процессинга, чем линкерный гистон. Но преимущество последнего заключается в том, что он обладает дипольным моментом. Основательный анализ структуры и функции линкерных гистонов, приведенный в обзорной статье (Ljubitelev et al., 2016) и сопоставление литературных данных с экспериментальными результатами нашей работы по молекулярно-генетическим основам инициации морфогенеза зрелых зародышей пшениц, сформировавшихся в разных условиях экологической среды; позволили предположить, что траектория эпигенетической памяти вполне может быть, прежде всего, взаимосвязана с функционированием Арг-Х протеазо-процессинга на уровне НГБ и НI. Весь объем вышеприведенной экспериментальной работы был проведен в условиях остановки клеточного цикла в фазе G0 /G1 бутиратом натрия, который является побочным продуктом углеводного обмена (Dong et al., 2015; Li et al., 2015) и ингибитором деацетилирования белков. Что касается ацетилирования гистонов, то оно наиболее широко исследовано и охарактеризовано как посттрансляционная модификация (Ivanova et al., 1975, Ivanova, Ahmetov, 1987; Wolffe, Hayes, 1999; Telles, Seto, 2012). Молекулярный механизм такой модификации заключается в добавлении ацетильной группы к аминогруппе терминальных остатков лизина в хвостовой области коровых гистонов, главным образом H3 и H4, с помощью класса белков названных ацетилтрансферазами гистонов (HATs). Отрицательно заряженные ацетильные фрагменты, добавленные к гистонам, отталкивают отрицательно заряженную фосфатную основу ДНК. Это отталкивание делает ДНК доступной для различных факторов инициации транскрипции (Majdzadeh et al., 2009). Релаксированная и открытая таким способом хроматиновая матрица становится легко доступной для механизма транскрипции, что облегчает связывание и прохождение РНК полимеразы (Schones et al., 2008; Wang et al., 2009, 2014). Таким образом, ацетилированные гистоны выступают в качестве платформы для связывания белков бромо-доменов, которые являются активаторами транскрипции и осуществляют поддержание состояния эухроматина (Shogren-Knaak et al., 2006; Parbin et al., 2013). Кроме того, ингибиторы гистондеацетилаз нацелены и на негистоновые белки, которые могут прямо или косвенно влиять на судьбу клеток, и весьма вероятно, что эти действия пересекаются с каноническими воздействиями ингибиторов гистондеацетилаз на экспрессию генов (Grant, Dai, 2012; Rosato, Grant, 2005; Bose et al., 2014).
Таким образом, в интерфазных клеточных ядрах: яровой и выведенной из неё озимой пшеницы, как в контрольном варианте эксперимента, так и в условиях ингибирования деацетилирования белков; наблюдается реорганизация экранируемости белковых блоков не только на поверхности супраструктур, но и в их внутренней негистоновой и гистоновой реорганизации в течение физиологических особенностей системы водопоглощения семенем. Что вполне может быть связано с активацией элементов LCR (locus control regions), имеющих отношение к гистоновому коду. В гипотезе гистонового кода протеолиз рассматривается как новый вид необратимых пост трансляционных модификаций гистонов. Однако экспериментального подтверждения эта гипотеза ещё не получила (Purohit et al. 2012). Тем не менее, поиск такой протеазы продолжается. Роль аргинина в организации динамики хроматиновой матрицы давно находится в центре внимания ученых (Smith et al., 1970). Длинные боковые гуанидиновые группы аргинина на поверхности надмолекулярных белковых комплексов выполняют роль восприятия как внутренних, так и внешних сигнальных систем, поступающих из окружающей среды. До сих пор не выясненной, интересной особенность аргинин-богатого гистона Н4, как у растений, так и у животных, является наличие определенных повторяющихся последовательностей, которые предстоит ещё расшифровать (Smith et al., 1970).
Представляя морфогенез как многоуровневый процесс, из всех межуровневых отношений при индукции прорастания яровых и озимых семян, их пространственно-временных периодов, мы для эксперимента выделили уровень организации интерфазной хроматиновой матрицы клеточного ядра и входящих в её архитектурный состав следующих гетерополимерных-надмолекулярных комплексов: нуклеоплазменного (лабильного), непрочно- и прочносвязанного с ядерным матриксом хроматина и собственно ЯМ. Расположение хромосомных территорий имеет важное значение для процессов репликации, транскрипции, репарации и рекомбинации. По всей вероятности филогенетическая принадлежность вида, клеточный цикл, состояние дифференциации влияют на архитектуру интерфазного ядра. Считают, что имеются морфологические ограничения и эпигенетические воздействия на ядерную архитектуру, эволюционную стабильность механизмов хромосомных территорий и изменения ядерной архитектуры (Schubert, Shaw, 2011). Мы предположили, что молекулярный морфогенез на уровне надмолекулярных структур клеточного ядра может быть связан с ослаблением межнадмолекулярных белковых связей, выраженных чувствительностью к Арг-Х протеолитическому процессингу. Для того чтобы судить о надмолекулярном морфопроцессе, мы выбрали определенный временной интервал эксперимента.
Возможно, наши экспериментальные данные будут полезны для тех, кто занимается разработкой логикоматематических схем теории биологической специфичности, о которых писали Ж-М Лен (1998), Р.Том (2002), в области сложной проблемы динамики молекулярного и супрамолекулярного морфогенеза.
Список литературы Особенности локализации обработки протеазы Arg-X в супраструктурах интерфазного хроматина в условиях остановки клеточного цикла бутиратом натрия при индукции роста морфогенеза зрелых эмбрионов зимней и яровой пшеницы
- Angel A., Song J., Yang H., Questa J.I., Dean C. and Howard M. (2015) Vernalizing cold is registered digitally at FLC. Proc Natl Acad Sci U S A., 112(13), 4146-4151 DOI: 10.1073/pnas.1503100112
- Azad G.K. and Tomar R.S. (2014) Proteolytic clipping of histone tails: the emerging role of histone proteases in regulation of various biological processes. Mol Biol Rep., 41(5), 2717-2730 DOI: 10.1007/s11033-014-3181-y
- Berry S. and Dean C. (2015) Environmental perception and epigenetic memory: mechanistic insight through FLC. Plant J., 83(1), 133-148 DOI: 10.1111/tpj.12869
- Bondarenko M. T., Maljuchenko N. V., Valieva M. E., Gerasimova N. S., Kulaeva O. I., Georgiev P. G. and Studitskij V. M. (2015) Struktura i funkcii shaperona gistonov FACT. Molekuljarnaja biologija, 49(6), 891-904.
- Bose P., Dai Y. and Grant S. (2014) Histone deacetylase inhibitor (HDACI) mechanisms of action: emerging insights. Pharmacol Ther., 143(3), 323-336 DOI: 10.1016/j.pharmthera.2014.04.004
- Dhaenens M., Glibert P., Meert P., Vossaert L. and Deforce D. (2014) Histone proteolysis: A proposal for categorization into clipping and degradation. Bioessays, 37(1), 70-79 DOI: 10.1002/bies.201400118
- Dong K, Zhen S, Cheng Z, Cao H, Ge P. and Yan Y. (2015) Proteomic Analysis Reveals Key Proteins and Phosphoproteins upon Seed Germination of Wheat (Triticum aestivum L.). Front Plant Sci., 6, 1017 DOI: 10.3389/fpls.2015.01017
- Ellis R. (1990) Molecular chaperones: the plant connection. Science, 250(4983), 954-959
- Grant S. and Dai Y. (2012) Histone deacetylase inhibitors and rational combination therapies. Adv Cancer Res., 116, 199-237 DOI: 10.1016/B978-0-12-394387-3.00006-9
- Ivanov R.S., Tereshchenko L.M., Vafina G.H. and Ivanova E.A. (2015) Molecular mechanisms of processing proteome reorganization of interphase chromatin during stress and adaptation to winter in wheat. Journal of stress physiology & biochemistry, 11(2), 5-15.
- Ivanova E.A. (1972) Frakcionirovanie rastitel'nyh gistonov na kolonkah s amberlitom IRC-50. Materialy III-j nauchnoj konferencii molodyh uchenyh. Ufa, 54-55.
- Ivanova E.A., Giljazetdinov S.Y. and Ahmetov R.R. (1975) Modifikacija gistonov rastenij i vlijanie fitogormonov na intensivnost' jetogo processa. Rastitel'nye belki i ih biosintez. M.: Nauka, 301-305
- Ivanova E.A. (1977) Modifikacija gistonov u rastenij i ee fiziologicheskoe znachenie: Dis. Kand. Biol. Nauk. M.: IFR AN SSSR. 150.
- Ivanova E.A. and Davletova R.G. (1986) Aktivnost' tripsinopodobnyh proteinaz i ih ingibitorov v kletochnyh jadrah prorostkov ozimyh i jarovyh pshenic. Jekologicheskie aspekty gomeostaza v biocenoze. Ufa. 34-43.
- Ivanova E.A. and Ahmetov R.R. (1987) Modifikacija negistonovyh belkov v prorostkah rastenij. Fiziologija rastenij, 34(3), 507-512.
- Ivanova E.A. and Vafina G.H. (1992) Sposob poluchenija jadernyh frakcij, obladajushhih proteinaznoj i ingibirujushhej aktivnost'ju. Avtorskoe svidetel'stvo № 1733471.
- Ivanova E.A. and Vafina G.H. (1998) Fiziologicheskaja rol' proteoliticheskoj aktivnosti kletochnyh jader v period geterotrofnoj fazy ontogeneza pshenicy. Fiziologija i biohimija kul'turnyh rastenij, 30(6), 472-475.
- Ivanova Е.A. and Vafina G.H. (2010) Sposob ocenki vlijanija ingibitora deacetilirovanija belkov na indukciju rostovogo morfogeneza rastenij. Patent № 2404585.
- Ivanova E.A. and Vafina G.H. (2011) Sposob preparativnogo vydelenija osnovnyh belkov iz suprastruktur kletochnyh jader rastenij. Patent № 2408602.
- Ivanova E.A., Vafina G.H. and Ivanov R.S. (2014) Analiz lokalizacii proteazochuvstvitel'nyh sajtov Arg-Xvdinamike suprastruktur interfaznogo hromatina pri indukcii rostovogo morofgeneza zrelyh zarodyshej jarovoj i ozimoj pshenicy. Fiziologija rastenij i genetika, 46(3), 202-211.
- Ivanova E.A., Vafina G.H. and Ivanov R.S. (2015a) Initial morphogenetic features of proteome of suprastructures of interphase chromatin for germination of mature germs in conditions of adapting to winter in wheat. Journal of stress physiology & biochemistry, 11(4), 29-42.
- Ivanova Е.A., Vafina G.H. and Ivanov R.S. (2015b) Supramolekuljarno-biohimicheskij podhod k analizu reorganizacii interfaznogo hromatina pshenicy v uslovijah stressa. Izvestija ufimskogo nauchnogo centra RAN, 3, 36-42.
- Ivanova Е.A., Vafina G.H. and Ivanov R.S. (2015c) Fiziologicheskie i molekuljarno-geneticheskie osobennosti zrelyh zarodyshej pshenic sformirovavshihsja v uslovijah jekologicheskogo stressa. Izvestija ufimskogo nauchnogo centra RAN, 4(1), 60-64.
- Konarev V.G. (2001) Morfogenez i molekuljarno-biologicheskij analiz rastenij. SPb.: VIR,. 370s.
- Len Zh-M. (1998) Supramolekuljarnaja himija: Koncepcii i perspektivy: Per. s angl. Novosibirsk: Nauka, 334.
- Li M, An F, Li W, Ma M, Feng Y, Zhang X. and Guo H. (2015) DELLA Proteins Interact with FLC to Repress the Flowering Transition. J Integr Plant Biol., 20 DOI: 10.1111/jipb.12451
- Ljubitelev A.V., Nikitin D.V., Shajtan A.K., Studitskij V.M. and Kirpichnikov M.P. (2016) Struktury i funkcii linkernyh gistonov. Biohimija, 81(3), 329-338
- Lutova L.A. (2010) Genetika razvitija rastenij: dlja biologicheskih special'nostej universitetov. 2-e izd. pererab. i dop. SPb.: Izd-vo N-L. 432 s.
- Majdzadeh N., Morrison B.E. and D'Mello S.R. (2009) Class IIA HDACs in the regulation of neurodegeneration. Front Biosci. 13, 1072-1082
- Panda P., Chaturvedi M.M., Panda A.K., Suar M. and Purohit J.S. (2013) Purification and characterization of a novel histone H2A specific protease (H2Asp) from chicken liver nuclear extract. Gene, 512, 47-54 DOI: 10.1016/j.gene.2012.09.098
- Parbin S., Kar S., Shilpi A., Sengupta D., Deb M., Rath S.K. and Patra S.K. (2013) Histone Deacetylases: A Saga of Perturbed Acetylation Homeostasis in Cancer. Journal of Histochemistry & Cytochemistry, 62(1), 11-33 DOI: 10.1369/0022155413506582
- Purohit J.S., Chaturvedi M.M. and Panda P. (2012) Histone Proteases: The tale of tail clippers. Int. J. Int sci. Inn. Tech. Sec. B, 1(1), 51-60
- Razin S.V. (2006) Prostranstvennaja organizacija jeukarioticheskogo genoma i rabota jepigeneticheskih mehanizmov. Genetika, 42(12), 1605-1614.
- Razin S.V., Borunova V.V., Jarovaja O.V. and Vaseckij E.S. (2014) Jadernyj matriks i strukturno-funkcional'naja kompartmentalizacija jadra jeukarioticheskoj kletki. Biohimija, 79(7), 770-781.
- Rosato R.R. and Grant S. (2005) Histone deacetylase inhibitors: insights into mechanisms of lethality. Expert Opin Ther Targets, 9(4), 809-824
- Schones D.E, Cui K., Cuddapah S., Roh T.Y., Barski A., Wang Z., Wei G. and Zhao K. (2008) Dynamic regulation of nucleosome positioning in the human genome. Cell, 132, 887-898 DOI: 10.1016/j.cell.2008.02.022
- Schubert I. and Shaw P. (2011) Organization and dynamics of plant interphase chromosomes. Trends in Plant Science, 16(5), 273-281
- Shogren-Knaak M., Ishii H., Sun J.M., Pazin M.J., Davie J.R. and Peterson C.L. (2006) Histone H4-K16 acetylation controls chromatin structure and protein interactions. Science, 311, 844-847
- Smith E.L., De Lange R.J. and Bonner J. (1970) Chemistry and biology of histones. Physiol. Revs., 50(2), 159-170
- Telles E. and Seto E. (2012) Modulation of Cell Cycle Regulators by HDACs. Front Biosci (Schol Ed), 4, 831-839
- Tom R. (2002) Strukturnaja ustojchivost' i morfogenez. M.: Logos, p. 9, 280
- Turk B., Turk D. and Turk V. (2012) Protease signalling: the cutting edge. The EMBO Journal, 31, 1630-1643 DOI: 10.1038/emboj.2012.42
- Vossaert L., Meert P., Scheerlinck E., Glibert P., Van Roy N., Heindryckx B., De Sutter P., Dhaenens M. and Deforce D. (2014) Identification of histone H3 clipping activity in human embryonic stem cells. Stem Cell Res., 13(1), 123-134 DOI: 10.1016/j.scr.2014.05.002
- Wang Z., Zang C., Cui K., Schones D.E., Barski A., Peng W. and Zhao K. (2009) Genome-wide mapping of HATs and HDACs reveals distinct functions in active and inactive genes. Cell, 138(5), 1019-1031 DOI: 10.1016/j.cell.2009.06.049
- Wang Z., Cao H., Chen F. and Liu Y. (2014) The roles of histone acetylation in seed performance and plant development. Plant Physiol Biochem., 84, 125-33 DOI: 10.1016/j.plaphy.2014.09.010
- Wolffe A.P. and Hayes J.J. (1999) Chromatin disruption and modification. Nucleic Acids Res., 27(3), 711-720


