ОСОБЕННОСТИ МАСС-СПЕКТРОМЕТРИЧЕСКОЙ ДЕТЕКЦИИ БЕТА-АМИЛОИДНЫХ ПЕПТИДОВ (ПЕПТИДОВ АЛЬЦГЕЙМЕРА)
Автор: О. А. Миргородская, А. В. Протасов, Ю. П. Козьмин, P. А. Бубляев, Й. Гобом
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Приборостроение для биологии и медицины
Статья в выпуске: 4 т.32, 2022 года.
Бесплатный доступ
Масс-спектрометрия в сочетании с использованием изотопно-меченных стандартов является одним из популярных методов количественного измерения концентрации бета-амилоидов в биологических средах. Данная статья посвящена предупреждению типичных систематических ошибок таких измерений, возникающих вследствие пренебрежения возможностью превращения бета-амилоидов в денатурированную форму, которая дает в масс-спектрах сигналы в 3 раза более интенсивные, чем нативная форма. Степень этой денатурации определялась по способности нативной формы образовывать комплекс с α-2-макроглобулином, чего денатурированная форма лишена. Показано, что денатурация может происходить при нагревании в кислой среде или при использовании диметилсульфоксида в качестве растворителя. Ошибка измерения возникает, когда изотопно-меченный стандарт и аналит относятся к разным формам. Предложены рекомендации для преодоления систематических ошибок количественного анализа этих соединений посредством принудительной денатурации смеси аналита со стандартом перед анализом.
Количественная масс-спектрометрия, бета-амилоиды, α-2-макроглобулин
Короткий адрес: https://sciup.org/142235504
IDR: 142235504 | УДК: 543.51: 577.1: 66.096.3 | DOI: 10.18358/np-32-4-i3548
FEATURES OF MASS SPECTROMETRIC DETECTION BETA OF AMYLOID PEPTIDES (ALZHEIMER'S PEPTIDES)
Mass spectrometry combined with the use of isotope-labeled standards is one of the favored methods for the quantitative measurement of beta-amyloid concentrations in biological media. This article is devoted to the prevention of typical systematic errors in such measurements arising from the neglect of the possibility of betaamyloid transformation into the denatured form, which gives in mass spectra signals three times more intensity than the native form. The degree of this denaturation was determined by the ability of the native form to set up a complex with α-2-macroglobulin. The denatured form lacks this point. It was shown that denaturation can occur in the case of heat treatment in an acidic environment or when DMSO is used as a solvent. Measurement error occurs when the isotope-labeled standard and the analyte are of different forms. There are suggested recommendations to overcome systematic errors in the quantitative analysis of these compounds by forcing denaturation of the mixture of the analyte with the standard before analysis.
Текст научной статьи ОСОБЕННОСТИ МАСС-СПЕКТРОМЕТРИЧЕСКОЙ ДЕТЕКЦИИ БЕТА-АМИЛОИДНЫХ ПЕПТИДОВ (ПЕПТИДОВ АЛЬЦГЕЙМЕРА)
Количественное определение бета-амилоидов (Aβ) в биологических пробах имеет важное значение для диагностики болезни Альцгеймера. Одним из важных методов анализа Aβ является масс-спектрометрия с изотопно-меченным стандартом Aβ (15N или 18O). Эта статья является предупреждением о возникновении систематических ошибок такого определения в свете открывшихся обстоятельств. А именно, возможности существования Aβ в виде двух форм — нативной и денатурированной. Последняя образуется при нагревании Aβ в кислой среде или растворении его в DMSO. Причем денатурированная форма дает в масс- спектрах сигнал в несколько раз (примерно в 3 раза) более интенсивный, чем нативная.
Однако столь значительное изменение интенсивности сигналов в масс-спектре явилось для нас неожиданностью, побудившей предпринять исследование этого феномена. Эта задача представлялась нам тем более важной, что при анализе бе-та-амилоидов в крови человека в целях диагностики болезни Альцгеймера такая ошибка могла бы привести к ошибочному отнесению патологии к норме.
Принципиальные ошибки измерения концентрации Aβ методом количественной масс-спектрометрии возникают тогда, когда определяемый Aβ относится к нативной форме, а его изотопно-меченный стандарт — к денатурированной. Такая ситуация типична, когда анализируемый Aβ имеет природное происхождение, а стандарт используется в виде раствора в DMSO (этот растворитель часто применяется для приготовления растворов Aβ, поскольку он не летуч и хорошо растворяет Aβ в отличие от других растворителей). При этом DMSO действует как денатурирующий агент. Ранее в работе [1] 2015 г. уже отмечалось, что при использовании DMSO в качестве растворителя могут происходить изменения физико-химических свойств пептидов, однако конкретно бета-амилоиды в ней не были упомянуты.
В предыдущей нашей работе [2] было обнаружено, что нативные Aβ образуют комплекс с α2M, вследствие чего тот перестает взаимодействовать с трипсином. Т.е. Aβ способны выступать в роли ингибитора этого взаимодействия, тогда как денатурированные Aβ теряют такую способность. Это обстоятельство позволяет называть нативную форму Aβ активной, а денатурированную — неактивной. Кинетика дезактивации Aβ была нами ранее [2] изучена на основании измерения количества фрагмента Pep-α2M, отщепляемого трипсином от человеческого α2M (у мышиного α2M такого отщепления не наблюдается). Метод работы с α2M и трипсином [2] позволил точно определять соотношение активной и неактивной форм Aβ в их смеси, а следовательно, и следить за процессом дезактивации Aβ в различных условиях. Недостатками указанного метода являются его трудоемкость и нетехнологичность.
МАТЕРИАЛЫ И МЕТОДЫ
Материалы
Пептид VGFYESDVMGR, синтезированный в ООО "НПФ Верта". Трипсин свиной "Promega". DMSO "Sigma-Aldrich". H 2 18O (97% 18O) "Sigma-Aldrich". TFA "Sigma-Aldrich". α-1-антитрипсин "Abcam". Низкомолекулярный ингибитор трипсина PMSF "Sigma-Aldrich". α-циано-4-гидрокси-коричная кислота "Bruker". Деионизированная вода Li Chrosolv "Merck". Пептиды Aβ и их 15N-содержащие стандарты фирмы "rPeptide".
α2M выделен из сыворотки крови человека гель-фильтрацией и любезно предоставлен сотрудником ФГБУ "НИИ гриппа им. А.А. Смородин-цева" Арамом Шалджяном.
Масс-спектрометрия
Масс-спектры получены с помощью масс-спектрометра Ultraflex II MALDI-ToF/ToF (Bruker Daltonics, Германия), оборудованного Nd:YAG (Neodymium-doped Yttrium Aluminium Garnet; Nd:Y3Al5O12) лазером.
Пептиды детектировали в виде положительных ионов с использованием в качестве матрицы α-циано-4-гидроксикоричной кислоты (HCCA) (BrukerDaltonics, Германия). Точность измерения моноизотопных масс была не хуже 50 миллионных долей (ppm).
Растворы пептидов Альцгеймера
Все анализируемые пептиды были растворены в буфере, содержащем 20% ацетонитрила и 1% NH 4 OH. Концентрация пептидов в растворах составляла 23 мкM. 15N-изотопно-меченные стандарты пептидов Альцгеймера были растворены в 100% DMSO. Концентрация составляла 11.5 мкM.
Получение 18О-изотопно-меченного стандарта пептидов Альцгеймера
Растворы пептидов Альцгеймера в концентрации 23 мкM смешивались с H 2 18O, ацетонитрилом и 100% трифторуксусной кислотой в соотношении 1:4:4:1 об. (пептид : H 2 18O : ацетонитрил : TFA). Смесь инкубировалась в твердотельном термостате при температуре 50 °C в течение 30 мин для протекания изотопного обмена. После инкубации стандарт оставался в растворе, высушивание не производилось.
Термоактивация пептидов Альцгеймера в TFA
Растворы пептидов Альцгеймера в концентрации 23 мкM смешивались с водой, ацетонитрилом и 100% трифторуксусной кислотой в соотношении 1:4:4:1 об. (пептид : вода : ацетонитрил : TFA). Смесь инкубировалась в твердотельном термостате "Гном" ("ДНК-Технология", Россия) при температуре 50 °C в течение 30 мин.
Термоактивация в растворе матрицы
Растворы пептидов Альцгеймера в концентрации 23 мкM смешивались с раствором матрицы (α-циано-4-гидроксикоричной кислотой) в 70% ацетонитриле с 1% TFA и добавлением 10 нM ок-тил-β-D-глюкопиранозида. Смесь инкубировалась в течение 30 мин при температуре 50 °C.
Термоактивация в буферном растворе
Растворы пептидов Альцгеймера в концентрации 23 мкM смешивались с буфером, в котором они растворены (20% ацетонитрил, 1% NH 4 OH). Раствор инкубировался в течение 30 мин при температуре 50 °C.
Инкубация пептидов Альцгеймера в DMSO
Исходный раствор пептида в буфере (20% ацетонитрила, 1% NH 4 OH) разбавлялся в 10 раз 100% DMSO. Пептид в DMSO выдерживался в течение 4, 24 и 48 ч при температуре 23 °C. Часть раствора пептида, выдержанная в течение 24 и 48 ч, подвергалась инкубированию в течение 1 ч при температуре 50 °C.
РЕЗУЛЬТАТЫ ЭКСПЕРИМЕНТА И ИХ ОБСУЖДЕНИЕ
Общее описание
В экспериментах использовался ряд пептидов Альцгеймера. В качестве изотопного стандарта применялись как синтетические их аналоги с изотопом 15N, так и аналоги с изотопом 18O, получаемые изотопным обменом с тяжелой водой H 2 18O.
Табл. 1. Пептиды, испо л ьзо в анные в экспе ри менте (обо з начен и я, аминоки с лотн ые посл е доват е льнос т и, мо-н о изотоп н ые в е личи н ы м олек у лярн ой м асс ы и отн ош ен и е ин т ен с ивн ос ти сигнал а в м а с с-спе к тре посл е терм ообра ботк и в п ри сутствии TFA к исходному сигналу)
|
Пепт и ды |
Аминокислотная последовательность |
Mr |
I тер м. /о |
|
Aβ(1–21)* |
DAEFRH DS GYEV HHQ KKLVFF |
2588.3 |
1 . 0 |
|
Aβ(1–3 8) |
DAEFRH DS GYEV HHQ KLVFFAEDVGS N KGAII GLM VG G |
4129.0 |
3 . 1 |
|
Aβ(1–4 0) |
DAEFRH DS GYEV HHQ KLVFFAEDVGS N KGAII GLM VG G |
4327.2 |
3 . 1 |
|
15N-Aβ(1– 40) |
VV |
4381.2 |
1 . 0 |
|
Aβ(1–4 2) |
DAEFRH DS GYEV HHQ KLVFFAEDVGS N KGAII GLM VG G |
4511.3 |
2 . 5 |
|
15N-Aβ(1– 42) |
VVIA |
4567.3 |
1 . 0 |
|
α2М- hum an (705– 7 17) |
VGFYESD VM GR |
1259.7 |
1 . 0 |
Примечан ие : * — анал ог пе п тид а Aβ(1–20)
Поми мо э того на ми был п ол у че н п еп ти дны й ф ра г ме нт Pep-α2M п утем трипсинолиза человеческого α2M. С п и сок ис п ользова н ны х пе п тид о в и от дельн ые х а р ак т ерис т ики представлены в табл. 1.
Полученный нами стандарт с изотопом 18O не является гомогенным, поскольку представляет собой смесь пептидов с разным числом замещенных атомов кислорода, число которых зависит как от продолжительности обмена с тяжелой водой H218O, так и от изотопной чистоты самой воды. В нашем случае не требуется, чтобы стандарт был индивидуальным соединением, а является вполне достаточным, чтобы смесь с разным числом включенных атомов 18O давала в масс-спектре сигналы, не перекрывающиеся с сигналами аналита. В нашем случае статистическое распределение вклада каждого индивидуального компонента в зависимости от числа включенных в его состав атомов 18O приведено на рис. 1. Масс-спектр такого стандарта в смеси с незамещенным пептидом Aβ(1–40) приведен на рис. 2.
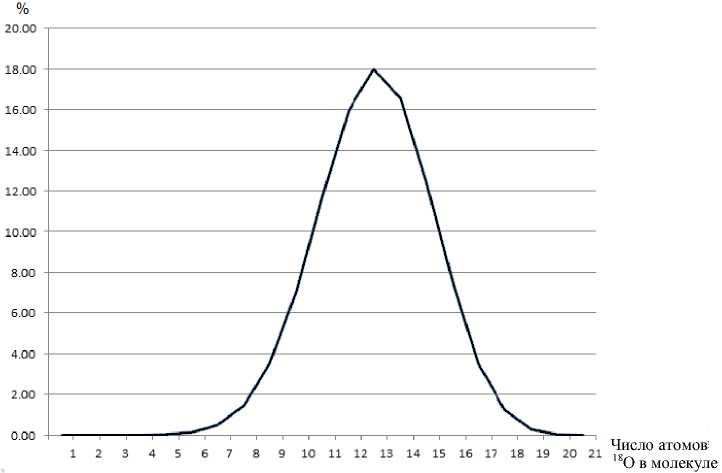
Рис. 1. Проце н тное содержание 18O-з а м е щенных компонентов стандарта в зависимости от чи с ла в к л ю че нн ых в е го состав атомов 18O
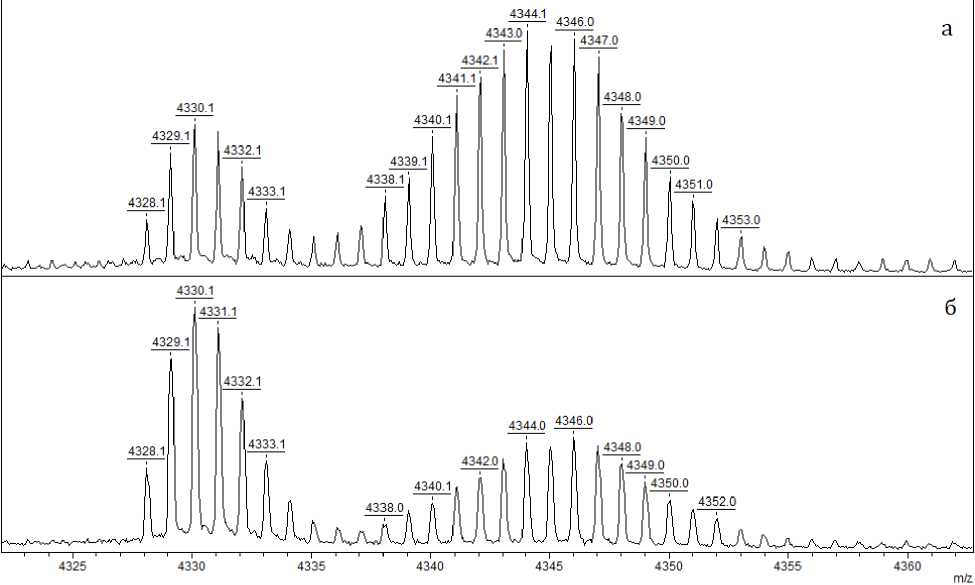
Рис. 2. Изотопное распределение пептида Aβ(1–40) в смеси со стандартом.
а — исходное соотношение; б — соотношение после инкубации пептида в смеси 10% TFA и 40% ацетонитрила в течение 30 мин при температуре 50 °C
Табл. 2. Оценка влияния инкубации пептида Aβ(1–38) в 10% TFA + 40% ацетонитрил при 50 °C на соотношение интенсивностей молекулярных ионов аналита и его стандарта
|
Проба |
Инкубация в 10% TFA + 40% ацетонитрил |
Отношение сумм площадей пептид/стандарт |
|
1 |
– |
1.02 |
|
2 |
30 мин, 50 °C |
2.99 |
Вместе с тем выяснилось, что при смешивании эквимолярных количеств анализируемого образца и полученного из него стандарта интенсивность стандарта в спектре оказалась примерно в 3 раза выше интенсивности исходного пептида. Однако если анализируемый образец выдержать в условиях, аналогичных получению стандарта, то его интенсивность вырастет (см. рис. 2, б) и их интенсивности станут равными. В этой связи нами было предпринято детальное изучение этого эффекта как имеющего важнейшее значение для количественного анализа этих пептидов.
Изменение интенсивности сигнала пептида Aβ(1–40) в кислых средах (в присутствии TFA)
Известно, что TFA традиционно используется в составе растворов при приготовлении матриц при масс-спектрометрической детекции пептидов. Кроме того, 10% TFA при повышенной температуре используется для получения 18О-содержащих стандартов пептидов Aβ. В то время как при получении 18О-содержащего стандарта применяются исключительно жесткие условия — высокая концентрация TFA и повышенная температура. Вместе с тем использование TFA при работе с пептидами часто необходимо при масс-спектрометрической детекции (в наших экспериментах около 9% TFA в составе растворителя для матриц). В связи с этим представляло интерес оценить возможность предподготовки проб с использованием достаточной концентрации TFA и в том числе использовать непосредственно предподготовку образцов в матрице при одномоментном присутствии как анализируемого образца, так и его стандарта.
Температурное воздействие на пептид Aβ(1– 40), находящийся в кислой среде, привело к увеличению интенсивности иона пептида относительно стандарта в 2.5 раза (см. табл. 2).
Специальными экспериментами было показано, что одинаковое возрастание интенсивности всех используемых пептидов достигается, начиная с использования 1–2% TFA при инкубации при 50 °C в течение 30 мин для всех образцов, и достигает тех же значений при инкубации в растворе матриц. При этом, как показали дополнительные эксперименты с пептидом, представленные на рис. 3, для достижения аналогичного эффекта увеличения интенсивности можно при этой же температуре ограничиться добавлением TFA в концентрации 1–2%.
Таким образом, при использовании полученного путем изотопного обмена стандарта пептида для получения корректных данных количественного анализа пептидов имеются два пути: либо ввести коэффициент пропорциональности, либо перед масс-спектрометрической детекцией провести термообработку анализируемого образца.
Из полученных результатов два вывода. Первый заключается в том, что интенсивность пептидов при масс-спектрометрической детекции зависит от предобработки анализируемых образцов. В частности, увеличение интенсивности при термостатировании при 50 °C в течение 30 мин в присутствии TFA с концентрацией более 1%. Учитывая, что в состав матрицы входит 7%-я TFA, представляется целесообразным просто термостатировать образец в этом растворе в течение 30 мин. Экспериментально показано, что в этих условиях достигается максимальное увеличение интенсивности, близкое к З.0.
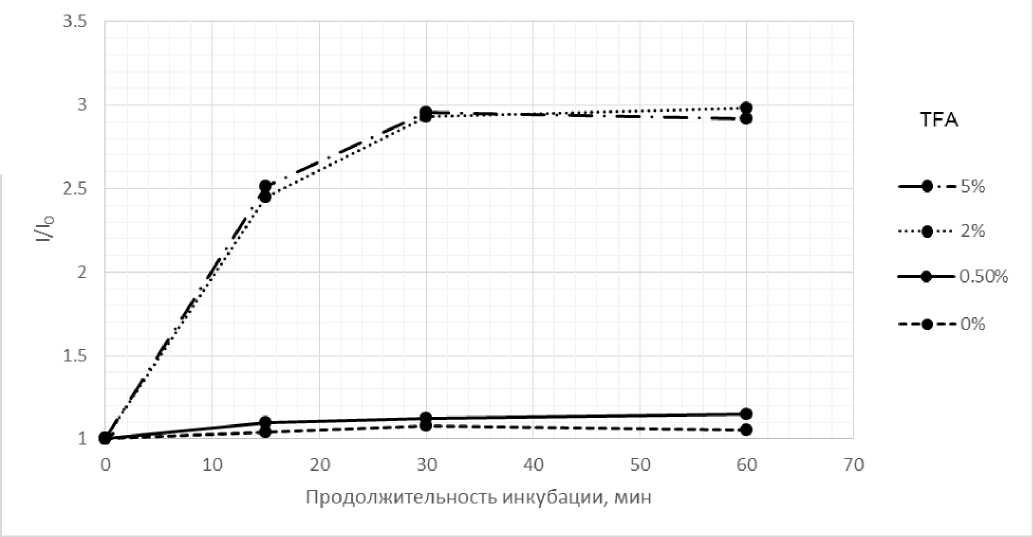
Рис. 3. Изменение в интенсивности при масс-спектрометрическом анализе пептида Aβ(1–38) относительно его стандарта после инкубации пептида в TFA.
По вертикальной оси отложено отношение интенсивности после инкубации к начальной интенсивности
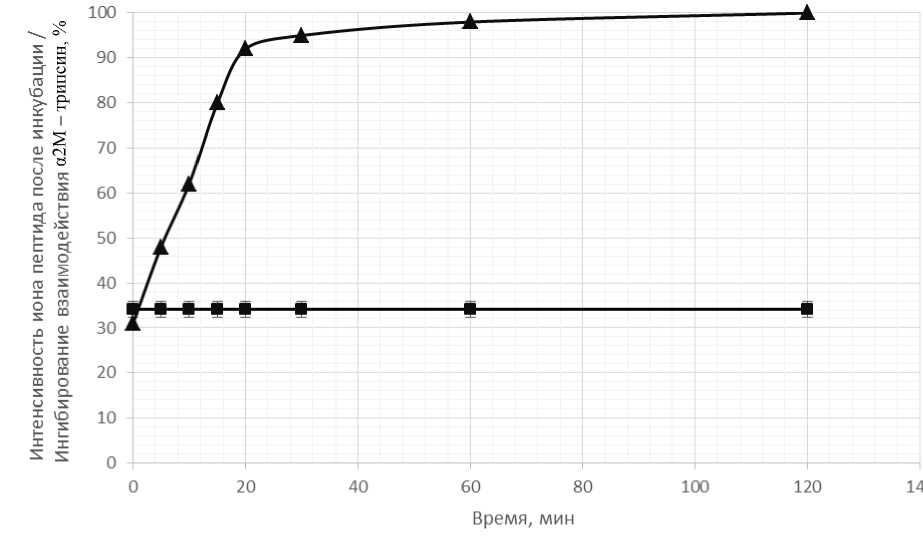
Рис. 4. Способность пептида Aβ(1–40) к ингибированию взаимодействия α2M с трипсином при термостатировании пептида при 50 °C.
■ — активность ингибирования a2M; ▲ — изменение масс-спектрометрической интенсивности иона пептида Aβ(1–40) при термостатировании
Влияние термообработки пептида на активность Aβ(1–40)
В представленном следующем эксперименте проведена термообработка пептида Aβ(1–40) и его триптического гидролизата при 50 оС. Повышение температуры было выбрано из необходимости ускорения процесса, поскольку даже при 50 °C время полуинактивации пептида Aβ(1–40) составляет примерно 24 ч. В связи с этим предстояло оценить устойчивость этого пептида при термообработке при 50 °C в отсутствие DMSO. Результаты этого эксперимента при инкубации пептида при 50 °C представлены на рис. 4.
Из полученных данных следует: при масс-спектрометрической детекции при полном сохранении активности быстро возрастает интенсивность сигнала по отношению к стандарту (растворенному в DMSO), внесенному после термоактивации уже в матрицу (см. Материалы и методы). Этот факт необходимо учитывать при использовании масс-спектрометрии для количественного определения концентраций этих пептидов с использованием изотоп-содержащих стандартов (в представленном выше случае ошибка в определении может составлять порядка 300%).
Влияние термообработки на смесь пептидов Aβ(1–38), Aβ(1–40) и Aβ(1–42)
В тех же условиях была подвергнута термообработке смесь всех трех имеющихся пептидов β-амилоида — Aβ(1–38), Aβ(1–40) и Aβ(1–42) — в надежде, что инкубация смеси этих пептидов в кислой среде позволит выровнять детектируемые интенсивности. Однако на деле соотношение интенсивностей пептидов осталось тем же. Тем не менее детектируемость пептидов от этой операции все же улучшилась, что особенно ценно в отношении пептида Aβ(1–42), интенсивность иона которого обычно мала.
В сравнении со стандартом каждый из пептидов показал одинаковое увеличение интенсивности (табл. 3).
Изменение активности пептида Aβ(1–40) при инкубации в DMSO
DMSO — часто используемый растворитель для гидрофобных пептидов, в том числе и для растворения пептидов Альцгеймера. Именно этот растворитель был использован нами для приготовления растворов 15N-стандарта.
Табл. 3. Изменения в соотношении интенсивностей пептидов Aβ по отношению к стандарту 18O – Aβ(1–40)
|
Пептид |
Соотношение сумм площадей пептид / стандарт до инкубации |
Соотношение сумм площадей пептид / стандарт после инкубации |
|
Aβ(1–38) |
1.83 |
3.63 |
|
Aβ(1–40) |
0.38 |
0.70 |
|
Aβ(1–42) |
0.04 |
0.08 |
Экспериментально выяснилось, что стандарты пептидов не обладают способностью ингибировать α2M. В связи с этим нами была проведена проверка влияние DMSO на активность пептида Aβ(1–40). Для этого пептид Aβ(1–40) из буферного раствора (20% ацетонитрил, 1% аммиак) разбавлялся в 10 раз 100%-м DMSO. Пептид с DMSO выдерживался в течение 4, 24 и 48 ч. После этого часть пробы подвергалась дополнительному инкубированию в течение 1 ч при температуре 50 °C.
В качестве контроля количества α2M в сыворотке была подготовлена проба из сыворотки без добавления пептида Aβ(1–40). Вместо пептида добавлялся бикарбонатный буфер. В качестве контроля за протеканием ингибирования была приготовлена проба из сыворотки с добавлением пептида без DMSO. Результаты измерения активности α2M после инкубации с Aβ(1–40), предварительно выдержанным в DMSO, представлены на рис. 4. Как следует из представленных данных, ингибирующая способности пептида Aβ(1–40) существенно снижается со временем и в конечном итоге получается полностью неактивный пептид, что и наблюдается у стандартов, растворенных в DMSO.
Полученные результаты указывают на то, что инкубация пептидов Альцгеймера с DMSO приводит к утрате способности ингибировать взаимодействие α2M с трипсином. Нагревание при этом не оказывает существенного влияния. Подобный результат, возможно, объясняется изменением пространственной структуры пептида. Это согласуется с результатами, ранее полученными при инкубации сыворотки с 15N-изотопно-меченными стандартами пептидов Aβ, которые, будучи растворенными в 100% DMSO, не обладали ингибирующей способностью. Это не противоречит данным по термоактивации пептидов, которая не приводила к утрате ингибирующей способности, но приводила к увеличению интенсивности при масс-спектрометрической детекции.
Показано, что Aβ при выдерживании в растворе DMSO теряет способность связываться с α2M и, соответственно, ингибировать его способность к взаимодействию с протеазами на примере трипсина. Скорость инактивации зависит от концентрации DMSO. Это, в свою очередь, позволило по взаимодействию с α2M предложить метод, дающий количественную оценку содержания пептидов Aβ, способных (активных) или теряющих способность (неактивных) ингибировать α2M.
В качестве примера использования этого подхода на рис. 5 представлен процесс потери ингибирующей способности по отношению к α2M для пептида Aβ(1–38) в растворе, содержащем 20% DMSO.
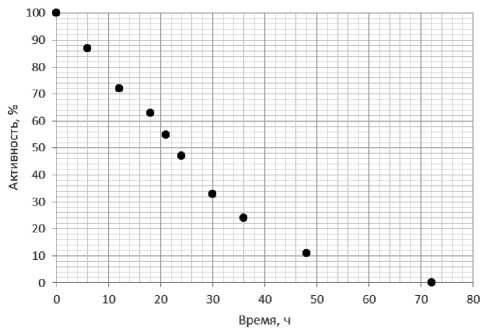
Рис. 5. Кинетика ингибирования пептида Aβ(1–38) в 20% DMSO
Тот факт, что DMSO дезактивирует возможность Aβ связываться с α2M, позволяет предположить, что такой Aβ теряет способность взаимодействия с теми рецепторами, с которыми он взаимодействует в организме больного. Об этом косвенно свидетельствует и то, что DMSO может служить полезным адъювантом для противодействия Aβ-опосредованной синаптотоксичности [3].
Зависимость масс-спектрометрической детекции пептида Aβ(1–38) от его активности
Влияние состояния пептида Aβ(1–38) на его масс-спектрометрическую детекцию проверялось относительно 15N-стандарта этого пептида. Стандарт растворен в 100% DMSO, и его интенсивность стабильна независимо от проводимых с ним манипуляций.
Небольшой объем каждого из образцов пептида, инактивированного в DMSO, смешивался с равным объемом стандарта и анализировался масс-спектрометрически. В качестве контроля максимального изменения интенсивности был взят не подвергавшийся инкубации в DMSO пептид, который инкубировался в 2.5% TFA (равные объемы раствора пептида и 5% TFA) в течение 30 мин при температуре 50 оС. Все образцы, инкубированные в DMSO, также смешивались с TFA для оцен- ки изменения интенсивности вследствие действия TFA. Для каждого образца было сделано 3 повторных измерения.
У не подвергавшихся действию DMSO образцов наблюдалось увеличение интенсивности в 3 раза относительно неинкубированных в TFA. При этом образцы после воздействия DMSO показали четкую зависимость в изменении интенсивности ионов в зависимости от активности этих пептидов (рис. 6).
Эта зависимость позволяет оценить активность пептида Aβ по интенсивности его сигнала в масс-спектрометре. Для этого достаточно получить масс-спектры образца относительно стандарта без инкубации в TFA и после инкубации. После инкубации в TFA достигается максимальная интенсивность, соответствующая троекратной интенсивности по сравнению с активным пептидом Aβ. Если пептид был частично неактивен, то изменение интенсивности после инкубации в TFA будет меньше 3. В последнем случае делением на 3 изменения интенсивности мы получим активность исследуемого пептида. Например, если после инкубации с TFA изменение интенсивности составило 1.8 раза, то на графике необходимо отложить значение по оси изменения интенсивности 3/1.8 = = 1.67, что соответствует активности 60%.
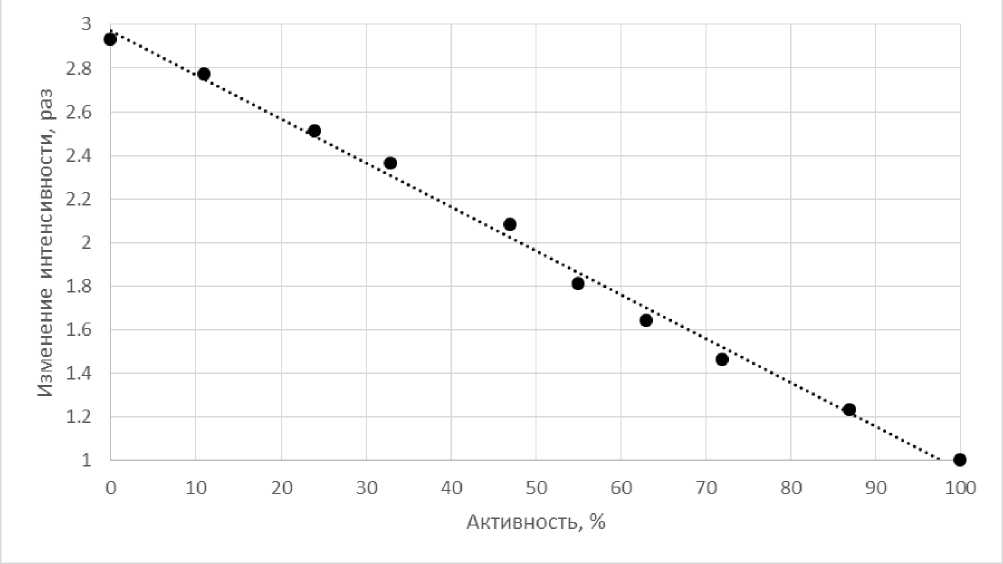
Рис. 6. Зависимость интенсивности масс-спектрометрической детекции пептида Aβ(1–38) от активности пептида
ЗАКЛЮЧЕНИЕ
Из нашего исследования логически вытекает рекомендация: перед анализом прогревать смесь аналита Aβ со стандартом в присутствии 0.5% TFA, что ведет к денатурации обоих компонентов смеси. Этим способом достигается единообразие их форм, заодно повышая интенсивность их сигналов в масс-спектре.
При анализе необходимо учитывать различную интенсивность сигналов от Aβ(1–38), Aβ(1–40) и Aβ(1–42) — в этом ряду она убывает. Что не позволяет количественно измерить всех их с помощью одного изотопно-меченного стандарта.
Список литературы ОСОБЕННОСТИ МАСС-СПЕКТРОМЕТРИЧЕСКОЙ ДЕТЕКЦИИ БЕТА-АМИЛОИДНЫХ ПЕПТИДОВ (ПЕПТИДОВ АЛЬЦГЕЙМЕРА)
- 1. Laurents D.V., Pantoja-Uceda D., Lopez C., Carrodeguas A., Mompean M., Jimenez M.A., Sancho J. DMSO affects Aβ(1–40)' s conformation and interactions with aggregation inhibitors as revealed by NMR // Rsc Advances. 2015. Vol. 5, is. 85, P. 69761–69764. DOI: 10.1039/C5RA12100K
- 2. Protasov A.V., Mirgorodskaya O.A., Kozmin Y.P., Gobom J. A mass spectrometric approach to study the interaction of amyloid β peptides with human α-2-macroglobulin // Biochimie. 2021. Vol. 191. P. 62–68. DOI: 10.1016/j.biochi.2021.08.008
- 3. Penazzi L., Lorengel J., Sundermann F., Golovyashkina N., Marre S., Mathis C.M.B., Lewejohann L., Brandt R., Bakota L. DMSO modulates CNS function in a preclinical Alzheimer's disease model // Neuropharmacology. 2017. Vol. 113, Part A. P. 434–444. DOI: 10.1016/j.neuropharm.2016.10.020


