Особенности необратимой сорбции катионов тяжелых металлов гранулированным сорбентом на основе силикатов и алюмосиликатов кальция
Автор: Михайлов Геннадий Георгиевич, Морозова Алла Георгиевна, Лонзингер Татьяна Мопровна, Лонзингер Александра Владимировна, Пашкеев Игорь Юльевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 12 (229), 2011 года.
Бесплатный доступ
Разработан состав и способ получения гранулированного сорбента тяжелых металлов на основе саморассыпающегося шлака (γ-2CaO∙SiO2) и модифицированного гидроалюмосиликата в качестве связующего. Исследована природа сорбционного взаимодействия силикатов и алюмосиликатов кальция с водными растворами, содержащими катионы Fe3+, Се3+, Сu2+, Ni2+. Показано, что присутствие в составе сорбента дополнительных к Са2+ иновалентных катионов (Na+, К+) активирует дефектообразование и массоперенос при обменном взаимодействии. Необратимость сорбционного взаимодействия обеспечивается внедрением Се3+, Сu2+, Ni2+, Fe3+ в решетку силикатов и алюмосиликатов кальция с сохранением исходного каркаса гранулированного сорбента.
Гранулированный сорбент, тяжелые металлы, топохимические реакции, активирование, кинетика сорбции, новообразования
Короткий адрес: https://sciup.org/147160189
IDR: 147160189 | УДК: 544.723
Features of irreversible sorption of heavy metal cations with granulated sorbents based on silicates and calcium aluminosiliicates
The composition and method for producing granulated sorbent for heavy metals on the basis of spontaneously refining slag (γ-2CaO∙SiO2) and modified hydroaluminosilicate as a binder have been developed. The nature of the sorption interaction of calcium silicates and aluminosilicates with aqueous solutions of the cations Fe3+, Се3+, Сu2+ Ni2+ have been studied. It has been shown that the presence of cations with different valence (Na+, K+) in addition to Ca2+ in the sorbent activates the defect formation and mass transfer at the exchange interaction. The irreversibility of the sorption interaction is provided by introduction of Се3+, Сu2+, Ni2+, Fe3+ into the lattice of calcium silicates and aluminosilicates, preserving the original framework of the granulated sorbent.
Текст научной статьи Особенности необратимой сорбции катионов тяжелых металлов гранулированным сорбентом на основе силикатов и алюмосиликатов кальция
В литературе описаны возможности использования силикатов и алюмосиликатов кальция для связывания и иммобилизации токсичных тяжелых металлов из кислых промышленных стоков при использовании цемента в замкнутых системах [1-9]. Основными фазовыми составляющими, ответственными за формирование цементного камня, являются P-2CaO SiO2 и 3CaO SiO2. В отличие от P-2CaOSiO2, y-2CaO SiO2 имеет низкую гидравлическую активность и не обладает способностью образовывать твердеющие гидратные формы. Неспособность y-2CaO SiO2 к образованию прочного цементного камня может быть использована как преимущество при создании сорбента на его основе.
Представления о природе сорбционного действия силикатов кальция противоречивы. В работах [10-12] показано, что сорбент на основе y-2CaOSiO2 необратимо фиксирует радионуклиды и тяжелые металлы, что подтверждает низкая степень выщелачивания последних из отработанного сорбента. Приведенные в патенте [10] данные о полной обменной емкости свидетельствуют о возможности протекания реакций ионного обмена. По мнению авторов [11, 12], сорбционный процесс реализуется не по механизму ионного обмена, а за счет частичного растворения компонентов сорбента при pH рабочего раствора более 2.
Возможность ионных замещений и регулирования дефектообразования в структуре, например, p-2CaOSiO2 с участием ионов переходных металлов рассмотрена в работе [13] при синтезе фаз клинкера. Механизм взаимодействия силикатов кальция с водными растворами тяжелых металлов и радионуклидов не исследован.
При использовании в качестве сорбента 0-2CaO SiO2 реакции извлечения и связывания токсичных веществ из растворов электролитов конкурируют с реакциями гидратации и твердения (образования цементного камня). В свою очередь, взаимодействие y-2CaO SiO2 с растворами тяжелых металлов не сопровождается процессом твердения. Последнее создает предпосылки для создания на основе y-2CaO SiO2 диффузионно-проницаемого сорбента, удерживающего ионы металлов в широком интервале pH и концентраций растворов электролитов. y-2CaO SiO2 является основной фазовой составляющей саморассыпающихся шлаковых отвалов металлургических производств. Естественное порошкообразное состояние y-2CaO SiO2 и высокая дисперсность продуктов сорбции, к сожалению, ограничивает область технического применения данного материала.
В связи с последним, целью настоящей работы является получение гранулированного сорбента на основе саморассыпающегося шлака и изучение природы его сорбционного взаимодей- ствия с растворами тяжелых металлов. В отличие от порошкообразного, гранулированный сорбент легко отделяется от рабочих растворов сорбируемых веществ, поэтому может использоваться для создания барьеров и фильтров в съемных кассетах.
Для достижения поставленной цели сформулированы следующие задачи:
-
1. Поиск связующего и способа грануляции порошкообразного шлака.
-
2. Обеспечение достаточной прочности гранул при контакте с растворами электролитов в широком интервале pH и концентраций при сохранении высокой пористости в результате низкотемпературного обжига.
-
3. Исследование природы необратимого удерживания ионов металлов гранулированным сорбентом. '
-
4. Изучение возможности активирования сорбционного процесса за счет дополнительных иновалентных катионов в составе сорбента.
-
5. Сохранение диффузионной проницаемости сорбента до полного извлечения ионов металлов из растворов электролитов или максимального насыщения.
Экспериментальная часть
Гранулы сорбента синтезировали из саморассыпающегося шлака (y-2CaOSiO2) с использованием гидроалюмосиликата в качестве связующего. Для обеспечения заданных свойств связующее модифицировано органическими и неорганическими добавками. Грануляцию осуществляли с помощью лабораторного гранулятора. Состав гранул и температура обжига были выбраны таким образом, чтобы при синтезе гранул был сформирован общий каркас. Прочность каркаса, обеспечивающая устойчивость гранул в водных растворах тяжелых металлов, связана с частичным замещением ионов кремния в тетраэдрах SiO/” на ионы алюминия.
Физико-химические характеристики гранулированного сорбента представлены в табл. 1.
Таблица 1 Физико-химические характеристики гранулированного сорбента
|
Форма |
Средний диаметр, мм |
Открытая пористость, % |
Кажущаяся плотность, г/см3 |
Водопогло-щение, % |
^ СЖ. ИСХ / О сж. обрэ МПа |
|
Сферическая |
10-1 |
53-55 |
1,38-1,39 |
39-40 |
8/10 |
Примечание. асж исх - предел прочности при сжатии исходных гранул; а сж о6р - предел прочности при сжатии гранул после контакта с модельным раствором.
Сорбционный процесс изучали в статическом режиме методом ограниченного объема на комплексном модельном растворе тяжелых металлов в воде при соотношении твердое-жидкое 1:10.
Состав модельного раствора приведен в табл. 2. В качестве имитатора радионуклидов использовали ион церия.
Таблица 2
Состав модельного раствора
|
Наименование реагента |
Концентрация реагента, г/л |
|
Се (NO3)3-6H2O |
1 |
|
CuSO4-5H2O |
0,5 |
|
FeCl3 |
1 |
|
NiCl26H2O |
0,25 |
|
pH |
1,85 |
Выбор данного модельного раствора обусловлен тем, что промышленные стоки, содержащие тяжелые металлы и радионуклиды, представляют собой, как правило, кислые водные электролиты, в которых токсичные элементы присутствуют в виде ионов.
Определение концентрации катионов железа, церия, никеля, меди после контакта модельного раствора с гранулированным сорбентом проводили на атомно-эмиссионном спектрометре
OPTIMA 2100 DV через заданные промежутки времени до установления равновесного значения pH раствора.
Коэффициент распределения Кд (мл/г), показывающий избирательность сорбента по отношению к исследуемому веществу при определенном отношении твердое/жидкое, рассчитывали по результатам измерений исходной Со (до сорбции) и равновесной С (после сорбции) концентрации измеряемых элементов в растворе по известной формуле:
где V— объем модельного раствора, мл; т - масса сорбента, г.
Десорбцию составляющих модельного раствора оценивали путем химического анализа дистиллированной воды после выдержки в ней отработанных гранул в течение 30 дней.
Распределение сорбируемых элементов по поверхности гранул, морфологические особенности новообразований, строение и состав реакционной зоны изучали на электронном микроскопе JEOL JSM 648 CLV с приставкой для микрорентгеноспектрального анализа. Фазовый состав сорбента до и после сорбции определяли методом порошковой рентгенографии на дифрактометре ADVANCE D8.
Результаты и их обсуждение
Создание прочной поверхности гранул происходит в результате формирования валентных связей между ионами кристаллической решетки сорбента и ионами сорбируемых веществ с образованием общих структурных элементов.
Гранулированный сорбент благодаря наличию в своем составе катионов Са2+, К+, Na+, А13+, Si4+, Mg2+ представляет собой открытую термодинамическую систему, способную обмениваться с внешней средой веществом и энергией. На основании известных представлений [14-17] о механизме гидратации силикатов кальция, включающих как стадии частичного выщелачивания (переход ионов Са2+ в раствор), так и топохимических процессов взаимодействия Са2+ из раствора с активными центрами поверхности сорбента, можно прогнозировать участие топохимических обменных реакций в процессе сорбции ионов тяжелых металлов и радионуклидов из водных растворов тяжелых металлов, контактирующих с гранулированным сорбентом на основе силикатов кальция.
Действительно, при контакте с кислым модельным раствором тяжелых металлов на границе раздела гранула-раствор возникает градиент pH и разность электрохимических потенциалов, обуславливающие реакционную противодиффузию обменных катионов сорбента и катионов тяжелых металлов. В результате противодиффузии на поверхности гранул формируются неоднородные в химическом и структурном отношении слои новообразований, содержащие в своем составе элементы модельного раствора.
На рис. 1 представлены микрофотографии вида поверхности исходной и гранулы сорбента после контакта с модельными растворами тяжелых металлов в течение 4 часов.

Рис. 1. Электронные микрофотографии, сделанные в режиме упруго рассеянных электронов, поверхности гранул исходного сорбентов (а) и эпитаксиальных пленок на поверхности сорбента после контакта с модельным раствором (6)
В табл. 3 приведен общий химический состав поверхности исходной гранулы и состав характерных поверхностных новообразований.
Таблица 3
Результаты микрорентгеноспектрального анализа
|
Спектр |
С |
О |
Na |
Mg |
Al |
Si |
S |
Cl |
к |
Ca |
Fe |
Ni |
Cu |
Ce |
Сумма |
|
Рис. 1, а |
9,10 |
44,01 |
0,25 |
2,97 |
4,22 |
13,05 |
0,11 |
- |
0,26 |
25,33 |
- |
- |
- |
- |
100,00 |
|
Рис. 1, б |
- |
8,04 |
- |
- |
- |
2,03 |
0,45 |
0,59 |
- |
4,51 |
0,49 |
- |
50,90 |
32,98 |
100,00 |
|
Рис. 2, а |
7,54 |
35,10 |
- |
1,37 |
1,79 |
27,49 |
- |
- |
- |
8,55 |
4,68 |
0,44 |
3,31 |
9,73 |
100,00 |
На поверхности гранул, контактирующих с модельным раствором в течение 4 часов, наблюдаются два характерных вида новообразований: эпитаксиальные пленки и дисперсные конгломераты. По сравнению с исходным элементный состав поверхности меняется неодинаково для разных видов продуктов сорбционного взаимодействия. Эпитаксиальные пленки представляют собой атомные группировки кластерного типа, обогащенные атомами меди и церия. Содержание кислорода, кальция, кремния в составе пленок значительно занижено по сравнению с исходным составом поверхности гранулы.
Эпитаксиальные пленки распределяются по поверхности сорбента и, по-видимому, представляют границу раздела между сорбентом и сорбированными веществами, на которой и происходит формирование конгломератных новообразований. Если медь и церий можно считать пленкообразующими элементами, то никель и железо концентрируются преимущественно в составе конгломератов.
Наблюдаемые после 24 часов выдержки гранулированного сорбента в модельном растворе (рис. 2) трещинообразование и фрагментация пленочного покрытия увеличивают удельную поверхность гранулированного сорбента и тем самым расширяют реакционную зону между сорбентом и рабочим раствором.

Рис. 2. Электронные микрофотографии адсорбированных новообразований, сделанные в режиме упруго рассеянных электронов: дисперсные (а) и фрагментированные (б)
Результаты экспериментов по кинетике сорбционного взаимодействия гранулированного сорбента с модельным раствором показали, что зависимость сорбции от времени имеют немонотонный характер для меди, церия, никеля, в то время как 100 %-ное извлечение железа достигается после 2 часов контакта сорбента с модельным раствором (рис. 3).
Для церия, меди, никеля характерна стадия торможения сорбционного процесса после двухчасовой выдержки гранул в модельном растворе. Временной интервал торможения сорбционного процесса совпадает с торможением изменения pH модельного раствора. Последующее активирование совпадает со стадией трещинообразования и фрагментации пленочного покрытия гранул. Значение Kd, вычисленное при равновесных концентрациях после завершения сорбционного процесса, составили для церия - 5 • 105 мл/г, никеля - 1,2 • 104 мл/г, меди - 2,5 • 104 мл/г.
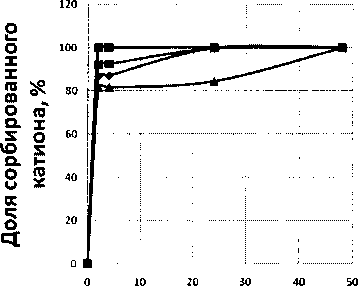
। •' Церий
Н^Медь
Время контакта фаз, час
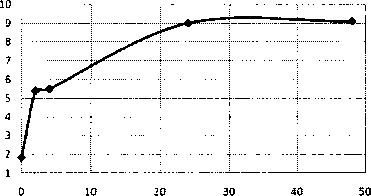
Время контакта фаз, час
а) б)
Рис. 3. Зависимость доли сорбированных катионов (а) и значения pH модельного раствора (б) от времени контакта фаз
На основании полученных данных можно заключить, что процесс сорбции носит топохимический характер, и его элементарные акты связаны с реакциями катионного обмена.
Первичным актом взаимодействия гранулированного сорбента с модельным водным раствором тяжелых металлов является диссоциативная адсорбция воды на активных центрах поверхности гранулированного сорбента. В результате поляризующего влияния ОН" происходит разрыв связи Са-O-Si и перевод Са2+ в раствор. В кислой среде (рН<7) реакция выщелачивания активируется за счет адсорбции Н* на О2" силиката кальция, ослабления связи между Са2+ и О2", делающим переход Са2+ в жидкую фазу более выгодными. В результате образуются катионные вакансии и обогащенный кремнием отрицательно заряженный слой =Si-O“, способный химически взаимодействовать не только с ионами Са2+ через гидроксильную оболочку, но и с ионами тяжелых металлов, присутствующими в растворе электролита. Движущей силой массопереноса ионов из раствора электролита к поверхности гранулированного сорбента является разность электрохимических потенциалов, в результате которой катионы тяжелых металлов занимают освободившиеся после выщелачивания Са2+ вакантные позиции, обеспечивая электронейтральность алю-мокремнекислородного каркаса.
Основные обменные реакции Са2+<->Си2+; ЗСа2+<-»2Се3+; Ca2+<->Ni2+; ЗСа2+<->2Ре3+ приводят к сохранению структурной устойчивости алюмокремнекислородного каркаса и образованию пленочных гидросиликатов тяжелых металлов, играющих роль эпитаксиальной границы раздела между сорбентом и раствором сорбируемых веществ.
Для эффективного массопереноса при реакционной диффузии необходимо наличие как катионных, так и анионных вакансий. Для ускорения диффузии и массопереноса по вакансионному механизму при разработке состава гранулированного сорбента предусмотрена возможность химического регулирования дефектообразования. Наличие в составе сорбента дополнительных к Са2+ обменных катионов К+, Na+, А13+, иновалентных по отношению к сорбируемым катионам, приводит к образованию в реакциях катионного обмена с тяжелыми металлами стехиометрического количества вакансий как в катионной, так и анионной подрешетках. Процесс необратимой сорбции реализуется по комплексному механизму реакционной диффузии, ускоряемой реакциями дефектообразования.
Представления об активировании сорбционного взаимодействия находят подтверждение при сопоставлении результатов исследования кинетики сорбции, изменения pH модельного раствора в процессе контакта с гранулами сорбента и данных электронно-микроскопического анализа морфологических особенностей и состава продуктов сорбционного взаимодействия.
Кластерные эпитаксиальные пленки не содержат видимых дефектов (сколов, трещин). На данной стадии сорбционный процесс контролируется на границе раздела сорбента и сорбата, при этом скорость его пропорциональна активной поверхности, не вступившей в реакцию [18]. Формирование пленочного продукта сорбции, а также исчерпывание первичных поверхностноактивных центров, приводит к торможению реакции выщелачивания, и тем самым - к торможению реакций катионного обмена.
При более длительной выдержке гранулированного сорбента в модельном растворе увеличение внутренних напряжений в эпитаксиальных пленках приводит к трещинообразованию и их фрагментации. В результате увеличивается поверхность, доступная для сорбционного взаимодействия, появляются вторичные активные центры, активируются реакции выщелачивания и катионного обмена.
По данным рентгенофазового анализа выпадающие из модельного раствора осадки не содержат токсичных металлов. В составе осадков рентгенографически идентифицируются: CaSO4, Са(ОН)2, СаСОз, NaCI, СаС12, Fe2O3.
Следует отметить, что основные фазовые составляющие исходных веществ сохраняются в составе гранулированного сорбента до и после завершения сорбционного процесса (табл. 4).
Таблица 4
Дифракционные характеристики основных фазовых составляющих гранулированного сорбента
|
№ п/п |
Характеристика объекта |
Основные фазовые составляющие |
Межплоскостные расстояния d, A |
|
1 |
Саморассыпающийся шлак металлургического производства |
2СаО-А12О3 ■ SiO2 у 2CaOSiO2 3CaOMgO-2SiO2 |
2,85; 3,06; 2,72 2,74; 3,01; 2,66 2,84; 2,74 |
|
2 |
Гранулы сорбента |
2CaOAl2O3SiO2 у 2CaOSiO2 3CaOMgO-2SiO2 |
2,85; 3,06; 2,72 2,74; 3,01; 2,66 2,84; 2,74 |
|
3 |
Гранулы сорбента после контакта с модельным раствором |
2CaO ■ А12Оз ■ SiO2 у 2CaOSiO2 3CaOMgO-2SiO2 |
2,85; 3,06; 2,72 2,74; 3,01; 2,66 2,84; 2,74 |
Выводы
-
1. Структурная устойчивость кальций-алюмокремнекислородного каркаса обеспечивается, по-видимому, замещением Са2+ стехиометрическим количеством катионов тяжелых металлов.
-
2. Особенностью механизма необратимой сорбции тяжелых металлов гранулированным сорбентом является многостадийность процесса, включающая ряд последовательных и параллельных стадий:
-
а) диссоциативная двухточечная адсорбция воды на активных центрах поверхности гранулированного сорбента;
-
б) переход Са2+, Na+, К+ в раствор с образованием катионных вакансий;
-
в) противодиффузия катионов Се3+, Cu2+, Ni2+, Fe3+ с образованием на поверхности сорбента эпитаксиальных пленок;
-
г) торможение реакции катионного обмена, осаждение на поверхности гранулированного сорбента гидроалюмосиликатов кальция, в которых катионные позиции частично замещены сорбированными элементами;
-
д) трещинообразование и фрагментация пленочных новообразований, увеличение удельной поверхности, появление вторичных активных центров, расширение реакционной зоны;
-
е) активирование реакций выщелачивания и реакций катионного обмена;
-
д) взаимодействие Са2+ с анионами в растворе с образованием солей кальция, гидроксида и карбоната кальция.
-
3. Внедрение катионов тяжелых металлов в решетку силикатов и алюмосиликатов кальция без изменения структурных параметров обуславливает необратимость сорбционного процесса и механическую устойчивость гранул в агрессивных растворах, так как катионы Се3+, Cu2+, Ni2+, Fe3+, замещая обменные катионы Са2+, Na+, К+, обеспечивают устойчивость алюмокремнекисло-родного каркаса.
Работа проведена при поддержке Федеральной целевой программы «Научные и научнопедагогические кадры инновационной России» на 2009-2013 годы», конкурс №НК-409П, государственный контракт №П2268.
Список литературы Особенности необратимой сорбции катионов тяжелых металлов гранулированным сорбентом на основе силикатов и алюмосиликатов кальция
- Glasser, F.P. Environmental uses of cement in waste conditioning Proceedings of the sixth/F.P. Glasser//Engineering foundation Conference «Advances in cement and concrиte», Durham. -1994. -P. 499-507.
- Bonen, D. The present state-of-the-art of immobilization of hazardous heavy metals in cement-based material/D. Bonen, Sh.L. Sarcar//Engineering foundation Conference «Advances in cement and concrete», Durham. -1994. -P. 481-498.
- Glasser, F.P. Application of cements to the treatment and conditioning of toxic wastes/F.P. Glasser//Proceedings 9 International Congress on the chemistry of cement, New Delhi. -1992. -Vol. 6. -P. 114-118.
- Grutzeck, M.W. Hazardous waste (organic heavy metal): cement disposal/M.W. Grutzeck//Proceedings 9 International Congress on the chemistry of cement, New Delhi. -1992. -Vol. 6. -P. 119-125.
- Rossoty, V. Inertization of toxic metals in cement matrices: effects on hydration setting and hardening/V. Rossoty, F. Medicu//Cement and Concrete Research. -1995. -Vol. 25, № 6. -P. 1147-1152.
- Sprung, S. Spurenelemente-Arneichrung und Minderungsmassanahmen/S. Sprung//Zement-Kalk-Gips. -1988. -№ 5. -P. 251-257.
- Коугия, M.B. Использование цемента для связывания отходов, содержащих тяжелые металлы/М.В. Коугия//Цемент и его применение. -2000. -№ 4. -С. 37-39.
- Овчаренко, Г.И. Цеолиты в строительных материалах/Г.И. Овчаренко, В.Л. Свиридов. -Барнаул: Изд-во АлтГТУ, 1995. -102 с.
- El-Korashy, S.A. Synthetic Crystalline Calcium Cilicate Hydrate (I): Cation Exchange and Caesium Selectivity/S.A. El-Korashy//Monatshefte für Chemie. -2002. -Vol. 133. -P. 333-343.
- Пат. 2230609 Российская Федерация. Сорбент на основе силикатов кальция/И.Ю. Пашкеев, И.А. Семенова, Г.Г. Михайлов и др.; заявитель и патентообладатель Южно-Уральский государственный ун-т. -№ 2003111532/15; заявл. 21.04.2003; опубл. 20.06.2004, Бюл. № 17. -4 с.
- Пат. 2297275 РФ. Способ извлечения ионов металлов из водных растворов/Е.В. Поляков, Н.М. Барышева, Г.П. Швейкин и др.; заявитель и патентообладатель Государственной учреждение «Институт химии твердого тела» Уральского Отделения российской Академии наук. -№ 2005118547/15; заявл. 20.12.2006; опубл. 20.04.2007, Бюл. № 11. -4 с.
- Пат. 2330340 Российская Федерация. Способ извлечения радионуклидов из водных растворов/E.H. Аврорин, В.Г. Бамбуров, Н.М. Барышева и др.; заявитель и патентообладатель Федеральное государственное предприятие «Российский Федеральный ядерный центр -Всероссийский научно-исследовательский институт технической физики им. академика Е.И. Забабахина (ФГУП РФЯЦ-ВНИИТФ)». -№ 2006107769/06; заявл. 27.09.2007; опубл. 27.07.2008, Бюл. № 21. -5 с.
- Беляков, A.B. Полиморфизм в двухкальциевом силикате и вакансии по кислороду/A.B. Беляков//Цемент и его применение. -1999. -№ 1. -С. 27-31.
- Сычев, М.М. Проблемные вопросы гидратации и твердения цементов/М.М. Сычев//Цемент и его применение. -1986. -№ 9. -С. 11-14.
- Шабров, A.A. Эволюция активных центров в процессе твердения вяжущих веществ/A.A. Шабров, М.С. Гаркави//Цемент и его применение. -2000. -№ 1. -С. 17-19.
- Бабушкин, В.И. О некоторых новых породах к использованию методов термодинамики в решении проблем технологии вяжущих и бетона/В.И. Бабушкин//Цемент и его применение. -1999. -№ 3. -С. 50-56.
- Школьник, Я.Ш. О механизме формирования гидросиликатов кальция/Я.Ш. Школьник//Цемент и его применение. -1983. -№ 1. -С. 19-21.
- Третьяков, Ю.Д. Твердофазные реакции/Ю.Д. Третьяков. -М.: Химия, 1978. -360 с.


