Особенности окисления трехкомпонентных сплавов на основе системы железо-никель-кобальт
Автор: Биронт В.С., Дроздова Т.Н., Блохин И.В., Лындина Е.Н., Якимов И.С., Пономарева С.В., Гусев А.О., Симаков Д.А.
Журнал: Журнал Сибирского федерального университета. Серия: Техника и технологии @technologies-sfu
Статья в выпуске: 2 т.2, 2009 года.
Бесплатный доступ
В статье рассмотрены закономерности процессов окисления трехкомпонентных сплавов системы Fe - Ni - Co. Показано, что состав оксидов определяется преимущественно химическим составом сплавов. В меньшей степени состав оксидов зависит от температурно-временных режимов окислительной обработки. Установлен состав сплава и режим его окисления, обеспечивающие получение в составе оксидов 97,5 % оксида типа NiFe2O4. Показано, что в присутствии в составе сплавов кобальта в пределах исследованной области составов сплавов уменьшается вероятность формирования оксида никеля NiO. При этом никель в составе сплавов преимущественно расходуется на образование оксидов с железом и кобальтом типа NiFe2O4, NiCo2O4 и некоторых других.
Система железо-никель-кобальт, оксиды, окислительный отжиг, фазовые переходы, условия окисления
Короткий адрес: https://sciup.org/146114491
IDR: 146114491 | УДК: 669.295
Features of the oxidation of three-components alloys on the basis of the iron-nickel-cobalt system
The article deals with characteristics of oxidation of three-component alloy of the Fe - Ni - Co system. We demonstrate that the oxides composition is determined by the chemical composition of alloys primarily. To a lesser extent, oxides composition depends on the temperature-time profiles of oxidative treatment. Identified alloys composition and of oxidation Technology its, to obtain in the composition of oxides 97.5% oxide type NiFe2O4. It has been shown that the presence of cobalt in the alloys, within the investigated area of the alloy, decreases the likelihood of forming of nickel oxide NiO. This nickel in the alloys composed mainly spent on formation with iron oxide and cobalt-type NiFe2O4, NiCo2O4 and some others.
Текст научной статьи Особенности окисления трехкомпонентных сплавов на основе системы железо-никель-кобальт
Высокотемпературная коррозионная стойкость (жаростойкость) многокомпонентных сплавов в существенной степени определяется природой оксидных пленок, формирующихся на их поверхности как при предварительном окислительном отжиге, так и при эксплуатационных нагревах в окислительных средах. Роль наносимой оксидной пленки в качестве фактора, определяющего стойкость к высокотемпературному коррозионному разрушению поверхности, существенным образом зависит от ее строения, плотности, пористости, химического состава, предыстории образца, методов механической обработки поверхности и других обстоятельств.
Такими обстоятельствами, например, могут стать: химический состав окисляемого материала, а следовательно, химический состав пленки и технология ее получения, в том числе температурно-временные режимы окислительной обработки.
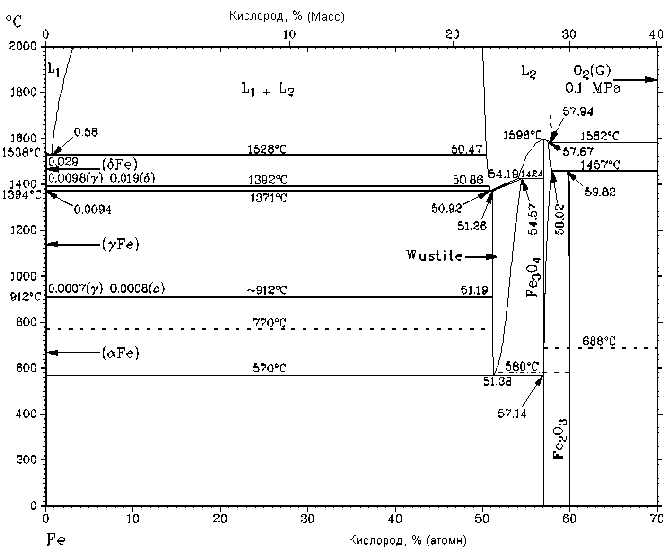
Рис.1. Диаграмма фазового равновесия в системе Fe-O [2]
Имеющиеся сведения об использовании жаростойких многокомпонентных сплавов в качестве малорасходуемых металлических конструкций в металлургических агрегатах, например инертных металлических анодов, свидетельствуют о том, что в поверхностных слоях таких изделий самообновляющиеся оксидные слои могут формироваться в ходе окислительных процессов, в т.ч. анодных электрохимических реакций, протекающих на поверхности сплавов. Формирующиеся непрерывно в процессах эксплуатации оксидные пленки фактически и являются рабочей поверхностью таких конструкций. В таком случае задача поиска новых конструкционных материалов для коррозионно-стойких конструкций сводится к задаче поиска таких металлических систем, окисление которых в условиях эксплуатации будет приводить к формированию на поверхности оксидных пленок такого состава и строения, которые обеспечивали бы оптимальную скорость окисления и наименьшую возможную скорость разрушения металлической основы. Управлять процессами формирования оксидных пленок можно лишь после установления объективных закономерностей процессов окисления, включая фазовые превращения в оксидных пленках, и определения количественных соотношений в сложных смесях образующихся оксидов, в зависимости от состава окисляемых сплавов и температурных условий окисления. При этом важно знать, при каких соотношениях основных компонентов в сплавах будут создаваться условия для формирования оксидных пленок заданного состава и строения, например, пленок типа NiFe2O4, которые, как известно [1], характеризуются наибольшей устойчивостью в электролитных расплавах. Одной из перспективных систем для создания жаростойких сплавов для сложных условий эксплуатации является система железо-никель-кобальт.
Формирование оксидных фаз на основе отдельных чистых компонентов этой системы достаточно полно исследовано, что выражается наличием построенных диаграмм со-– 140 – стояния металл-кислород. Наиболее подробно исследовано окисление в системе железо-кислород (рис. 1).
В соответствии с приведенной фазовой диаграммой, фазовые превращения в оксидных фазах на основе железа протекают при 570, 580, 688 °С и других значениях температуры. Аналогичные сведения можно получить из анализа диаграмм никеля и кобальта с кислородом. Известны оксиды никеля NiO, кобальта: CoO, Co2O3, Co3O4, которые могут иметь различные кристаллографические модификации. Формирование оксидов в трех и более многокомпонентных системах происходит более сложно, поскольку, кроме двойных оксидов, в этом случае образуются комплексные двух-, трехкомпонентные оксиды, смеси оксидных частиц [3; 4].
При этом количественные соотношения между металлическими компонентами в оксидах определяются не только соотношением этих компонентов в сплаве, но и различной способностью их к взаимодействию с кислородом (различным сродством к кислороду).
Фазовые переходы в оксидах
Наиболее объективные сведения о критических точках фазовых переходов в оксидах и металлической основе можно получить экспериментальными методами, которыми в первую очередь являются методы термического анализа и, в частности, методы дифференциальной сканирующей калориметрии (ДСК), термогравиметрии (ТГА). Для систем, содержащих ферромагнитные составляющие, существенные результаты могут быть получены при сочетании термогравиметрии с магнитным анализом таких систем (ТГМА). На первом этапе исследований этими методами проведено изучение процессов образования оксидных пленок на поверхности чистых металлов и фазовых переходов в них при непрерывном изменении температуры, а также при изотермических выдержках.
Исследования проведены на установке STA 449 Jupiter, позволяющей в режиме синхронных измерений определять изменение массы вещества с разрешающей способностью 0,1 мкг, измерять температуру с точностью до 0,1 °С, с возможностью оценки первой и второй производных, а также с абсолютной точностью отслеживать развивающиеся превращения с выделением или поглощением теплоты и изменением массы.
На рис. 2 приведены кривые ДСК и ТГА компактных микрообразцов (масса 200 мг) из чистого железа, никеля и кобальта, снятые при нагреве в интервале температур от 100 до 1000 °С в воздушной среде при атмосферном давлении.
Наименьшие экзотермические эффекты, относящиеся к образованию оксидов при взаимодействии металлов с кислородом, имеет никель (верхняя сиреневая ДСК-кривая). Это характеризует наибольшую коррозионную устойчивость никеля по сравнению как с железом, так и с кобальтом. Наиболее высокую коррозионную стойкость никеля подтверждает также сравнение термогравиметрических кривых (ТГ-кривых). В отличие от кобальта и железа, у никеля во всем интервале температур от 100 до 700 °С прироста массы не наблюдается.
При температурах 700 - 1000 °С прирост массы не превышает одного процента. Наименьшей коррозионной стойкостью из трех сравниваемых металлов характеризуется железо. Кобальт занимает промежуточное положение. Наиболее сложный характер ТГ-кривой для железа связан со сложной последовательностью окислительных процессов, включающих как экзотермические, так и эндотермические стадии. Характерные на ДСК-кривой для железа температу-
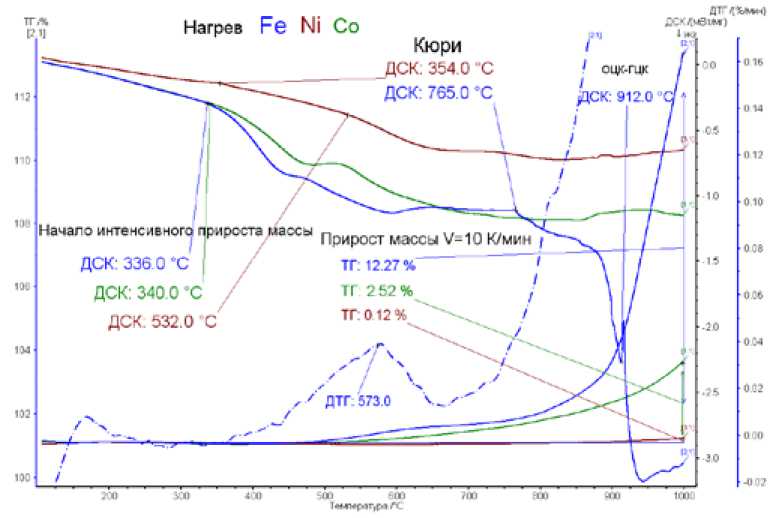
Рис. 2. Кривые ДСК (верхние линии) и ТГА (нижние) микрообразцов железа, никеля и кобальта ры 336, 439, 588 и 877 °С, отвечающие различным стадиям развития окислительных процессов. Причины появления этих температурных точек еще требуют дальнейшего изучения, однако можно полагать, что их наличие обусловлено как взаимодействием железа в различных аллотропических формах (а или у) с кислородом, так и фазовыми превращениями в оксидных пленках, которые могут иметь строение вюстита (FeO), магнетита (Fe3O4) или гематита (Fe2O3).
Нами изучен фазовый переход в оксидной пленке малоуглеродистой стали в области прямого и обратного эвтектоидного превращения в системе железо-кислород при температуре 570 °С.
Показано (рис.3), что в условиях переохлаждения (565 °С) эвтектоидное превращение высокотемпературного оксида FeO сопровождается появлением ферромагнитных свойств исследуемой микропробы, что связано с образованием кристаллов свободного железа в результате развития указанного превращения:
FeO ^ Fe + Fe3O4.
Кобальт проявляет ряд критических точек, аналогично железу, поскольку ему присущи аналогичные три формы оксидов. Однако их проявление сдвинуто относительно точек железа в сторону более высоких температур.
Использование термогравиметрического анализа позволило установить значения критических точек, соответствующих фазовым превращениям в оксидных пленках, образованных на поверхности сплавов различного химического состава (табл. 1).
Множественность значений критических точек для каждого из исследованных составов сплавов (особенно при охлаждении) обусловлена присутствием в составе оксидных пленок, образующихся на их поверхности, разного количества оксидов различного химического состава.
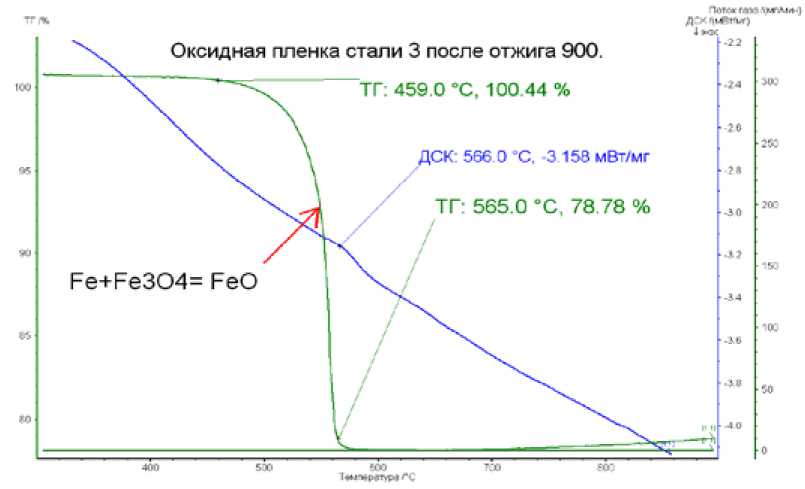
Рис. 3. Кривые ДСК (синяя линия) и ТГМА (зеленая) микрообразцов оксидов железа, отобранных от пленки (окалины), которая получена при высокотемпературном окислительном отжиге (950 °С) малоуглеродистой стали (Ст3)
Таблица 1. Значения температур критических точек превращений в оксидах сплавов системы Fe – Ni – Co
|
№ сплава |
Химический состав сплава |
Температура превращений в оксидных пленках, ºС |
|
|
При нагреве |
При охлаждении |
||
|
1 |
80Fe – 16Ni – 4Co |
336 842,1 – 852,9 874,4 – 874,6 |
866,4 857 833,5 |
|
3 |
71Fe – 14Ni – 15Co |
489 881,3 – 882,6 |
857,2 848,3 828,1 447,6 |
|
6 |
60Fe – 20Ni – 20Co |
- |
847 834 |
|
7 |
50Fe – 42Ni – 8Co |
531 – 536 845,5 – 847,5 |
859,8 840,1 |
|
9 |
50Fe – 24Ni – 26Co |
770,2 – 774,2 |
810,1 |
|
11 |
33Fe – 33Ni – 34Co |
301 – 347 811 – 836 |
- |
|
13 |
10Fe – 10Ni – 80Co |
828,9 – 830,9 |
821,3 – 822,2 |
|
15 |
55Fe – 28Ni – 15Co – 3Sn |
815,1 – 841,7 |
- |
|
16 |
44Fe – 46Ni – 10Co |
845,7 |
- |
Фазовый состав оксидов в сплавах
Изучение фазового состава оксидов, образующихся при термическом окислении, проведено на сплавах 16 составов системы Fe-Ni-Co, распределенных на концентрационном треугольнике системы. Для исследования выбраны сплавы от высокожелезистых до высококобальтовых, с различным содержанием никеля. Химический состав исследованных сплавов представлен в табл. 2.
В этой же таблице представлены режимы термического окисления выбранных для изучения сплавов.
Для реализации порошковой методики количественного рентгенофазового анализа образцы готовились путем предварительного получения опилок металлических образцов сплавов каждого химического состава с помощью мелкого напильника. Размер частиц от 50 до 200 мкм. Режимы термического окисления подбирались таким образом, чтобы при использовании максимальных температур и длительностей обработки внутри частиц сохранялось некоторое количество металлической основы. При этих условиях анализируемые оксиды могут моделировать составы оксидных слоев, формирующихся на поверхности изделий в виде пленок.
Для окисления опилки на керамической подставке помещались в печь с окислительной атмосферой, нагретой до температуры окисления. В первой серии экспериментов все сплавы окислялись при 650 °С с длительностью 180 мин., во второй – по разным температурновременным схемам: от 650 до 870 °С с длительностью от 180 до 60 мин., в третьей – все сплавы по единой методике: 950 °С с длительностью 30 мин. Кроме того, сплавы № 12 и 13 окисляли при 1100 °С с длительностью выдержки 15 мин. После завершения выдержки образцы быстро охлаждались на воздухе путем извлечения подставки с оксидами из печи. Таким образом, обеспечивались условия, исключающие развитие фазовых превращений в оксидах, что позволяет судить о составах оксидов, непосредственно образующихся в результате окисления при заданных температурных режимах эксперимента. Полученные крупнопорошковые пробы не подвергались тщательному перетиранию (размолу), что позволило уменьшить долю вторичного рентгеновского излучения от металлической основы порошков и увеличить вклад отражений от оксидных пленок, образованных на поверхности частиц порошка.
Рентгенофазовый анализ проводили на дифрактометре Шимадзу. Дифрактограммы расшифровывали полуавтоматическим компьютерным методом с использованием известных банков эталонных дифрактограмм.
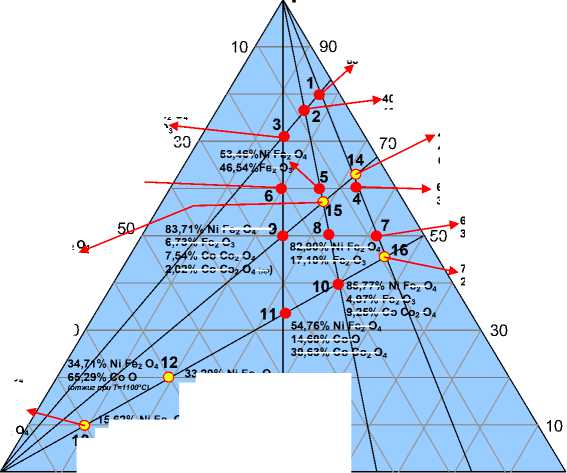
Систематические сведения о составе оксидных фаз, образующихся в результате окисления при указанных выше температурно-временных условиях в зависимости от химического состава сплавов, приведены на рис. 4-6. Все сведения о количестве индивидуальных оксидов в оксидных продуктах, полученные рентгенофазовым методом и представленные на рис. 4-10, выражены в массовых процентах.
Температурные режимы изменяют не только количественные соотношения между оксидами, соответствующими тому или иному химическому составу сплавов, но также в ряде случаев изменяют состав и кристаллографическую форму образующихся оксидов.
Сравнение сведений о составе оксидных фаз, образующихся в сплавах тройной системы Fe-Ni-Co, показывает, что формирование тройного оксида типа NiFe2O4 происходит преимущественно в области составов сплавов 8,9,10, где количество этого оксида превышает 80 %. При – 144 –
Таблица 2. Температурные режимы окислительного нагрева опилок из сплавов системы Fe – Ni – Co для изучения фазового состава оксидов, образующихся при различных температурах и разном составе сплавов
|
№ сплава |
Состав сплава |
Температура и длительность термообработки образцов опилок в трех сериях эксперимента |
||
|
1-я серия |
2-я серия |
3-я серия |
||
|
1 |
80Fe – 16Ni – 4Co |
650 °С, 180 мин. |
710 °С,120 мин. |
950 °С, 30 мин. |
|
2 |
76Fe – 15Ni – 9Co |
650 °С, 180 мин. |
710 °С,120 мин. |
950 °С, 30 мин. |
|
3 |
71Fe – 14Ni – 15Co |
650 °С, 180 мин. |
650 °С, 180 мин. |
950 °С, 30 мин. |
|
4 |
60Fe – 33Ni – 7Co |
650 °С, 180 мин. |
800 °С, 90 мин. |
950 °С, 30 мин. |
|
5 |
60Fe – 27Ni – 13Co |
650 °С, 180 мин. |
750 °С, 90 мин. |
950 °С, 30 мин. |
|
6 |
60Fe – 20Ni – 20Co |
650 °С, 180 мин. |
650°С, 180 мин. |
950 °С, 30 мин. |
|
7 |
50Fe – 42Ni – 8Co |
650 °С, 180 мин. |
800 °С, 90 мин. |
950 °С, 30 мин. |
|
8 |
50Fe – 33Ni – 17Co |
650 °С, 180 мин. |
800°С, 90 мин. |
950 °С, 30 мин. |
|
9 |
50Fe – 24Ni – 26Co |
650 °С, 180 мин. |
750°С, 90 мин. |
950 °С, 30 мин. |
|
10 |
40Fe – 40Ni – 20Co |
650 °С, 180 мин. |
870 °С, 60 мин. |
950 °С, 30 мин. |
|
11 |
33Fe – 33Ni – 34Co |
650 °С, 180 мин. |
870 °С, 60 мин. |
950 °С, 30 мин. |
|
12 |
20Fe – 20Ni – 60Co |
650 °С, 180 мин. |
870 °С, 60 мин. |
950 °С, 30 мин. |
|
13 |
10Fe – 10Ni – 80Co |
650 °С, 180 мин. |
870 °С, 60 мин. |
950 °С, 30 мин. |
|
14 |
61Fe – 31Ni – 6Co – 2Sn |
650 °С, 180 мин. |
800 °С, 90 мин. |
950 °С, 30 мин. |
|
15 |
55Fe – 28Ni – 15Co – 3Sn |
650 °С, 180 мин. |
750 °С, 90 мин. |
950 °С, 30 мин. |
|
16 |
44Fe – 46Ni – 10Co |
650 °С, 180 мин. |
800 °С, 90 мин. |
950 °С, 30 мин. |
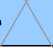
Рис. 4. Состав оксидных фаз, образующихся в результате окисления при 650 ºС, 3 ч (первая серия экспериментов), в зависимости от химического состава сплавов. Для сплавов 12 и 13, кроме того, приведены сведения об оксидах после нагрева до 1100 ºС, 10 мин.
7,41% Ni Fe 2 O 4
3,87% Fe 2 O 3
3,54% Fe 3 O 4
77,88% Co O
7,30% Co Co 2
(отжиг при Т=1100оС)
Fe
57,56% Ni Fe 2
35,99% Fe 2 O 3
6,44% Ni 3 Sn
74,56% Ni Fe 2 O 4
17,67% Fe 2 O 3
7,76% Co Fe 2 O 4
68,85% Ni Fe 2 O 4
31,15% Fe 2 O 3
71,19% Ni Fe 2 O 4
28,81% Fe 2 O 3
45,24% Ni Fe 2 O 4
48,50% Fe 2 O 3
6,26% Ni 3 Sn
49,03% Ni Fe 2 O 4
50,97% Fe 2 O 3
64,62% Ni Fe 2 O 4
35,38% Fe 2 O 3
46,54% Ni Fe 2 O 4 0,48% Fe 2 O 3
12,99% CoFe 2 O 4
59,23%Ni Fe 2 O 4
40,77%Fe 2 O 3
3,29% Ni Fe 2 O 4
31,64% Co O
35,07% Co Co 2 O 4
5,62% Ni Fe 2 O 4
82,90% Ni Fe 2 O
17,10% Fe 2 O 3
i Fe2 O e2 O i Fe2 O4 9
6,73% Fe 2 O 3
% Co Co 2 O
,02% Co Co
4 (др )
85,77%
Fe2 O
4,97% Fe 2 O 3
9,25% Co
2 O e2 O
14,60% Co O
30,63% Co Co 2 O
53,46%
Co 10
46,74% Co O
13 37,64% Co 3 O 4
Ni
Fe
(710 о С;
2ч)
68% Fe 2 O 3
8,8% Fe 2 O 3
2,5% Fe O
20,7% Ni Fe 2 O 4
(650 о С;
3ч) 36,4% Fe z O 3
63,6% Ni Fe 2 O 4
(710 оС;
(750 оС;
(800 о С;
Ni, Fe) Fe 2 O 4
(870 ^С;
1^г % Fe z
97,3% ( Ni,
e) Fe 2 O 4
2ч)7 о Fe 2 O 3
10,9% Fe 2 O 3
26,1% Ni Fe 2 O 4
1,5^) 9,3% Fe 2 O 3
50,7% ( Ni, Fe) Fe 2 O 4 (750 оС;
1,5ч)
37,4% Fe 2 O 3
60,8% ( Ni, Fe) Fe 2 O 4
1,8% Sn O 2
(750 о С;
1,5ч)
6,3% Fe 2 O 3
81,4% ( Ni, Fe) Fe 2 O 4
12,3% Co Co 2 O 4
(870 оС;
1ч)
0,7% Fe 2 O 3
1,1% ( Ni, Fe) Fe 2 O
25,1% Ni Co 2 O 4
23,2% Co O
42% Co Co 2 O 4 8% Co 3 Fe 7
Co
(750 о С; 1,5ч)
61,4% Fe 2 O 3
37% ( Ni, Fe) Fe 2 O 4
1,6% Sn O 2
(870 оС; 1ч)
62,3% Fe 2 O 3
36,2% ( Ni, Fe) Fe 2 O 4
1,5% Sn O 2
(800 оС; 1,5ч)
57,8% Fe 2 O 3
40,6% ( Ni, Fe) Fe 2 O 4
1,6% Sn O 2
(870 оС; /\ /
1ч) % Fe2 O3 \ /
9,7% Fe 3 O 4
10,2% ( Ni, Fe) Fe 2 O 4
15,7% Co Ni O 2
20,9% Co O 37% Co Co 2 O 4
(870 оС;
9,7% Fe 2 O 3
34,5% Ni Fe 2 O 4
32,6% Ni Co 2 O 4
15,4% Co Ni
7,9% Co O
(800 оС;
1,5ч)
48,2% Fe 2 O 3
51,8% ( Ni, Fe) Fe 2 O 4
(800 оС;
1,5ч)
42% Fe 2 O 3
58% ( Ni, Fe) Fe 2 O 4
(800 оС;
^ 1,5ч)
26,1% Fe 2 O 3
30 73,9% ( Ni, Fe) Fe 2 O 4
Ni
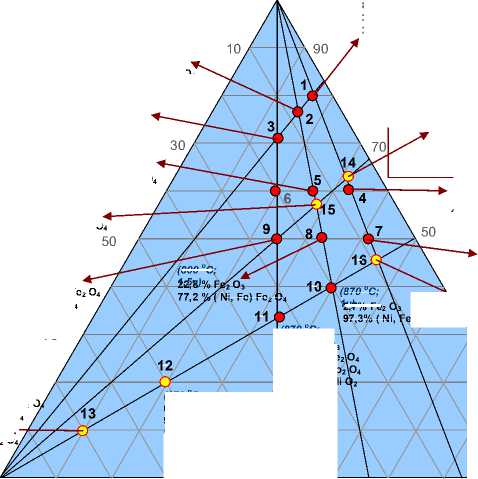
Рис. 5. Состав оксидных фаз, образующихся в результате окисления при температурах от 650 до 870 ºС (вторая серия экспериментов) в зависимости от химического состава сплавов
Fe
85,7% Ni 0.6 Fe 2.4 O 4
59% (Ni,Fe)Fe 2 O 4
6,9% Fe 2 O 3
7,4% Co O
29,9% Fe 2 O 3
3,9% Fe 2 O 3
7,2% Ni O
36,9% (Ni,Fe)Fe 2 O 4
51% Fe 2 O 3
7,6% Fe 2 O 3
4,4% Ni O
18,7% (Ni,Fe)Fe 2 O 4
59,6% Fe 2 O 3
12,7% Fe 2 O 3
5,3% Co Fe 2 O 4
3,7% Ni O
56,5% CoO
43,5% Co 3 O 4
89,4% e2 O
87,3% (Ni,Fe)Fe2 O
4,3% Fe
8,5% Co O
42,8% (Ni,Fe) Fe2 O
43,8% (Ni,Fe)Fe 2 O 4
41,3% Fe 2 O 3
6,3% Fe 2 O 3
3,0% Ni Co 2 O 4
5,7% Ni O
50 70,2%(Ni,Fe)Fe 2 O 4
19,2%Fe 2 O 3
2,8%NiO
7,8%CoO
13,9% (Ni,Fe)Fe 2 O 4
4% Fe 2 O 3
75,1% Co O
7% Co Co 2 O 4
,5% (Ni,Fe)Fe 2 O 4
6,8% Fe 2 O 3
79,4% Co O
6,3% Co Co 2 O 4
19,3% Fe 2 O 3
4,8% Fe 2 O 3 33% Co O
Отжиг при Τ=950 оС; τ = 30 мин
28% (Ni,Fe)Fe 2 O 4
58% Fe 2 O 3
8,8% Fe 2 O 3
5,2% Ni O
56,4% (Ni,Fe)Fe 2 O 4
31,5% Fe 2 O 3
7,5% Fe 2 O 3
4,6% Ni O
76,9% (Ni,Fe)Fe 2 O 4
17,9% Fe 2 O 3
3% Ni O
2,2% Co O
76,2% (Ni,Fe)Fe 2 O 4
17,8% Fe 2 O 3
4,2% Ni O
1,9% Co O
7_26 31,1%Ni Fe 2 O 4 27,5%Fe .942 O 19,1%Fe 3 O 4 16%Ni O 6,3%CuO
76,0 % (Ni,Fe)Fe 2 O 4
8,3 % Fe 2 O 3
10,9 % Ni O
4,8 % Co O
Co
Ni
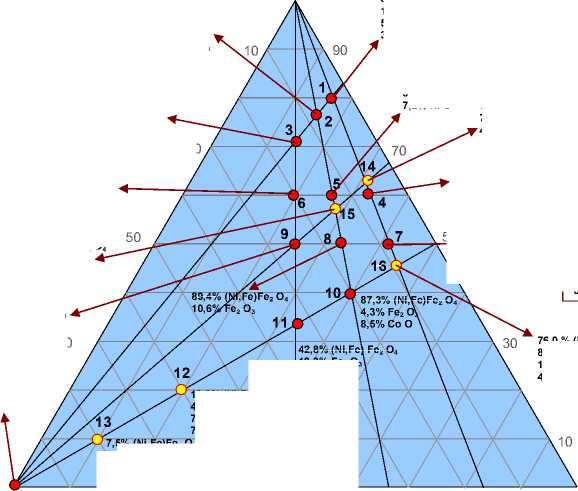
Рис. 6. Состав оксидных фаз (третья серия экспериментов), образующихся в результате окисления при температуре 950 ºС 30 мин, в зависимости от химического состава сплавов температуре окислительного отжига 870 ºС в сплаве 10 количество такого оксида достигает 97,3 %.
При приближении к концентрационным углам диаграммы (при увеличении количества того или иного компонента в сплавах) нарастает количество индивидуальных оксидов на основе этих компонентов. Такими основными оксидами являются: для железа – Fe2O3, для кобальта – CoO, для никеля – NiO. С повышением температуры окисления увеличивается количество таких индивидуальных оксидов вблизи соответствующих углов диаграммы. При температурах окислительного отжига ниже 870 ºС ни в одном из исследованных сплавов не образуется оксид никеля (NiO). Этот оксид обнаруживается только после отжига 950 ºС. Причем даже в самом высоконикелевом из исследованных сплавов (16-м) количество NiO составляет только 10,9 %.
Таким образом, в присутствии кобальта в системе основными оксидными фазами становятся тройные оксиды типа NiFe 2 O 4 с различным соотношением между железом и никелем (NixFe2-xO4). Такие оксиды присутствуют во всех исследуемых сплавах, окисленных при всех изученных температурных режимах, количество которых уменьшается по мере отклонения от составов, отвечающих сплавам 8, 9ф и 10 во всех направлениях изменения концентраций на концентрационном треугольнике.
В порядке возрастания способности сплавов к формированию оксидов типа NiFe2O4 сплавы можно выстроить в ряд: 1-2-14-3-4-15-5-6-7-16-8-9-10. Дальнейшее продолжение этого ряда: 10-11-12-13, определяет уменьшение количества оксида NiFe2O4 и рост количества оксида кобальта CoO (рис. 7, 10).
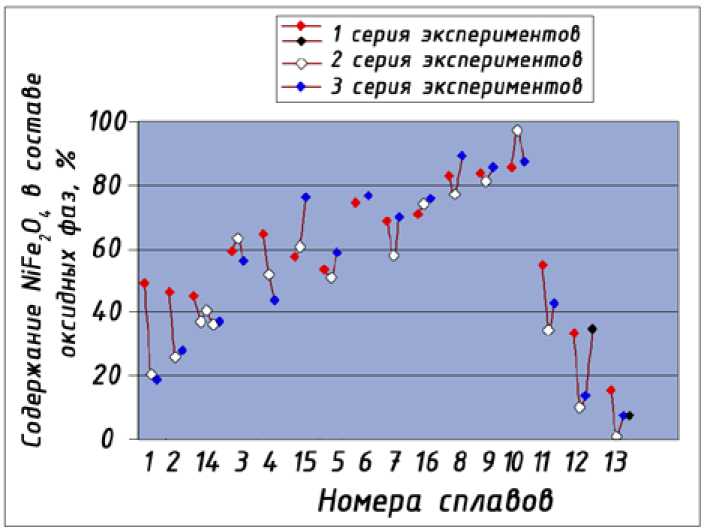
Рис. 7. Изменение процентного содержания оксида NiFe 2 O 4 в составе оксидных фаз в ряду сплавов 1 – 16 согласно табл. 2. Несколько точек для каждого сплава, последовательно для каждого сплава слева-направо – образцы серий 1 – 3
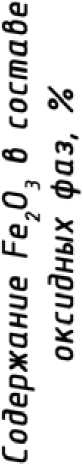
♦ 1 серия экспериментов -о— 2 серия экспериментов —♦— 3 серия экспериментов
Номера сплавов
Рис. 8. Изменение процентного содержания оксида Fe 2 O 3 в составе оксидных фаз в ряду сплавов 1 – 16 согласно табл. 2
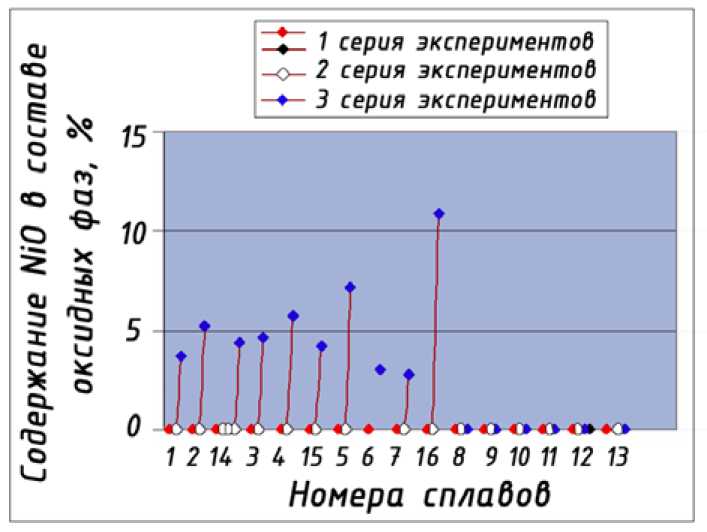
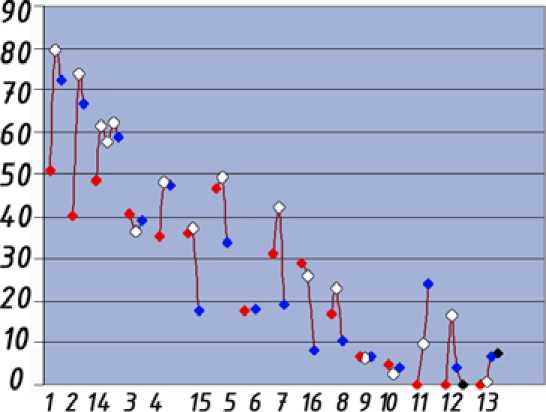
Рис. 9. Изменение процентного содержания оксида NiO в составе оксидных фаз в ряду сплавов 1 – 16 согласно табл. 2
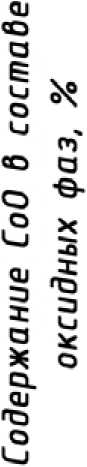
♦ 1 серия экспериментов ^^ 2 серия экспериментов —•— 3 серия экспериментов
Номера сплабоб
Рис. 10. Изменение процентного содержания оксида CoO в составе оксидных фаз в ряду сплавов 1 – 16 согласно табл. 2
С повышением температуры окислительного отжига выше 650 ºС существенно возрастает в составе оксидных фаз количество оксида на основе железа, преимущественно гематита. Причем его содержание становится заметным даже в высококобальтовых сплавах (11, 12, 13) после окисления при температурах 870 и 950 ºС (рис. 8).
В присутствии кобальта в сплавах существенно снижается содержание образующегося оксида никеля NiO (рис.9) или вообще исключается его образование при относительно невысоких температурах (до 870 ºС) окислительной обработки.
В высококобальтовых сплавах с увеличением содержания кобальта резко возрастает доля оксида кобальта CoO, особенно после высокотемпературной окислительной обработки при 950 – 1100 ºС (рис. 10).
Выводы
Установлены закономерности влияния химического состава сплавов на изменение фазового и химического составов оксидов, образующихся при термическом методе окисления поверхности сплавов системы Fe – Ni – Co. Экспериментально определены значения критических точек фазовых превращений в оксидах, которые несколько отличаются при нагреве и охлаждении. Установлены области сплавов, на поверхности которых возможно получение оксида NiFe2O4 в количестве более 80 - 85 %; показано, что в сплаве 40Fe - 40Ni - 20Co при температуре окислительной обработки 870 ºС достигается 97,5 % этого оксида; образование оксида кобальта CoO в количестве до 75 - 80 % достигается в высококобальтовых сплавах в случае использования высокотемпературного окисления при температурах 950 - 1100 °С; при более низких температурах образуются различные кристаллографические формы оксида типа Co3O4.


