Особенности патогенеза, диагностики и лечения ишемии миокарда без обструкции коронарных артерий
Автор: Хачирова Э.А., Яровой М.Д.
Журнал: Евразийский кардиологический журнал @eurasian-cardiology-journal
Рубрика: Обзор
Статья в выпуске: 1, 2025 года.
Бесплатный доступ
Среди наиболее распространённых причин смертности во всём мире ведущая роль остаётся за ишемической болезнью сердца (ИБС). Несмотря на то, что атеросклероз коронарных артерий - это основная причина развития ИБС, всё чаще клиницисты выявляют у пациентов наличие инфаркта миокарда без обструкции коронарного русла. Инфаркт миокарда без обструкции коронарных артерий (ИМБОКА) характеризуется клиническими признаками инфаркта миокарда (ИМ) с признаками стеноза коронарных артерий при ангиографии менее 50%. В последние годы были достигнуты значительные успехи в понимании патофизиологических изменений, которые лежат в основе этого состояния, однако предикторы развития этого состояния остаются не до конца ясными. Постановка диагноза ИНОКА по сей день остаётся сложной задачей для клинициста. Определение механизма ИНОКА и исключение других возможных причин повышения сердечного тропонина имеет важное значение для разработки мер вторичной профилактики, направленных на улучшение прогноза пациентов после перенесенного острого инфаркта миокарда (ОИМ). Тщательный сбор анамнеза и использование инвазивной и неинвазивной визуализации должны приводить к выявлению возможных вазоспастических или микрососудистых причин ИНОКА и их дифференциации от повреждения миокарда, вызванного другими заболеваниями. По сравнению с пациентами с ОИМ при обструктивной ишемической болезни сердца (ИБС), пациенты с ИНОКА чаще женщины и, как правило, имеют меньше традиционных факторов риска сердечно-сосудистых заболеваний (ССЗ). Целью данной статьи был обзор литературы и оценка клинических особенностей, этиологии, диагностики, лечения и прогноза при ИНОКА. В настоящем обзоре обобщены текущие знания об ИНОКА в области эпидемиологии, патофизиологии и лечения, с акцентом на современные диагностические инструменты этого заболевания.
Инока, ибс, необструктивное поражение миокарда, микроваскулярное поражение
Короткий адрес: https://sciup.org/143184209
IDR: 143184209 | УДК: 616.1+615.03 | DOI: 10.38109/2225-1685-2025-1-50-57
Features of the pathogenesis, diagnosis and treatment of myocardial ischemia with non-obstructive coronary arteries
Among the most dangerous causes of mortality worldwide, coronary artery disease (CAD) remains the leading cause. Despite the fact that atherosclerosis of the coronary arteries is the main cause of the development of coronary artery disease, clinicians are increasingly identifying myocardial ischemia without coronary obstruction. Myocardial ischemia with non-obstructive coronary arteries (INOCA) is characterized by clinical signs of myocardial infarction (MI) with evidence of coronary artery stenosis on angiography of less than 50%. In recent years, significant advances have been made in understanding the pathophysiological changes that underlie this condition, but the predictors of development of this condition remain unclear. And a diagnosis of INOCA remains a difficult task for the clinician to this day. Determining the mechanism of INOCA and excluding other possible causes of elevated cardiac troponin is important for the development of secondary prevention measures aimed at improving the prognosis of patients after acute myocardial infarction (AMI). A history of disease and use of invasive and noninvasive imaging should lead to the identification of possible vasospastic or microvascular causes of INOCA and their differentiation from myocardial injury caused by other diseases. Compared with patients with AMI due to obstructive coronary artery disease (CAD), patients with INOCA are more often women and tend to have fewer traditional cardiovascular disease (CVD) risk factors.The aim of this article was to review the literature and evaluate the clinical features, ethiology, diagnosis, treatment, and prognosis of INOCA. This review summarizes the current knowledge of INOCA in the areas of epidemiology, pathophysiology and treatment, with an emphasis on modern diagnostic tools for this disease.
Текст обзорной статьи Особенности патогенеза, диагностики и лечения ишемии миокарда без обструкции коронарных артерий
Данная статья распространяется на условиях «открытого доступа», в соответствии с лицензией CC BY-NC-SA 4.0 («Attribution-NonCommercial-ShareAlike» / «Атрибуция-Не-коммерчески-Сохранение Условий» 4.0), которая разрешает неограниченное некоммерческое использование, распространение и воспроизведение на любом носителе при условии указания автора и источника. Чтобы ознакомиться с полными условиями данной лицензии на русском языке, посетите сайт: by-nc-sa/4.0/
50 ЕВРАЗИЙСКИЙ КАРДИОЛОГИЧЕСКИЙ ЖУРНАЛ, 1, 2025
REVIEW
*1) Check for updates
*Elvira A. Khachirova, Maksim D. Iarovoi
FEATURES OF THE PATHOGENESIS, DIAGNOSIS AND TREATMENT OFMYOCARDIAL ISCHEMIA WITH NON-OBSTRUCTIVE CORONARY ARTERIES
Pirogov Russian National Research Medical University,
1 bld. Ostrovityanova st., Moscow 117997, Russian Federation
Authors’ contributions. All authors meet the ICMJE criteria for authorship. CRediT author statement: Elvira A. Khachirova – concept of the article, searching for literature sources, writing – review & editing, approval of the final version of the article; Maksim D. Iarovoi – concept of the article, searching for literature sources, writing – review & editing, approval of the final version of the article.
Conflict of interest: The authors declare no apparent and potential conflicts of interest or personal relationships related to the publication of this article. The authors did not declare any other conflicts of interest.
Funding for the article. Manuscript was prepared with the Servier pharmaceutical company informational and financial support that did not impact on authors' opinion.
И ELCHIK09@MAIL.RU
This is an open access article distributed under the terms of the Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International (CC BY-NC-SA 4.0) License , which permits unrestricted use, distribution, and reproduction in any medium, provided the original author and source are credited.
Ишемическая болезнь сердца (ИБС) – поражение миокарда, вызванное нарушением кровотока по коронарным артериям (КА). В этиологии ИБС лежат органические (необратимые) и функциональные (преходящие) изменения. К наиболее распространённым органическим поражениям относится атеросклероз. Среди функциональных нарушений лидируют спазм и внутрисосудистый тромбоз [1].
По данным Росстата, ежегодно в России доля погибших от ИБС составляет 27%. Более 10% женщин старше 65 страдают различными видами стенокардий, среди мужчин старше 45 лет – 12-14% [1].
Несмотря на то, что первым по значимости фактором развития коронарной недостаточности является атеросклероз КА, большее значение в структуре ИБС занимают необструктивные поражения коронарного русла. Denby KJ и соавт. (2024) указывают, что практически у каждого второго пациента по данным коронароангиографии (КАГ) выявляется ишемия без обструкции КА (Ischemia With Nonobstructive Coronary Artery Disease, INOCA, ИНОКА). В структуру ИНОКА на данный момент входят такие состояния как микрососудистая (МСС) и вазоспастическая стенокардия (ВСС), маскированное диффузное поражение КА (Masked diffuse disease) [2]. Среди них на долю МСС и ВСС приходится 84-89% [3,4].
Ранее ИНОКА рассматривалась как заболевание с благоприятным прогнозом, но в настоящее время появились данные об увеличении частоты летального исхода и сердечно-сосудистых осложнений практически в 4 раза по сравнению с пациентами, не имеющими ИНОКА [5-7].
Недавно полученные данные J. Huang и соавт. (2024) указывают на более высокий риск развития острого инфаркта миокарда (ОИМ) у пациентов с ИНОКА при воздействии низких температур по сравнению с теми, кто имел обструкцию КА [8].
Средний возраст пациентов с МСС и ВСС составляет 56-59 лет. Мужчины чаще имеют ВСС (60% против 30%), однако в группе пациентов с МСС превалируют женщины (61%) [9]. Характеристика ИНОКА представлена на рисунке 1.
Выявлено большое количество этиологических факторов развития ИНОКА: ремоделирование сосудистой стенки в результате воспалительных процессов, изменения внесосудистой интерстициальной ткани, а также системные нарушения (капиллярное разряжение, дисфункция артериол). Спазм КА, лежащий в основе патогенеза ИНОКА, не является генерализованным, чаще очаговый и вызван гиперреактивностью гладких миоцитов в ответ на какой-либо пусковой механизм. Эндотелиальная дисфункция напрямую связана с сахарным диабетом, одним из факторов риска ИНОКА [10]. Это понятие подразумевает под собой нарушение механизмов сосудистой регуляции, которая проявляется патологическим ответом на различные раздражители [11]. Существует несколько типов дисфункции эндотелия: вазомоторная, гемостатическая, адгезионная, ангиогенная. Для ВСС и МСС характерен вазомоторный тип, однако в большинстве случаев встречается сочетание сразу нескольких типов эндотелиальной дисфункции. Главным звеном в патогенезе эндотелиальной дисфункции является нарушение выработки оксида азота (II) – NO, обеспечивающего вазодилатацию, предотвращение тромбообразования и пролиферацию гладких миоцитов сосудистой стенки [12].
Некоторые авторы рассматривают развитие ИНОКА и микро-сосудистой дисфункции в качестве звеньев патогенеза хронической сердечной недостаточности (ХСН) с сохраненной фракцией выброса [13].
Основным методом диагностики ИНОКА является КАГ. Более совершенным методом, по данным метаанализа Huang FY и соавт. (2016), является КТ-ангиография. Авторы утверждают, что ангиографически интактные КА оказывались стенозированными при КТ-ангиографии. Это связывают с тем, что КТ-ангиография фокусируется на обнаружении люминальной обструкции (закупорка сосуда клетками крови, эмболами) [14].
Эхокардиография используется для оценки функции миокарда. Так, Teragawa H. и соавт. (2024) сообщают о корреляции между высоким индексом E’/e и наличием микрососудистой дисфункции на основе данных 84 пациентов. Однако некоторые авторы считают, что такая связь больше характерна для ХСН с
ФАКТОРЫ РИСКА
ДИАГНОСТИКА
-
• Возраст
-
• Артериальная гипертензия
-
• Инсулинорезистентность
-
• Дислипидемия
-
• Курения
-
• Воспаление
-
• Оксидативный стресс
-
• Дисфункция автономной нервной системы
Неинвазивные методы
Оценка резерва сердечного кровотока
Инвазивные методы Оценка эпикардиальной и микрососудистой функции
Диффузный атеросклероз КА

Вазоспазм
Мужчины=женщины
Эпикардиальная и микрососудистая дисфункция
Женщины>мужчины
-
• Инфаркт миокарда
-
• Инсульт
-
• Сердечная недостаточность
-
• Летальный исход
ОСНОВНЫЕ ОСЛОЖНЕНИЯ
-
• Рецидивирующая стенокардия
-
• Снижение качества жизни
-
• Повышенное количество госпитализаций
ПОСЛЕДСТВИЯ
Рисунок 1. ИНОКА [23]Figure 1. INOCA [23]
52 ЕВРАЗИЙСКИЙ КАРДИОЛОГИЧЕСКИЙ ЖУРНАЛ, 1, 2025
сохранённой фракцией выброса, нежели на ИНОКА [15]. Конечно, гипотеза о наличии взаимосвязи между ИНОКА и определёнными показателями эхокардиографии требует проведения более крупных исследований с большой выборкой пациентов.
Особого внимания заслуживает маскированное диффузное поражение КА, о котором заговорили относительно недавно. Так, даже у пациентов с ИНОКА в более чем половине случаев выявляется атеросклероз при использовании внутрисосудистых визуализирующих методик. Исследователи D. Hwang, S. Park заявляют, что только у 30 из 100 женщин были продемонстрированы истинно микрососудистые изменения, у остальных с помощью интракоронарной визуализации выявили атеросклероз эпикардиального русла, что диктует необходимость опираться не только на результаты КАГ, но и прибегать к применению более информативных внутрисосудистых визуализирующих методик с оценкой коронарного резерва кровотока (КРК) [2].
ВАЗОСПАСТИЧЕСКАЯ СТЕНОКАРДИЯ
Вазоспастическая стенокардия определяется как заболевание, характеризующееся возникновением ангинозных приступов, вызванных спазмом эпикардиальных КА, что приводит к динамическому нарушению кровоснабжения миокарда [16].
Патогенетически возможны два варианта возникновения болевого синдрома:
-
1) в покое, например, утром, что связано с циркадными ритмами и выбросом катехоламинов в утренние и ночные часы;
-
2) вазоспазм, возникающий при физической нагрузке, обусловлен активацией адренергической системы в ответ на нагрузку [17,18].
Патогенез ВСС представлен на рисунке 2.
Для постановки диагноза ВСС используются критерии COVADIS (Coronary Vasomotor Disorders International Study Group) (табл. 1).
Первым этапом диагностики является проведение КАГ для исключения обструкции КА. Также используются провокационные пробы с ацетилхолином, воздействующие на мускариновые холинэргические рецепторы. Препарат вводят утром, когда вероятность возникновения ангиоспазма выше, первая доза составляет 20 мг с последующим повышением до 100 мг, при отсутствии эффекта можно ввести 200 мг. При этом тесте выявляется спазм микроциркуляторного русла без сужения просвета крупных КА [21, 22].
Тест считается положительным при возникновении стенокардии, ишемических изменений на ЭКГ (депрессия или подъем
Гиперконстриктивность гладких мышц сосудов (повышенная активность Rho-киназы)
Эндотелиальная дисфункция (дефицит NO)
Генетическая предрасположенность (мутации генов NO-синтазы, адренергических и серотониновых рецепторов, ангиотензинпревращающего фермента; микроРНК)
Гиперактивность симпатической или парасимпатической нервной системы
Хроническое воспаление
Дефицит Mg2+ (является антагонистом Ca2+)
Рисунок 2. Патогенез вазоспастической стенокардии [19]
Figure 2. Pathogenesis of vasospastic angina [19]
Таблица 1. Критерии COVADIS для постановки вазоспастической стенокардии [20]
Table 1. COVADIS criteria for vasospastic angina [20]
|
№ Критерий |
Дополнительные признаки |
|
Нитрат-зависимая стенокардия во время спонтанного I приступа в сочетании с одним из следующих признаков: |
|
|
Транзиторные ишемические заряды ЭКГ – во время II спонтанного эпизода, включая любой из следующих по крайней мере в двух смежных отведениях |
|
|
III Спазм КА |
Транзиторная полная или субтотальная окклюзия КА (стеноз более 90%) со стенокардией и ишемическими изменениями на ЭКГ, возникающими либо спонтанно, либо в ответ на провокационный стимул (обычно ацетилхолин, спорынья или гипервентиляция) |
|
Диагноз ставится при сочетании критерия I с критерием II либо III. «Подозрительная вазоспастическая стенокардия» при наличии стенокардии, реагирующей на нитраты, но критерии II и III сомнительны или отсутствуют. |
|
сегмента ST ≥ 0,1 мВ (1 мм) или новые отрицательные волны U) минимум в двух смежных отведениях и ≥ 90% вазоконстрикции. Кроме ацетилхолина для проведения провокационных проб применяется эргоновин (действует на серотониновые рецепторы) [23]. Для получения более достоверных результатов провокационного вазоспастического теста необходимо отменить блокаторы кальциевых каналов и нитраты за 48 часов до процедуры [24].
Для лечения рекомендовано использование блокаторов кальциевых каналов (особенно эффективным является нифедипин), нитратов длительного действия и нитратов короткого действия для купирования ангинозных приступов. β -адреноблокаторы противопоказаны, т. к. могут быть триггером вазоспазма [1].
МИКРОСОСУДИСТАЯ СТЕНОКАРДИЯ
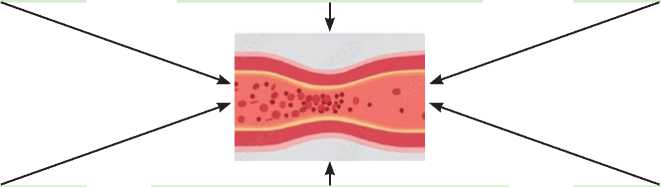
Под термином МСС понимают нарушение функции и структуры микроциркуляторного русла миокарда, что ведет к патологическим изменениям в ответ на введение вазодилататоров (аденозин, папаверин). В основе патогенеза лежит развитие структурного ремоделирования сосудов вследствие гипертонической болезни, сахарного диабета, наличия кардиомиопатий, гипертрофии левого желудочка, а также атеросклеротического поражения. Эти факторы приводят к дисфункции гладких миоцитов в стенке артериол, а также к нарушению процесса вазодилатации, что вызывает снижение коронарного резерва [25]. Для МСС также характерно развитие спазма эпикардиальных КА, вызванного Rho-киназой, что подтверждается данными Suda A. и соавт. (2019) [26].
Диагноз МСС устанавливается согласно критериям COVADIS (табл. 2).
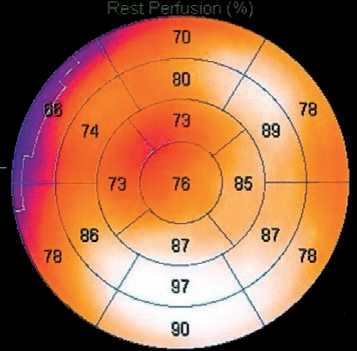
А. в покое
В. при физической нагрузке
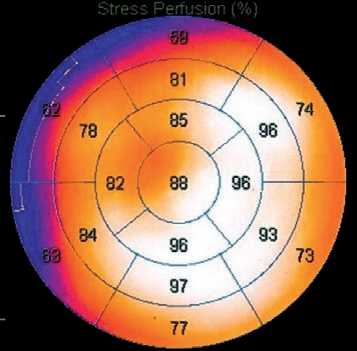
Рисунок 3. Перфузионная сцинтиграмма пациентки М., 64 лет, с МСС. Выявляются преходящие дефекты перфузии миокарда в переднеперегородочной области левого желудочка [из личного архива Хачировой Э.А.]
Figure 3. Perfusion scintigram of patient M., 64 y.o. Transient defects in myocardial perfusion are detected in the anteroseptal region of the left ventricle [from the personal archive of Khachirova E.A.]
Таблица 2. Критерии COVADIS для постановки микрососудистой стенокардии [20]
Table 2. COVADIS criteria for microvascular angina [20]
|
№ Критерий |
Дополнительные признаки |
|
I Симптомы ишемии миокарда |
|
|
Отсутствие обструкции КА II (уменьшение диаметра <50% или фракционный резерв кровотока >0,80) |
1) Ишемические изменения на ЭКГ во время приступа стенокардии |
|
III Объективные доказательства ишемии миокарда |
|
|
III Признаки нарушения функции микроциркуляторного русла |
iMR > 25)
|
Диагноз ставится при сочетании критерия I с критерием II либо III.
«Под озрительная МСС» при наличии стенокар дии, реагирующей на нитраты, но критерии II и III сомнительны или отсутствуют.
54 ЕВРАЗИЙСКИЙ КАРДИОЛОГИЧЕСКИЙ ЖУРНАЛ, 1, 2025
Факторами риска МСС, как и у большинства сердечно-сосудистых заболеваний, являются возраст, артериальная гипертония, дислипидемии, сахарный диабет и др. [27].
Прогноз пациентов с МСС и ВСС в целом благоприятный, однако, он отличается от основной популяции: по данным метаанализа Odanovi c N. и соавт., вероятность развития неблагоприятных сердечно-сосудистых событий выше у пациентов с МСС по сравнению с теми, кто имеет ВСС [9]. Авторы указывают, что более высокий риск развития осложнений наблюдается у тех, кто имел низкий КРК. В то же время, согласно проведённому в 2006 г. исследованию The Women's Ischemia Syndrome Evaluation (WISE), пациентки с МСС имеют больший риск повторных госпитализаций (в 1,8 раз чаще) и повторных КАГ [28]. Можно предположить, что это связано с тем, что пациенты с МСС имеют большее число комобридных состояний, чем пациенты с ВСС.
Оценку коронарного кровотока проводят с помощью КАГ – полуколичественно оценивается количество кадров TIMI (Thrombolysis in Myocardial Infarction, тромболизис при инфаркте миокарда). Если пациент имеет нестенозированные эпикардиальные КА, то количество кадров TIMI >27 (изображения, полученные со скоростью 30 кадров/с), предполагают МСС, что объясняется нарушением кровотока в состоянии покоя [29].
К инвазивным диагностическим методикам относится расчёт КРК и индекса микроциркуляторной резистентности (определяется при КАГ) при введении в кровоток вазодилататоров (аденозин, папаверин). Нормальное значение КРК >2,5, значение <2,0 указывает на нарушение процесса вазодилатации, значения 2,02,5 являются промежуточными. Измерение данного показателя проводят методом термоделюции (используется датчик температуры и давления) либо методом допплера [30, 31].
Другим методом диагностики является верификация эндотелиальной дисфункции с помощью ацетилхолиновой пробы: препарат вводят в одну из крупных артерий эпикарда через микрокатетер. Спазм микроциркуляторного русла проявляется симптомами стенокардии и изменениями на ЭКГ, которые не сопровождаются спазмом эпикардиальных артерий. Регистрируется снижение КРК и нормальное значение индекса микро-циркуляторной резистентности [32, 33].
Согласно клиническим рекомендациям министерства здравоохранения Российской Федерации 2024 года [1], лечение МСС включает в себя комбинированную терапию препаратами из нескольких фармакологических групп. Лечение следует начинать при значении КРК <2,0 или ИКР ≥ 25 условных единиц и при отсутствии признаков вазоспазма. Кроме того, описано множество других препаратов, которые на данный момент не зарегистрированы в России (табл. 3).
К противоишемическим препаратам первой линии относятся b -адреноблокаторы и блокаторы кальциевых каналов. Необходимо рассмотреть вопрос антиагрегантной терапии (препараты ацетилсалициловой кислоты) и статинотерапии, дозировки которых титруются под контролем ЛПНП, печёночных ферментов. Высокий уровень доказательности имеют и ингибиторы ангиотензинпревращающего фермента, которые улучшают сердечно-сосудистый прогноз за счёт улучшения эндотелиальной функции.
Согласно клиническим рекомендациям, контроль эффективности антиангинальной терапии предусматривает оценку частоты приступов стенокардии в неделю, снижение функционального класса стенокардии и потребности в приёме нитратов короткого действия [1]. Триметазидин относится к препаратам второй линии антиангинальной терапии. Антиангинальный эффект триметазидина неспецифический, благодаря воздействию на все механизмы развития ишемии.
Интересные данные публикуют Kamish Y., Che Hassan H.H., которые отмечают положительное влияние триметазидина на эндотелиальную функцию за счёт регуляции ангиогенеза и апоптоза, снижение окислительного стресса и воспаление, а также увеличение эндотелиальной биодоступности NO [38].
По данным Nassiri S., Van de Bovenkamp A.A. триметазидин может быть использован при лечении ХСН с сохранной фракцией выброса. В метанализ были включены более 2500 пациентов
Таблица 3. Группы препаратов для лечения МСС [1, 34]
Table 3. Groups of drugs for the treatment of microvascular angina [1, 34]
К новым методам лечения ИНОКА относят редукцию коронарного синуса и инфузию стволовых клеток CD34+. Смысл операции по редукции коронарного синуса заключается в изменении соотношения эндокардиального и эпикардиального кровотока, которое при стенокардии значительно уменьшается (в норме составляет 1,2). Доступом через правую внутреннюю яремную вену в полость коронарного синуса вводится стент в форме песочных часов, создающий определённый градиент в венозном оттоке от миокарда [35]. Механизм действия данных стволовых клеток заключается в индукции ангиогенеза и увеличении плотности капилляров в миокарде [37].
Проведенное в 2022 году исследование IMPROvE-CED подтвердило положительный эффект от инфузии стволовых клеток CD34+ на состояние пациентов с эндотелиозависимой микро-сосудистой дисфункцией. Основную группу пациентов в исследовании составили 20 человек, период наблюдения составил 6 месяцев, проводилась оценка изменения функционального класса стенокардии по Нью-Йоркской классификации, частота использования нитроглицерина за определённый период времени, опросник Сиэтла по стенокардии. Исследователи пришли к выводу, что проводимая терапия эффективна и безопасна и может быть использована у пациентов с микрососудистой дисфункцией [36]. Однако стоит учитывать небольшое количество пациентов, включённых в исследование, небольшой промежуток наблюдения. Безусловно, данное направление может стать одним из наиболее эффективных и безопасных методов терапии пациентов с ИНОКА, но на сегодняшний день нуждается в дальнейших наблюдениях на большем количестве пациентов и более длительных исследованиях.


