Особенности патоморфологических проявлений хронического миелоидного лейкоза у кур
Автор: Вахрушева Т.И.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Ветеринария и зоотехния
Статья в выпуске: 1, 2020 года.
Бесплатный доступ
Изучена патоморфологическая картина изменений органов и тканей павших и вынужденно убитых кур с клиническими признаками хронического миелоидного лейкоза, установлены характерные патогномоничные для основного заболевания макро- и микроскопические изменения, а также развившиеся на их фоне осложнения, проведена дифференциальная диагностика от инфекционных болезней со сходными клиническими и морфологическими признаками. Объектами исследования являлись куры-несушки, содержащиеся в одном из фермерских хозяйств Красноярского края, в течение 2018-2019 гг. было проведено патологоанатомическое вскрытие 12 трупов птиц. Проводился забор материала для гистологического исследования - фрагменты тканей костного мозга, селезенки, печени, почек, сердца, тонкого и толстого отделов кишечника, легких, поджелудочной железы, яичника, головного мозга. Срезы изготавливались на микротоме «Техном МЗП-01», окрашивались гематоксилином Эрлиха и эозином. Для проведения серологических исследований сыворотки крови кур на наличие антител к ALV-J проводился забор крови от птиц с клиническими признаками болезни - 6 голов, специфические антитела выявлялись во всех случаях в реакции ИФА...
Куры, хронический миелоидный лейкоз, гемобластозы, миелобластоз, миелолейкоз, болезни птицы
Короткий адрес: https://sciup.org/140245719
IDR: 140245719 | УДК: 619: | DOI: 10.36718/1819-4036-2020-1-62-75
The peculiarities of pathomorphological manifestations of chronic myeloid leukemia in hens
Pathomorphological picture of the organs and tissues of dead and involuntarily killed chickens with clinical signs of chronic myeloid leukemia was studied, macro-microscopic changes characteristic pathognomonic for underlying disease, as well as the complications which developed against their background, the differential diagnosis of infectious diseases with similar clinical findings was established and morphological features. The objects of the study were laying hens kept on one of the farms of the Krasnoyarsk Territory during 2018-2019. The autopsy was performed on 12 corpses of birds. The material intake for histological research was taken - fragments of bone marrow, spleen, liver, kidney, heart, small and large intestine, lung, pancreas, ovary, brain tissue sections, sections were made. The cuts were made with the help of Tekhnom MZP-01 microtome, stained with Ehrlich hematoxylin and eosin. To conduct serological studies of chicken blood serum for the presence of antibodies to ALV-J, the blood was collected from birds with clinical signs of the disease, - 6 heads, specific antibodies came to light in all cases in reaction of IFA...
Текст научной статьи Особенности патоморфологических проявлений хронического миелоидного лейкоза у кур
Введение. Развитие и интенсификация птицеводства сопровождаются увеличением количества болезней сельскохозяйственной птицы и частоты их проявления, среди которых важное место занимают патологии опухолевой природы, в частности лейкоз.
Лейкоз птиц (Leucosis avium) - вирусное заболевание, характеризующееся системным опухолевидным разрастанием кроветворной ткани и латентным течением, обострения наблюдаются в первые месяцы яйцекладки. В зависимости от клеточного состава опухолевых новообразований различают лимфоидный, миелоидный, эритробластический лейкоз, а также гемоцитобластоз и ретику-лоэндотелиоз. Болезнь поражает различные виды птиц, из сельскохозяйственной птицы диагностируется в основном у кур. Лейкоз птиц широко распространен во многих странах мира, в том числе и на территории Российской Федерации, причиняя существенный экономический ущерб, который складывается из гибели и вынужденного убоя птицы, снижения продуктивности, нарушения процессов воспроизводства в племенном птицеводстве, ограничительными мероприятиями [1-5].
Вирус лейкоза птиц (ALV) относится к семейству Retroviridae типа С, подразделяется на несколько антигенных подгрупп: A, B, C, D, E, J, которые имеют в своем составе множество штаммов [6–8]. Формы новообразований, индуцируемые вирусом, зависят от штамма вируса, дозы и способа заражения, а также от генотипа, возраста и пола восприимчивого организма. По данным исследований различных авторов, наиболее распространенной формой лейкоза птиц является лимфоидный лейкоз, или В-клеточная лимфома, вызванная в большинстве случаев вирусом лейкоза птиц группы А, первично развивающаяся в тканях фабрициевой бурсы и индуцирующая метастазы в висцеральных органах. У птиц, пораженных миелоидным лейкозом, выявляется вирус группы J (ALV-J), который является возбудителем целого спектра заболеваний миелоидной природы, в том числе эритробластозов, гемангиом и иных неопластических образований [9–12]. Вирус миелоидного лейкоза птиц (ALV-J) распространен в коммерческих хозяйствах различных стран мира, в том числе и в Российской Федерации. Степень распространения ALV-J в родительских стадах бройлерных хозяйств составляет от 9 до 88 % и сопровождается высокой смертностью птицы [3, 13]. Вирус также может обнаруживаться у несушек [14]. ALV-J способен передаваться как горизонтальным, так и вертикальным путем [15]. Данные современных исследований сви- детельствуют о том, что к инфекции ALV-J чувствителен широкий спектр линий и пород кур [6, 3]. Особенно восприимчивы к данной инфекции породы кур мясного направления. Выраженные клинические симптомы у особей родительского поголовья бройлеров выявляются в возрасте 6–12 месяцев, при этом происходит инфицирование их потомства, что значительно ухудшает производственные показатели птицы, так как инфекция может вызывать у цыплят отставание в росте, иммуносупрессию, и, следовательно, повышенную восприимчивость к другим заболеваниям. У птицы яичных пород заболевание может протекать как субклиническая инфекция, снижая ряд важных характеристик, включая производство и качество яиц [16, 17].
Миелоидный лейкоз птиц (синонимы: ми-елобластоз, миелолейкоз, миелоз) диагностируется достаточно редко, в среднем в 1,5-2 % от общего количества случаев заболевания лейкозом. Болезнь характеризуется избыточной пролиферацией в органах малодифференцированных клеток миелоидного ряда миелобла-стов, промиелоцитов, миелоцитов с присутствием псевдоэозинофилов, проявляется в виде алейкемии и лейкемии. Основными клиническими симптомами миелоидного лейкоза являются снижение аппетита, вялость, истощение, диарея, бледность и цианоз, реже иктеричность, гребешка и бородок, появление новообразований в области головы, грудной клетки и голеней, часто выявляются признаки асцита, отеки подкожной клетчатки, разрывы печени и яичников с кровоизлиянием в грудобрюшную полость. Для миелоидного лейкоза характерно поражение печени, почек, селезенки и яичников, костного мозга, при этом, в отличие от лимфоидного лейкоза, в тканях фабрициевой бурсы и тимуса изменений не обнаруживают. Несмотря на то, что миелоидный лейкоз птиц -медленно развивающееся заболевание, экономические потери могут составлять до 20 % [1].
На данный момент лечение ретровирусных инфекций не приводит к сколько-нибудь значительному положительному результату, также не получены эффективные вакцины против вируса лейкоза птиц. Основные меры борьбы с инфекцией заключаются в формировании «безлейкоз- ных» стад птиц путем выбраковки больных особей и вирусоносителей, поэтому важную роль в мероприятиях по предупреждению появления и распространения лейкоза играет ранняя диагностика. Для разработки эффективных программ профилактики и борьбы с лейкозом птиц необходимо изучение биологических свойств возбудителя, а также особенностей патогенеза, клинической и патолого-анатомической картины болезни [18].
Учитывая то, что рядом исследователей было установлено широкое распространение вируса миелоидного лейкоза (ALV-J) у поголовья кур, разводимого на птицефабриках Российской Федерации, а также то, что данные о клинической картине и характерных изменениях органов и тканей в современной научной литературе представлены ограниченно, изучение патоморфологической картины миелоидного лейкоза птиц для оптимизации комплексной диагностики болезни, в том числе дифференциальной, является актуальной темой [1].
Цель исследования : анализ патоморфоло-гической картины изменений органов и тканей у кур при миелоидном лейкозе с установлением патогномоничных макро- и микроскопических признаков заболевания и проведением дифференциальной диагностики.
Объекты, материалы и методы исследования: объектом исследования являлись куры-несушки, содержащиеся в одном из фермерских хозяйств Красноярского края, в течение 2018– 2019 гг. было проведено патолого-анатомическое вскрытие 12 трупов павших (8 голов) и вынужденно убитых (4 головы) кур в возрасте от 1,2 месяцев до 1,8 лет, из которых 6 трупов кур кросса Хайсекс Браун породы Леггорн, 6 трупов - породы Леггорн белый. Во время вскрытия проводился забор материала для гистологического исследования - фрагменты тканей костного мозга, селезенки, печени, почек, сердца, тонкого и толстого отделов кишечника, легких, поджелудочной железы, яичника, головного мозга. Патолого-анатомический материал фиксировался в 10 % нейтральном растворе формалина, срезы изготавливались на микротоме «Техном МЗП-01», окрашивались гематоксилином Эрлиха и эозином, микроскопия про- водилась на микроскопе «Levenhuk 320». Микрофотосъемку и анализ микрофотографий проводили на фотоаппарате Canon EOS 1100D.
Для проведения серологических исследований сыворотки крови кур на наличие антител к ALV-J проводился забор крови от птиц с клиническими признаками болезни - 16 голов, материал отправлялся в КГКУ «Красноярский отдел ветеринарии», специфические антитела выявлялись во всех случаях в реакции ИФА. Для проведения дифференциальной диагностики в лабораторию отправлялся патолого-анатомический материал - кусочки легких, селезенки, печени, почек, фрагмент кишечника, инфекция была исключена во всех случаях.
Результаты исследования: при исследовании данных анамнеза больной и павшей птицы установлено, что куры содержались в отдельном помещении, тип содержания - напольный, тип кормления - концентратный. До достижения 10–11 месяцев птица была клинически здорова, хорошо набирала вес, в возрасте 11– 13 месяцев у кур наблюдались следующие клинические признаки - вялость, снижение аппетита, цианоз, сухость и бледность гребешков и бородок, аллопеции в области шеи и спины, снижение яйценоскости на 50 % и живой массы тела, периодически наблюдалась диарея, признаки острого серозно-катарального ринита -водянисто-слизистые выделения из носовых отверстий, чихание. Для лечения больной птицы использовалась схема, включающая антибиотики - «Энрофлоксацин», противовирусные и иммуномоделирующие средства - «Фоспре-нил», комплексная кормовая добавка «Чикто-ник». Лечебные мероприятия не имели стойкого эффекта, рецидивы заболевания наблюдались через 45–60 дней, смертность составляла 60– 75 % от количества заболевшей птицы и наблюдалась через 3–5 месяцев после проявления первых клинических признаков заболевания.
При макроскопическом исследовании органов и тканей павших и вынужденно убитых кур выявлялась однотипная картина патоморфоло-гических изменений, характеризующаяся умеренно выраженной кахексией, общим венозным застоем, наиболее выраженным в кожных покровах, печени, селезенки, почек, легких, миокарда, головного мозга и поджелудочной железы. В костном мозге во всех случаях вскрытия выявлялись признаки отека, гиперемии, кровоизлияний и размягчения ткани. В тканях паренхиматозных органов - печени, почек, а также миокарде, - обнаруживались признаки белковожировой дистрофии, в желудочно-кишечном тракте во всех случаях вскрытия - картина острого и подострого серозного или слизистого катара тонкого отдела кишечника и геморрагического диатеза, в 9 случаях (75 %) - острого серозно-катарального колита. У 83,3 % особей выявлялось увеличение размеров лимфоидных миндалин слепых кишок, расположенных в их устьях, в среднем размеры которых составляли 0,6-0,7 х 0,3-0,4 мм, на разрезе представляющих собой гомогенную серо-белую «саловидную ткань». У всех птиц выявлялась картина острого серозно-катарального или катаральногеморрагического оварио-сальпингита, сопровождающегося у 33,3 % особей разрывом фолликулов яичника с дальнейшим развитием желточного перитонита. Характерные для лейкоза птиц очаги лейкемических разращений макроскопически выявлялись у 4 особей (33,3 %), представляли собой единичные участки незначительного размера от 3,0 до 5,6 мм, серожелтого цвета, не имели четких очертаний, локализовались преимущественно в печени (25 %), почках и легких (16,6 %), также не обнаруживалось изменений тимуса и фабрициевой бурсы, характерных для лимфоидного лейкоза птиц (рис. 1,2).
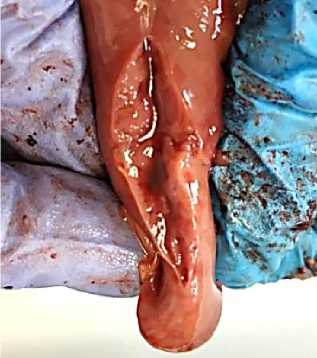
Рис. 1. Участок разрастания опухолевой ткани в печени курицы без четких границ
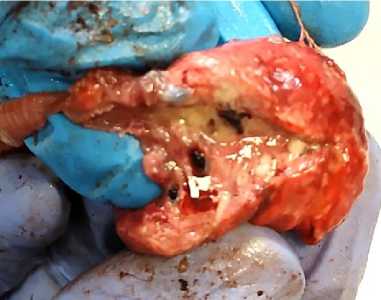
Рис. 2. Очажки разрастания неопластической лейкозной ткани в легких курицы
При гистологическом исследовании в ткани органов обнаруживались агрегаты клеток миелоидного ряда на различных стадиях дифференциации – скопления бластных форм, состоявшие из миелобластов, промиелоцитов – клеток с центрально расположенным ядром и незначительным количеством базофильной, зернистой цитоплазмы и, в меньшей степени, из миелоцитов и матамиелоцитов – клеток с овальными или бобовидными ядрами, расположенными чаще всего эксцентрично, слабобазофильной зернистой цитоплазмой и более низким ядерно-цитоплазматическим соотношением, причем подобные находки в основном обнаруживались в паренхиматозных органах (рис. 3, 4).
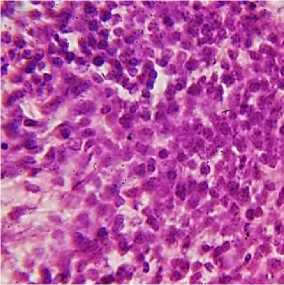
Рис. 3. Инфильтрация ткани легких курицы опухолевыми клетками типа миелобластов (окраска гематоксилином и эозином; × 400)
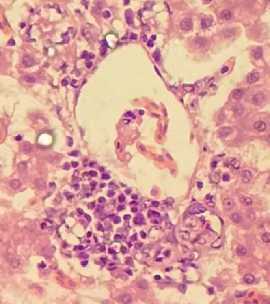
Рис. 4. Инфильтрация ткани печени курицы опухолевыми клетками типа миелобластов и миелоцитов (окраска гематоксилином и эозином; × 400)
Микроскопическая картина печени характеризовалась локализацией опухолевых клеток типа миелобластов в просветах портальных сосудов, в периваскулярных пространствах портальных трактов, синусоидных капиллярах, пространствах Диссе, а также в ткани долек, вокруг ге-патоцитов. Участки инфильтратов, состоящие из менее дифференцированных клеток – миелобластов, локализовались преимущественно вокруг крупных кровеносных сосудов. В клетках печени выявлялись при- знаки белковой и жировой дистрофии и некробиоза. Пространства Диссе – расширены и переполнены кровью (рис. 5, 6).
Макроскопически в печени у всех исследуемых особей обнаруживались признаки острого венозного застоя и зернисто-жировой дистрофии различной степени выраженности, опухолевые инфильтраты выявлялись у 4 птиц, представляя собой единичные очажки незначительного размера, неправильной округлой формы, серо-желтого цвета, на разрезе – однородные.
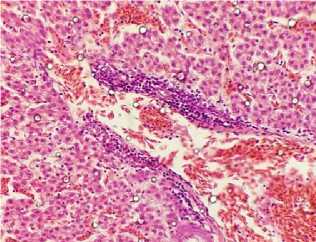
Рис. 5. Печень курицы: скопление бластных форм клеток в периваскулярных пространствах (окраска гематоксилином и эозином; × 400)
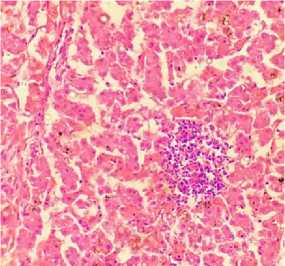
Рис. 6. Печень курицы: скопление бластных форм клеток в дольке между гепатоцитами (окраска гематоксилином и эозином; × 400)
При макроскопическом исследовании селезенки обнаруживались признаки острой застойной гиперемии и умеренной спленомагалии, специфические очаги разроста лейкозной ткани не выявлялись ни в одном случае вскрытия. Гистологически обнаруживалась выраженная диффузная инфильтрация ткани красной пульпы бластными формами клеток миелоидного ряда: синусы красной пульпы раздвинуты и ат-
Вестник КрасГАУ. 2020. № 1 рофированы вследствие пролиферации промиелоцитов, выявлялись множественные гранулы гемосидерина. Фолликулы белой пульпы резко уменьшены в размерах – вокруг центральных артерий обнаруживается узкий ободок из лимфоидных элементов, в некоторых случаях фолликулы полностью исчезают, замещаясь бластными клетками (рис. 7, 8).
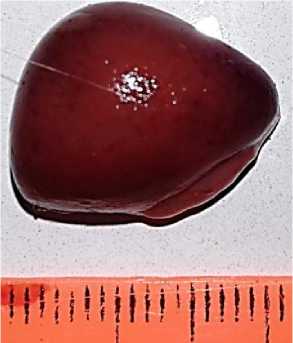
Рис. 7. Селезенка курицы: застойная гиперемия, увеличение линейных размеров органа
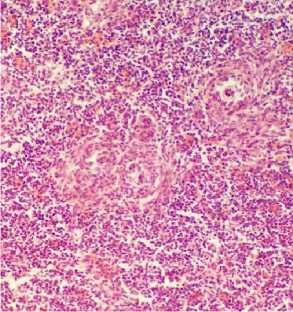
Рис. 8. Селезенка курицы: инфильтрация фолликулов белой пульпы промиелоцитами (окраска гематоксилином и эозином; × 400)
В ткани почек инфильтраты незрелых клеточных форм выявлялись в основном в виде единичных очагов незначительного размера в межуточном веществе между канальцами и почечными тельцами. В участках инфильтрации промиелоцитов тканевые структуры раздвину- ты, деформированы, резко уменьшены в размерах вследствие компрессии, эпителиоциты канальцев – в состоянии атрофии, глубокой дегенерации и некроза. В ткани почек наблюдается острое диффузное венозно-капиллярное полнокровие (рис. 9, 10).
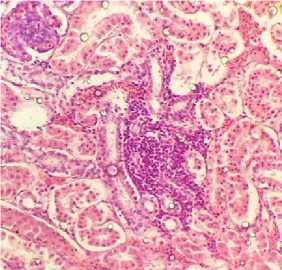
Рис. 9. Почки курицы: очаги бластных форм клеток в межуточном веществе, дистрофия эпителиоцитов (окраска гематоксилином и эозином; × 400)
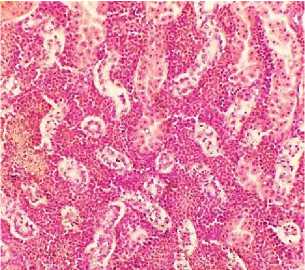
Рис. 10. Почки курицы: атрофия канальцев в участке инфильтрации межуточной ткани промиелоцитами (окраска гематоксилином и эозином; × 400)
При исследовании гистологической картины легких очаги пролифератов лейкозных клеток, состоящие преимущественно из слабодифференцированных форм клеток миелоидного ряда – промиелоцитов, локализовались в основном в периваскулярной и перибронхиальной ткани, в некоторых участках пролифератов, чаще на их периферии, обнаруживаются более зрелые клетки с бобовидными ядрами и значительным количеством цитоплазмы – миелоциты. Агрегаты бла- стных форм клеток также выявлялись в полости крупных сосудов – «лейкозные тромбы», диффузная лейкемическая инфильтрация определялась в альвеолярных стенках, характеризуя картину «лейкозного пневмонита» (рис. 11, 12). В ткани органа наблюдалось диффузное венознокапиллярное полнокровие, признаки эмфиземы и умеренного фиброза, в альвеолах, бронхиолах и бронхах – атрофия и десквамация эпителия.
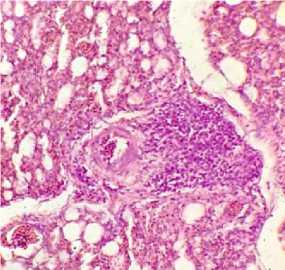
Рис. 11. Легкие курицы: очаги пролиферации бластных клеток (окраска гематоксилином и эозином; × 400)
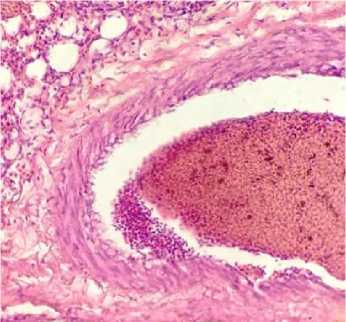
Рис. 12. Легкие курицы: лейкозный тромб в полости сосуда (окраска гематоксилином и эозином; × 400)
Характерные для миелоидного лейкоза изменения обнаруживались в тканях кишечника – в тонком и толстом отделе наблюдалась выраженная диффузная инфильтрация слизистой оболочки слабодифференцированными формами клеток миелобластического ряда с крупными округлыми ядрами и незначительным количеством базофильной цитоплазмы, ворсинки – утолщены, отечны, деформированы, эпителий слизистой – в состоянии слизистой дистрофии и некробиоза, местами полностью десквамиро-ван, в подслизистой основе и мышечной оболочке выявлялись признаки воспалительной гиперемии сосудов, серозного отека, диапедеза эритроцитов и лейкозные тромбы в просветах сосудов (рис. 13, 14). В лимфоидных миндалинах слепых кишок выявлялась очаговая лейкозная инфильтрация – рисунок строения стерт, опухолевые клетки формируют фолликулоподобные структуры, также выявлялась их диф- фузная пролиферация, в результате чего лимфоидная ткань вытесняется и замещается неопластическими клетками (рис. 15).
При исследовании костного мозга трубчатых и плоских костей ни в одном случае вскрытия не наблюдалось замещения красного костного мозга желтым, что не является нормальным физиологическим процессом для организма птицы данной возрастной группы (рис. 16). Макроскопически ткани костного мозга были полнокровны, сочные, серо-красного цвета с точечными кровоизлияниями, при гистологическом исследовании в ткани в значительном количестве обнаруживались миелобласты, а также промиелоциты и миелоциты, при этом количественное соотношение клеток миелоидного ряда к клеткам эритроидного ряда составляло 10:1, что указывало на миелоидную гиперплазию и эритроидную гипоплазию.
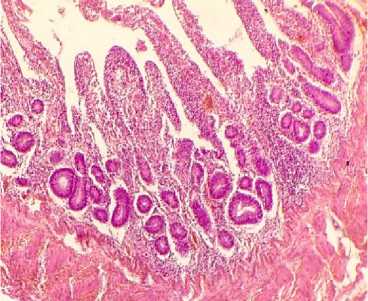
Рис. 13. Тонкий отдел кишечника курицы: пролиферации бластных форм клеток в слизистой оболочке (окраска гематоксилином и эозином; × 400)
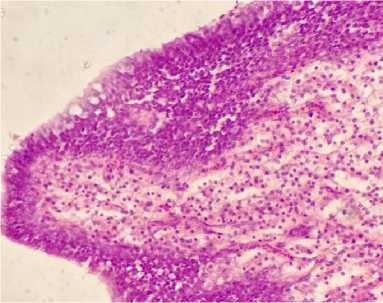
Рис. 14. Инфильтрация лейкозным пролифератом ворсинок тонкого отдела кишечника, серозный отек стромы (окраска гематоксилином и эозином; × 400)
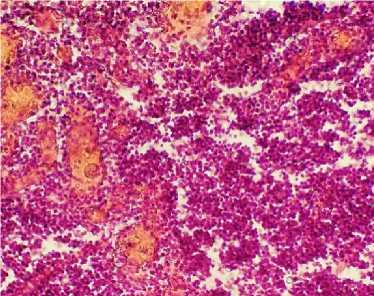
Рис. 15. Лимфоидные миндалины слепых кишок курицы: диффузно-очаговая лейкозная инфильтрация (окраска гематоксилином и эозином; * 400)
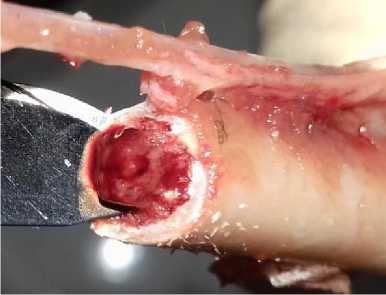
Рис. 16. Костный мозг курицы (возраст 1 год 8 месяцев): острая застойная гиперемия, отек (окраска гематоксилином и эозином; * 400)
При исследовании поджелудочной железы в 65 % случаев отмечалась картина острого серозного отека, при гистологическом исследовании выявлялись единичные агрегаты неопластических клеток в просвете крупных сосудов и периваскулярных пространствах, состоящие преимущественно из миелоцитов, среди кото- рых выявлялись единичные метамиелоциты, имеющие бобовидное, эксцентрично расположенное ядро (рис. 17).
При макро- и микроскопическом исследовании сердца в миокарде выявлялись признаки застойной гиперемии, очаги умеренно выраженной белковой (65 % случаев) и белково-жировой дистрофии (30 % случаев), у 70 % особей обнаруживалась острая дилатация правых сердечных полостей. При гистологическом исследовании в трех случая вскрытия выявлялись опухо- левые инфильтраты, состоящие из миелоцитов, представляющие собой очажки, располагающиеся как между кардиомиоцитами, так и в периваскулярных пространствах (рис. 18).
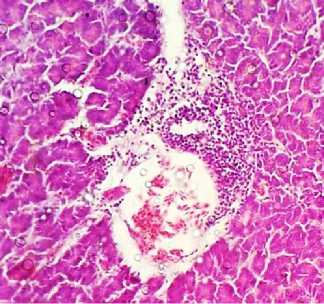
Рис. 17. Поджелудочная железа курицы: очаговая лейкозная инфильтрация периваскулярной ткани (окраска гематоксилином и эозином; × 400)
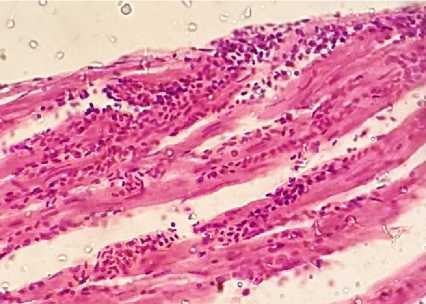
Рис. 18. Миокард курицы: белковая дистрофия, агрегаты неопластических клеток (окраска гематоксилином и эозином; × 400)
Обсуждение полученных результатов. На основании анализа результатов макро- и микроскопического исследования органов и тканей, а также данных анамнеза и лабораторного исследования установлено следующее: у всех падших и вынужденно убитых птиц выявлены признаки хронического миелоидного лейкоза, клинически характеризующегося длительным, вялотекущим течением с периодами обострения, пик смертности птиц наблюдался в возрасте от 1,3 до 1,7 года. Обнаруженная при патологоанатомическом вскрытии трафаретная картина патоморфологических изменений не была патогномоничной для данной болезни. Выявлялись признаки, указывающие на алиментарное истощение, резкое снижение общей резистент- ности, нарушение обмена веществ и функции сердечно-сосудистой системы в организме птицы: атрофия жира в жировых депо, белковожировая дистрофия паренхиматозных органов и миокарда, острый и подострый катар тонкого и толстого отделов кишечника в сочетании с умеренным геморрагическим диатезом (100 и 75 % соответственно), острый серозно-катаральный или катарально-геморрагический оварио-сальпингит (100 %), осложненный у 4 особей (33,3 %) желточным перитонитом. Специфичные для лейкоза изменения были слабо выражены и характеризовались образованием неопластических очагов незначительного размера в легких и печени – у 33,3 % птиц, увеличением лимфоидных миндалин слепых кишок – у 10
птиц (83,3 %), отсутствием признаков замещения красного мозга желтым и отеком его тканей у всех исследуемых птиц.
Микроскопическая картина характеризовалась выявлением у всех птиц лейкозных про-лифератов, локализующихся преимущественно в ткани костного мозга и периферических органов иммунопоэза – селезенке и лимфоидных узелках и миндалинах кишечника, представляющих собой чаще диффузную инфильтрацию паренхимы и стромы бластными формами клеток миелоидного ряда – промиелоцитами и миелоцитами. Также разрост неопластической ткани в виде единичных очагов выявлялся в ткани печени, легких, почек, поджелудочной железы, слизистой оболочке кишечника и бронхов, при этом агрегаты опухолевых клеток состояли преимущественно из более дифференцированных форм – миелоцитов и метамиелоцитов.
Дифференциальная диагностика от лимфоидного лейкоза была проведена на основании отсутствия характерной картины лейкозных разращений, состоящих из лимфобластов, а также изменений центральных органов иммуно-поэза – тимуса и фабрициевой бурсы. Опухолевидные разрастания в тканях различных органов обнаруживаются и при болезни Марека, но представляют собой скопления клеток различной степени зрелости – псевдоэозинофилов, плазмоцитов, гистиоцитов. Картина выраженного лейкоцитоза у птиц может наблюдаться при хроническом воспалении неспецифического характера, опухолевых процессах, а также при различных инфекционных заболеваниях: туберкулезе, аспиргеллезе, сальмонеллезе, колибак-териозе, орнитозе, микоплазмозе, респираторном микоплазмозе, – которые были исключены при комплексной дифференциальной диагностике.
Заключение. Таким образом, можно заключить, что опорными пунктами прижизненной диагностики хронического миелоидного лейкоза могут являться следующие клинические признаки: длительное течение болезни – более 3 месяцев, с чередованием ремиссий и рецидивов, отсутствие признаков специфической инфекции и положительного результата лечебных мероприятий. Ведущую роль при посмертной пато-морфологической диагностике играют гистопатологические исследования, которые основы- ваются на обнаружении диффузных и очаговых инфильтратов бластных форм клеток миелоидного ряда в органах и тканях, располагающихся преимущественно в периваскулярной ткани, при этом в ряде случаев макроскопическая картина изменений может быть неспецифичной, характеризуя глубокие метаболические нарушения и снижения общей резистентности.
Список литературы Особенности патоморфологических проявлений хронического миелоидного лейкоза у кур
- Шульпин М.И., Меньщикова А.Э., Лазарева С.П. Изучение распространения вируса лейкоза птиц подгруппы J на территории Российской Федерации // Тр. Федерального центра охраны здоровья животных. - Владимир, 2013. - Т. 11, № 1. - С. 64-70.
- Fadly A.M., Smith E.J. Isolation and some characteristics of a subgroup J-like avian leukosis virus associated with myeloid leukosis in meat-type chickens in the United States // Avian Diseases. - 1999. - Vol. 43. - P. 391-400.
- Гребенникова Т.В. и др. Исследование птицы на наличие вируса лейкоза методом ПЦР // Птица и птицепродукты. - 2003. - № 6. - С. 35-37.
- Spencer J.L., Chan M. Nadin-Daat-type chickens // Avian Diseases. - 2007. - Vol. 51 (3). - P. 725-732.
- Sun S., Cui Z. Epidemiological and pathological studies of subgroup J avian leukosis virus infections in Chinese local "yellowchickens" // Avian Pathology. - 2007. - Vol. 36 (3). - P. 221-226.
- Плотников В.А. Молекулярно-генетический анализ и биологическая характеристика полевых изолятов вируса лейкоза птиц, циркулирующих на территории Российской Федерации: дис. … канд. биол. наук. - М., 2014. - 146 с.
- Bagust Т., Fenton S., Reddy M. Avian leukosis virus subgroup J (ALV-J): Developing laboratory technologies for diagnosis in Australia: A report for the Rural Industries Research and Development Corporation. - Melbourne, 2004. - 66 p.
- Payne L.N., Nair V. Thelongview: 40 year sofavianleukosisresearch // AvianPathol. - 2012. - Vol. 41, № 1. - P. 1-9.
- Payne L.N. HPRS-103: A retro virus strikes back. The emergence of subgroup J avian leukosis virus // Avian Pathology, 2007. - P. 36-45.
- Ewert D.L., DeBoer Ewert G.F. Avian lymphoidleukosis: Mechanism of lymphomagenesis // Advances in Veterinary Science and Comparative Medicine. - 1988. -Vol. 32. - P. 37-55.
- Fadly A.M., Smith E.J. Isolation and some characteristics of a subgroup J-like avian leukosis virus associated with myeloidleukosis in meat-type chickens in the United States // Avian Diseases. - 1999. - Vol. 43. - P. 391-400.
- Payne L.N., Gillespie A.M., Howes K. MyeloidLeukemia and transmission of the HPRS-103 strain of avianleukosis virus // Leukemia, 1992. - Vol. 6. - P. 1167-1176.
- Pandiri A.R., Reed W.M., Mays J.K., Fadly A.M. Influence of strain, dose of virus, and age at inoculation on subgroup J avian leukosis virus persistence, antibody response, and oncogenicity in commercial me // Avian Diseases, 2007. - Vol. 51 (3). - Р. 725-732.
- Лазарева С.П., Ушакова А.Н. Культивирование полевых изолятов вируса лейкоза птиц подгруппы J, выявленных в период 2008-2010 гг. на территории Российской Федерации // Тр. Федерального центра охраны здоровья животных. - 2012. - Т. 10. - С. 139-145.
- Witter R.L., Fadly A.M. Reduction of horizontal transmission of avian leukosis virus subgroup J in broiler breeder chickens hatched and reared in small groups // Avian Pathology. - 2001. - Vol. 30 (6). - P. 641-654.
- Лазарева С.П., Ерошина Т.И., Мудрак Н.С., Чвала И.А. Особенности лейкоза птиц при экспериментальном заражении 40-суточных цыплят-бройлеров // Ветеринария сегодня. - 2014. - № 2 (9). - С. 34-39.
- Вахрушева Т.И. Особенности патоморфологических изменений органов и тканей у кур-несушек при патологии репродуктивной системы // Вестн. КрасГАУ. - 2015.- № 11. - С. 198-206.
- Плотников В.А., Гребенникова Т. В., Южаков А. Г., Дудникова Е.К. и др. Молекулярно-генетический анализ полевых изолятов вируса лейкоза птиц, циркулирующих на территории Российской Федерации // Вопросы вирусологии. - 2012. - Т. 57, № 5. - С. 38-43.


