Особенности проявлений метаболического синдрома в различных возрастных группах
Автор: Чернавский С.В., Фурсов А.Н., Потехин Н.П., Яковлев В.Н.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.6, 2011 года.
Бесплатный доступ
В результате исследования особенностей МС в различных возрастных группах 634 (457 мужчин и 177 женщин) пациентов было установлено, что в возрастном диапазоне до 50 лет основными компонентами МС являются «нарушения углеводного обмена», «гипертрофия миокарда», «атерогенная дислипидемия», «центральная гемодинамика» и «факторы риска»; у пациентов старше 50 лет - «нарушения липидного обмена», «абдоминальное ожирение», «артериальная гипертония», «ремоделирование сосудов»и «гипертрофия миокарда».
Метаболический синдром
Короткий адрес: https://sciup.org/140188013
IDR: 140188013 | УДК: 616-008.6-053
Текст научной статьи Особенности проявлений метаболического синдрома в различных возрастных группах
Взаимосвязь между ожирением, нарушениями углеводного обмена, гиперхолестеринемией (ГХС) и артериальной гипертензией (АГ) еще в начале прошлого столетия отмечали Г. А. Ланг и А. Л. Мясников (11). Однако начало широких исследований в этой области связано с работами G. Reaven, который в знаменитой Бантингской лекции сформулировал понятие о «синдроме Х», отметив, что комплекс метаболических и сердечно-сосудистых факторов риска (АГ, гипертриглицеридемия, гипоаль-фахолестеринемия и гиперинсулинемия) имеет общую этиологию – инсулинорезистентность [15].
В настоящее время метаболический синдром (МС) является одной из актуальных проблем медицины. Особое внимание, уделяемое МС, связано с его высокой распространенностью среди населения экономически развитых стран, в которой он составляет от 15 до 50% и выше. В России МС в возрасте старше 30 лет диагностируется у 30% населения, причем число больных непрерывно растет [8, 12, 17]. Доля больных МС по данным терапевтических отделений ГВКГ имени Н.Н. Бурденко составляет 16% [10].
Клиническая значимость полиметаболических нарушений заключается в ускоренном формировании у пациентов трудоспособного возраста таких нозологических форм как ишемическая болезнь сердца (ИБС) и сахарный диабет 2 типа (СД 2 типа) с развитием сопутствующих им кардио-васкулярных осложнений [3, 4, 12]. Возрастание сум-мационного индивидуального сердечно-сосудистого риска в несколько раз при сочетании компонентов МС обусловливает его медико-социальную значимость [5, 6]. У больных с МС в 6–7 раз чаще развиваются инфаркты головного мозга (ИГМ) и в 10 раз – инфаркты миокарда (ИМ), общая смертность возрастает в 2,4 раза [7, 14]. Кроме этого выделение МС имеет большое клиническое значение, поскольку, это состояние является обратимым, и при соответствующем лечении можно добиться исчезновения или, по крайней мере, уменьшения выраженности основных его проявлений и осложнений [7, 12, 16]. Согласно данным проспективных исследований имеется определенная последовательность в развитии компонентов МС. Чаще всего дислипидемия (ДЛП) и манифестация нарушений углеводного обмена развиваются после 35 лет. В среднем срок формирования полного кластера МС составляет не менее 8–10 лет [1, 3, 6].
В клинической практике все чаще применяются методы математического моделирования [2, 9, 13]. Интегральный подход к анализу патологических процессов дает возможность выявить ведущие симптомокомплексы заболевания (2). Оценка факторной нагрузки ведущих сим-птомокомплексов заболевания позволяет выявить новые взаимосвязи разнообразных проявлений болезни, разработать комплекс лечебно-диагностических мероприятий, направленных на профилактику осложнений [9, 13].
По нашему мнению, целесообразно приоритетные лечебные мероприятия при МС проводить не только с учетом ведущих его патогенетических звеньев, но и с учетом возрастных характеристик пациентов.
Материалы и методы
Нами проанализировано 634 истории болезни больных с МС согласно критериев включения, рекомендованных ВНОК (2009 г.). Выполнен анализ компонентов МС с учетом возраста обследованных больных. Первую группу (до 50 лет) составили 209 человек (156 мужчин и 53 женщины), вторую (старше 50 лет) – 425 человека (301 мужчина и 124 женщины). Характеристика обследованных лиц представлена в таблице 1. Средний возраст пациентов был 50,8±2,9 года, АГ соответствовала 1 степени (систолическое артериальное давление (АДс) 143,1±4,1 мм рт.ст. и диастолическое артериальное давление (АДд) 89,1±2,4 мм рт.ст.), индекс массы тела (ИМТ) составлял 32,5±1,3. Длительность МС составила 4,9±1,6 года.
Табл. 1. Характеристика обследованных больных с метаболическим синдромом
|
Признак |
1 группа (n=209) |
2 группа (n=425) |
|
Возраст, лет |
47,5±2,3 |
54,3±3,5 |
|
Пол, м/ж |
156/53 |
301/124 |
|
Абдоминальное ожирение
|
94 (45%)** 58 (27,8%)** 40 (19,1%)** 17 (8,1%)** |
86 (20,2%) 130 (30,6%) 129 (30,4%) 80 (18,8%) |
|
ИМТ, ед. |
31,2±1,3** |
33,9±2,2 |
|
Адс, мм рт.ст. |
138,2± 4,1** |
148,1±5,2 |
|
АДд, мм рт.ст. |
88,1±2,0* |
90,2±4,1 |
|
Гликем. натощ., ммоль/л |
6,4±0,2** |
6,0±0,1 |
|
ТГ, ммоль/л |
1,5±0,02** |
2,0±0,03 |
|
ХС ЛПВП, ммоль/л |
1,0±0,04 |
1,1±0,01 |
|
ХС ЛПНП, ммоль/л |
2,8±0,03** |
3,4±0,05 |
Примечание: * – достоверность различий -p<0,05; ** – р<0,01.
Всем больным наряду с общепринятым обследованием выполнялись эхокардиография (ЭхоКГ), при которой оценивали конечный систолический (КСО) и конечный диастолический объем (КДО), диастолическую толщину задней стенки левого желудочка (ДТ ЗСЛЖ) и межжелудочковой перегородки (ДТ МЖП), массу миокарда (ММЛЖ); велоэргометрия (ВЭМ); холтеровское мониторирование ЭКГ (ХМ ЭКГ) с подсчетом количества предсердных (SVT Ex) и желудочковых (V Ex) экстрасистол; суточное мониторирование АД (СМАД); ультразвуковое допплеровское исследование магистральных артерий головы (УЗДГ МАГ) с оценкой скорости кровотока и наличия начальных атеросклеротических изменений в средней (СМА), передней (ПМА) мозговой, общей сонной (ОСА), внутренней сонной (ВСА) артерии. Также исследовался уровень ряда гормонов сыворотки крови (кортизол, альдостерон). Полученные результаты вошли в формализованный протокол, что позволило в последующем создать базу данных для обработки ЭВМ.
Статистическая обработка результатов исследований
В качестве статистического критерия достоверности различий использовали t-критерий Стьюдента, рассчитанный по следующей формуле:
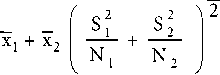
где Xi – среднее значение в первой группе; X2 – среднее значение во второй группе; S1 – стандартное отклонение в первой группе; S2 – стандартное отклонение во второй группе; N1 – количество больных в первой группе; N2 – количество больных во второй группе. Различия считали достоверными при р≤0,05.
После получения матрицы коэффициентов корреляции для уменьшения объема информации об исследу- емом медицинском объекте был выполнен факторный анализ, который позволяет создавать математические модели синдромологического подхода в медицине. В результате факторизации матрицы коэффициентов корреляции клинические признаки были сведены в группы, идентичные понятию «синдрома болезни», причем первый фактор отражал максимальную информацию о связях исследуемого явления, а каждый из последующих факторов дополнял информацию о связях признаков.
Результаты собственных исследований
В 1 группе обследованных чаще диагностировалось абдоминальное ожирение (АО) первой и второй степени, тогда как во 2 – преимущественно второй и третьей. У больных МС старше 50 лет (2 группа) были достоверно выше показатели как АДс (р<0,01), так и АДд (p<0,05), чем у пациентов 1 группы. Уровень гликемии натощак был выше у пациентов в возрасте до 50 лет (1 группа), тогда как значения триглицеридов (ТГ) и холестерина липопротеидов низкой плотности (ХС ЛПНП) – в возрасте старше 50 лет (2 группа) (табл. 1). Таким образом, достоверные различия в выраженности АО, степени АГ, как АДс, так и АДд, показателей липидограммы у пациентов до 50 лет (1 группа) и старше 50 лет (2 группа) свидетельствуют о «накоплении» данных признаков с возрастом. В то же время, превалирование в 1 группе нарушений углеводного обмена можно расценивать как более раннее формирование СД 2 типа у этой категории больных.
Оценка ведущих симптомокомплексов метаболического синдрома
При факторном анализе 110 признаков, внесенных в формализованную историю болезни каждого пациента с МС, в итоге было выделено пять факторов или ведущих симптомокомплексов, объясняющих 62% всей использованной дисперсии системы (табл. 2).
Первый фактор (симптомокомплекс) несет наибольшую информацию об исследованном явлении, что определяется процентом использованной дисперсии. Каждый последующий фактор несет меньшую информацию, но она ортогональна предыдущей, т.е. факторы не имеют корреляционной связи между собой.
Уже первый фактор, отражающий наибольший процент дисперсии системы, выявил определенные различия в группах сравнения (в 1-й он составил 28%, во 2-й – 30%). Так, если наиболее весомым признаком, определившим и название фактора («нарушение углеводного обмена»), у лиц до 50 лет тощаковое содержание глюкозы крови и уровень постпрандиальной гликемии, то у лиц старше 50 лет наибольшим удельным весом обладали признаки, характеризующие нарушения липидного обмена по атерогенному сценарию [общий холестерин (ОХС), ХС ЛПНП, ТГ] – фактор «нарушение липидного обмена».
Обращает на себя внимание то, что именно в этот симптомокомплекс вошел признак «наследственность по АО», свидетельствующий о генетической детерминирован-
Табл. 2. Ведущие симптомокомплекса метаболического синдрома в различных возрастных группах
|
Фактор |
Группа 1 (n=209) |
Группа 2 (n= 425) |
|
Первый |
Нарушение углеводного обмена (28%) Глюкоза натощак +0,799 Глюкоза постпр. +0,618 SVT Ex +0,598 V Ex +0,530 F1= 1/26,2/0,799 Х1+…/ |
Нарушение липидного обмена (30%) ОХС +0,619 ХС ЛПНП +0,598 ТГ +0,578 Альдостерон (утро) +0,520 Кортизол (утро) +0,478 КДО +0,420 КСО +0,401 Наследств. по АО +0,370 F1= 1/34,1/0,948 Х1+…/ |
|
Второй |
Гипертрофия миокарда (12%) ДТ ЗСЛЖ +0,887 ДТ МЖП +0,869 ММЛЖ +0,729 ЛП +0,714 F2= 1/19,1/0,887 Х1+…/ |
Абдоминальное ожирение (16%) ИМТ +0,961 Глюкоза натощ. +0,807 Глюкоза постпр. +0,675 ММЛЖ +0,650 Неспец. измен. зубца Т (ВЭМ) +0,545 F2= 1/21,7/0,961 Х1+…/ |
|
Третий |
Атероген. дислипидемия (9%) ОХС +0,811 ХС ЛПНП +0,768 ТГ +0,711 ЧСС субмакс. (ВЭМ) +0,561 ХС ЛПВП -0,650 F3= 1/11,0/0,811 Х1+…/ |
Артериальная гипертензия (7%) АДд мах (СМАД) +0,678 Глюкоза постпр. +0,650 АДc +0,597 АДср (СМАД) +0,504 F3= 1/13,0/0,678 Х1+…/ |
|
Четвертый |
Центральная гемодинамика (7%) Мин.объем.кровооб. +0,861 Скор.кровотока СМА +0,844 АДс +0,821 КДО +0,588 КСО +0,522 F4= 1/7,9/0,861 Х1+…/ |
Ремоделирование сосудов (5%) Атеросклероз ОСА +0,795 Атеросклероз ВСА +0,766 ММЛЖ +0,598 Скор. кровотока ПА +0,622 Скор. кровотока ВСА +0,567 F4= 1/5,6/0,795 Х1+…/ |
|
Пятый |
Факторы риска (5%) АСТ +0,671 АЛТ +0,582 Курение +0,493 Тромбоциты -0,578 Возраст -0,532 F5= 1/3,12/0,671 Х1+…/ |
Гипертрофия миокарда (4%) ДТ ЗСЛЖ +0,870 ДТ МЖП +0,862 ММЛЖ +0,451 Неспец. измен. зубца T (ВЭМ) +0,430 F5= 1/3,9/0,870 Х1+…/ |
|
Общий % дисперсии |
62 |
62 |
ности вышеназванных изменений, а так же такие признаки, как уровень альдостерона и кортизола плазмы крови. Все признаки, составляющие первый симптомокомплекс у лиц старше 50 лет, показали тесную положительную связь между собой. Полученные данные подтверждают, в частности, мнение о существовании взаимозависимости между выраженностью висцерального ожирения и активностью ренин-ангиотензин-альдостероновой и гипофизарно-надпочечниковой систем [1, 3, 17].
По своим характеристикам у лиц до и после 50 лет различался и второй фактор, который, соответственно, объединил 12% и 16% дисперсии системы в группах. У лиц 1 группы в этот симптомокомплекс вошли исключительно признаки, отражающие состояние сердечной мышцы, а именно, ее гипертрофию. Гипертрофия миокарда (масса миокарда ЛЖ) сохраняет свое значение в формировании второго фактора и в группе лиц после
50 лет, но, при этом, не играет доминирующей роли. Наибольший удельный вес здесь выпадает опять же на обменные нарушения (ИМТ, тощаковая и постпранди-альная гликемия). Все названные признаки имеют положительную связь между собой, но ИМТ превалирует: чем выше он и, следовательно, абдоминальное ожирение, тем значимее нарушения углеводного обмена, выраженность гипертрофии мышцы сердца, и, связанные с ней, изменения ЭКГ, в частности, зубца Т.
Интересные данные получены при сравнительном анализе третьего фактора. Если среди лиц старше 50 лет фактор, подтверждающий нарушения липидного обмена при МС, был определяющим (фактор 1), то для лиц более молодого возраста он по своей значимости занял лишь третье место, не имея в качестве составляющей положительной связи с признаками дисфункцией надпочечников, что мы видим у лиц старшей возрастной группы. Это заставляет предполагать, что дисфункция надпочечников при МС по времени развивается позднее, чем нарушения липидного обмена и зависит от него.
В то же время, фактор «артериальной гипертензии» у лиц старше 50 лет вошел в группу пяти ведущих сим-птомокомплексов, в то время как для пациентов более молодого возраста он оказался не актуальным вообще. Все это свидетельствует в пользу того, что АГ, как и нарушения липидного обмена, лишь с возрастом приобретают все большее и большее значение в рамках МС.
Четвертый фактор при всех различиях между первой и второй группами (соответственно, 7% и 5% дисперсии) в сравнении логично отражает динамику событий, обусловленных возрастом. У пациентов до 50 лет по ведущему признаку он обозначен нами как «центральная гемодинамика», для пациентов старшего возраста – как «ремоделирование сосудов». Наибольшим удельным весом в факторе «центральная гемодинамика» обладает признак минутный объем кровообращения. От его величины напрямую зависят скоростные показатели по сосудам головного мозга, в частности, по средней мозговой артерии, уровень диастолического АД и конечный систолический и диастолический объем ЛЖ. Это касается лиц в возрасте до 50 лет. Набор признаков в сим-птомокомплексе «ремоделирование сосудов» у лиц старше 50 лет позволяет говорить о том, что существовавшие ранее гемодинамические нарушения к этому времени реализуются не только в виде локального уменьшения просвета в ряде сосудистых бассейнов (общая и внутренняя сонные артерии) с параллельным увеличением скорости кровотока по ним, но и увеличением массы миокарда ЛЖ.
И, наконец, пятый фактор. Для лиц до 50 лет он объединил 5% дисперсии системы, вобрав в себя признаки, позволившие обозначить его как «факторы риска» – повышение АлАТ и АсАТ вызванное, вероятнее всего, сопутствующим жировым гепатозом, возможно и алиментарного генеза, курение, возраст. Эти признаки не вошли ни в один из факторов, присущих лицам старше 50 лет, вероятно, потому что к этому возрасту, они уже успели реализовать себя и отошли на второй план. В старшей возрастной группе сохранил свое значение фактор «гипертрофия миокарда», но процент дисперсии, объясняющий данный фактор, уменьшился до 4%, по сравнению с группой до 50 лет, где он равнялся 12%. В старшем возрасте гипертрофия миокарда ЛЖ уже успела сформироваться. Наибольшее значение в общей структуре МС стали приобретать иные симптомокомплексы и признаки.
Заключение
Факторный анализ продемонстрировал определенные различия как в ведущих симптомокомплексах (факторах), определяющих МС, так и в наборе составляющих их признаков, свидетельствующих о его «возрастной» неоднородности.
В возрастном диапазоне до 50 лет основными компонентами МС являются «нарушения углеводного обмена», в частности повышение уровня постпранди- альной гликемии, что наряду с «гипертрофией миокарда», процессами ремоделирования сердечной мышцы, «атерогенной дислипидемией» вызывают изменения «центральной гемодинамики», что на фоне «факторов риска», в частности курения, нарушения реологии крови способствует формированию отдельных нозологических форм заболеваний (сахарный диабет 2 типа, ИБС).
Напротив, у пациентов старше 50 лет «нарушения липидного обмена» на фоне «абдоминального ожирения» способствуют развитию «артериальной гипертонии», носящей вторичный характер, что наряду с «ремоделированием сосудов», «гипертрофией миокарда» и определяет в дальнейшем характер развития сердечно-сосудистых осложнений (ИБС, в т.ч. инфаркт миокарда и мозговой инсульт).
Полученные данные позволяют оптимизировать лечебно-диагностические мероприятия у больных с по-лиметаболическими нарушениями с учетом возрастного ценза и проводить более целенаправленную вторичную профилактику осложнений.
Список литературы Особенности проявлений метаболического синдрома в различных возрастных группах
- Бутрова С. А. Метаболический синдром: патогенез, клиника, диагностика, подходы к лечению. Русский медицинский журнал 2001; 2: -С. 56-60.
- Гельфанд И.М. Обзор некоторых задач медицинской диагностики и прогнозирования. в кн. «Вопросы кибернетики» -1983. -вып.85. -С. 111-113.
- Гинзбург М.М., Крюков Н.Н. Ожирение. Влияние на развитие метаболического синдрома. Профилактика и лечение. -М.: Медпрактика -М. -2002 -128 с.
- Дедов И.И. Инсулиновая резистентность в патогенезе сахарного диабета типа 2 и медикаментозная возможность ее преодоления/И.И. Дедов, М.И. Балаболкин//Врач. -2006. -№ 11. -С 8-13.
- Козиолова Н.В., Конради А.О. Оптимизация критериев метаболического синдрома. Российский институт метаболического синдрома -согласованная позиция//Артериальная гипертензия. -2007. -№ 3. -C. 197-198
- Константинов В.О., Сайфулина Я.Р. Метаболический синдром -болезнь или случайный набор риск-факторов//Артериальная гипертензия. -2007. -№ 3. -С. 195-196.
- Рекомендации экспертов ВНОК по диагностике и лечению метаболического синдрома (второй пересмотр)//Кардиоваскулярная терапия и профилактика. 2009; 6 (Прил. 2).
- Старкова Н.Т., Дворяшина И.В. Метаболический синдром инсулинорезистентности: основная концепция и следствие (обзор). Тер. архив, 2004; 10: 54-58
- Флетчер Р., Флетчер С., Вагнер Э. Клиническая эпидемиология: основы доказательной медицины. Пер. с англ. М: Медиа Сфеpа 1998; 347 с.
- Фурсов А.Н., Потехин Н.П., Чернов С.А, Мычка В.Б., Чернавский С.В. Метаболический синдром: взгляд на проблему и подходы к лечению//Военномедицинский журн. -2008. -№ 9. -С. 39-43
- Чазов Е.И. Руководство по кардиологии. Т. 4. Болезни сердца и сосудов. Москва. -«Медицина» -1982. -608 с.
- Чазова И.Е., Мычка В.Б. Метаболический синдром/М.: Mеdia Medica, 2004. -163 с.
- Шевченко Ю.Л., Шехвердиев Н.Н., Оточкин А.В. Прогнозирование в кардиохирургии. Санкт-Петербург, Москва, Харьков, Минск. Питер., 1988, 200 с.
- Naruse M., Tanabe A., Takagi S., Tago K., Takano K. Insulin resistance and vascular function. Nippon Rinsho 2000 Feb;58(2):344-7
- Reaven G.M. Banting Lecture 1988. Role of insulin resistance in human disease//Diabetes. -1988. -№37. -Р. 1595-1607.
- Zarich S et al. Prevalence of metabolic syndrome in young patients with acute MI: does the Framingham Risk Score underestimate cardiovascular risk in this population//Diabetes and Vascular Disease Research. 2006. Vol. 3. P. 103-106.
- Zimmet P. et al. The Metabolic Syndrome: A Global Public Health Problem and A New Definition//Journal of Atherosclerosis and Thrombosis. 2005. Vol. 12. P. 295-300.


