Особенности пролиферации и апоптоза эпителиоцитов толстой кишки крыс после облучения в дозе 8 гр
Автор: Саакян С.В., Каракаева Э.Б.Г., Шаповалова Е.Ю., Зорин И.А., Демяшкин Г.А.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.31, 2023 года.
Бесплатный доступ
Эпителиальные клетки кишечника характеризуются высокой митотической активностью и обладают высокой радиочувствительностью ко всем видам ионизирующего облучения, которые вызывают их повреждение. В современной морфологии и радиологии отсутствуют данные о воздействии активных электронов на слизистую оболочку кишечника, несмотря на перспективность и активное внедрение этого вида излучения для терапевтических целей в онкологии. Цель исследования: иммуногистохимическая оценка пролиферации и апоптоза клеток эпителия толстой кишки самцов крыс линии Вистар после локального облучения электронами в дозе 8 Гр. Облучение животных производили на линейном ускорителе NOVAC-11, при мощности дозы 1 Гр/мин, энергии 10 МэВ и частоте 9 Гц, диаметр поля облучения тазово-абдоминальной области составил 100 мм. Животных из каждой группы выводили из эксперимента на первые и третьи сутки. Гистологические препараты ободочной кишки (n=30) двух групп, первой - контрольной (n=10) и второй, опытной группы (n=20) исследовали иммуногистохимическим методом с антителами к Ki-67 и Cas3. В препаратах крыс, выведенных через сутки после облучения, выявили преобладание апоптотических процессов. Количество позитивных клеток на окраску с антителами к каспазе 3 было увеличено в 1,5 раза в опытной группе по сравнению с контрольной, а количество Ki-67-позитивных клеток, напротив, было снижено, в 1,5 раза. На 3 сутки после облучения электронами в эпителии толстой кишки количество иммунопозитивных клеток не отличалось от контрольных значений. Таким образом, при локальном однократном облучении электронами тазово-абдоминальной области крыс в дозе 8 Гр через сутки отмечается снижение количества стволовых эпителиальных клеток кишечных крипт ободочной кишки, что подтверждено сдвигом пролиферативно-апоптотического баланса в сторону гибели клеток. В динамике наблюдения на третьи сутки эксперимента наблюдается увеличение пула пролиферирующих клеток с последующим восстановлением кишечных крипт.
Слизистая оболочка толстой кишки, ионизирующее облучение энтероциты, апоптоз, пролиферация, иммуногистохимия
Короткий адрес: https://sciup.org/143181185
IDR: 143181185 | DOI: 10.20340/mv-mn.2023.31(3).790
Features of proliferation and apoptosis of colonic epitheliocytes after electron irradiation at a dose of 8 gy
Intestinal epithelial cells are characterized by high mitotic activity and have high radiosensitivity to all types of ionizing radiation that cause their damage. In modern morphology and radiology, there is no data on the effect of active electrons on the intestinal mucosa, despite the promise and active implementation of this type of radiation for therapeutic purposes in oncology. Purpose of the study: immunohistochemical assessment of proliferation and apoptosis of colon epithelial cells in male Wistar rats after local irradiation with electrons at a dose of 8 Gy. Animals were irradiated using a linear accelerator NOVAC-11, at a dose rate of 1 Gy/min, energy of 10 MeV and frequency of 9 Hz, the diameter of the irradiation field of the pelvic-abdominal region was 100 mm. Animals from each group were removed from the experiment on the first and third days. Histological preparations of the colon (n=30) from two groups, the first control group (n=10) and the second experimental group (n=20), were examined by immunohistochemical method with antibodies to Ki-67 and Cas3. In preparations of rats bred one day after irradiation, a predominance of apoptotic processes was revealed. The number of positive cells stained with antibodies to caspase 3 was increased by 1.5 times in the experimental group compared to the control group, and the number of Ki-67-positive cells, on the contrary, was reduced by 1.5 times. On day 3 after electron irradiation in the epithelium of the colon, the number of immunopositive cells did not differ from control values. Thus, with local single irradiation of the pelvic-abdominal region of rats with electrons at a dose of 8 Gy, a decrease in the number of stem epithelial cells of the intestinal crypts of the colon is observed every other day, which is confirmed by a shift in the proliferative-apoptotic balance towards cell death. In the dynamics of observation on the third day of the experiment, an increase in the pool of proliferating cells is observed, followed by restoration of intestinal crypts.
Текст научной статьи Особенности пролиферации и апоптоза эпителиоцитов толстой кишки крыс после облучения в дозе 8 гр
Саакян С.В., Каракаева Э.Б-Г., Шаповалова Е.Ю., Зорин И.А., Демяшкин Г.А. Особенности пролиферации и апоптоз эпителиоцитов толстой кишки после облучения электронами в дозе 8 Гр. Морфологические ведомости. 2023;31(3):790. mn.2023.31(3).790
Saakian SV, Karakaeva EB-G, Shapovalova EY, Zorin IA, Demyashkin GA. Eatures of proliferation and apoptosis of colonic epitheliocytes after electron irradiation at a dose of 8 Gy. Morfologicheskie Vedomosti – Morphological newsletter. 2023;31(3):790. (3).790
Введение. Эпителиальные клетки толстой кишки характеризуются высокой митотической активностью. Считается, что они обладают повышенной радиочувствительностью ко всем видам излучения, причем не только к локальному (тазовоабдоминальному), но и к общему облучению [1-2]. Влияние радиоизлучения на эпителиальные стволовые клетки кишечных крипт было подробно изучено в предыдущих работах других авторов. Известно, что инициация постлучевого гастроинтестинального синдрома происходит вследствие повреждения клеток кишечных крипт и сопровождается отеком, гиперемией, слущиванием эпителия, изъязвлениями, стриктурами и некрозом стенки кишки [3]. Ионизирующее излучение вызывает повреждение клеток и субклеточных структур. Аберрации ДНК приводят к нарушению сигнальных внутриклеточных путей, ответственных за нормальное функционирование жизненного цикла, инициацию апоптоза и репарацию молекул генетической информации [4-5].
Активация апоптоза происходит, как в условиях клеточного и тканевого гомеостаза, так и при разных патологических состояниях, таких как ишемия, неврологические нарушения, неоплазии и различные инфекции, а также при повреждениях ДНК [4]. В настоящий момент известны два механизма, которые активируют апоптоз в клетках. Внутренний путь, регулируемый митохондриями и внешний, индуцированный лигандами клеточной гибели. Эти лиганды способны индуцировать инициаторные протеазы, такие как каспаза-9, что приводит к активации терминальной протеазы - каспазы-3 [6]. В немногочисленных исследованиях было показано, что каспаза-3 является ключевой молекулой при активации апоптоза в эпителиоцитах толстой кишки после воздействия облучения. После повреждения ДНК запускается внутренний путь апоптоза, приводящий к высвобождению проапоптотических молекул и увеличению проницаемости митохондрий, что в свою очередь запускает активность терминальных молекул, таких как каспаза-7 и -3 [7-8].
В современной морфологии и радиологии отсутствует информация о воздействии электронов на слизистую оболочку толстой кишки, несмотря на перспективность и активное внедрение этого вида излучения для терапевтической практики в онкологии. Данные о воздействии других видов облучения на толстую кишку, в основном используемых в лучевой терапии, - противоречивы [2, 9-10]. В этом смысле морфологическое и молекулярно-биологическое исследования эффектов облучения электронами является актуальным, так как установлено, что оно обладает меньшим повреждающим эффектом на ткани [11]. В то же время при изучении влияния облучения электронами на эпителий толстой кишки важно оценить не только степень и глубину повреждений, но и пролиферативную активность эпителиоцитов, то есть их регенеративный потенциал.
Цель исследования: иммуногистохимическая оценка пролиферации и апоптоза эпителия толстой кишки после локального облучения электронами в дозе 8 Гр в эксперименте.
Материалы и методы исследования. В эксперименте использованы половозрелые крысы-самцы линии Вистар (n=30), которые были поделены на две группы: I - контрольная (n=10); II - опытная группа (n=20). Локальное однократное облучение электронами в дозе 2 Гр тазовоабдоминальной области производили на линейном ускорителе NOVAC-11 при мощности дозы 1 Гр/мин, энергии 10 МэВ и частоте 9 Гц, с диаметром поля облучения 100 мм. Животных каждой группы выводили из эксперимента на 1 и 3 сутки. Все манипуляции выполняли согласно «Международным рекомендациям по проведению медико-биологических исследований с использованием животных» (ЕЭС, Страсбург, 1985) и Хельсинской декларации (1985).
Фрагменты толстой (ободочной) кишки фиксировали в забуференом формалине, заливали в парафиновые блоки, гистологические срезы нарезали на микротоме толщиной 3 мкм, окрашивали гематоксилином и эозином. Микроскопический анализ выполняли с помощью систе- мы видеомикроскопии микроскопа Leica DM2000 (Германия), видеокамерой Leica ICC50 HD. Ключевые периоды жизненного цикла эпителия толстой кишки изучены с помощью маркеров терминации апоптоза (каспазы-3) и пролиферации (Ki-67). Иммуногистохимическое исследование проводили по стандартному протоколу в автоматическом режиме в иммуногистостейнере Bond-Max («Leica», Германия). Первичные антитела: к каспазе-3 (Invitrogen/Thermo Fisher Scientific; 74T2, 1:50) и Ki-67 (Abcam; ab15580, 1:100); вторичные – универсальные антитела (HiDef Detection™ HRP Polymer system, «Cell Marque», США). Количество иммунопози-тивных клеток подсчитывали в 10 полях зрения, при увеличении х400. Полученные данные были представлены в виде относительного числа позитивных клеток в %, как среднее значение доли (P) и ошибки средней доли (pm). Значимыми считали различия между показателями при p≤0,05.
Результаты исследования и обсуждение. Во всех гистологических препаратах толстой кишки животных через сутки после локального облучения электронами в дозе 8 Гр наблюдали типичную морфологическую картину постлучевого колита, которая проявлялась в дезорганизации однослойного цилиндрического эпителия с апоптотическими тельцами и воспалительной инфильтрации в подслизистой основе, слабом интерстициальном отеке. Количество бокаловидных клеток было снижено, а сами кишечные крипты расширены. На 3-и сутки эксперимента отмечали восстановление гистоархитектоники эпителия слизистой оболочки толстой кишки, расположение и строение кишечных крипт, количество бокаловидных клеток приблизилось к контрольным значениям. При иммуногистохимическом исследовании через сутки после локального облучения электронами выявили преобладание апоптотических процессов. Количество каспаза-3-позитивных клеток было увеличено в 1,56 раза в опытной группе по сравнению с контрольной с до 33,5% до 52,5% (табл. 1). Количество Ki-67-позитивных клеток, напротив, было после облучения снижено в 1,54 раза с 49% до 31,2%. На 3-и сутки после облучения элек- тронами в эпителии толстой кишки количество иммунопозитивных клеток статистически не отличалось от контрольных значений (табл. 1, рис. 1).
Таблица 1
Доля позитивно окрашенных к антигенам энтероцитов в гистологических препаратах толстой кишки контрольной и опытных групп крыс в % (P±p m )
|
Маркер |
Группа II (облучение) |
Группа I (контроль) |
|
|
1 сутки |
3 сутки |
||
|
Сaspase-3 |
52,4715,13 ' |
39,6113,27 |
33,4812,35 |
|
Ki-67 |
31,212,97 ; |
43,6214,73 |
49,2714,53 |
Примечание: ↑ - статистически значимое увеличение и ↓ -уменьшение по сравнению с контрольной группой
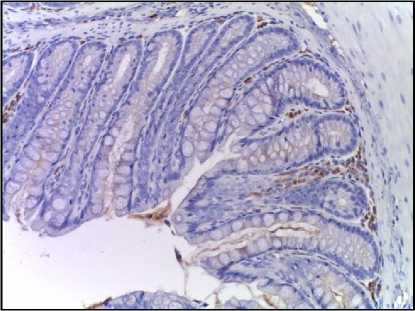
Электронотерапия является перспективным методом, обладающим терапевтическим эффектом при кратковременном облучении в высоких дозах, что значительно сокращает число осложнений по сравнению с лечением традиционными видами излучения. Значительная частота заболеваемости колоректальным раком и отсутствие данных об эффективности его лечения электронным излучением, как потенциальной альтернативы другим видам радиотерапии, стимулируют его экспериментальные исследования [11-12]. В проведенном эксперименте установлено, что эпителий толстой кишки обладает высокой радиочувствительностью, о чем свидетельствует морфологическая картина постлучевого колита, обнаруженная уже на первые сутки после облучения тазовоабдоминальной зоны крыс. Это явление подтверждает ранее проведенные исследования по аналогичным эффектам других видов ионизирующего излучения [1315]. В эксперименте было обнаружено, что уже на первые сутки после облучения электронами в эпителии значительно возрастает количество каспаза-3-позитивных клеток. Можно полагать, что результатом прямого воздействия электронов на энте-роциты толстой кишки является фрагментация ДНК и клеточных мембран, запуск апоптоза, завершающийся активацией каспазы-3 [7, 16]. Увеличение количества активированной каспазы-3 приводит к прекращению жизненного цикла энтеро-цитов. Наиболее интенсивно окрашенными на каспазу-3 были клетки, располагающиеся в области дна крип, являющиеся стволовыми для кишечного эпителия и обладающие, как известно, высокой митотической активностью (рис. 1).
Иммуногистохимические маркеры
Сaspase-3
8 Гр 1-е сутки
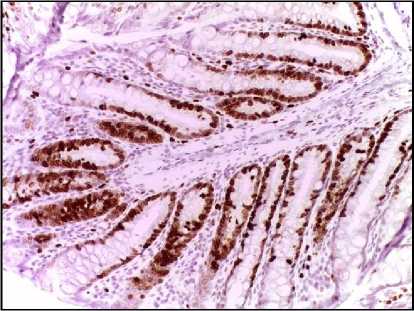
Ki-67
8 Гр 3-и сутки
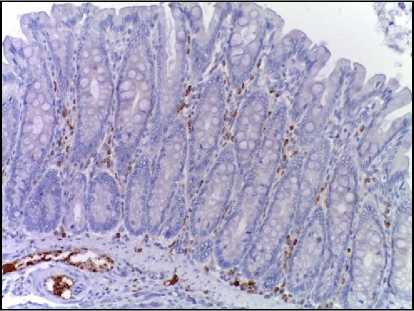
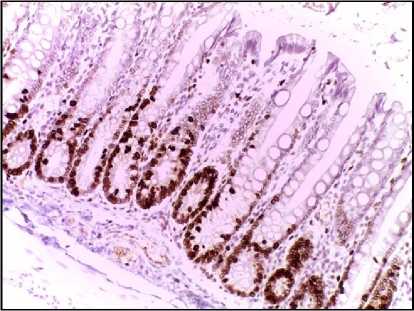
контроль
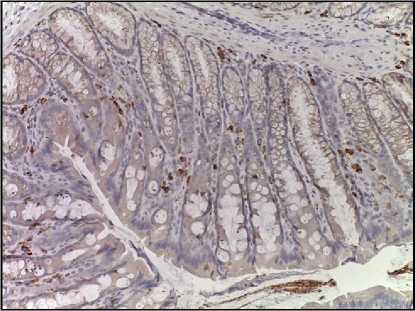
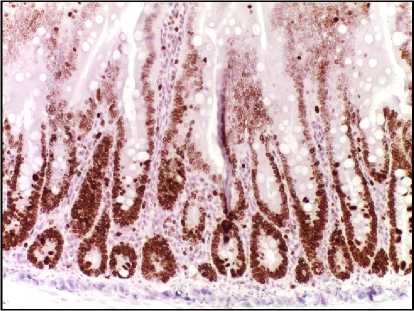
Рис. 1. Микрофото гистологических препаратов толстой кишки крыс после локального однократного облучения электронами в дозе 8 Гр. Окр.: иммуногистохимическая (см. в тексте) с докраской ядер гематоксилином. Ув.: ×200
Известно, что при вступлении в апоптоз энтероциты толстой кишки способны выделять молекулы, которые стимулируют сохранные стволовые клетки к ускоренной пролиферации [17-18]. Поэтому, наряду с указанным выше на первые сутки эксперимента эффектом облучения электронами, отмечали снижение количества Ki-67-позитивно окрашенных клеток в области дна кишечных крипт.
Однако уже на 3 сутки показатели пролиферации в опытной группе приблизились к значениям контрольной группы. Для восстановления пула эпителиоцитов кишечных крипт в такие кратчайшие сроки, очевидно вполне достаточно сохранившегося количества интактных стволовых клеток.
Заключение. Таким образом, при локальном однократном облучении элек- тронами тазово-абдоминальной области крыс Вистар в дозе 8 Гр через сутки отмечается снижение количества стволовых эпителиальных клеток кишечных крипт в толстой (ободочной) кишке, что подтверждается сдвигом пролиферативно-апоп-тотического баланса в сторону гибели клеток, оцененного соотношением каспа- зы-3 и Ki-67. В динамике, на третьи сутки эксперимента, наблюдается увеличение пула стволовых клеток с последующим восстановлением кишечных крипт.
Список литературы Особенности пролиферации и апоптоза эпителиоцитов толстой кишки крыс после облучения в дозе 8 гр
- Zhang L, Yu J. Role of apoptosis in colon cancer biology, therapy, and prevention. Curr Colorectal Cancer Rep. 2013;9(4):10.1007/s11888-013-0188-z. D0I:m1007/s11888-013-0188-z
- Booth C, Tudor G, Tudor J, et al. The Acute Gastrointestinal Syndrome in High-Dose Irradiated Mice. Health Phys 2012;103:383-399
- Akpolat M, Oz ZS, Gulle K, et al. X irradiation induced colonic mucosal injury and the detection of apoptosis through PARP-1/p53 regulatory pathway. Biomedicine & Pharmacotherapy 2020;127:110134. D0I:10.1016/j.biopha.2020.110134
- Hauer-Jensen M, Denham JW, Andreyev HJN. Radiation enteropathy — pathogenesis, treatment and prevention. Nat Rev Gastroenterol Hepatol 2014;11:470-479. D0I:10.1038/nrgastro.2014.46
- Araujo IK, Munoz-Guglielmetti D, Molla M. Radiation-induced damage in the lower gastrointestinal tract: Clinical presentation, diagnostic tests and treatment options. Best Pract Res Clin Gastroenterol 2020;48-49:101707. D0I:10.1016/j.bpg.2020.101707.
- Negroni A, Cucchiara S, Stronati L. Apoptosis, Necrosis, and Necroptosis in the Gut and Intestinal Homeostasis. Mediators Inflamm 2015;2015:250762. DOI: 10.1155Д015/250762
- McIntosh A, Meikle LM, Ormsby MJ, et al. SipA Activation of Caspase-3 Is a Decisive Mediator of Host Cell Survival at Early Stages of Salmonella enterica Serovar Typhimurium Infection. Infection and Immunity 2017;85:e00393-17. DOI: 10.1128/IAI.00393-17
- Beroske L, Van den Wyngaert T, Stroobants S, et al. Molecular Imaging of Apoptosis: The Case of Caspase-3 Radiotracers. IJMS 2021;22:3948. DOI: 10.3390/ijms22083948
- Rubio CA, Jalnäs M. Dose-time-dependent histological changes following irradiation of the small intestine of rats. Digest Dis Sci 1996;41:392-401. DOI:10.1007/BF02093834
- Otsuka K, Suzuki K. Differences in Radiation Dose Response between Small and Large Intestinal Crypts. Radiation Research 2016;186:302-314. DOI: 10.1667/RR14455.1
- Schüler E, Acharya M, Montay-Gruel P, et al. Ultra-high dose rate electron beams and the FLASH effect: From preclinical evidence to a new radiotherapy paradigm. Medical Physics 2022;49:2082-2095. DOI:10.1002/mp.15442
- Tam SY, Wu VWC. A Review on the Special Radiotherapy Techniques of Colorectal Cancer. Frontiers in Oncology 2019;9:208. DOI: 10.3389/fonc.2019.00208
- Muschel RJ, Hammond EM, Dewhirst MW. A New Assay to Measure Intestinal Crypt Survival after Irradiation: Challenges and Opportunities. Cancer Research 2020;80:927-928. DOI:10.1158/0008-5472.CAN-19-4045
- Moussa L, Usunier B, Demarquay C, et al. Bowel Radiation Injury: Complexity of the Pathophysiology and Promises of Cell and Tissue Engineering. Cell Transplant 2016;25:1723-1746. DOI:10.3727/096368916X691664
- Weiber S, Bjelkengren Gör, et al. Radiation Effects in the Colon: An Experimental Study in the Rat. Acta Oncologica 1993;32:565-569. DOI:10.3109/02841869309096119
- Pejchal J, Novotny J, Mafäk V, et al. Activation of p38 MAPK and expression of TGF-ß1 in rat colon enterocytes after whole body y-irradiation. International Journal of Radiation Biology 2012;88:348-358. DOI:10.3109/09553002.2012.654044
- Karmakar S, Deng L, He XC, Li L. Intestinal epithelial regeneration: active versus reserve stem cells and plasticity mechanisms. American Journal of Physiology-Gastrointestinal and Liver Physiology 2020;318:G796-802. DOI:10.1152/ajpgi.00126.2019
- Rees WD, Tandun R, Yau E, et al. Regenerative Intestinal Stem Cells Induced by Acute and Chronic Injury: The Saving Grace of the Epithelium? Front. Cell Dev. Biol. 2020;8:583919. DOI:10.3389/fcell.2020.583919


