Особенности протонирования поверхности силикагелей, модифицированных моноэтаноламином
Автор: Шаров Артем Владимирович, Воронцов Борис Сергеевич, Филистеев Олег Владимирович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 4 т.5, 2013 года.
Бесплатный доступ
Адсорбция ионов водорода на силикагелях, модифицированных моноэтаноламином с разной плотностью прививки модификатора, описана с применением модели химических реакций. Установлено протекание при протонировании двух поверхностных процессов, для которых определены константы равновесия при ионной силе, равной 1.
Силикагель, моноэтаноламин, модель химических реакций, константа равновесия
Короткий адрес: https://sciup.org/147160274
IDR: 147160274 | УДК: 544.723.54
Protonation features of the silica surfase, monoethanolamine modified
The adsorption of hydrogen ions on silica modified by monoethanolamine with different grafting densities is described using the chemical reactions model. It is established that two surface processes run at protonation, and their equilibrium constants are calculated at ionic strength equaling 1.
Текст научной статьи Особенности протонирования поверхности силикагелей, модифицированных моноэтаноламином
Аморфные кремнеземы с привитыми на поверхность функциональными группировками находят широкое применение в таких областях, как сорбция, катализ, хроматография и т. д. Особое место среди многочисленного класса этих материалов занимают кремнеземы с привитыми веществами, содержащими аминогруппы. Такие сорбенты представляют интерес благодаря наличию групп основного характера, способных к комплексообразованию с переходными металлами и ионному обмену. Эти особенности объясняют широкий спектр работ, посвященных протолитическим и комплексообразующим свойствам данных сорбентов.
Одним из веществ, способных химически взаимодействовать с гидроксильной поверхностью является моноэтаноламин (МЭА). Известно, что молекулы МЭА взаимодействуют с терминальными силанольными группами поверхности аэросилов с образованием сложноэфирной связи [1]. Нами были сделаны аналогичные выводы при изучении взаимодействия моноэтаноламина с промышленными силикагелями марок КСКГ и КСМГ. Исследование протолитических свойств привитых аминоэтоксигрупп выявило эффекты энергетической неоднородности поверхности, которая описывалась с применением модели непрерывного распределения констант [2]. При этом было сделано допущение о протекании только одной поверхностной реакции. Однако зачастую протонирование поверхностных аминогрупп включает в себя несколько равновесных реакций. Их учет возможен при применении модели химических реакций [3]. Основной постулат модели – прочность поверхностных комплексов зависит только от их стехиометрического состава. Адекватное применение модели позволяет рассчитать кажущиеся константы равновесия всех процессов в системе.
В работе проводится учет максимально возможного количества процессов при протонировании модифицированной моноэтаноламином поверхности.
Экспериментальная часть
Использовали образцы промышленных силикагелей марок КСКГ и КСМГ с характеристиками, приведенными в табл. 1.
Таблица 1
Характеристики использованных силикагелей
|
Марка силикагеля |
S уд , м /г |
d частиц , мкм |
ρ н , г/см3 |
|
КСКГ |
232 |
36 |
0,42 |
|
КСМГ |
460 |
45 |
0,78 |
Примечание. S уд – удельная площадь поверхности, определенная по методу адсорбции азота [7]; d ч астиц – эффективный диаметр частиц, определенный по методу седиментационного анализа; ρ н – насыпная плотность силикагелей, определенная по ГОСТ 9758-86.
Предварительно образцы прокаливали при температуре 150 °С в паровоздушной атмосфере до постоянной массы. Модифицирование осуществляли путем выдерживания силикагелей в обезвоженном моноэтаноламине. Различное количество МЭА на поверхности получали, варьи- руя температуру и время контакта сорбента и модификатора [2]. Полученные образцы промывались водой, высушивались при температуре 150 °С и хранились в эксикаторе с прокаленным хлоридом кальция. Всего исследовано 23 образца с плотностью прививки от 0,21 до 2,18 мкмоль/м2 (табл. 2). Поверхностные аминоэтоксигруппы устойчивы к гидролизу при выдерживании модифицированных силикагелей в воде в течение часа.
Для получения зависимостей состав-свойство проводили потенциометрическое титрование суспензий модифицированных силикагелей в 1 М растворе хлорида калия 0,1000 Н раствором соляной кислоты в термостатированной ячейке при 25 °С. Использовали иономер И-500, стеклянный индикаторный электрод ЭСЛ-430-07СР, хлорсеребряный электрод сравнения ЭВЛ 1М [4, 5]. Время достижения сорбционного равновесия после прибавления каждой порции титранта не превышало пятнадцати минут. Титрование каждого образца повторяли три раза.
Обработку экспериментальных данных в рамках модели химических реакций на модифицированной поверхности осуществляли с применением программы CLINP 2.1 (авторы С.А. Мерный, Д.С. Коняев, Ю.В. Холин, Харьковский национальный университет им. В. Н. Каразина, Украина ). Программа предназначена для расчета неизвестных констант равновесия и так называемых факторов интенсивности (например, в методе спектрофотометрии – это коэффициенты светопоглощения) для реакций в растворе и на поверхности. Способ расчета – минимизация отклонения расчетных точек зависимости состав равновесной системы – ее свойство от экспериментальных данных путем повторяющихся итераций [6, 7]. Для проверки адекватности примененной модели рассчитываемые программой критерии А (среднее значение невязок А = Увыч - Уэксп), А (среднее значение модулей невязок А = ^выч — ^эксп), Y2 (эксцесс распределения) сравнивали с их табличными значениями. Меньшие по сравнению с табличными величины статистических критериев свидетельствуют в пользу адекватности применения модели. Следующим инструментом проверки являлся анализ взвешенных невязок ^ = w1/2A , где w - статистический вес. Для его проведения строили зависимость величин ^ от степени оттитрованности или объема прибавляемого титранта. Визуальный анализ вида такой зависимости позволяет обнаружить грубые промахи и неполноту модели. Если одна из взвешенных невязок намного превосходит остальные, соответствующую экспериментальную точку считают грубым промахом. О неполноте модели (недостаточном количестве описываемых процессов) свидетельствует систематический характер ^, при изменении степени оттитрованно-сти. В пользу полноты модели свидетельствует случайный характер взвешенных невязок, подчиняющийся нормальному распределению [7, 8].
Обсуждение результатов
Примеры кривых титрования некоторых образцов приведены на рис. 1. Форма кривых указывает на наличие на поверхности слабых оснований. Энергетическая неоднородность поверхности, упомянутая выше, выявлена после преобразования кривых в изотермы адсорбции и последующей их обработки с нахождением концентрационных констант равновесия при ионной силе, равной 1. При этом выявлены достоверные изменения данных констант при увеличении плотности прививки моноэтаноламина. Кроме того, расчет концентрационных констант в каждой точке кривых титрования также выявил их зависимость от степени протонирования. Все это говорит об энергетической неоднородности поверхности в реакциях протонирования [2, 3]. Для образцов с плотностью прививки аминогрупп менее 0,7 мкмоль/м2 (обозначены знаком «*» в табл. 2) энергетическая неоднородность в реакциях протонирования не выявлена [2]. Это позволяет предположить отсутствие влияния привитых групп друг на друга при их малой концентрации. По этой причине для всех образцов в рамках модели химических реакций в первую очередь описывали протонирование, сопровождающееся протеканием одного процесса:
-
- NH 2 + H + =- NH 3 + (1)
Чертой в уравнении (1) обозначены группы, «прикрепленные» к поверхности. Константа равновесия этого процесса – K H (константа протонирования).
Рассчитанные таким образом константы равновесия при ионной силе, равной 1, показаны в табл. 2 в столбце lgKH''. Для всех образцов такие критерии адекватности, как средние значения невязок и их модулей, а также эксцесс распределения меньше соответствующих табличных зна- чений для доверительной вероятности p=0,95. Однако для силикагелей, не отмеченных знаком «*», величины взвешенных невязок достаточно велики и при увеличении доли титранта изменяются систематически, что свидетельствует о неполноте модели протонирования с учетом одного процесса (рис. 2) [3, 7].
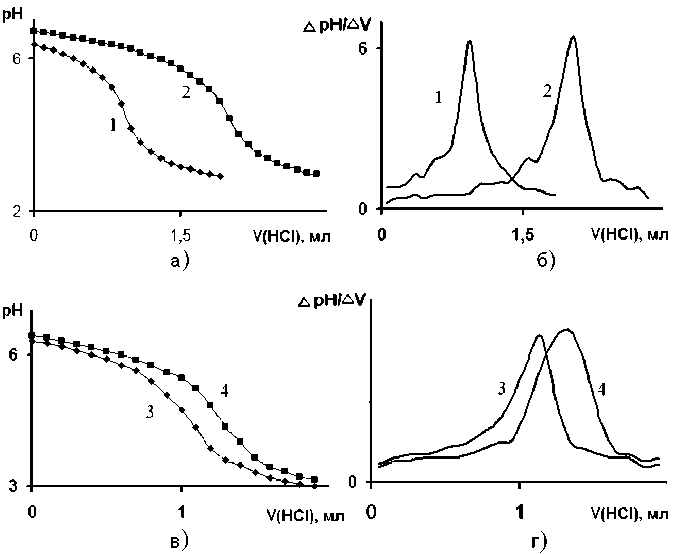
Рис. 1. Примеры кривых титрования модифицированных силикагелей: а, б – интегральные и дифференциальные кривые силикагелей КСКГ с плотностью прививки МЭА: 1 – 0,15±0,05 ммоль/г, 2 – 0,30±0,04 ммоль/г; в, г – интегральные и дифференциальные кривые силикагелей КСМГ с плотностью прививки МЭА: 3 – 0,19±0,03 ммоль/г, 4 – 0,24±0,03 ммоль/г
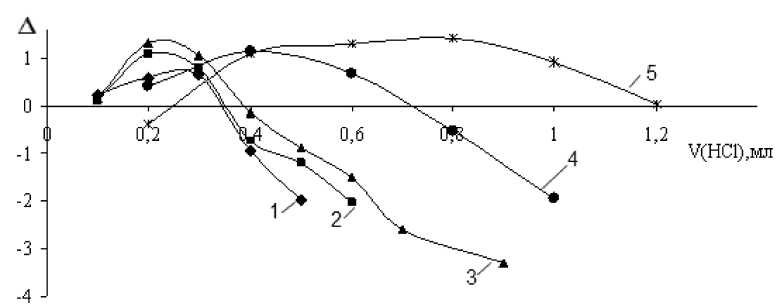
Рис. 2. Изменение взвешенных невязок Δ при увеличении объема прибавляемого титранта: 1, 2, 3 – модифицированные силикагели КСКГ с плотностью прививки аминогрупп 0,79, 1,01 и 1,29 мкмоль/м2; 4, 5 – силикагели КМСГ с плотностью прививки 1,20 и 1,90 мкмоль/м2
Протонирование образцов, обозначенных в табл. 2 номерами 1–5 и 15, можно считать удачно описываемым данной моделью, что подтверждает случайный характер взвешенных невязок (рис. 3). Для более адекватного описания протолитических равновесий на поверхности образцов под номерами 6 – 14 и 16 – 23 в табл. 2 необходимо дополнить исходную модель еще каким-либо равновесным процессом. Опыт использования программы CLINP для описания равновесий на поверхности комплексообразующих модифицированных кремнеземов показывает на возможност ь протек ания на поверхности так называемого процесса гомосопряжения [3]:
-
- NH 3 + + - NH 2 = - NH 2 H 3 N + - (2)
Константу такого процесса, обозначаемую КГ , называют константой гомосопряжения. Процесс (2) можно представи ть и в другом виде:
H + + 2 - NH 2 = - NH 2 H 3 N + - (3)
Исходя из стехиометрии уравнений (2) и (3), константа равновесия процесса (3) равна:
K = K H K r . (4)
Таблица 2
Кажущиеся константы поверхностных равновесий (lgK H для жидкого МЭА равен 9,25 [9])
|
№ |
Марка сорбента |
Плотность прививки аминогрупп, мкмоль/м2 |
Логарифмы констант равновесия при I = 1 |
|||
|
lg K H ' |
lg K H '' |
lg K H ''' |
lg K Г |
|||
|
1* |
КСКГ, S уд = 232 м2/г, |
0,21±0,07 |
5,92±0,10 |
6,04±0,09 |
6,01±0,07 |
– |
|
2* |
0,40±0,09 |
6,20 ± 0,09 |
6,26±0,07 |
6,26±0,05 |
– |
|
|
3* |
0,46±0,09 |
6,04±0,04 |
6,15±0,02 |
6,14±0,08 |
– |
|
|
4* |
0,50±0,08 |
6,28 ± 0,08 |
6,33±0,05 |
6,36±0,07 |
– |
|
|
5* |
0,65±0,06 |
6,02±0,05 |
6,11±0,04 |
6,12±0,05 |
– |
|
|
6 |
0,69±0,10 |
6,22±0,09 |
6,29±0,05 |
6,31±0,06 |
0,54±0,06 |
|
|
7 |
0,79±0,08 |
6,40 ± 0,09 |
6,53±0,08 |
6,51±0,04 |
0,56±0,03 |
|
|
8 |
0,91±0,09 |
6,62±0,08 |
6,70±0,07 |
6,70±0,05 |
0,56±0,04 |
|
|
9 |
0,99±0,07 |
6,95±0,11 |
7,08±0,09 |
6,99±0,11 |
0,53±0,04 |
|
|
10 |
1,01±0,14 |
6,52 ± 0,06 |
6,66±0,07 |
6,63±0,07 |
0,56±0,04 |
|
|
11 |
1,12±0,08 |
7,12±0,12 |
7,26±0,06 |
7,22±0,08 |
0,59±0,04 |
|
|
12 |
1,29±0,09 |
6,59±0,06 |
6,78±0,05 |
6,68±0,09 |
0,54±0,03 |
|
|
13 |
1,29±0,11 |
6,43±0,11 |
6,53±0,06 |
6,53±0,04 |
0,55±0,04 |
|
|
14 |
1,29±0,11 |
6,62 ± 0,10 |
6,71±0,09 |
6,71±0,07 |
0,70±0,07 |
|
|
15* |
КСМГ, S уд = 460 м2/г |
0,51±0,08 |
6,18±0,08 |
6,34±0,08 |
6,32±0,09 |
– |
|
16 |
0,79±0,09 |
6,51±0,06 |
6,68±0,04 |
6,50±0,06 |
0,42±0,03 |
|
|
17 |
0,79±0,09 |
6,56 ± 0,09 |
6,78±0,09 |
6,64±0,07 |
0,41±0,05 |
|
|
18 |
0,88±0,09 |
6,58±0,07 |
6,69±0,07 |
6,62±0,05 |
0,39±0,04 |
|
|
19 |
1,20±0,12 |
6,32±0,06 |
6,49±0,06 |
6,41±0,05 |
0,38±0,03 |
|
|
20 |
1,20±0,11 |
6,44 ± 0,09 |
6,73±0,05 |
6,56±0,09 |
0,44±0,03 |
|
|
21 |
1,59±0,08 |
6,67±0,06 |
6,82±0,04 |
6,74±0,06 |
0,40±0,05 |
|
|
22 |
1,90±0,12 |
7,18 ± 0,07 |
7,45±0,08 |
7,29±0,04 |
0,29±0,05 |
|
|
23 |
2,18±0,10 |
7,16 ± 0,10 |
7,43±0,07 |
7,28±0,06 |
0,38±0,06 |
|
Примечание. lg K H ' – логарифм константы протонирования, рассчитанной при обработке изотерм сорбции по уравнению Лэнгмюра [2]; lg KH'' – логарифм константы протонирования, рассчитанной в рамках модели химических реакций при условии протекания только процесса (1); lg KH''' – логарифм константы протонирования, рассчитанной в рамках модели химических реакций с учетом протекания гомосопряжения привитых групп; lg KГ – логарифм константы гомосопряжения привитых групп.
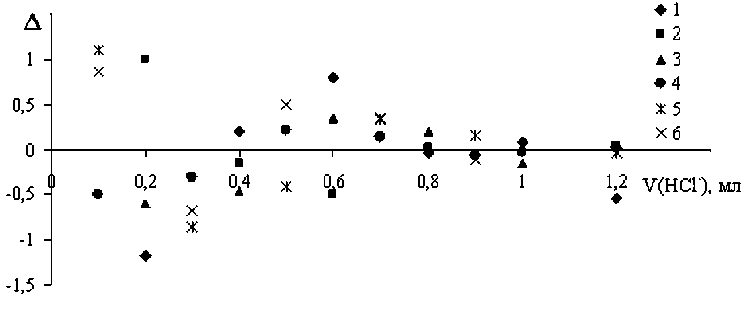
Рис. 3. Взвешенные невязки Δ для образцов 1 – 5 и 15, характеризующие расчет по модели с применением одной реакции: 1 – 5: модифицированные силикагели КСКГ с плотностью прививки аминогрупп 0,21, 0,40, 0,46, 0,50 и 0,65 мкмоль/м2; 6 – силикагели КСМГ с плотностью прививки 0,51 мкмоль/м2
Логарифмы констант протонирования (процесс (1)) и гомосопряжения (процесс (2)) указаны в табл. 2 в столбцах lg KH''' и lg Kr соответственно. Для образцов под номерами 1-5 и 15 величины логарифмов констант гомосопряжения лежат в пределах ошибки опыта, что еще раз подтверждает вывод о единственности процесса (1), протекающего при их протонировании. В пользу этого же вывода свидетельствует то, что значимых различий между логарифмами констант указанных образцов в столбцах lg KH''' и lg K H '' не зафиксировано. Допустимые значения статистических параметров Δ , Δ , γ2, а также случайное распределение взвешенных невязок свидетельствует в пользу адекватности и полноты модели, учитывающей гомосопряжение. Отсутствие процессов (2) и (3) при протонировании образцов 1–5 и 15 является вполне логичным и объясняется большими расстояниями между привитыми аминогруппами вследствие малой плотности прививки. Увеличение же поверхностной концентрации привитых групп происходит неравномерно. Другими словами, на поверхности появляются участки с повышенной и пониженной плотностью аминоэтоксигрупп, что соответствует их «островковой» топографии. Это позволяет предположить, что гомосопряжение происходит внутри «островков».
С высокой долей вероятности можно предположить первоначальное протекани е проце сса (3) с константой (4), который включает как непосредственное протонирование группы - NH 2 , так и последующее межмолекулярное взаимодействие получившегося аммонийного иона с другой аминогруппой. И лишь при достижении некоторой степени заполнения поверхности ионами водорода протекает процесс (1).
Следует отметить увеличение указанных в табл. 2 констант с увеличением плотности прививки. Объяснением этому является влияние «рельефа», химического строения поверхности на привитые аминоэтоксигруппы. Причем величина такого влияния на каждую отдельно взятую группу различна вследствие их жесткой фиксации на кремнекислородном каркасе. Из-за этого на поверхности имеется набор групп, одинаковых по строению и различных по химической активности. Очевидно, что при увеличении плотности прививки изменяется соотношение более и менее химически активных групп, а следовательно, и константа равновесия.
Заключение
Протонирование закрепленного на поверхности силикагелей моноэтаноламина с плотностью прививки менее 0,7 мкмоль/м2 характеризуется протеканием одного равновесного процесса непосредственного взаимодействия аминогрупп с ионами водорода (уравнение (1)) с логарифмами кажущихся констант равновесия, изменяющимися от 6,04 до 6,11 при I=1.
Увеличение содержания привитых групп сопровождающееся образованием областей с их повышенной и пониженной концентрацией на поверхности, ведет к протеканию еще одного равновесного процесса, в котором две аминогруппы взаимодействуют с одним ионом водорода (гомосопряжение). Логарифм кажущейся константы равновесия такого процесса при I=1 изменяется в пределах 6,85–7,66 при увеличении плотности прививки МЭА.
Изменение величин кажущихся констант протонирования при изменении поверхностной концентрации привитых групп объясняется энергетической неоднородностью поверхности, включающей воздействие «рельефа» и соседних поверхностных групп. Для определения термодинамических констант поверхностного равновесия наряду с учетом влияния ионной силы требуется учет данных факторов. Модель непрерывного распределения констант, примененная нами в [2], хорошо согласуется с моделью химических реакций, так как протекание реакции (3) является одной из причин возникновения неоднородности поверхности и оба этих явления фиксируются при достижении определенной степени заполнения поверхности.
Список литературы Особенности протонирования поверхности силикагелей, модифицированных моноэтаноламином
- Киселев, А.В. Исследование монослоев моноэтаноламина на кремнеземе и алюмосиликагеле методом инфракрасной спектроскопии/А.В. Киселев, В.И. Лыгин, И.Н. Соломонова//Журн. физ. химии. -1970. -№ 5. -С. 1249-1255.
- Шаров, А.В. Протолитические свойства моноэтаноламина, привитого на поверхность силикагелей/А.В. Шаров, О.В. Филистеев//Вестник Курганского университета. Серия «Естественные науки». -2011. -№ 4. -С. 116-120.
- Холин, Ю.В. Количественный физико-химический анализ комплексообразования в растворах и на поверхности химически модифицированных кремнеземов: содержательные модели, математические методы и их приложения/Ю.В. Холин. -Харьков: Фолио, 2000. -290 с.
- Химия привитых поверхностных соединений/под ред. Г.В. Лисичкина. -М.: Физматлит, 2003. -592 с.
- Сравнение протолитических свойств кремнеземов с привитыми аминогруппами для моделирования внутренних градиентов рН/А.Б. Тессман, А.В. Иванов, М.С. Вакштейн, П.Н. Нестеренко//Вестн. Моск. ун-та. Серия 2. Химия. -2002. -№ 1. -С. 223-229.
- Мерный, С.А. Робастное оценивание параметров в задачах количественного физико-химического анализа/С.А. Мерный, Д.С. Коняев, Ю.В. Холин//Вiсник Харьк. ун-ту. № 395. Хiмiчнi науки. -№ 2. -1998. -С. 112-120.
- Холин, Ю.В. Построение модели комплексообразования: от результатов измерений к окончательному вердикту/Ю.В. Холин, С.А. Мерный, Д.С. Коняев//Вiсник Харк. ун-ту. №. 437. -Хiмiчнi науки. -№ 3. -1999. -С. 17-35.
- Большев, Х.Н. Таблицы математической статистики/Х.Н. Большев, Н.В. Смирнов. -М.: Наука, 1983. -413 с.
- Лурье, Ю.Ю. Справочник по аналитической химии/Ю.Ю. Лурье. -М.: Химия, 1971. -454 с.


