Особенности семенного размножения Hedysarum grandiflorum Pall. ex situ и in vitro
Автор: Супрун Н.А., Малаева Е.В., Шумихин С.А.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Ботаника
Статья в выпуске: 4, 2020 года.
Бесплатный доступ
В условиях ex situ и in vitro изучены особенности семенного размножения Hedysarum grandiflorum из 7 природных популяций Волгоградской, Самарской и Луганской обл. Выявлена оптимальная температура прорастания семян и зависимость всхожести и энергии их прорастания от срока хранения. Максимальная всхожесть наблюдалась у скарифицированных семян H grandiflorum 2018 г сбора и составила 70%. Установлено, что всхожесть и энергия прорастания семян невысокие и быстро снижаются с годами хранения, при этом их скарификация позволяет увеличить эти показатели. Экспериментально был подобран оптимальный режим стерилизации семян H. grandiflorum -10% раствор Лизоформин 3000 в течении 5 минут. При этом процент стерильных проростков составил 60%.
Hedysarum grandiflorum, семенное размножение, in vitro, Волгоградская обл.
Короткий адрес: https://sciup.org/147229664
IDR: 147229664 | УДК: 58.084.1 | DOI: 10.17072/1994-9952-2020-4-286-293
Features seed reproduction of Hedysarum grandiflorum Pall. ex situ and in vitro
Hedysarum grandiflorum samples were collected from 7 natural populations of the Volgograd, Samara and Lugansk People's Republic and the features of seed reproduction were studied under ex situ and in vitro conditions. The optimal temperature for seed germination and the dependence of germination and seed vigor on the storage were revealed. We observed the maximum germination rate in the scarified seeds of H. grandiflorum of 2018 collection and it was equal to 70%.It was found that the seed germination and seed vigor are low and quickly decrease with years of storage, while their scarification allows to increase these indicators. It is noted that the relatively low germination of the studied seeds is leveled by the rather high productivity of species in general. The optimal mode of sterilization of H. grandiflorum seeds was experimentally determined - 10% Lysofomin® 3000 solution for 5 minutes. The percentage of sterile seedlings was 60%.
Текст научной статьи Особенности семенного размножения Hedysarum grandiflorum Pall. ex situ и in vitro
Одним из вариантов сохранения редких видов и увеличения их численности, наравне с созданием природных заповедных территорий (сети ООПТ) в естественных местообитаниях (in situ), является интродукция растений и их культивирование (сохранение биоразнообразия ex situ). Выращивание в ботанических садах позволяет проводить углубленные стационарные исследования по биологии, экологии и систематике редких видов, организовать изучение их семенного и вегетативного размножения [Белолипов, 1974; Прилипко, 1980; Davy, Jefferies, 1981; Скворцов, 1983; Тихомиров, 1986; Луконина, 2005; Супрун, 2014; Малаева, Супрун, 2018]. Коллекции интродуцированных дикорастущих растений «позволяют застраховать вид от полного исчезновения в природе, дают материал для реинтродукции, размножения рас- тений и их сберегающего использования, так же как и для использования в исследовательских и образовательных целях» [Стратегия ..., 2003].
В настоящее время для сохранения редких видов растений широкое применение получил метод культуры in vitrо . Многие исследователи указывают на важнейшее значение использования биотехнологического метода как дополнительного варианта сохранения видов ex situ, выступающего в качестве их страхового фонда [Андреев, Горбунов, 2000; Benson at al, 2000; Малаева, 2019].
Следует отметить, что исследования в области культуры ткани для решения проблем сохранения генофонда растений имеют свои особенности [Ве-чернина, 2006]. Довольно часто они связаны с отсутствием возможности свободного выбора объек-
та, а также дефицитом исходного материала нужного растения. В связи с этим, при введении в культуру in vitro редких видов, в качестве исходного материала предпочтительно использовать семена из природных популяций, поскольку таким образом обеспечивается генетическое разнообразие [Молканова, 2017].
Одним из главных направлений работы ГБУ ВО «Волгоградский региональный ботанический сад» (далее ВРБС) является интродукция растений природной флоры Волгоградской обл. с целью их сохранения и увеличения численности. Особый интерес для интродукции представляет своеобразная флора меловых обнажений, выходы которых приурочены к долинам некоторых рек юга России. Сложная история формирования данной флоры обусловила наличие особых растительных группировок и высокую степень эндемизма кальцефильных растений. Резко выраженный своеобразный химизм и механический состав почвы, температурные условия и световой режим, связанный с большим альбедо меловых местообитаний, представляет комплекс факторов, обусловливающих развитие особых адаптационных приспособлений у растений-кальцефилов, имеющих немалый научный интерес.
Особый интерес для нашей работы представляет Hedysarum grandiflorum Pall., который включен в Красную книгу Волгоградской области и Красную книгу Российской Федерации, что подчеркивает важность его введения в культуру [Красная книга…, 2017]. Семенной способ размножения является приоритетным для H. grandiflorum и является основным путем поддержания и увеличения численности [Супрун, 2014].
Ряд авторов изучали семенное размножение копеечника крупноцветкового [Кузнецова, 2008; Ильина, 2013; Лаврентьев, 2016]. Однако в работах недостаточно сведений по семенному размножению H. grandiflorum , связанных с особенностями местообитания данного вида в условиях ex situ и in vitro .
В связи с этим, цель исследования – изучение особенностей семенного размножения H. grandi-florum в условиях ex situ и in vitro .
Объекты и методы исследования
Исследования проводились в 2017–2019 гг. на базе ВРБС (г. Волгоград).
Измерения плодов и семян осуществлялись штангенциркулем. Для определения массы семян и члеников плодов (далее везде – плодов) проводилось взвешивание 100 образцов в 5-кратной повторности из каждой популяции.
Проводилось морфологическое описание внешних покровов плодов и семян. Для анализа биометрических данных (Д – длина; Ш – ширина) се- мян и плодов выборка составляла 50 шт. образцов (данные обрабатывались с помощью компьютерной программы STATISTICA 6.0 – различия достоверны по плодам и семенам) [STATISTICA, 2001].
Для изучения семенного размножения семена H. grandiflorum Pall. были собраны из семи различных природных популяций. Для сравнения величины плодов и семян растений из разных популяций брали по 100 плодов и семян; масса плодов определялась взвешиванием 100 шт. в 3-кратной повторности. Лабораторное проращивание семян проводили в чашках Петри на подложке из фильтровальной бумаги по 100 семян в чашке в 3-кратной повторности. Скарификация проводилась непосредственно перед посевом, так как прошедшие такую обработку семена плохо хранятся вследствие нарушения структуры оболочки. Энергия прорастания семян исследованного вида учитывалась за первые 7 дней. Абсолютная всхожесть выявлялась в течение 30 дней. Для определения грунтовой всхожести семена высеивали в рассадные ящики. Поскольку цветение и созревание плодов у копеечника крупноцветкового происходит не одновременно, то в образцах присутствовали как зрелые, так и незрелые плоды, и семена. Для лабораторных и полевых опытов отбирали только зрелые плоды и семена [Николаева, 1985].
Методика биотехнологических исследований базировалась на общепринятых классических приемах с культурами изолированных тканей и органов растений [Бутенко, 1999].
Семена предварительно обрабатывали 95%-ным этиловым спиртом в течение 50‒60 сек. В качестве стерилизатора использовали различные концентрации Белизны и «Лизоформина 3000» (действующее вещество – глутаровый альдегид, глиоксаль и дидецилдиметиламмоний хлорид) с различной временной экспозицией. Методика по применению стерилизующего вещества – «Лизо-формин 3000» ‒ устанавливалась опытным путем сотрудниками лаборатории биотехнологии ВРБС.
После многократного промывания в стерильной дистиллированной воде семена высаживали на безгормональную питательную среду с минеральной основой по прописи Мурасиге-Скуга [Murashige, Skoog, 1962]. При оценке оптимального режима стерилизации учитывали количество заросших и количество проросших семян.
Проростки делили на фрагменты и пересаживали на модифицированные питательные среды для получения пролиферирующей культуры.
В условиях in vitro растения культивировали в чашках Петри и биологических пробирках при освещении с интенсивностью 3‒5 клк, при 16часовом фотопериоде, температуре 24ºС и относительной влажности воздуха 70%. Все опыты про- водили трижды, повторность в каждом варианте 10-кратная.
Статистическая обработка результатов исследования проводилась общепринятыми методами с применением интегрированной системы «Statis-tica» версии 6.0, Microsoft Office Excel 2013 и Past 6.1.
Результаты и их обсуждение
Плод H. grandiflorum – членистый боб. Членики его почти округлые, сильно сдавленные лате-рально, сетчато-ребристые, беловойлочные, покрыты шипами с крючковатой верхушкой. Такое строение члеников при разделении способствует анемохории, реже зоохории. Кроме того, явным признаком анемохории является не распадающий-

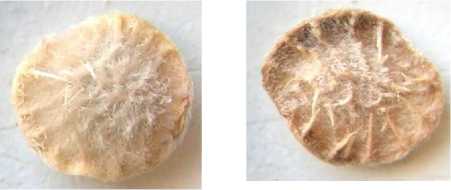
ся после отцветания околоцветник. В среднем в одном бобе закладывается 4 членика, при этом среднее количество развитых семян равно 4. Размеры и масса семян и плодов (члеников бобов) варьируют в зависимости от места произрастания вида. Семена имеют плоско-выпуклую почковидную форму и окрашены в коричневый или темнокоричневый цвет. Поверхность семян блестящая, имеет гладкую скульптуру, без опушения. Рубчиковый след округлой формы, беловатого цвета, в среднем около 0.15 мм в диаметре. Длина плодов в среднем составляет 3.37±0.02 мм, ширина – 3.59±0.02 мм; масса плодов (100 шт.) – 0.459±0.005 г, масса семян (100 шт.) – 0.336 ±0.007 г. (рис. 1, табл. 1, 2).
Масштаб |__| ‒ 1 мм
Рис. 1 . Структура плодов Hedysarum grandiflorum
Таблица 1
Размеры плодов Hedysarum grandiflorum из разных географических популяций
|
Место сбора |
Измерение |
M±m, мм |
σ |
V |
Масса, г |
|
Sm |
Длина |
4.11±0.07 |
0.24 |
5.84 |
0.503 |
|
Ширина |
4.37±0.04 |
0.38 |
8.69 |
||
|
Lk |
Длина |
3.77±0.04 |
0.39 |
10.34 |
0.423 |
|
Ширина |
3.81±0.03 |
0.30 |
7.87 |
||
|
LA |
Длина |
3.40±0.06 |
0.43 |
12.64 |
0.398 |
|
Ширина |
3.58±0.06 |
0.42 |
11.73 |
||
|
KK |
Длина |
3.45±0.07 |
0.18 |
5.22 |
0.465 |
|
Ширина |
3.56±0.04 |
0.28 |
7.86 |
||
|
KI |
Длина |
3.32±0.06 |
0.32 |
9.64 |
0.430 |
|
Ширина |
3.70±0.05 |
0.26 |
7.03 |
Примечание. В этой и следующей таблице: Sm – Самарская обл., Кинельский р-н, окр. пос. Усть-Кинелький; Lk – Луганская обл., окр. с. Камышное, степные балки по р. Дерлуп; LA – Луганская обл., юго-западнее г. Луганска, окр. пос. Александровка и пос. Бахлут; KK – Волгоградская обл., Камышинский р-н, балка Кривцовская; КI – Волгоградская обл., Иловлинский р-н, хут. Александровка.
Таблица 2
Размеры семян Hedysarum grandiflorum из разных географических популяций
|
Место сбора |
Измерение |
M±m, мм |
σ |
V |
Масса, г |
|
Sm |
Длина |
2.20±0.06 |
0.32 |
14.54 |
0.313 |
|
Ширина |
2.52±0.06 |
0.31 |
12.30 |
||
|
Lk |
Длина |
2.15±0.03 |
0.15 |
6.98 |
0.378 |
|
Ширина |
2.49±0.03 |
0.16 |
6.42 |
||
|
LA |
Длина |
2.20±0.03 |
0.22 |
10 |
0.301 |
|
Ширина |
2.51±0.05 |
0.29 |
11.55 |
||
|
KK |
Длина |
1.90±0.05 |
0.16 |
8.42 |
0.321 |
|
Ширина |
2.28±0.09 |
0.18 |
7.89 |
||
|
KI |
Длина |
1.90±0.05 |
0.21 |
11.05 |
0.378 |
|
Ширина |
2.14±0.07 |
0.25 |
11.68 |
Исследования биометрических показателей плодов в различных популяциях, показали, что коэффициент вариации длины и ширины ниже среднего (V = 5‒13%), что говорит о небольшом варьировании этих признаков. Таким образом, высокие значения длины и ширины наблюдаются у популяций, собранных в Луганской обл., юго-западнее г. Луганска, в окрестностях пос. Александровка и пос. Бахлут; низкие значения вариации длины плодов обнаружены в Самарской обл., в Кинельском р-не, в окрестностях пос. Усть-Кинелький и в Волгоградской обл., Камышинском р-не, в балке Кривцовская.
Биометрический анализ семян показал, что их размеры тесно связаны с географическим расположением популяций. По индексу длина – ширина все популяции достоверно различаются между собой (табл. 2).
Исследуя биометрические показатели семян в различных популяциях, обнаружили, что коэффициент вариации по длине и ширине незначителен (V = 6‒15%), следовательно, это свидетельствует о стабильности данного признака. Максимальные значения длины составляют 2.20 мм, ширины – 2.52 мм, минимальные – соответственно 1.90 и
-
2.14 мм.
По внешним признакам плоды копеечника крупноцветкового из популяций различного географического расположения отличяются по следующим показателям:
-
• плоды имеют цвет: светло-желтый, желтооранжевый и серо-коричневый. Окраска плодов каждой отдельной популяции имеет свой цвет, но есть присутствие других цветов;
-
• опушение на плодах присутствует всегда. Степень его может быть различным: густым или редким;
-
• выраженность сетчатости на поверхности плодов зависит от высоты, расположения ребер и расстояния между ними;
-
• длина шипиков у плодов отличается. Для некоторых плодов характерно наличие разной длины шипиков на окаймлении, а на других по всей поверхности плода, но с разной степенью выраженности.
В условиях ВРБС нами проведена серия опытов по определению всхожести семян H. grandiflorum различного срока хранения (сборы 2017 – 2019 гг.) (табл. 3‒5).
Таблица 3
Влияние различных способов предпосевной обработки на прорастание семян H. grandiflorum (сбор 2017 г.)
|
Условия прорастания |
Всхожесть (%) |
||||||||
|
7 дней |
15 дней |
30 дней |
|||||||
|
1 |
2 |
3 |
1 |
2 |
3 |
1 |
2 |
3 |
|
|
Скарификация (наждачная бумага) |
25 |
27 |
31 |
30 |
36 |
38 |
46 |
54 |
58 |
|
Обработка горячей водой (3 мин.) |
2 |
6 |
4 |
4 |
9 |
5 |
4.1 |
23 |
10 |
|
Стратификация (холодильник t = 0…+5ºC) |
0 |
0 |
0 |
8 |
8 |
6 |
26 |
29 |
25 |
|
Обработка этиловым спиртом |
39 |
41 |
24 |
44 |
48 |
29 |
54 |
57 |
41 |
|
Контроль |
13 |
23 |
18 |
16 |
26 |
21 |
20 |
31 |
28 |
Таблица 4
Влияние различных способов предпосевной обработки на прорастание семян H. grandiflorum (сбор 2018 г.)
|
Условия прорастания |
Всхожесть (%) |
||||||||
|
7 дней |
15 дней |
30 дней |
|||||||
|
1 |
2 |
3 |
1 |
2 |
3 |
1 |
2 |
3 |
|
|
Скарификация (наждачная бумага) |
39 |
27 |
40 |
60 |
81 |
67 |
69 |
82 |
70 |
|
Обработка горячей водой (3 мин.) |
2 |
6 |
5 |
3 |
6 |
10 |
5 |
12 |
10 |
|
Стратификация (холодильник t = 0…+5ºC) |
6 |
0 |
4 |
14 |
11 |
12 |
21 |
28 |
25 |
|
Обработка этиловым спиртом |
39 |
41 |
24 |
44 |
48 |
29 |
54 |
57 |
41 |
|
Контроль |
25 |
34 |
41 |
49 |
58 |
76 |
76 |
66 |
79 |
Таблица 5
Влияние различных способов предпосевной обработки на прорастание семян H. grandiflorum (сбор 2019 г., на момент проведения опыта свежесобранный материал)
|
Условия прорастания |
Всхожесть (%) |
||||||||
|
7 дней |
15 дней |
30 дней |
|||||||
|
1 |
2 |
3 |
1 |
2 |
3 |
1 |
2 |
3 |
|
|
Скарификация (наждачная бумага) |
20 |
21 |
18 |
51 |
28 |
41 |
72 |
60 |
65 |
|
Обработка горячей водой (3 мин.) |
8 |
6 |
2 |
11 |
10 |
3 |
12 |
20 |
12 |
|
Стратификация (холодильник t = 0…+5ºC) |
1 |
6 |
0 |
6 |
9 |
10 |
18 |
25 |
29 |
|
Обработка этиловым спиртом |
30 |
24 |
23 |
45 |
47 |
29 |
54 |
59 |
56 |
|
Контроль |
10 |
16 |
20 |
13 |
24 |
45 |
27 |
39 |
48 |
H. grandiflorum не размножается вегетативным путем, в связи с чем способ размножения только семенной. Семенное размножение вида затруднено, так как для вида характерна твердосемянность, которую можно нарушить механическим, температурным и химическим воздействием [Попцов, 1976; Николаева, 1985]. У видов, обладающих твердосемянностью и гетерокарпией, лишь часть семян прорастают относительно быстро. Семена различных видов копеечников способны длительное время храниться в почве. Всходы появляются периодически за счет семян нового урожая и запаса их в почве.
Из полученных данных видно, что семена H. grandiflorum обладают различной энергией прорастания. Абсолютная всхожесть определялась на 30-й день.
При стратификации отдельные семена копеечника крупноцветкового начинают прорастать уже на 7-й день. Обработка этиловым спиртом и наждачной бумагой увеличивает число проросших семян. Обработка кипятком в течение 3 мин. оказалась губительной для семян H. grandiflorum , вероятно, температурный предел для них ниже, чем предполагалось, или такая обработка вызвала более глубокий физиологический покой семян. Спирт играет роль не растворителя каких-либо веществ, а промокашки, т.е. лишь смачивает стенки пор, мельчайших канальцев, что способствует проникновению в них воды.
Опыты показали, что семена копеечника крупноцветкового прорастают в широком температурном диапазоне – от +5 до +28ºС. Однако интервал постоянных температур, в пределах которого наблюдается достаточно высокая всхожесть, составляет +20…+25ºС. При этих температурах максимальная всхожесть сочетается с максимальной скоростью прорастания.
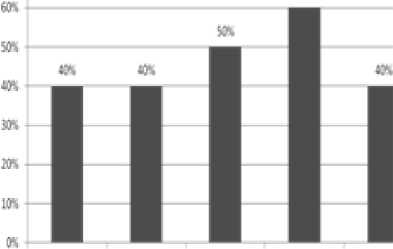
В условиях лаборатории биотехнологии эмпирическим путем определяли время поверхностной стерилизации, которое зависело от процента жизнеспособных регенерантов. Использование препарата «Лизоформин 3000» позволило получить максимальный выход стерильных эксплантов H. gran-diflorum. Оптимальным режимом стерилизации является 10%-ный раствор «Лизоформин 3000» в течение 5 мин. В данном случае был получен самый большой процент стерильных эксплантов – 60% (рис. 2).
1Л-- ж
1 2 3 4 5
Рис. 2. Выход жизнеспособных эксплантов H. grandiflorum в зависимости от режима стерилизации:
-
1 – контроль, дистилированная вода; 2 – Белизна 20%-ная, 5 мин.; 3 – Белизна 20%-ная, 7 мин.; 4
– «Лизоформин 3000» 10%-ный, 5 мин.; 5 – «Лизоформин 3000» 10%-ный, 7 мин.
При увеличении времени стерилизации увеличивался процент стерильных, но повышался процент непрорастающих семян и растягивались сроки прорастания.
Также были исследованы всхожесть и динамика прорастания в зависимости от состава питательной среды.
Для изучения семенного размножения копеечника крупноцветкового был заложен эксперимент по проращиванию семян на питательной среде (рис. 3).
Семена на жидкой питательной среде начали прорастать на 9-й день после введения в культуру in vitro, тогда как на агаризованной ‒ на 10-й день. Кроме того, динамика прорастания семян H. gran-diflorum на жидкой и агаризованной питательных средах отличались. Так, на 12-й день на жидкой питательной среде – 4 проростка, на агаризован-ной – 2; на 14-й – 5 и 3 проростка соответственно. Следует отметить, что на жидкой питательной сре- де развивались проростки нормальной морфологии, тогда как на агаризованной среде некоторые из них имели уродства. Стерильные проростки в дальнейшем делили на фрагменты и использовали в качестве вторичных эксплантов на следующих этапах культивирования in vitro.
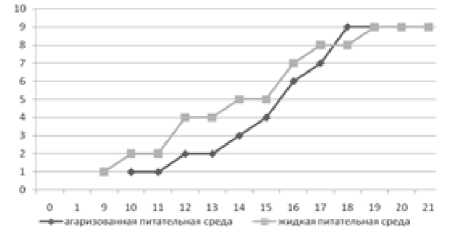
Рис. 3 . Динамика прорастания семян H. grandiflorum на агаризированной и жидкой питательных средах МС
Таким образом, использование жидких питательных сред для проращивания семян редких видов растений, в том числе и H. grandiflorum , весьма перспективно.
Заключение
В результате проведенных исследований по изменчивости семян копеечника крупноцветкового исследуемых популяций, обнаружено небольшое варьирование по индексу длина-ширина, что свидетельствует о стабильности данного признака. Наличие изменчивости морфологических признаков плодов вида свидетельствует о влиянии широкого диапазона различных факторов внешней среды (район произрастания, сообщество, субстрат, антропогенные воздействия и т. д.).
Для интродукционных исследований рекомендуется использовать только семенной материал, так как в условиях культивирования H. grandiflo-rum проходит неполный онтогенез (нет постгенеративного периода): вегетирует, цветет, плодоносит и отмирает на генеративной стадии развития, как правило, уже в конце первого года. Посев следует производить в осенний период для прохождения семенами естественной стратификации.
В результате исследований по стерилизации семян при введении в культуру in vitro установлено влияние режимов стерилизации на сроки прорастания. Так, при увеличении времени стерилизации увеличивался процент стерильных семян, но повышался процент непрорастающих и растягивались сроки прорастания. Экспериментально был подобран оптимальный режим стерилизации семян копеечника крупноцветкового – 10%-ный раствор «Лизоформин 3000» в течение 5 мин., процент стерильных эксплантов достигал 60%.
Разработанные приемы получения растений-регенерантов в культуре изолированных тканей могут быть использованы для сохранения генофонда редких видов копеечников в коллекциях in vitro .
Список литературы Особенности семенного размножения Hedysarum grandiflorum Pall. ex situ и in vitro
- Андреев Л.Н., Горбунов Ю.Н. Сохранение редких и исчезающих растений ex situ: достижения и проблемы // Изучение и охрана разнообразия фауны, флоры и основных экосистем Евразии: материалы междунар. конф. М., 2000. С. 19-23.
- Белолипов И.В. О сохранении и размножении редких, реликтовых, эндемичных видов растений природной флоры Средней Азии на примере интродукционных работ ботанического сада АН УзССР // Узбекский биологический журнал. 1974. № 1. С. 34-37.
- Бутенко Р.Г. Биология клеток высших растений in vitro и биотехнологии на их основе: учеб. пособие. М.: ФБК-Пресс, 1999. 160 с.
- Вечернина Н.А. Сохранение биологического разнообразия редких, исчезающих видов, уникальных форм и сортов растений методами биотехнологии: автореф. дис. ... д-ра биол. наук. Барнаул, 2006. 33 с.
- Ильина В.Н. Перспективы интродукции некоторых видов семейства бобовые в связи с особенностями начальных периодов онтогенеза // Самарский научный вестник. 2013. № 3 (4). С. 44-47.
- Красная книга Волгоградской области. Воронеж: Издат-Принт, 2017. Т. 2. Растения и другие организмы. 268 с.
- Кузнецова М.Н. Семенное воспроизведение копеечника крупноцветкового (Hedysarum grandiflorum Pall.) // Современные проблемы морфологии и репродуктивной биологии семенных растений: материалы междунар. конф. Ульяновск, 2008. С. 76-84.
- Лаврентьев М.В. Характеристика репродуктивных особенностей Hedysarum grandiflorum (Faba-ceae) в южной части приволжской возвышенности // Бюллетень Ботанического сада Саратовского государственного университета. 2016. Т. 14, вып. 2. С. 35-43.
- Луконина А.В. Растительный покров Волгоградской области как источник растений для интродукции: автореф. дис. ... канд. биол. наук. М., 2005. 24 с.
- Малаева Е.В. Сохранение редких видов растений в коллекции in vitro Волгоградского регионального ботанического сада // Проблемы ботаники Южной Сибири и Монголии. 2019. № 18. С. 606-610.
- Малаева Е.В., Супрун Н.А. Изучение и сохранение редких видов растений в Волгоградском региональном ботаническом саду // Ботаника в современном мире: тр. XIV Съезда РБО. Махачкала: Алеф, 2018. Т. 2. С. 283-285.
- Молканова О.И. Использование биотехнологических методов для размножения и сохранения редких видов растений // Бюллетень Главного ботанического сада. 2017. № 1(203). С. 42-48.
- Николаева М.Г., Разумова М.В., Гладкова В.Н. Справочник по проращиванию покоящихся семян. Л.: Наука, 1985. 348 с.
- Попцов А.В. Биология твердосемянности. М.: Наука, 1976. 157 с.
- Прилипко Л.И. Задачи ботанических садов в сохранении редких и исчезающих видов растений местной природной флоры // Бюллетень Главного ботанического сада. 1980. Вып. 118. С. 3-8.
- Скворцов А.К. Перспективы и задачи изучения и культивирования редких и исчезающих видов природной флоры СССР // Редкие и исчезающие виды природной флоры СССР, культивируемые в ботанических садах и других интродукционных центрах страны. М.: Наука, 1983. С. 15-21.
- Стратегия ботанических садов России по сохранению биологического разнообразия растений. М.: Красная Звезда, 2003. 32 с.
- Супрун Н.А. Копеечники (Hedysarum L.) Нижнего Поволжья (изменчивость и систематика): авто-реф. дис. ... канд. биол. наук. М., 2014. 22 с.
- Тихомиров В.Н. Культивирование редких и исчезающих видов растений в ботанических садах как один из методов охраны генофонда флоры // Особенности развития редких растений при культивировании в центре европейской части СССР. М., 1986. С. 4-7.
- Benson E.E. et al. In vitro micropropagation of Primula scotica: a rare Scotish plant // Biodiversity and conservation. 2000. Vol. 9. P. 711-726.
- Davy A.J., Jefferies R.L. Approaches to the monitoring of rare plant populations // Biol. aspects rare plant conserv. Proc. Intern. Conf. Cambridge, 1981. P. 219-232.
- Murashige T., Skoog F. A revised medium for rapid growth and bioassays with tobacco tissue cultures // Phsiol. plant. 1962. Vol. 15, № 3. P. 473-497.


