Особенности сорбционного процесса очистки вод от поверхностно-активных веществ с использованием органоминеральных сорбционных материалов
Автор: А.В. Святченко, Ж.А. Сапронова, Я.А. Мурзаханов
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Экология - технические науки
Статья в выпуске: 4 т.27, 2025 года.
Бесплатный доступ
Сорбционный метод очистки широко применяется для извлечения различных поллютантов, включая поверхностно-активные вещества (ПАВ). В работе рассмотрены особенности сорбционного процесса при очистке модельных вод от анионных ПАВ. В качестве ПАВ использовался лаурилсульфат натрия. Сорбционные материалы были получены из карбонатсодержащего отхода сахарной промышленности и диатомитового шлама пивоваренной промышленности путем термической модификации. В исследованиях использовались как отдельные сорбционные материалы, так и их смеси в различных пропорциях. В процессе очистки модельных вод было установлено, что наибольшая эффективность извлечения ПАВ достигается при использовании диатомитового шлама, термообработанного при 450 °С и гидрофобизованного стеариновой кислотой. Высокие значения эффективности были получены также при использовании гидрофобизованного шлама карбонатсодержащего отхода, термообработанного при 450 °С и гидрофобизованного диатомитового шлама, термообработанного при 550 °С. Для лучшего понимания сорбционных процессов была построена изотерма сорбции для диатомитового шлама, термообработанного при 450 °С и гидрофобизованного стеариновой кислотой. По классификации Международного союза теоретической и прикладной химии полученную кривую можно отнести к I типу изотерм. Проведенные расчеты с использованием математических моделей Ленгмюра, Фрейндлиха, БЭТ, ТОЗМ, Дубинина-Радушкевича, Темкина показали, что механизм сорбционного взаимодействия лучше всего описывается моделью Ленгмюра. Это позволяет предположить протекание процесса адсорбции по мономолекулярному типу, с распределением сорбата между энергетически равнозначными активными центрами.
Очистка, отход, диатомит, сорбент
Короткий адрес: https://sciup.org/148331825
IDR: 148331825 | УДК: 628.316.12:544.723.21 | DOI: 10.37313/1990-5378-2025-27-4-215-222
Features of the Sorption Process of Water Purifi cation from Surfactants Using Organomineral Sorption Materials
The sorption purifi cation method is widely used to extract various pollutants, including surfactants. The paper considers the features of the sorption process in the purifi cation of model waters from anionic surfactants. Sodium lauryl sulfate was used as a surfactant. Sorption materials were obtained from carbonate-containing waste from the sugar industry and diatomaceous sludge from the brewing industry by thermal modifi cation. The studies used both individual sorption materials and their mixtures in various proportions. In the process of model water purifi cation, it was found that the highest effi ciency of surfactant extraction is achieved by using diatomaceous sludge, heat-treated at 450 °C and hydrophobized with stearic acid. High effi ciency values were also obtained using hydrophobized carbonate-containing sludge, heat-treated at 450 °C. and hydrophobized diatomaceous sludge, heat-treated at 550 °C. For a better understanding of sorption processes, a sorption isotherm was constructed for diatomaceous sludge heat-treated at 450 °C and hydrophobized with stearic acid. According to the classifi cation of the International Union of Pure and Applied Chemistry, the resulting curve can be attributed to type I isotherms. The calculations performed using the mathematical models of Langmuir, Freundlich, BET, TOSM, Dubinin-Radostkevich, Temkin showed that the mechanism of sorption interaction is best described by the Langmuir model. This suggests that the adsorption process proceeds according to the monomolecular type, with the distribution of sorbate between energetically equivalent active centers.
Текст научной статьи Особенности сорбционного процесса очистки вод от поверхностно-активных веществ с использованием органоминеральных сорбционных материалов
EDN: HYUXKQ
Работа выполнена в рамках реализации федеральной программы поддержки университетов «Приоритет 2030» с использованием оборудования на базе Центра высоких технологий БГТУ им. В. Г. Шухова.
Получение новых сорбционных материалов, особенно на основе отходов промышленности, является актуальной задачей современности. Для успешного их использования в водоочистке необходимо исследовать особенности сорбционных взаимодействий в водных средах, протекающих в ходе извлечения поллютантов.
Использование поверхностно-активных веществ (ПАВ) в быту и промышленности увеличилось в результате экономического роста, что приводит к возрастанию их количества в сточных водах. Лаурилсульфат натрия (рисунок 1), одно из самых известных анионных ПАВ, является распространенным загрязнителем водных объектов [1].
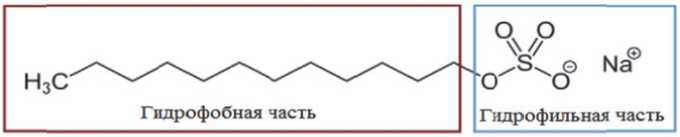
Рис. 1. Структурная формула лаурилсульфата натрия
Удаление ПАВ из водных сред является одной из основных задач, стоящих перед предприятиями, занимающимися водоочисткой. Это довольно непростой процесс, учитывая широкий ассорти мент современных детергентов и их негативное влияние на установки биологической очистки [2].
ПАВ обычно состоят из двух частей: полярной головной группы (заряженной или незаряженной), которая хорошо растворяется в воде, и углеводородного хвоста, который плохо растворим в полярных растворителях. Таким образом, ПАВ сочетают в себе гидрофобные и гидрофильные свойства в одной молекуле. ПАВ в широком смысле могут быть определены как соединения, которые изменяют энергетические отношения на границах раздела фаз. Когда ПАВ присутствуют в низких концентрациях, они уменьшают количество межфазной свободной энергии и способствуют расширению одной из границ раздела в системе, тем самым влияя на эффективность многих процессов [2-4].
Использование ПАВ чрезвычайно распространено и неуклонно возрастает в последние десятилетия. Согласно прогнозам на территории РФ в ближайшие 3 года объем производства ПАВ составим более 2,4 млн т [5]. Они находят широкое применение в быту, в производстве фармацевтических препаратов и средств личной гигиены, красок и лаков, пищевых продуктов, пластмасс и пестицидов, а также в фармацевтической, горнодобывающей, нефтедобывающей и целлюлозно-бумажной промышленности. Более того, в последние десятилетия они все чаще используются в высокотехнологичных секторах, таких как биотехнология и микроэлектроника [2, 4].
Обычно ПАВ можно разделить на четыре типа: анионные, неионогенные, катионные и амфотерные [3].
Анионные поверхностно-активные вещества (АПАВ) состоят из преимущественно линейной алифатической углеводородной цепи (длина от C8 до C18) с полярной сульфатной или сульфонатной группой, нейтрализованной противоионом (например, Na2+, K+, NH4+). Многие АПАВ представляют собой вещества, состоящие из нескольких гомологов. Было подсчитано, что АПАВ составляют около 60% ПАВ, производимых в мире [1, 6].
Существует множество публикаций о негативном влиянии ПАВ на окружающую среду, дикую природу и людей. Эти соединения обладают токсическим и канцерогенным воздействием, способны к биоаккумуляции и могут передаваться по пищевым цепям, повреждают жабры и слизистые оболочки, убивают икру и вызывают эндокринные нарушения у рыб [2, 7].
ПАВ могут увеличивать количество органических углеводородных соединений, которые растворяются в водных источниках или сорбируются в почве и отложениях, где они потенциально могут стать вредными для сельскохозяйственных культур, а также влияют на разложение гидрофобных органических соединений [2].
Хотя очистные сооружения имеют высокую эффективность удаления ПАВ (95-99%), эти вещества можно найти в водных экосистемах в различных концентрациях. Ими также могут быть загрязнены и почвы [1, 6].
Большое количество ПАВ плохо поддается биологическому разложению. Они вызывают нарушение функции и структуры бактериальных мембран за счет увеличения их проницаемости. В микроорганизмах адсорбция ПАВ вызывает деполяризацию клеточных мембран и, как следствие, влияет на метаболизм [8]. Чтобы улучшить работу биологических очистных сооружений, необходимо разработать методы предварительной обработки сточных вод с ПАВ.
Адсорбция - популярный физико-химический метод удаления ПАВ из стоков [7, 9]. В настоящее время активированный уголь стал наиболее широко используемым адсорбентом для очистки от различных загрязнителей. Тем не менее, из-за высокой стоимости его широкое использование для очистки сточных вод часто ограничено.
За последние годы широкий спектр недорогих адсорбентов был протестирован на их способность устранять загрязняющие вещества из сточных вод. В качестве сорбентов были использованы сельскохозяйственные и бытовые отходы, побочные продукты производств, отходы морепродуктов, почва и минеральные компоненты и др., но по-прежнему необходимы дальнейшие работы по поиску недорогого и эффективного адсорбента для крупномасштабного удаления ПАВ [9-10].
Для лучшего понимания механизма сорбционных процессов используются математические модели Ленгмюра, Фрейндлиха, Темкина и БЭТ (Брунауэра, Эммета и Теллера) и другие, которые позволяют получить информацию о взаимодействии между поверхностью адсорбента и адсорбатом.
Эта работа посвящена изучению сорбционных процессов при очистке модельных вод от ПАВ при помощи органоминеральных сорбционных материалов, полученных на основе карбонатсодержащего отхода сахарной промышленности и диатомитового шлама пивоваренной промышленности. Особенности состава и физико-химических трансформаций в процессе модификации материалов изложены в работах [11-12].
Целью исследования являлось определение оптимального способа модификации исследуемых органоминеральных отходов для получения эффективного в отношении лаурилсульфата натрия сорбционного материала, а также изучение особенностей коллоидно-химических взаимодействий, возникающих в ходе очистки модельных растворов.
Основными задачами были выбраны следующие:
-
- получение органоминеральных сорбционных материалов различных модификаций;
-
- выявление наиболее эффективного в текущих условиях эксперимента сорбционного материала;
-
- исследование особенностей сорбционного процесса на примере полученного сорбционного материала.
МАТЕРИАЛЫ И МЕТОДЫ
В качестве исходного сырья сорбционных материалов были использованы карбонатсодержащий отход сахарной промышленности – сатурационный осадок и диатомитовый шлам пивоваренной промышленности. Модификацию отходов проводили путем обработки в муфельной печи (LOIP LF-7/13) при различных температурах в течение 60 мин.
Обозначения полученных сорбционных материалов и их комбинаций представлены в таблице 1.
Таблица 1. Сорбционные материалы, используемые в работе
|
Обозначение |
Исходное сырье |
Модификация |
|
СО боо |
сатурационный осадок |
600 °С |
|
ДШ 450 |
диатомитовый шлам |
450°С |
|
ДШ 550 |
диатомитовый шлам |
550°С |
|
СОДШ 600 |
сатурационный осадок и диатомитовый шлам (1:1) |
600 °С |
|
СО боо :ДШ 55о |
СО боо : ДШ 550 (5:1) |
- |
|
СО боог |
СО боо |
гидрофобизованный стеариновой кислотой в соотношении (1:0,005) |
|
ДШ 450Г |
ДШ 450 |
гидрофобизованный стеариновой кислотой в соотношении (1:0,005) |
|
ДШ 550Г |
ДШ 550 |
гидрофобизованный стеариновой кислотой в соотношении (1:0,005) |
В эксперименте использовали модельные растворы, содержащие лаирисульфат натрия в концентрации 0,1 г/дм3.
Очистка была проведена в статических условиях, путем добавления навесок сорбционного материала к модельному раствору. Содержимое колб перемешивали в течение 20 минут при температуре 25 °C, затем отфильтровывали через бумажный фильтр «синяя лента».
Концентрацию загрязняющего вещества до и после очистки определяли фотометрическим методом [13]. Все эксперименты проводились в трехкратной повторности.
По полученным значениям, начальных и конечных концентраций в растворе определялась сорбционная емкость (А, ммоль/г) по формуле [14]:
■ = (cH-Cp)-1Q0 m-1000 ’
где Cн – начальная концентрация, ммоль/дм3; Cк – равновесная концентрация, ммоль/дм3; m – масса сорбционного материала, г.
Изотерма адсорбции строилась по полученным значениям сорбционной емкости (A) материала и равновесным концентрациям.
Эффективность очистки (Э, %) растворов определяли по формуле:
э= (c^ -100 % , (2)
CH где Сн – начальная концентрация вещества в растворе, мг/дм3; Ск – конечная концентрация вещества в растворе, мг/дм3.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В ходе проведения исследования по очистке модельных растворов при помощи различных сорбционных материалов, были получены следующие данные (рисунок 2). Наиболее эффективным в данной серии экспериментов показал себя ДШ450Г, немногим уступили ему СО600Г и ДШ550Г. Сорбционные материалы ДШ450, ДШ550 и СО600 также показывают высокую эффективность извлечения лаурилсульфата натрия. Комбинирование сорбционных материалов в данном случае имело негативный эффект на процесс водоочистки, хотя в экспериментах с другими загрязнителями отмечалось повышение эффективности при совместном использовании СО600 и ДШ450 для очистки модельных вод от красителей [15].
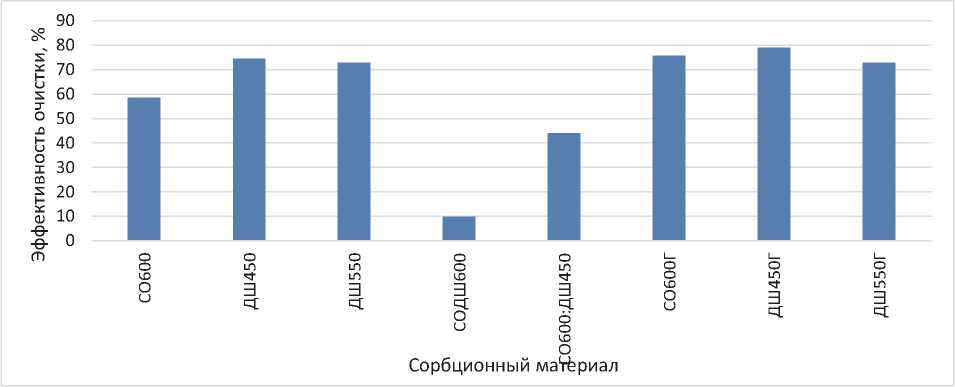
Рис. 2. Эффективность очистки модельных растворов сорбционными материалами
Поскольку наибольшая эффективность очистки была получена при использовании ДШ450Г, была построена изотерма адсорбции для этого материала (рисунок 3).
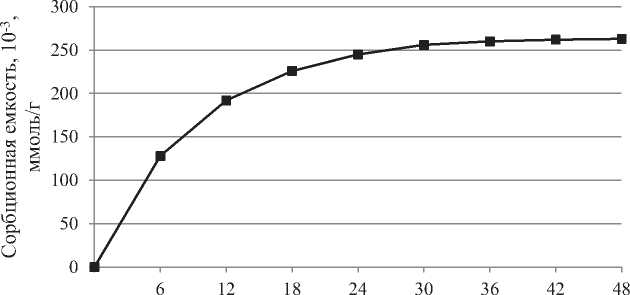
Равновесная концентрация, 10 " 1, ммоль/дм3
Рис. 3. Изотерма адсорбции и десорбции (Т=20 °С) лаурилсульфата натрия на поверхности ДШ450Г
Полученная изотерма относится к I типу по классификации, принятой международным союзом теоретической и прикладной химии, что указывает на микропористую структуру сорбционного материала [16]. Для уточнения механизма сорбции была применена обработка данных с использованием математических моделей Ленгмюра, Фрейндлиха, БЭТ, ТОЗМ, Дубинина-Радушкевича, Темкина [17-19].
Модель Ленгмюра описывает процесс мономолекулярной адсорбции на поверхности твердого тела, активные центры которого энергетически равнозначны, с учетом уравновешивания относительных скоростей адсорбции и десорбции.
Модель Фрейндлиха предполагает, что поверхность сорбента неоднородна и в первую очередь происходит заполнение активных сорбционных положений с максимальной энергией.
Модель БЭТ предусматривает многослойное присоединение молекул сорбата на поверхность адсорбента, активные центры которого энергетически равноценны.
Теория объемного заполнения микропор, или ТОЗМ, описывает объемное заполнение микропор на микропористых сорбентах, где поры сопоставимы по размеру с молекулами сорбата, поэтому взаимодействие протекает не на поверхности материала, а во всем объеме микропоры, в так называемом «сорбционном поле». В этом случае извлечение вещества может рассматриваться как вариант абсорбции, где сорбат растворяется в сорбенте, поскольку весь объем внутреннего порового пространства представляет собой объем эффективно действующего сорбционного поля.
Модель Дубинина-Радушкевича обычно применяется для выражения механизма многослойной адсорбции с гауссовым распределением энергии на неоднородных поверхностях.
Модель Темкина относится к случаю мономолекулярной адсорбции на неоднородной поверхности адсорбента; при этом что теплота адсорбции всех молекул в слое линейно снижается по мере заполнения слоя из-за взаимного отталкивания молекул сорбата и что адсорбция происходит с равномерным распределением максимальной энергии связывания [20-21].
Полученные зависимости отображены на рисунке 4, уравнения и коэффициенты корреляции представлены в таблице 2.
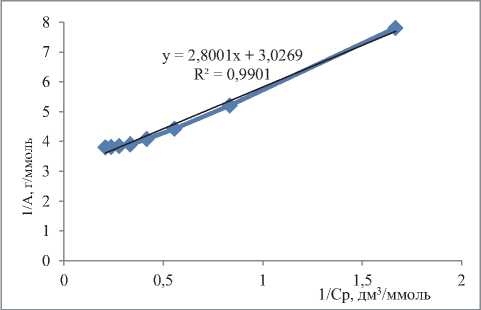
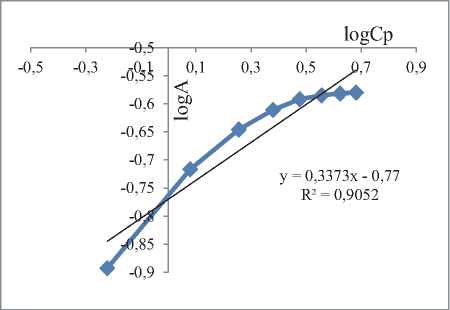
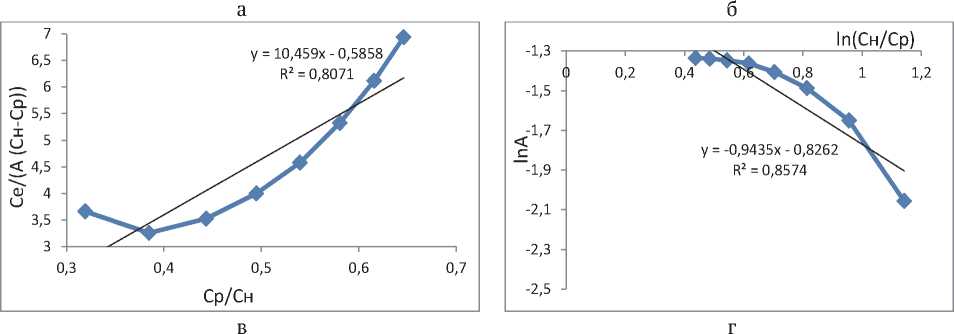
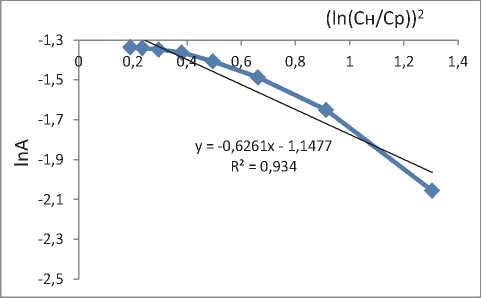
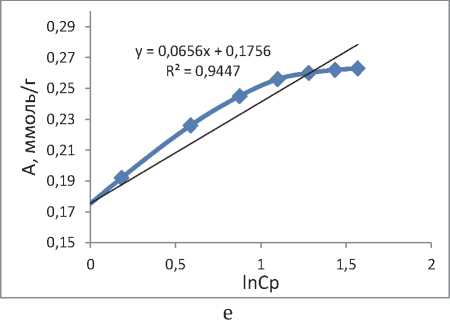
Рис. 4. Изотермы адсорбции, построенные с использованием моделей: а – Ленгмюра, б – Фрейндлиха, в – БЭТ, г – ТОЗМ, д – Дубинина-Радушкевича, е – Темкина
Таблица 2 – Результаты обработки изотерм адсорбции
|
Математическая модель |
Уравнение |
Коэффициент корреляции |
|
Ленгмюра |
1/A = 1/A« + 1/(KLA~Cp) |
0,99504 |
|
Фрейндлиха |
logA = logKF + 1/n logCp |
0,95144 |
|
БЭТ |
Ce/(A (Сн-Ср)) = 1/(А“Кбэт) + (Кбэт-1)/(А“Кбэт) (Ср/Сн) |
0,898396 |
|
ТОЗМ |
lnA=lnA~-(R*T/E)*ln(Cн-Cp) |
-0,92594 |
|
Дубинина-Радушкевича |
lnA=LnA~-(R*T/E)2*(ln(Cн/Cp))2 |
-0,96645 |
|
Темкина |
A = (R • T) / Ь те • Ina TE + (R • T) / Ь те • 1пСр |
0,97198 |
Из приведенных расчетов видно, что ближе всего к единице коэффициент корреляции, полученный с использованием модели Ленгмюра, что указывает на наиболее полное совпадение полученных в ходе исследований экспериментальных данных указанной аналитической модели [17-19, 21].
Изотерма адсорбции Ленгмюра является одной из наиболее часто используемых моделей адсорбции для количественной оценки связывания адсорбата с поверхностью адсорбента [22-24].
Многие ученые сообщают, что примененный в данной работе метод линеаризации изотермы Ленгмюра адекватно описывает экспериментальные данные по применению сорбентов [25].
В то же время, поскольку поверхности большинства природных адсорбентов неоднородны, при использовании упомянутой модели имеются погрешности, не позволяющие четко объяснить механизм адсорбции. Эта модель применима к описанию процессов только при определенных условиях и в большинстве случаев не может быть использована для механизмов адсорбции в многокомпонентных сточных водах [22]. Кроме того, константа равновесия Ленгмюра не подходит для расчета термодинамических параметров адсорбции [23]. Следовательно, в будущих исследованиях, направленных на моделирование изотерм адсорбции из жидкой фазы, следует учитывать особенности используемых моделей и условий экспериментов при описании механизмов сорбционного взаимодействия.
ВЫВОД
Проведенные исследования по использованию сорбционных материалов, полученных термической модификацией сатурационного осадка, диатомитового шлама, их смесей и применение дополнительной гидрофобизации стеариновой кислотой позволили установить, что наиболее эффективным в данной серии экспериментов является материал ДШ450Г. Высокую эффективность извлечения лаурилсульфата натрия также продемонстрировали СО600Г и ДШ550Г, сорбционные материалы ДШ450, ДШ550 и СО600 немногим им уступают.
Изотерма адсорбции для ДШ450Г соответствует материалу с микропористой структурой, применение математических моделей Ленгмюра, Фрейндлиха, БЭТ, ТОЗМ, Дубинина-Радушкевича, Темкина позволили установить, что сорбция лучше всего описывается моделью Ленгмюра, т.е. мономолекулярной адсорбции на поверхности твердого тела, активные центры которого энергетически равнозначны.


