Особенности состояния недоношенных новорожденных с бронхолегочной дисплазией
Автор: Черненков Ю.В., Нечаев В.Н., Нестерова Д.И.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Педиатрия
Статья в выпуске: 2 т.13, 2017 года.
Бесплатный доступ
Цель: изучить частоту бронхолегочной дисплазии (БЛД) у недоношенных детей, оценить степень функционального поражения респираторного тракта и эффективность респираторной поддержки. Материал и методы. Проведено обследование 36 женщин и 38 недоношенных детей (две двойни). Результаты. У 99% обследованных женщин беременность была осложнена хронической внутриутробной гипоксией плода; у 2,1 % резус-конфликтом. В 43,2% случаев во время беременности выявлена ОРВИ; у 15,3% отягощенный акушерский анамнез; 5% женщин имели вредные привычки (курение, прием алкоголя). В 2015 г. зарегистрировано 5 летальных исходов (13,2%). Переведены в другие ЛПУ для дальнейшего лечения 14 детей (36,8%); остальные 19 (50%) выписаны домой. Один ребенок доношенный, остальные недоношенные. У 87,7% детей с БЛД первичным диагнозом был РДСН; у 4,2% — аспирация мекония, у 8,1 % — врожденная пневмония. Получили терапию сур-фактантом однократно 15 детей (30,5%), из них 9 новорожденных (23,7%) получили этот препарат повторно. Всем новорожденным проводилась посиндромная интенсивная терапия, включая респираторную поддержку. ИВЛ осуществляли 8,4±2,3 дня 14 детям; 17,3±3,8 дня — 13 детям; 23,4±4,1 дня — одиннадцати. Назальный СРАР применялся у 23 новорожденных: у 4-6,8±1,9 дня; у 13 менее 16,8±2,9 дня; у 6 детей более 23,2±3,8 дня. Заключение. Необходимы: профилактика во время беременности глюкокортикоидами, пролонгирование беременности; у недоношенных новорожденных — сурфактантная терапия; адекватное оказание реанимационной помощи в родильном зале, проведение оксигенотерапии и респираторной поддержки. Уменьшение времени ИВЛ и расширение показаний для неинвазивных методов респираторной терапии позволило сократить число случаев БЛД, снизить тяжесть течения этого заболевания и улучшить прогноз.
Блд, недоношенные дети, профилактика блд, респираторная терапия
Короткий адрес: https://sciup.org/14918443
IDR: 14918443
Analysis of status of preterm infants with bronchopulmonary dysplasia
Objective: the combination frequency of BPD in premature infants, assessment of the degree of functional lesion of the respiratory tract and the efficiency of respiratory support. Material and Methods. The survey included 36 women and 38 preterm infants (two twins). Results. In 99% of the surveyed women pregnancy was complicated by chronic intrauterine fetal hypoxia, 2.1% — RH-conflict. At 43.2% of cases acute respiratory viral infection during pregnancy was revealed, 15.3% of bad obstetric history, 5% of women who had bad habits (smoking, alcohol intake). In 2015 there were 5 deaths (13.2%). 14 children (36.8%) were transferred to other hospitals for further treatment, the remaining 19 (50%) were discharged from the hospital. One child — full-term, the other— premature. At 87.7% of children with BPD, the diagnosis was RDS, in 4.2% — aspiration of meconium, 8.1% — congenital pneumonia. 15 children (30.5%) received therapy with surfactant once, including 9 newborns (23.7%) received medication twice. All newborns were carried out intensive care, including respiratory support. Mechanical ventilation in 14 children had been conducting for 8.4±2.3 day, in 13 cases for 17.3±3.8 day, in 11 cases for 23.4±4.1 day. Nasal CPAP was conducted in 23 newborns: from 4 to 6.8±1.9 day, 13 — less of 16.8±2.9 per day, 6 children have had more than 23.2±3.8 day. Conclusion. There is necessity for prevention during pregnancy with glucocorticoids, the prolongation of pregnancy; preterm neonates — surfactant therapy; adequate provision of resuscitation care in the delivery room and respiratory support. The reduction of time of mechanical ventilation and the expansion of the indications for non-invasive methods of respiratory therapy reduced the incidence of BPD, the severity of the disease and improve the prognosis.
Текст научной статьи Особенности состояния недоношенных новорожденных с бронхолегочной дисплазией
1 Введение. Бронхолегочная дисплазия (БЛД) новорожденных — хроническое полиэтиологическое заболевание легких, возникающее преимущественно у глубоко недоношенных детей. Частота БЛД обратно пропорциональна гестационному возрасту и массе тела при рождении. Так, у детей с весом при рождении 501–750 г, по результатам различных исследований, БЛД отмечается в 35-67%, а у детей с массой тела 1251-1500 г при рождении — в 1,1-3,6% случаев. Выхаживание таких детей достаточно сложное и порой носит затяжной характер.
Первое описание БЛД опубликовано W. Н. Northway в 1967 г. и представляло собой обзор историй болезней, данных рентгенограмм и патологоанатомических заключений 32 недоношенных детей, перенесших СДР и требовавших ИВЛ и кислородной поддержки в течение 24 часов и более [1]. Наблюдавшиеся дети имели средний гестационный возраст 32 недели и среднюю массу тела при рождении 2200 г. На основании этих данных W. Н. Northway сделал заключение о появлении нового хронического заболевания легких — БЛД, развитие которого он связывал с проведением ИВЛ и длительным (более 150 часов) использованием для дыхания высоких концентраций кислорода. Сегодня многими признается неудачность этого термина для обозначения по сути ятрогенного заболевания, имеющего мало сходства с врожденными состояниями, однако альтернативного наименования не предложено. В России диагноз БЛД впервые поставлен в 1989 г. в Санкт-Петербурге. В 1995 г. БЛД была включена в классификацию клинических форм бронхолегочных заболеваний у детей [1].
Основные факторы, способствующие развитию БЛД, следующие:
-
1. Незрелость легких недоношенного ребенка.
-
2. Токсическое действие кислорода. Экспериментально показано, что кислород может участвовать в патогенезе поражений, наблюдаемых на разных
-
3. Баротравма легких.
-
4. Инфекция. Одной из причин развития вторичной инфекции является интубация трахеи и респираторная терапия [2].
стадиях БЛД. Токсическое действие высоких концентраций кислорода во вдыхаемой смеси приводит к повреждению эпителиального и эндотелиального клеточных барьеров и развитию протеинсодер-жащего отека легочной ткани, что сопровождается снижением растяжимости альвеол, уже нарушенных вследствие дефицита сурфактанта.
Значительное сужение малых и средних артерий вследствие утолщения интимы существенно затрудняет легочный кровоток. Под действием оксигеноте-рапии, проводимой по поводу РДСН и БЛД с легочной гипертензией, реактивность сосудистого русла остается сохранной, а вазоконстрикция обратимой [3]. Патогенез БЛД представлен на рис. 1.
Сопротивление легочной ткани повышается у новорожденных на первой неделе жизни, у которых в дальнейшем развивается бронхолегочная дисплазия. Дыхательные расстройства, наблюдаемые в течение первого года жизни, проявляются относительной гипоксией, задержкой углекислого газа (гиперкапнией), учащением дыхания (тахипноэ), снижением дыхательного объема, увеличением минутной вентиляции, низкой динамической растяжимостью и нарушением вентиляции. К факторам, которые определяют слабость дыхательной мускулатуры, относят повышенное потребление кислорода и возросшую работу дыхания. Эмфизему и ателектазы легких при бронхолегочной дисплазии можно объяснить затруднением оттока воздуха из легких. Тяжелое обструктивное поражение дыхательных путей может быть связано с гиперреактивностью бронхов [4].
В дальнейшем в зависимости от тяжести состояния используется дифференцированная тактика лечения.
До 28 суток жизни можно только заподозрить диагноз бронхолегочной дисплазии новорожденного; с 7 суток предположить развитие БЛД (при длительной ИВЛ и оксигенотерапии, которые не дают положительной динамики).
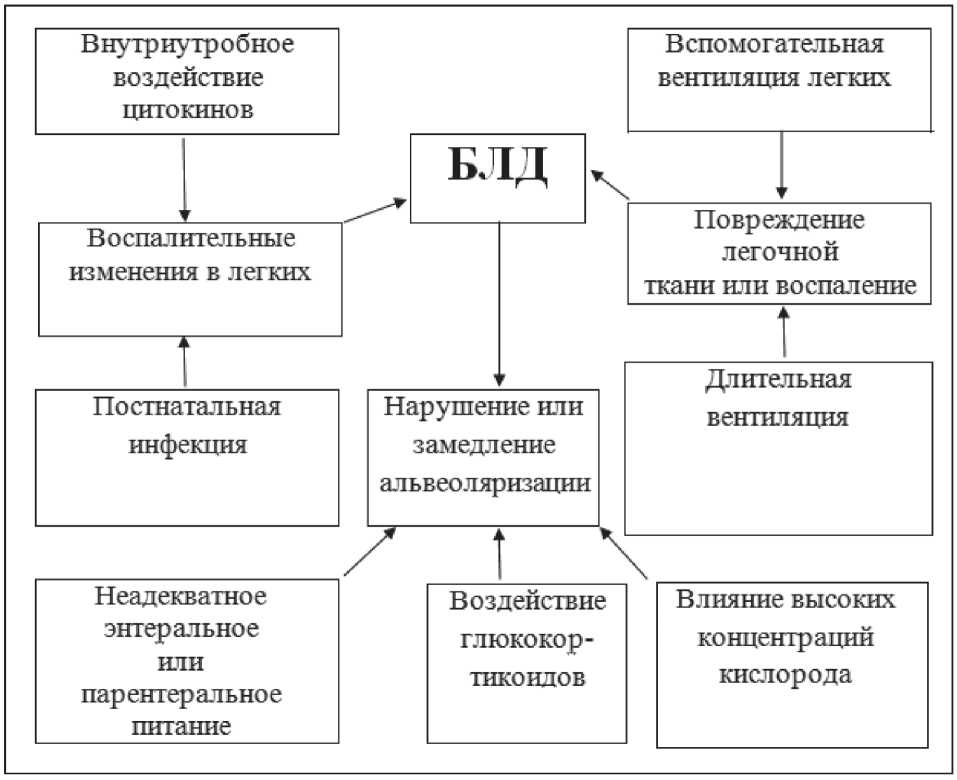
Рис. 1. Схема патогенеза БЛД [4]
Тяжесть состояния определяем путем мониторинга SpO2, ЧДД, ЧСС, кислотно-основного и газового состояния крови (КОС), также используются другие вспомогательные инструментально-лабораторные данные (рентгенография органов грудной клетки, УЗИ-диагностика и др.). Основываясь на них, выставляют определенные параметры респираторной поддержки. Важную роль играет положительное давление вдоха и концентрация кислорода. Терапия направлена на то, чтобы у ребенка стимулировать самостоятельное дыхание, дающее возможность применять неинвазивные методы респираторной поддержки и, по возможности, осуществлять дотацию увлажненного кислорода низкими концентрациями (до 30%). Лечение бронхолегочной дисплазии включает в себя также симптоматическую терапию: ингаляционные бронходилататоры и глюкокортикостероиды [5, 6]. На рис. 2 представлена респираторная поддержка при БЛД.
Формирование БЛД происходит в ранний неонатальный период жизни ребенка с респираторным дистресс-синдромом, и чаще на этапе реанимации и интенсивной терапии [8]. Первым важным шагом при ведении глубоко недоношенных детей, особенно с очень низкой массой тела и экстремально низкой массой тела, является адекватное оказание первичной реанимационной помощи в родильном зале. Ключевыми моментами при этом выступают следующие:
-
1. Профилактика гипотермии.
-
2. Респираторная терапия в рамках концепции «защиты легких».
-
3. Раннее использование респираторной поддержки с постоянным положительным давлением в легких в конце выдоха, которое способствует созданию и поддержанию функциональной остаточной емкости легких, препятствует ателектазированию, снижает работу дыхания.
-
4. До начала вентиляции осуществить маневр «продленного раздувания легких» с помощью аппарата ИВЛ с задержкой давления на вдохе для наиболее эффективного расправления альвеол.
-
5. Раннее введение сурфактанта новорожденным до 27 недели гестации, новорожденным 27–29 недели гестации, а также новорожденным менее 32 недель гестации. Сурфактант должен быть введен в течение 20 минут после рождения в дозе не менее 200 мг/кг массы тела (у новорожденных с ЭНМТ и ОНМТ возможно повторное введение сурфактанта).
-
6. Контроль оксигенации: целевой уровень сатурации в пределах 91-95%.
-
7. Предотвращение перегрузки жидкостью при проведении инфузионной терапии (контроль водного баланса).
-
8. Потеря массы тела в первые пять суток жизни у недоношенных детей должна быть не более 10-15%, но и не должно быть значительной прибавки веса.
-
9. Назначение системных кортикостероидов, особенно новорожденным с очень низкой или экс-
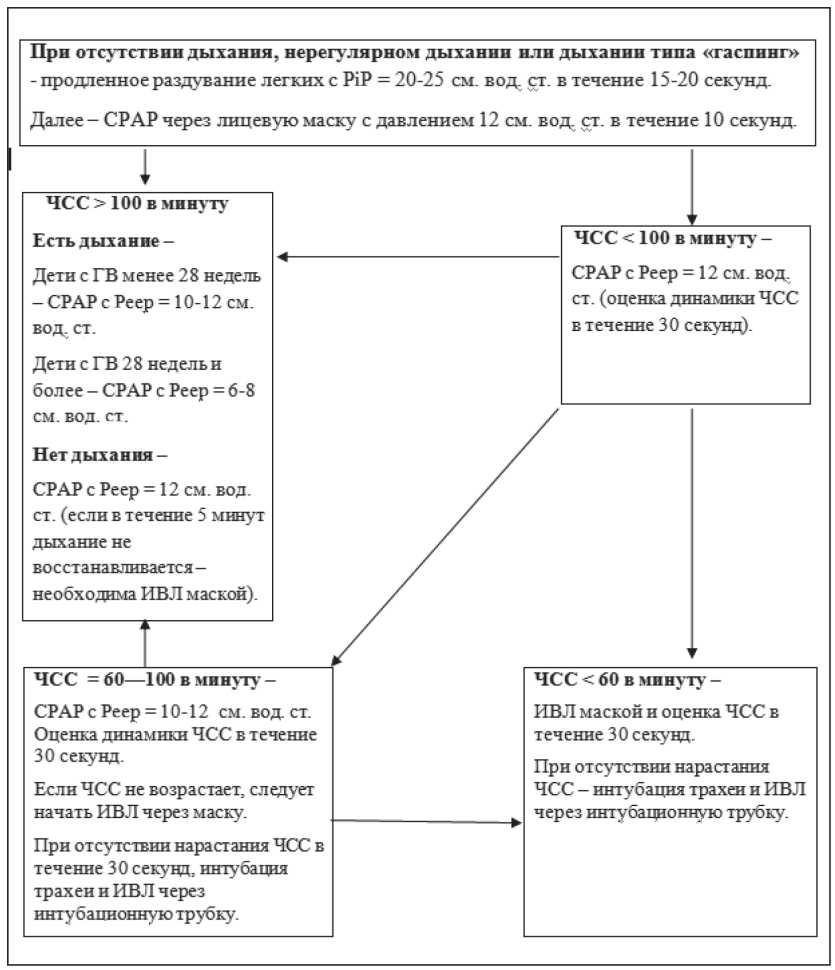
Рис. 2. Схема респираторной поддержки при БЛД [7]
-
10. Назначение кофеина детям с очень низкой или экстремально низкой массой тела (20% в нагрузочной дозе 20 мг/кг, затем 5–10 мг/кг) для поддержания неинвазивных методов респираторной терапии.
-
11. Применение диуретиков только по строгим показаниям (например, при рентгенологических признаках отека легких).
-
12. Применение бронходилататоров: беродуал по 1 капле в 1,5-2,0 мл NaCl 0,9% каждые 6-8 часов ингаляционно. По показаниям — ингаляции с глюкокортикоидами.
-
13. Нутритивная поддержка: 130–140 ккал/кг к концу второй недели жизни [6, 9].
тремально низкой массой тела, внутривенно. Кроме того, возможно назначение ингаляционных глюкокортикостероидных препаратов.
В последние годы стали широко использовать в лечении недоношенных детей неинвазивные и малоинвазивные методы интенсивной респираторной терапии и введения сурфактантов.
Цель исследования: изучить частоту БЛД у недоношенных детей, оценить степень функционального поражения респираторного тракта, эффективность респираторной поддержки.
Материал и методы . За 2015 г. в Клиническом перинатальном центре Саратовской области проведено обследование 36 женщин и 38 недоношенных детей (две двойни), 27 находящихся в ОРИТН и 11 в ОПННД. Материалом для исследования послужили анкеты матерей и медицинская документация: диспансерные карты беременных, заключения об ультразвуковом скрининге плода, истории родов и развития новорожденных. Методы исследования: анализ анкет и медицинской документации, осмотр, оценка степени ОДН, кислотно-основного состояния и газов крови, рентгенологического обследования органов грудной клетки, оценка эффективности сурфактантной терапии, методов респираторной поддержки и оксигенотерапии.
Результаты. У 99% обследованных женщин беременность осложнилась хронической внутриутробной гипоксией плода (ХВГП); у 2,1% резус-конфликтом. В 43,2% случаев выявлена острая респираторно-вирусная инфекция (ОРВИ) во время беременности; у 15,3% женщин оказался отягощенный акушерский анамнез, из них 5% имели вредные привычки (курение, прием алкоголя). Первородящих пациенток было 27,4%, повторнородящих 72,6%. В сельской местности проживали 33,5%.
Учитывая большое количество детей с очень низкой и экстремально низкой массой тела, в 2015 г. зарегистрированы 5 летальных исходов (13,2%). Для дальнейшего лечения переведены в другие ЛПУ (в стабильном состоянии) 14 детей (36,8%); остальные 19 пациентов (50%) выписаны домой. Всего один ребенок был доношенным (аспирационная бронхопневмония); остальные недоношенные. Частота развития БЛД у новорожденных с ЭНМТ составила 60,5%; у детей с ОНМТ 27,9%.
Распределение детей по сроку гестации и массе тела представлено в табл. 1, 2.
Таблица 1
Распределение новорожденных по массе тела
|
Масса новорожденного |
Количество детей |
|
500–1000 |
4 |
|
1000–1500 |
3 |
|
1500–2000 |
11 |
|
2000–2500 |
7 |
|
2500–3000 |
12 |
|
3000–3500 |
1 |
|
Более 3500 |
- |
Таблица 2
Распределение новорожденных по срокам гестации
|
Срок гестации |
Общее число новорожденных |
|
Менее 28 недель гестации |
4 |
|
27–28 |
3 |
|
29–30 |
7 |
|
31–32 |
4 |
|
33–34 |
8 |
|
35–36 недель |
11 |
|
37 недель и более |
1 |
Обсуждение. У большинства детей с БЛД (87,7%) первичный диагноз был РДСН; у 8,1% врожденная пневмония; у 4,2% аспирация мекония (аспирационная мекониальная бронхопневмония). Факторами риска развития БЛД у новорожденных также стали срок гестации менее 30 недель и низкая масса тела при рождении (менее 1500 г), низкая оценка по шкале Апгар (на 1-й минуте: 3,7±1,6; на 5-й минуте: 4,9±1,8). Получили сурфактантную терапию однократно15 (30,5%) детей; из них 9 (23,7%) новорожденным сурфактант эндотрахеально вводили повторно. Всем новорожденным проводилась интенсивная терапия, включая респираторную поддержку. ИВЛ осуществлялась 14 детям в течение 8,4±2,3 дня (в 2014 г. 19 случаев); 13 детям в течение 17,3±3,8 дня; 11 новорожденным в течение 23,4±4,1 дня. Назальный СPAP потребовался 23 новорожденным (в 2014 г. 17 случаев): у 4 пациентов длительность проведения составила 6,8±1,9 дня; у 13 менее 16,8±2,9; у 6 новорожденных более 23,2±3,8 дня.
Применяемая тактика лечения в виде профилактики во время беременности глюкокортикоидами и ее пролонгирование; проведение у новорожденного сурфактантной терапии: инвазивным методом через интубационную трубку (INSURE) (15 детей) и малоинвазивно через тонкий катетер (LISА) (9 пациентов); адекватное оказание реанимационной помощи в родильном зале и респираторная поддержка (nСРАР) позволили снизить количество БЛД, в том числе тяжелых форм, повысить качество помощи при этой патологии.
Заключение. Снижение времени проведения оксигенотерапии с высокими концентрациями кислорода и искусственной вентиляции легких, а также расширение показаний для малоинвазивных методов сурфактантной (LISA) и респираторной терапии (назальный СРАР), адекватное вскармливание позволяют заметно уменьшить число случаев БЛД и тяжесть течения, повысить эффективность терапии, сократить сроки лечения (на 12%) и улучшить качество жизни недоношенных детей.
Список литературы Особенности состояния недоношенных новорожденных с бронхолегочной дисплазией
- Овсянников Д.Ю., Кузьменко Л.Г., Дегтярева Е.А. Бронхолегочная дисплазия у детей. М., 2011; с. 122-128
- Александрович Ю.С., Гордеев В.И. Базисная и расширенная реанимация у детей. СПб.: Сотис, 2007; 187 с.
- Любименко В.А., Мостовой А.В., Иванов С.Л. Высокочастотная искусственная вентиляция легких в неонато-логии. М.: Медицина, 2002; 257 с.
- Володин H.H. Heонатология: национальное руководство. M.: ГЭОТАР-Медиа, 2008; 138 с.
- The primary and emergency care to babies: Metodical letter of the Russian Ministry of Health from April 21, 2010 №15-4/10/2-3204. Russian (Первичная и реанимационная помощь новорожденным детям: методическое письмо Минздрава России от 21 апр. 2010 г. №15-4/10/2-3204
- Шабалов Н.П. Неонатология: учеб. пособие. М.: МЕДпресс-информ, 2006; 316 с.
- Интенсивная терапия и принципы выхаживания детей с экстремально низкой и очень низкой массой тела при рождении: методическое письмо Минздрава России от 16.11.2011 г. №15-0/10/2-11336; 41 с.
- Черненков Ю.В., Нечаев В.Н. Диагностика, профилактика и коррекция врожденных пороков развития. Саратовский научно-медицинский журнал 2009; 5 (3): 379-383
- Александрович Ю.С., Пшениснов К.В. Интенсивная терапия новорожденных: руководство для врачей. СПб.: Изд-во Н-Л, 2013; 82 с.


