Особенности строения (диметилсульфоксидо)пентабромоплатината метилтрифенилфосфония
Автор: Зыкова Ална Романовна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Неорганическая химия
Статья в выпуске: 2 т.14, 2022 года.
Бесплатный доступ
Перекристаллизацией гексабромоплатината метилтрифенилфосфония из диметилсульфоксида получен с выходом 85 % (диметилсульфоксидо)пентабромоплатинат метилтрифенилфосфония [Ph3PCH3][PtBr5(dmso)] (1). Строение комплекса 1 установлено методом рентгеноструктурного анализа. Рентгеноструктурный анализ комплекса проводили на автоматическом четырехкружном дифрактометре D8 Quest Bruker (Мо Kα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 293 К. Кристаллографические характеристики: 1 - моноклинная сингония, пространственная группа P21, a = 12,51(5), b = 12,80(5), c = 16,44(7) Å, a = 90,00 град., β = 93,98(12) град., g = 90,00 град., V = 2626(19) Å3 , Z = 4, rвыч = 2,403 г/см3, F(000) = 1768,0, размер кристалла 0,36 × 0,26 × 0,15 мм, интервалы индексов отражений -16 ≤ h ≤ 16, -17 ≤ k ≤ 17, -22 ≤ l ≤ 22, всего отражений 80827, независимых отражений 13179 (Rint = 0,1591), число уточняемых параметров 547, GOOF 1,279, окончательные значения факторов расходимости: R1 = 0,1630, wR2 = 0,2098 (по всем рефлексам), R1 = 0,1202 и wR2 = 0,1936 (по рефлексам F2 > 2s(F2), остаточная электронная плотность 4,29/-5,04 e/Å3. По данным РСА, в кристалле соединения 1 присутствуют по два типа кристаллографически независимых катиона и аниона, геометрические параметры которых незначительно отличаются друг от друга. Молекула диметилсульфоксида встраивается в координационную сферу платины. Параметры координированного диметилсульфоксидного лиганда отличаются от свободной молекулы диметилсульфоксида.
Гексабромоплатинат, диметилсульфоксид, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147237510
IDR: 147237510 | УДК: 546.185
Structural features of methyltriphenylphosphonium (dimethylsulfoxido)pentabromoplatinate
Methyltriphenylphosphonium (dimethylsulfoxido)pentabromoplatinate [Ph3PCH3][PtBr5(dmso)] (1) has been obtained by recrystallization of methyltriphenylphosphonium hexabromoplatinate from dimethyl sulfoxide, yielding 85%. Complex 1 has been characterized by X-ray structural analysis. The X-ray structural analysis of the complex has been carried out on an automatic four-circle D8 Quest Bruker diffractometer (МоКα-radiation, λ = 0.71073 Å, graphite monochromator) at 293 K. Crystallographic characteristics of complex 1: monoclinic syngony, space group P21, a = 12.51(5), b = 12.80(5), c = 16.44(7) Å, a = 90.00 deg., β = 93.98(12) deg., g = 90.00 deg., V = 2626(19) Å3, Z = 4, rcalc = 2.403 g/cm3, F(000) = 1768.0, crystal size 0.36 × 0.26 × 0.15 mm, reflection index intervals -16 ≤ h ≤ 16, -17 ≤ k ≤ 17, -22 ≤ l ≤ 22, total reflections 80827, independent reflections 13179 (Rint = 0.1591), number of refined parameters 547, GOOF 1.279, R1 = 0.1630, wR2 = 0.2098 (R-factors for all reflections), R1 = 0.1202, wR2 = 0.1936 (F2 > 2s(F2), residual electron density (max/min) 4.29/-5.04 e/Å3. According to the X-ray diffraction data, the crystal of compound 1 contains two types of crystallographically independent cations and anions, the geometric parameters of which are slightly different. The dimethyl sulfoxide molecule is embedded in the platinum coordination sphere. The parameters of the coordinated dimethyl sulfoxide ligand differ from the free dimethyl sulfoxide molecule
Текст научной статьи Особенности строения (диметилсульфоксидо)пентабромоплатината метилтрифенилфосфония
Диметилсульфоксидные комплексы платины привлекают внимание с момента их открытия Коттоном Ф.А. в середине XX века и по настоящее время [1–3]. Диметилсульфоксидные лиганды, являясь амбидентатными, могут координироваться на металл как атомом кислорода, так и атомом серы. Координация через атом серы представлена в основном в комплексах элементов платиновой группы [4, 5].
Для синтеза ионных диметилсульфоксидных комплексов платины(IV) используется две методики, одна из которых заключается во взаимодействии галогенида тетраорганилфосфония или -аммония с гексагалогеноплатиноводородной кислотой или ее солью непосредственно в растворе диметилсульфоксида, другая – в перекристаллизации гексагалогеноплатинатов(IV) из диметилсульфоксида [6–8]. В литературе представлено небольшое число ионных комплексов платины с анионами [PtBr6]– [9–13]. Комплексы с анионами [PtBr5(dmso)]– немногочисленны [14].
В настоящей работе определены структурные особенности (диметилсульфоксидо)пента-бромоплатината метилтрифенилфосфония методом рентгеноструктурного анализа.
Экспериментальная часть
Исходный реагент - гексабромоплатинат калия (K2PtBr6) выделяли из водного раствора платинобромистоводородной кислоты с бромидом калия. Красные кристаллы отфильтровывали, промывали водой и сушили.
Синтез (диметилсульфоксидо)пентабромоплатината метилтрифенилфосфония ( 1 ). 0,035 г (0,028 ммоль) гексабромоплатината метилтрифенилфосфония растворяли в 2 мл диметилсульфоксида. После испарения растворителя наблюдали образование кристаллов. Выход комплекса 0,023 г (85 %), красно-коричневые кристаллы, т. разл. 226 °С. ИК-спектр, ν , см–1: 3055,
2970, 2904, 1585, 1481, 1443, 1400, 1318, 1287, 1192, 1157, 1113, 1052, 995, 934, 896, 782, 747, 718, 688, 515, 499, 422. Найдено, %: С 26,91; Н 2,62. C 21 H 24 OSPPtBr 5 . Вычислено, %: С 26,95; Н 2,57.
Рентгеноструктурный анализ кристаллов комплекса 1 проведен на дифрактометре D8 Quest фирмы Bruker (Mo Kα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 293 К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [15]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [16] и OLEX2 [17]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Основные кристаллографические данные и результаты уточнения структуры 1 приведены в табл. 1, основные длины связей и валентные углы - в табл. 2. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1989715 для K2PtBr6; № 2126542 для 1; или .
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Параметр |
Значение |
|
М |
950,07 |
|
Сингония |
Моноклинная |
|
Пр. группа |
P2 1 |
|
Параметры решетки: |
|
|
a , Å |
12,51(5) |
|
b , Å |
12,80(5) |
|
c, Å |
16,44(7) |
|
α , град. |
90,00 |
|
β, град. |
93,98(12) |
|
γ , град. |
90,00 |
|
V , Å3 |
2626(19) |
|
Z |
4 |
|
ρ (выч.), г/см3 |
2,403 |
|
µ , мм - 1 |
13,103 |
|
F (000) |
1768,0 |
|
Размер кристалла, мм |
0,36 × 0,26 × 0,15 |
|
Область сбора данных по θ , град. |
6,4 - 57,58 |
|
Интервалы индексов отражений |
–16 ≤ h ≤ 16, –17 ≤ k ≤ 17, –22 ≤ l ≤ 22 |
|
Измерено отражений |
80827 |
|
Независимых отражений |
13179 ( R int = 0,1591) |
|
Число уточняемых параметров |
547 |
|
GOOF |
1,279 |
|
R -факторы по F 2> 2 σ ( F 2) |
R 1 = 0,1202, wR 2 = 0,1936 |
|
R -факторы по всем отражениям |
R 1 = 0,1630, wR 2 = 0,2098 |
|
Остаточная электронная плотность (min/max), e/A3 |
4,29/–5,04 |
Таблица 2
Длины связей ( d ) и валентные углы ( ω ) в структуре 1
|
Связь, d, Å |
Угол, ω , град |
||
|
Pt(1) - Br(2) |
2,441(8) |
Br(5)Pt(1)Br(2) |
89,9(2) |
|
Pt(1) - Br(5) |
2,433(9) |
Br(5)Pt(1)Br(3) |
178,27(14) |
Неорганическая химия
Окончание табл. 2
|
Связь, d, К |
Угол, ω , град |
||
|
Pt(1) - Br(1) |
2,437(8) |
Br(1)Pt(1)Br(2) |
178,55(14) |
|
Pt(1) - Br(3) |
2,434(9) |
Br(3)Pt(1)Br(2) |
88,6(2) |
|
Pt(1) - S(1) |
2,333(10) |
Br(3)Pt(1)Br(1) |
92,6(2) |
|
S(1) - O(1) |
1,41(2) |
S(1)Pt(1)Br(2) |
92,8(4) |
|
S(1) - С(7) |
1,79(4) |
S(1)Pt(1)Br(1) |
88,0(4) |
|
S(1) - С(8) |
1,75(3) |
S(1)Pt(1)Br(4) |
177,3(3) |
|
Pt(2) - Br(6) |
2,440(9) |
C(7)S(1)C(8) |
103(3) |
|
Pt(2) - Br(7) |
2,449(8) |
O(1)S(1)C(7) |
109,4(18) |
|
Pt(2) - Br(8) |
2,433(8) |
O(1)S(1)C(8) |
108,7(18) |
|
Pt(2) - Br(10) |
2,429(10) |
Br(9)Pt(2)Br(7) |
177,40(14) |
|
Pt(2) - S(2) |
2,329(11) |
Br(8)Pt(2)Br(6) |
179,32(12) |
|
S(2) - O(2) |
1,44(2) |
Br(8)Pt(2)Br(9) |
91,1(2) |
|
S(2) - C(9) |
1,75(3) |
Br(10)Pt(2)Br(9) |
87,6(3) |
|
S(2) - С(10) |
1,74(3) |
Br(10)Pt(2)Br(8) |
90,1(3) |
|
P(1) - С(1) |
1,75(2) |
S(2)Pt(2)Br(6) |
91,3(3) |
|
P(1) - С(11) |
1,77(3) |
S(2)Pt(2)Br(8) |
88,7(3) |
|
P(1) - С(27) |
1,79(3) |
S(2)Pt(2)Br(10) |
178,3(2) |
|
P(2) - С(51) |
1,76(3) |
C(9)S(2)C(10) |
100,6(16) |
|
P(2) - С(41) |
1,79(3) |
O(2)S(2)C(9) |
109,2(16) |
|
P(2) - С(47) |
1,78(3) |
O(2)S(2)C(10) |
110,5(17) |
|
C(1)P(1)C(11) |
104,5(13) |
||
|
C(1)P(1)C(27) |
108,3(15) |
||
|
C(11)P(1)C(21) |
109,1(13) |
||
|
C(21)P(1)C(27) |
115,4(15) |
||
|
C(31)P(2)C(41) |
111,6(12) |
||
|
C(31)P(2)C(47) |
108,3(13) |
||
Обсуждение результатов
В качестве исходного реагента был выбран гексабромоплатинат калия, полученный взаимодействием водного раствора гексабромоплатиноводородной кислоты с бромидом калия по методике [18]. Реакцией бромида метилтрифенилфосфония с гексабромоплатинатом калия в ацетонитриле был получен комплекс [Ph 3 PCH 3 ] 2 [PtBr 6 ], растворение которого в диметилсульфоксиде приводит к встраиванию молекулы растворителя в координационную сферу платины, при этом образуются красно-коричневые кристаллы комплекса [Ph 3 PCH 3 ][PtBr 5 (dmso)] 1 с выходом 85 %:
dmso
[Ph 3 PCH 3 ] 2 [PtBr 6 ] → [Ph 3 PCH 3 ][PtBr 5 (dmso)] + [Ph 3 PCH 3 ]Br
Структура комплекса 1 ранее была исследована методами ЯМР- (1Н, 13С, 195Pt), ИК-спектроскопии и рентгенофлуоресцентным энергодисперсионным анализом [19], однако рентгеноструктурные исследования комплекса 1 не проводились.
В настоящей работе его строение определено методом РСА. Показано, что в кристаллической ячейке комплекса 1 присутствуют по два типа кристаллографически независимых катиона и аниона, а и б , геометрические параметры которых несколько различаются (рис. 1).
Атом фосфора имеет тетраэдрическую координацию. Значения валентных углов СРС находятся в интервале 104,5(13)–115,4(15)° ( 1а ), 108,3(13)–111,6(12)° ( 1б ), расстояния P–C R равны 1,79(3) Å ( 1а ), 1,78(3) Å ( 1б ) и P–C Ph – 1,75(2)–1,77(3) Å ( 1а ), 1,76(3)–1,79(3) Å ( 1б ) близки между собой.
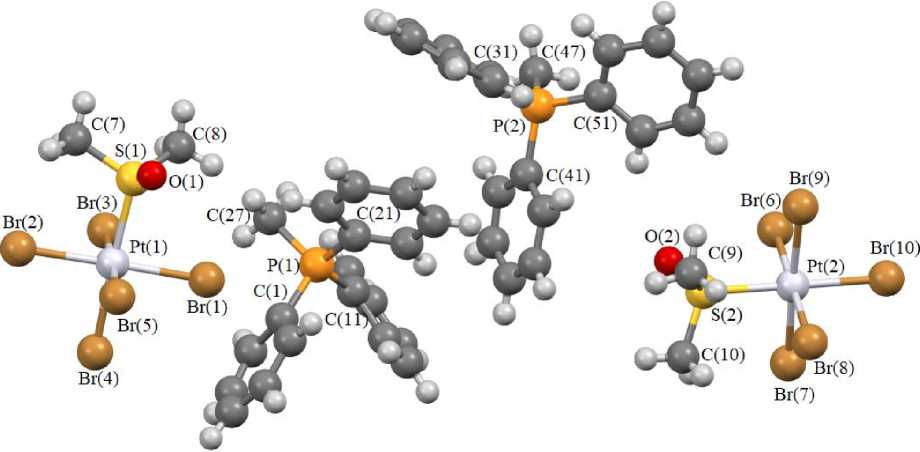
Рис. 1. Строение комплекса 1
В октаэдрических анионах комплекса 1 транс -углы BrPtBr составляют 178,27(14)° и 178,55(14)° ( 1а ), 177,40(14)° и 179,32(12)° ( 1б ), транс -угол SPtBr ‒ 177,3(3)° ( 1а ), 178,3(2)° ( 1б ), цис -углы BrPtBr и SPtBr изменяются в пределах 88,6(2)–92,6(2)° ( 1а ) 87,6(3)–91,1(2)° ( 1б ) и 88,0(4)–92,8(4)° ( 1а ) 88,7(3)–91,3(3)° ( 1б ). Длины связей Pt–Br находятся в интервале 2,433(9)– 2,441(8) Å ( 1а ), 2,429(10)–2,449 Å ( 1б ) и не превышают суммы ковалентных радиусов атомов платины и брома (2,56 Å [20]). Связь Pt–S в анионе укорочена (2,333(10) Å ( 1а ), 2,329(11) ( 1б )) по сравнению с суммой ковалентных радиусов (2,41 Å [20]) и близка к наблюдаемым значениям в (диметилсульфоксидо)пентабромоплатинатах [21–23].
Диметилсульфоксидный лиганд координирован к атому платины через атом серы. Параметры координированного диметилсульфоксидного лиганда отличаются от свободной молекулы диметилсульфоксида [24]. Углы CSC (103(3)° ( 1а ), 100,6(16)° ( 1б )) и OSC (108,7(18)°, 109,4(18)° ( 1а ), 109,2(16)°, 110,5(17)° ( 1б )) также отличаются от величин этих углов в несвязанной молекуле диметилсульфоксида (97,4° и 106,7°), что согласуется с литературными данными [24]. Можно предположить, что в тетраэдрическом окружении серы пара электронов, образующая координационную связь S-Pt, оказывает меньшее отталкивающее действие, чем неподелённая пара электронов атома S в свободном сульфоксиде [25].
В диметилсульфоксидном лиганде расстояния S–C (1,74(3) Å, 1,75(3) Å ( 1а ) 1,75(3) Å, 1,79(4) Å ( 1б )) короче, чем в свободной молекуле диметилсульфоксида (1,771(8) Å, 1,805(11) Å). Известно, что координация диметилсульфоксида через атом серы приводит к повышению порядка связи S=O [25, 26], так длина связи S–O (1,41(2) Å ( 1а ), 1,44(2) Å ( 1б )) в комплексе 1 короче, чем в свободной молекуле диметилсульфоксида (1,531 Å). Эти различия в расстояниях отражаются на положении частоты валентных колебаний ν (SO) координированного и свободного диметилсульфоксида [4, 5, 27]. Полосы поглощения SO-группы координированного диметилсульфоксида смещаются в высокочастотную область спектра (1158 см–1) по сравнению с полосой ν (SO) свободного 1055 см–1.
Структурная организация кристалла обусловлена наличием слабых контактов между катионами и анионами (C–H···Br - Pt 2,88–2,97 Å, C–H···O - S 2,65 Å, 2,64 Å). Наблюдаются короткие контакты между катионами (C–H···С 2,79–2,89 Å). В кристалле присутствуют два типа контактов между анионами: между атомами брома одного аниона и атомами брома другого аниона (Br···Br 3,46 Å), между атомами водорода метильных групп диметилсульфоксидного лиганда одного аниона и атомами брома другого аниона (Pt - Br···H–C 3,00 Å) (рис. 2).
Неорганическая химия
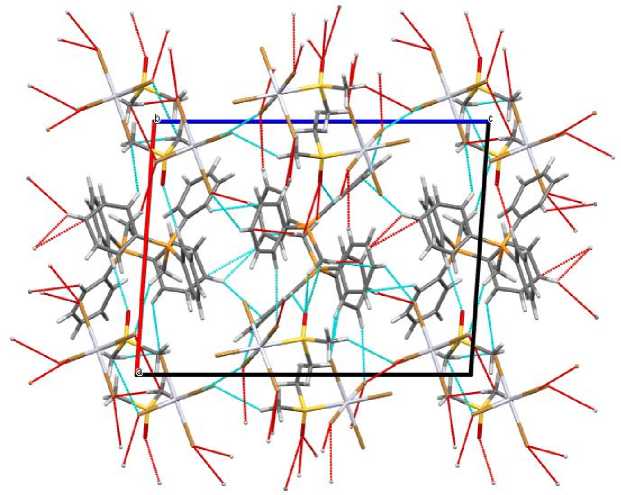
Рис. 2. Упаковка ионов в кристалле комплекса 1
Выводы
Таким образом, перекристаллизация гексабромоплатината метилтрифенилфосфония из диметилсульфоксида приводит к замещению хлорид-иона на молекулу растворителя в координационной сфере платины. Рентгеноструктурный анализ показал, что в кристалле соединения 1 присутствуют по два типа кристаллографически независимых катиона и аниона, а и б . Атомы фосфора в катионах а и б имеют искаженную тетраэдрическую координацию, атом платины гексако-ординирован.
Выражаю благодарность профессору В.В. Шарутину за проведенный рентгеноструктурный анализ образца.
Список литературы Особенности строения (диметилсульфоксидо)пентабромоплатината метилтрифенилфосфония
- Cotton, F.A. Sulfoxides as Ligands. I. A Preliminary Survey of Methyl Sulfoxide Complexes / F.A. Cotton, R. Francis // J. Am. Chem. Soc. - 1960. - V. 82. - P. 2986-2991.
- Cotton, F.A. Sulfoxides as Ligands. II. The Infrared Spectra of Some Dimethyl Sulfoxide Complexes / F.A. Cotton, R. Francis, W.D. Horrocks // J. Phys. Chem. - 1960. - V. 64. - P. 1534-1536.
- Meek, D.W. Transition Metal Complexes of Dimethyl Sulfoxide / D.W. Meek, D.K. Straub, R.S. Drago // J. Am. Chem. Soc. - 1960. - V. 82. - P. 6013-6016. DOI: 10.1021/ja01508a012.
- Кукушкин, Ю.Н. Вклад исследований диметилсульфоксидных комплексов в теории координационной химии / Ю.Н. Кукушкин // Коорд. химия. - 1997. - Т. 23, № 3. - C. 163-174.
- Calligaris, M. Stereochemical Aspects of Sulfoxides and Metal Sulfoxide Complexes / M. Calli-garis // Croat. Chem. Acta. - 1999. - V. 72, № 2-3. - P. 147-169.
- Синтез и строение комплексов платины [Ph4P]+[PtCl3(dmso)]- и [Ph4P]+[PtCl5(dmso)]- / B.В. Шарутин, В.С Cенчурин, О.К. Шарутина и др. // Журн. неорг. химии. - 2013. - Т. 58, № 1. - C. 36-40. DOI: 10.1134/S0036023613010191.
- Шарутин, В.В. ^нтез и строение комплекса платины [Ph4Sb(dmso)]+[PtCl5(dmso)]- / В.В. Шарутин, В.С Cенчурин, О.К. Шарутина // Бутлеровские сообщения. - 2011. - Т. 28, № 20. - C. 35-39.
- Окислительно-восстановительное превращение комплексов Pt(IV) с координационными молекулами диметилсульфоксида. Кристаллическая и молекулярная структуры трифенилбензил-фосфоний трихлоро(диметилсульфоксид)-платината(11) / C.C. ^тман, В.СФундаменский, В.Ю. Кукушкин и др. // Журн. Общ. Химии - 1988. - Т. 58, № 10. - C. 2297-2304.
- Hu, J. Novel Pt(II) Mono- and Biscarbene Complexes: Synthesis, Structural Characterization and Application in Hydrosilylation Catalysis / J.J. Hu, F. Li, A. Hor // J. Organomet. Chem. - 2009. - V. 28, № 4. - P. 1212-1220. DOI: 10.1021/om800978j.
- Kim, N.H. Crystal Structure of 57s(1,10-phenanthrolinium) Hexabromoplatinate(IV), [C:2H9N2]2[PtBr6] / N.H. Kim, K. Ha // Z. Kristallogr. NCS - 2010. - V. 225. - P. 37-38. DOI: 10.1524/ncrs.2010.0014.
- Rosokha, S. Anion-п Interaction in Metal-Organic Networks Formed by Metal Halides and Te-tracyanopyrazine / S. Rosokha, A. Kumar // J. Mol. Struct. - 2017. - V. 1138. - P. 129-135. DOI: 10.1016/j.molstruc.2017.03.009 0022-2860.
- Ha, K. Crystal structure of 57s(2-phenylpyridin-1-ium)hexabromidoplatinate(IV) Dihydrate, C22H24Br6N2O2Pt / K. Ha // Z. Kristallogr. - 2013. - V. 228, № 2. - P. 255. DOI: 10.1524/ncrs.2013.0130.
- Ha, K. 57s(1,10-phenanthrolin-1-ium) Hexabromidoplatinate(IV) Dehydrate / K. Ha // Acta Crystallogr. (E). - 2010. - V. 66, № 2. - P. 105. DOI: 10.1107/S1600536809055196.
- Cambridge Crystallografic Datebase. Release 2020. Cambridge.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. - 2009. - V. 42. - P. 339-341. DOI: 10.1107/S0021889808042726.
- Черняев, И.И. Синтез комплексных соединений металлов платиновой группы / И.И. Черняев. - Справочник М.: Наука, 1964. - 340 с.
- Зыкова, А.Р. Новые ионные комплексы платины(ГУ): [Ph3PCH3][PtBr5(dmso)] и [C(CH2OH)3NH3][K][Pt(SCN)6] / А.Р. Зыкова, Д.А. Жеребцов, О.С. Ельцов // Вестник ЮУрГУ. Серия «Химия». - 2022. - Т. 14, № 1. - С. 71-78. DOI: 10.14529/chem220108.
- Covalent Radii Revisited / B. Cordero, V. Gomez, A.E. Platero-Prats et al. // Dalton Trans. -2008. - V. 21. - P. 2832.
- Синтез и строение комплексов платины: [Bu4N]+[PtBr5(DMSO)]-, [Ph4P][PtBr5(DMSO)]- и [Ph3(n-Am)P]+[PtBr5(DMSO)]- / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журн. координац. химии. - 2011. - Т. 37, № 11. - С. 857-863.
- Шарутин, В.В. Синтез и строение комплекса платины [Ph3PC6Hn-cyc/o][PtBr5(DMSO-S)] / В.В. Шарутин, В.С. Сенчурин, Т.В. Мосунова // Вестник Южно-Уральского государственного университета. Серия «Химия». - 2017. - Т. 9, № 4. - С. 61-66. DOI: 10.14529/chem170410.
- Синтез и строение комплексов платины: [Ph4Sb]2[PtBr6]2-, [Bu4N]2[PtBr6]2-, [Ph4Sb(dmso)]+[PtBr5(dmso)r и [Bu4N]+[PtBr5(dmso)]- / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Бутлеровские сообщения. - 2012. - Т. 30, № 4. - С. 55-63.
- Thomas, R. The Molecular and Crystal Structure of Dimethyl Sulfoxide, (H3C)2SO / R. Thomas, C.B. Shoemaker, K. Eriks // Acta Crystallogr. - 1966. - V. 21, № 1. - P. 12-20.
- Calligaris, M. Structure and Bonding in Metal Sulfoxide Complexes / M. Calligaris, O. Carugo // Coord. Chem. Rev. - 1996. - V. 153. - P. 83-154. DOI: 10.1016/0010-8545(95)01193-5.
- Calligaris, M. Structure and Bonding in Metal Sulfoxide Complexes: an Update / M. Calligaris // Coord. Chem. Rev. - 2004. - V. 248. - P. 351-375. DOI: 10.1016/j.ccr.2004.02.005.
- Alessio, E. Synthesis and Reactivity of Ru-, Os-, Rh-, and Ir-halide-sulfoxide Complexes / E. Alessio // Chem. Rev. - 2004. - V. 104. - P. 4203-4242. DOI: 10.1021/cr0307291.


