Особенности течения артериальной гипертензии, связанные с распределением аллелей и генотипов полиморфного маркера C825t гена GNB3 среди больных, проживающих в Ростовской области
Автор: Арутюнян Л.В., Дроботя Н.В., Пироженко А.А., Торосян С.С., Калтыкова В.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.12, 2017 года.
Бесплатный доступ
Проанализированы клинические наблюдения и специально проведенные исследования у 47 больных с артериальной гипертензией (АГ), проживающих в Ростовской области. Среди обследованных мужчин было 21 (45%), женщин 26 (55%). Проведен анализ влияния полиморфизма гена гуанин связывающего белка (GNB3) на особенности течения АГ. При сравнении частот генотипов и аллелей гена GNB3, оказалось, что носительство генотипа C/T полиморфного маркера C825T гена GNB3 ассоциировано с отягощенным семейным анамнезом и ранним началом АГ. У больных АГ 3 степени оказалась достоверно ниже частота аллели С полиморфного маркера C825T гена GNB3. Носительство аллели T было ассоциировано с повышенной массой тела (ИМТ >325). Достоверной связи между изученным геном и стадией, а также с развитием осложнений АГ (инфаркт миокарда, нарушение мозгового кровообращения, хроническая сердечная недостаточностью), поражением органов мишеней в рамках данного исследования выявить не удалось.
Артериальная гипертензия, генетический полиморфизм, ген gnb3
Короткий адрес: https://sciup.org/140188641
IDR: 140188641 | УДК: 616.12-008.331.1:575.22
Tendencypeculiarities of arterial hypertension caused distribution of alleles and genotypes of polymorphic marker C825T gene GNB3 among patients, who live in Rostov region
The base of research was carried out by clinical observation and special investigations through 47 patients with arterial hypertension, who live in Rostov region. Among patients there were 21 men (45%) and 26 women (55%). Based on clinical difference which was found out during investigations, was carried out the analysis of gene guanine connecting protein (GNB3) effect on peculiarities of arterial hypertension. By comparison genotype frequency and gene GNB3 alleles was found out that genotype C/T polymorphic marker C825T gene GNB3 carriage associated with burdened family anamnesis and early start of arterial hypertension. Among patients with third stage of hypertension there were significantly less alleles C polymorphic marker C825T gene GNB3 frequency. The carriage of T allele was associated with increased weight (the body mass index>25). It was not found reliable relation between studied gene and hypertension stage and also between studied gene and complications of hypertension (myocardial infarction, stroke, chronic cardiac insufficiency), and between studied gene and target organs injury through the current investigation.
Текст научной статьи Особенности течения артериальной гипертензии, связанные с распределением аллелей и генотипов полиморфного маркера C825t гена GNB3 среди больных, проживающих в Ростовской области
В настоящее время в мире АГ страдает около 1 млрд человек. Несмотря на всеобщие усилия по профилактике и лечению АГ, она остается одним из ведущих факторов риска смертности населения от основных сердечно-сосудистых осложнений, таких как нарушение мозгового кровообращения и инфаркт миокарда, доля которых в структуре общей смертности составляет 20–50%.
Вклад АГ в смертность лиц среднего возраста от сердечно-сосудистых заболеваний составляет 40%, а в смертность от мозгового инсульта – 70–80% [2].
Растущая заинтересованность современных исследователей проблемой генетических полиморфизмов открывает широкие перспективы в переосмыслении и более глубоком понимании механизмов возникновения и прогрессирования большинства известных болезней. Не является исключением и АГ – многофакторное заболевание, при котором полиморфизмы в разных генах рассматривают в комплексе с экзогенными факторами [6].
В генетических исследованиях факторов развития АГ идентифицировано более 1500 генов, которые ассоциированы с повышением уровня АД [8].
Известно, что в большинстве случаев многофакторная природа АГ обусловлена генетическим полиморфизмом ренин-ангиотензин-альдостероновой (РААС) и брадикининовой систем [9]. Эти заключения основываются на многочисленных исследованиях по изучению ассоциации АГ с полиморфными вариантами соответствующих генов.
При исследовании связи генетических факторов АГ с особенностями ее течения, развитием осложнений и эффективностью терапии было показано, что наибольшее значение имели гены, кодирующие компоненты РААС [5].
С позиций современных представлений одним из патогенетических механизмов АГ является нарушение процессов передачи сигналов внутрь клеток. Как известно, в клетках организма присутствуют гуанин связывающие G-белки, представляющие собой ГТФ-азы – ферменты, которые связывают и гидролизуют гуанозинтрифосфат (ГТФ, GTP) и функционируют в качестве вторичных посредников во внутриклеточных сигнальных каскадах [3].
G-белки экспрессируются во всех клетках. G-белок, кодированный геном GNB3, опосредует передачу сигналов внутрь клеток, контролируя тонус сосудов и клеточную пролиферацию. Изменение активности синтезируемого G-белка может повлечь за собой нарушения в передаче внутриклеточных сигналов и привести к сужению сосудов, повышению артериального давления, гипертрофии левого желудочка, клеточной пролиферации и другим патологическим процессам. Многими работами подтверждена связь полиморфного маркера C825T гена GNB3 с развитием ожирения.
Раннее начало АГ ассоциировано с носительством генотипа Т/Т полиморфного маркера С825Т гена [4]. Некоторые исследования показывают, что генотип Т/Т предрасполагает к макрососудистым осложнениям, таким как инсульты и инфаркт миокарда, вне зависимости от уровня артериального давления и других факторов риска. Гомозиготы по Т аллели (генотип Т/Т) более предрасположены к повышению массы тела, чем носители аллели С.
На основании многочисленных исследований был определен круг генов-кандидатов, вовлеченных в формирование АГ [1, 7, 10, 12]. Однако, следует иметь в виду, что в разных популяциях вклад генов в развитие одного и того же заболевания может существенно различаться.
Соответственно, значительно различается в популяциях и уровень ассоциации одних и тех же маркеров. Например, аллель 825Т гена GNB3 достоверно ассоциирована с АГ в европейских популяциях, но не в восточно-азиатских. Вариабельность результатов генетикоэпидемиологических исследований может быть связана как с генетической гетерогенностью исследованных популяций, так и с патофизиологическими особенностями в патогенезе АГ у представителей разных этнических групп [11].
Исходя из вышеизложенного, цель исследования состояла в изучении ассоциации полиморфного маркера C825T гена GNB3 с особенностями течения АГ у больных, проживающих в Ростовской области.
Материалы и методы
В основу работы положены результаты комплексного клинического, инструментально и лабораторного исследования 47 больных АГ, проживающих в Ростовской области. Среди обследованных мужчин было 21 (45%), женщин 26 (55%). Средний возраст больных составил 53,9 ± 1,7 лет; продолжительность АГ – 5 лет и более. Диагноз АГ, степень, стадия и группа сердечно-сосудистого риска установлена на основании рекомендаций ВНОК по диагностике и лечению артериальной гипертонии. Критерием исключения являлась вторичная АГ.
Комплекс стандартного обследования больных включал электрокардиографию, ультразвуковое исследование сердца и почек (прибор «Acuson-128X» фирмы Acuson Cоrporation», США), суточное мониторирование артериального давления (прибор «Bplab», Россия), определение основных биохимических показателей крови.
Определение полиморфизма АГ осуществлялось на амплификаторе ДТ 96 (производство ДНК-технологии, Россия) на основании полимеразно-цепной реакции в режиме реального времени. В результате исследования определяли 9 вариантов однонуклеидных полиморфизмов генов (SNPs) – ADD1 (G1378T), AGT (T704C), AGT (C521T), AGTR1 (A1166C), AGTR2 (G1675A), CYP11B2 (C344T), GNB (C825T), NOS3 (T786C), NOS3 (G894T). Из генов-кандидатов, обуславливающих АГ, наиболее изучены гены, кодирующие ренин-ангиотензин-альдо-стероновую систему (РААС): AGT (T704C), AGT (C521T), AGTR1 (A1166C), AGTR2 (G1675A), CYP11B2 (C344T), в связи с чем в качестве гена кандидата особый интерес для нас представил один из менее изученных, ген GNB3 кодирующий бета-3-субъединицу G-белка.
Все пациенты участвовали в исследовании добровольно и были полностью информированы о его дизайне и целях. Протокол исследования был одобрен локальным этическим комитетом РостГМУ.
Математическая обработка полученных данных осуществлялась с использованием прикладных программ STATISTICA 10.
Результаты и обсуждение
Оценка семейного анамнеза больных АГ, включенных в исследование, с помощью стандартного опросника ВОЗ «Семейный анамнез» позволил установить, что подавляющее число пациентов (60%) имели отягощенный семейный анамнез по АГ.
При сравнении больных с отягощенным и неотяго-щенным семейным анамнезом оказалось, что больные с отягощенной по АГ наследственностью на момент обследования были сравнительно моложе (50 ± 2,25 лет и 59,8 ± 2,05 лет, соответственно, р = 0,003. Дебют гипертонии отмечался у данных больных в более молодом возрасте, чем у больных с неотягощенным анамнезом (40,8 ± 1,8 лет и 54,6 ± 2,3 лет, соответственно, р = 0,004). В группе больных с отягощенным семейным анамнезом была выше доля больных с АГ 3 степени тяжести (50% и 21%, соответственно, р = 0,037).
При анализе частоты встречаемости полиморфного маркера C8255T гена GNB3оказалось, что у больных АГ с отягощенным семейным анамнезом достоверно выше частота встречаемости данного гена (соответственно, 60,7% и 42,1%, p = 0,026 (рис. 1).
В табл. 1 представлена частота распределения аллелей и генотипов гена GNB3у больных с отягощенным и не-отягощенным семейным анамнезом.
При сравнении частот генотипов и аллелей изученного нами гена, оказалось, что носительство генотипа C/T полиморфного маркера C825T гена GNB3ассоциировано с отягощенным семейным анамнезом.
Нами также был проведен анализ частоты встречаемости гена GNB3 у больных с ранним началом и разной степенью тяжести АГ. Под «ранним» началом АГ понимали возникновение заболевания в возрасте менее 45 лет у
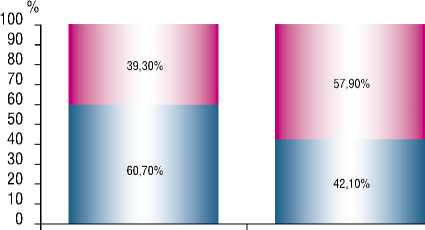
отягощенный анамнез не отягощенный анамнез
Табл. 1. Частота распределения аллелей и генотипов гена GNB3 у больных АГ с отягощенным и неотягощенным семейным анамнезом
|
Генотипы и аллели |
Отягощенный анамнез (n = 28) |
Не отягощенный анамнез (n = 19) |
P |
ОR |
Cl (95%) |
|
С/С |
11 (39,3%) |
11 (62,5%) |
НД |
– |
– |
|
C/T |
15 (53,6%) |
6 (31,6%) |
0,029 |
2,55 |
1,25–5,46 |
|
T/T |
2 (7,1%) |
2 (10,5%) |
НД |
– |
– |
|
T |
19 (25,7%) |
10 (26,3%) |
0,027 |
0,54 |
0,46–0,87 |
|
С |
37 (50%) |
28 (73,7%) |
НД |
– |
– |
■ ■ Ген GNB
I I Выборка
Рис. 1. Распределение частоты встречаемости гена GNB3 у больных АГ с отягощенным и неотягощенным семейным анамнезом мужчин и менее 55 лет у женщин. В обследованной группе было 28 больных с ранним началом АГ и 19 больных с поздним началом АГ (соответственно, 59,6% и 40,4%, р = 0,044).
Больные с ранним началом АГ имели достоверно большую длительность заболевания к моменту обследования (10,3 ± 1,76 лет и 5,2 ± 0,64 лет, р = 0,024), 32% больных этой группы имело АГ 3 степени тяжести. Эта группа больных чаще имела отягощенный семейный анамнез (75% и 21%, р = 0,013).
В табл. 2 представлена частота аллелей и генотипов гена GNB3, ассоциированных с ранним началом АГ.
При сравнении частот генотипов и аллелей изученного нами гена, оказалось, что раннее начало АГ ассоциировано с носительством генотипа C/T полиморфного маркера C825T гена GNB3 (рис. 2).
Для оценки ассоциации гена GNB3 с тяжестью АГ из числа обследованных мы сформировали 2 группы. В первую группу вошли больные АГ 1 и 2 ст., во вторую – больные АГ 3 ст. При сравнении групп выявлено, что среди больных АГ 3 ст. тяжести больше женщин (56% и 44%, p = 0,039). Длительность заболевания у них была больше (8,5 ± 1,2 лет и 7 ± 0,56 лет). По другим клиническим характеристикам группы достоверно не отличались.
В табл. 3 представлено сравнение частоты генотипов и аллелей гена GNB3 у больных АГ разной степени тяжести.
При анализе распределения частоты генотипов и аллелей оказалось, что у больных АГ3 степени тяжести достоверно меньше частота встречаемости аллели C полиморфного маркера C825T гена GNB3, т.е. носители аллели C имеют пониженный риск развития АГ 3 степени тяжести.
Учитывая то обстоятельство, что больные имели различные стадии АГ, нами была предпринята попытка установить ассоциацию полиморфного маркера C825T гена GNB3 со стадией заболевания.
Из числа обследованных I стадию заболевания имели 7 человек (15%), II стадию – 16 человек (34%), III стадию – 24 человек (51%). Больные с АГ различных
Табл. 2. Частота генотипов и аллелей гена GNB3 у больных АГ с ранним и поздним началом заболевания
|
Генотипы и аллели |
Раннее начало n = 28 |
Позднее начало n = 19 |
P |
ОR |
Cl (95%) |
|
C/C |
14 (50%) |
10 (52,6%) |
НД |
– |
– |
|
C/T |
14 (50%) |
6 (31,6%) |
0,039 |
1,46–4,57 |
1,23–5,43 |
|
T/T |
- (0%) |
3 (15,8%) |
НД |
– |
– |
|
T |
14 (25%) |
12 (31,6%) |
НД |
– |
– |
|
С |
42 (75%) |
26 (68,4%) |
НД |
– |
– |
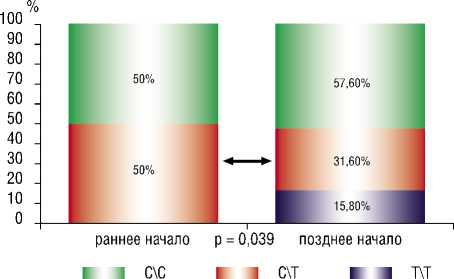
Рис. 2. Распределение частоты встречаемости генотипа C/T гена GNB3 у больных с ранним и поздним началом АГ
Табл. 3. Частота распределения генотипов и аллелей полиморфного маркера C825T гена GNB3 у больных АГ разной степени тяжести

Имеются многочисленные данные, свидетельствующие о том, что избыточная масса тела является фактором риска развития кардиальной патологии, поэтому можно предположить, что определение полиморфизма генов, ассоциированных с избыточной массой тела, требует особого внимания и представляется перспективным.
В обследованной группе больных 29 пациентов (61,7%) имели ИМТ ≥ 25 (повышенная масса тела), 18 пациентов (38,3%) – ИМТ < 25 (нормальная масса тела), р = 0,018. Больные с повышенной массой тела чаще характеризовались отягощенным семейным анамнезом (79% и 21%, р = 0,0067), длительность заболевания у них была больше, чем у больных с нормальной массой тела (10,2 ± 1,56 лет и 4,7 ± 0,64 лет, p = 0,01).
Частота распределения генотипов и аллелей гена GNB3 у больных АГс избыточной и нормальной массой тела представлена в табл. 4.
Приведенные в таблице данные свидетельствуют о том, что носительство аллели T полиморфного маркера C825T гена GNB3 ассоциировано с повышенной массой тела.
В рамках данного исследования нами не было установлено достоверной связи полиморфизма гена GNB с развитием осложнений АГ и поражением органов мишеней.
Выводы
-
1. Носительство генотипа C/T полиморфного маркера C/T гена GNB3 у больных АГ ассоциировано с отягощенным семейным анамнезом.
-
2. У больных АГ с отягощенным семейным анамнезом заболевание начинается в более молодом возрасте и характеризуется более высоким уровнем АД. Раннее начало АГ ассоциировано с носительством генотипа C/T полиморфного маркера C825T гена GNB.
-
3. У больных с АГ 3 степени тяжести оказалась достоверно меньшей частота аллели С полиморфного маркера C825T гена GNB, что может свидетельствовать о пониженном риске формирования АГ высокой степени тяжести у носителей аллели C.
-
4. Носительство аллели T полиморфного маркера C825T гена GNB3 ассоциировано с повышенной массой тела (ИМТ ≥ 25). Гомозиготы по T аллели (генотип T) более предрасположены к повышению массы тела, чем носители аллели С, следовательно, риск развития ожирения у людей с генотипом T/T выше по сравнению с C/C генотипом.
Табл. 4. Частота распределения генотипов и аллелей гена GNB3 у больных АГ с избыточной и нормальной массой тела
|
Генотипы и аллели |
ИМТ ≥ 25 |
ИМТ < 25 |
P |
ОR |
Cl (95%) |
|
C/C |
13 (44,8%) |
8 (44,4%) |
НД |
– |
– |
|
C/T |
13 (44,8%) |
9 (50%) |
НД |
– |
– |
|
T/T |
3 (10,3%) |
1 (5,6%) |
НД |
– |
– |
|
T |
19 (32,8%) |
11 (30,6%) |
0,04 |
1,08 |
0,98–2,25 |
|
С |
39 (67,2%) |
25 (69,4%) |
0,008 |
0,78 |
0,79–1,87 |
Список литературы Особенности течения артериальной гипертензии, связанные с распределением аллелей и генотипов полиморфного маркера C825t гена GNB3 среди больных, проживающих в Ростовской области
- Карпов Р.С. Полиморфные маркеры генов GNB3 (С825Т), AGTR1 (А1166) и АСЕ (A2350G и I/D) у больных артериальной гипертонией, сочетающейся с сахарным диабетом типа 2/Р.С. Карпов, К. В. Пузырев, О. А. Кошельская и др.//Терапевтический архив 2004. № 6. -С. 30-35.
- Кобалава Ж.Д. Артериальная гипертония. Ключи к диагностике и лечению/Ж.Д. Кобалава, Ю.В. Котовская, В.И. Моисеев. М.: ГЭОТАР-Медиа. 2009. -864 с.
- Люльман Х. Наглядная фармакология/Х. Люльман, К. Мор, Л. Хайн; Перевод с немецкого. -М.: Мир, 2008. -383 с.: ил. -(Наглядная медицина).
- Минушкина Л.О. Полиморфные маркеры гена ангиотензиногена у пациентов с артериальной гипертонией. Материалы Всероссийской научно-практической конференции «Современные возможности эффективной профилактики, диагностики и лечения артериальной гипертонии»/Л.О. Минушкина, Н.Б. Бабунова, А.А. Затейщикова, О.Ю. Кудряшова . -Москва, 2001. -С. 43.
- Минушкина Л.О. Генетические факторы при гипертонической болезни: связь с особенностями течения, развитием осложнений, эффективностью терапии: автореферат диссертации д.м.н./Минушкина Л.О-Москва, 2008.
- Сидоренкова М.Б. Изучение некоторых генетических полиморфизмов у пациентов европеоидной расы с артериальной гипертонией/М.Б. Сидоренкова, М.В.Терентьева, Г.И. Костюченко, А.В. Г ритчина, А.В. Манукян, М.А. Пляшешников//Биомедицина 2010, № 3. С. 138-140.
- Чистяков Д.А. Полиморфизм гена сосудистого рецептора ангиотензина II и сердечно-сосудистые заболевания/Д.А. Чистяков, Ж.Д. Кобалава, С.Н. Терещенко//Терапевтический архив, 2000. № 72. С. 27-30.
- Chiba S. Angiotensin II type 1 receptor gene polymorphism in patient with cardiac hypertrophy./S.Chiba,A. Ishanov, H. Okamoto, M. Watanabe//Japanese Heart Journal. 1998. Vol.39, № 1. P. 87-96.
- Naber C.K. Genetics of human arterial hypertension/C.K. Naber, W. Siffer//Minerva Med. 2004. Vol. 5, № 5. P. 346-356.
- O’Donnel С. J. The ACE Deletion Insertion Polymorphism and Hypertension: an Association Analysis in the Framingham Heart Study/C.J. O’Donnel, K. Lindpaintner, M. G. Larson.//European Heart Journal. 1997, P. 722-724.
- Ohmichi M. The genotype of the angiotensin-converting enzyme gene and global left ventricular dysfunction after myocardial infarction/M. Ohmichi, N. Ivai, Y.Nakamura//American Journal of Cardiology. 1995; 76: 326-329.
- Schunkert H. Polymorphism of the angiotensin-converting enzyme gene and cardiovascular disease/H. Schunkert//Journal of Molecular Medicine. 1997, Vol. 75, № 11-12. P. 876-875.


