Особенности влияния сульфат-ионов на коррозионно-электрохимическое поведение свинца, олова и их сплавов. Диаграммы электрохимического равновесия
Автор: Тюрин Александр Георгиевич, Бирюков Александр Игоревич, Тронов Артем Павлович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 3 т.8, 2016 года.
Бесплатный доступ
Построены диаграммы электрохимического равновесия Е - рН систем Pb -SO42- - H2O, Sn - SO42- - H2O и сплава Pb - Sn - SO42- - H2O. Изучены термодинамические особенности влияния сульфат-ионов на коррозионно-электрохимическое поведение свинца, олова и их сплавов.
Свинец, олово, сульфатные среды, коррозионно-электрохимическое поведения, диаграмма электрохимического поведения
Короткий адрес: https://sciup.org/147160362
IDR: 147160362 | УДК: 541.13:620.173:669.14 | DOI: 10.14529/chem160306
Features of sulphate influence on electrochemical corrosion behavior of lead, tin and their alloys. Diagrams of electrochemical equilibrium
Diagrams of electrochemical equilibrium E - pH of the Pb -SO42- - H2O and Sn - SO42- - H2O systems and the Pb- Sn - SO42-- H2O alloy have been constructed. The thermodynamic features of the effect of sulfate ions on electrochemical corrosion behavior of lead, tin and their alloys have been studied.
Текст научной статьи Особенности влияния сульфат-ионов на коррозионно-электрохимическое поведение свинца, олова и их сплавов. Диаграммы электрохимического равновесия
Коррозионно-электрохимическое поведение свинца и свинцово-оловянных сплавов с серной кислоте изучено в работах [1, 2]. Авторами установлено, что при анодном окислении свинцово-оловянных сплавов в области потенциалов от минус 0,7 до 0,3 В, в которой происходит образование сульфата свинца, олово присутствует и в пленке, и в электролите. Свинец в электролите не обнаружен. В области потенциалов от 1,9 до 2,4 В. наблюдается аналогичная картина. Сделан вывод о том, что при окислении свинцово-оловянных сплавов происходит активное растворение олова, которое накапливается в анодной пленке и переходит в раствор, повышая при этом пористость образующейся пленки. Происходит увеличение константы диффузионного процесса, что обеспечивает возрастание скорости прохождения сульфат ионов чрез пленку.
В представленных работах показано, что бинарные сплавы Pb–Sn сплавы с содержанием олова 1,5 и 2,0 % обладают наиболее высокой коррозионной стойкостью, а увеличение содержания олова в сплаве до 3 % приводит к сильному снижению стойкости. Также установлено, что при увеличении концентрации олова до 3 % сплав является гетерофазной системой и имеет разу-порядоченную микроструктуру с минимальным размером зерен. В работах методами электронной микроскопии показано, что на поверхности свинцового электрода формируется мелкокристаллическая пленка, в то время как на сплавах, легированных оловом, наблюдаются более крупные кристаллы, что может привести к увеличению пористости пленки.
В литературе отсутствует информация по термодинамическому анализу поведения свинца, олова и их сплавов в серной кислоте. Целью работы было проанализировать диаграммы электрохимического равновесия систем Pb – SO 4 2– – H 2 O, Sn – SO 4 2– – H 2 O и Pb – Sn – SO 4 2– – H 2 O.
Экспериментальная часть
Метод построения диаграмм электрохимического равновесия многокомпонентных металлических и смешанных систем предложен в работе [3]. Для подробного рассмотрения систем Ме – SO 4 2– – H 2 O необходимо проанализировать диаграмму электрохимического равновесия системы SO 4 2– – H 2 O. Данная диаграмма потенциал – рН при 25 ºС, давлении 1 бар (воздух) и a SO42- = 0,1 моль/л была рассчитана авторами и представлена в работах [4].
На ней можно выделить 13 основных областей преобладания фаз и фазовых составляющих системы. В зависимости от рН раствора и потенциала могут протекать катодные реакции восстановления сульфат- или гидросульфат-ионов до сернистой кислоты H2SO3, гидросульфит-ионов HSO 3 –, тетратионат-ионов S 4 O 6 2–, тиосульфат-ионов S 2 O 3 2–, свободной серы S (ромб), сероводородной кислоты H 2 S, гидросульфид-ионов HS– и сульфид-ионов S2–, и анодные реакции окисления сульфат- и гидросульфат-ионов HSO 4 – до персульфат-ионов S 2 O 8 2–.
Стационарный потенциал свинца в сернокислых растворах изменяется в области –0,2…–0,3 В (н.в.э.), что приходится на область термодинамической устойчивости сероводорода. Поэтому в сильнокислых сульфатных растворах необходимо учитывать конкурирующую катодную реакцию восстановления гидросульфат-ионов до сероводорода [5].
Диаграмма электрохимического равновесия свинца в сульфатных растворах приведена на рис. 1.
На данной диаграмме можно выделить 35 областей преобладания. I – Pb + H 2 S + H 2(г) , II – Pb + HS– + H 2(г) , III – Pb + S2– + H 2(г) , IV – PbS + S2– + H 2(г) , V – PbS + HS– + H 2(г) , VI – PbS + H 2 S + H 2(г) , VII – PbS + H 2 S, VIII – PbS + HS–, X – PbS 2 O 3 , XI – PbS + S 2 O 3 2–, XII – PbS + SO 4 2–, XIII – PbS + S 4 O 6 2–, XIV – Pb2+, S 4 O 6 2–, XVI – PbSO 3 , XVII – Pb2+, H 2 SO 3 , XVIII –Pb2+, HSO 4 –, XIX – PbSO 4 + HSO 4 –, XX – PbSO 4 + SO 4 2–, XXI – PbSO 4 *PbO + SO 4 2–, XXII – PbSO 4 *2PbO + SO 4 2– , XXIII – PbSO 4 *3PbO + SO 4 2–, XXIV – PbO + SO 4 2–, XXV – Pb 3 O 4 + SO 4 2–, XXVI – Pb 12 O 17 + SO 4 2–, XXVII – Pb 12 O 19 + SO 4 2–, XXVIII – Pb 12 O 19 + SO 4 2–+O 2(г) , XXXIII – Pb2+ + HSO 4 – +O 2(г) , XXXIV – PbO 2 + HSO 4 – +O 2(г) , XXXV – PbO 2 + S 2 O 8 2–– +O 2(г),
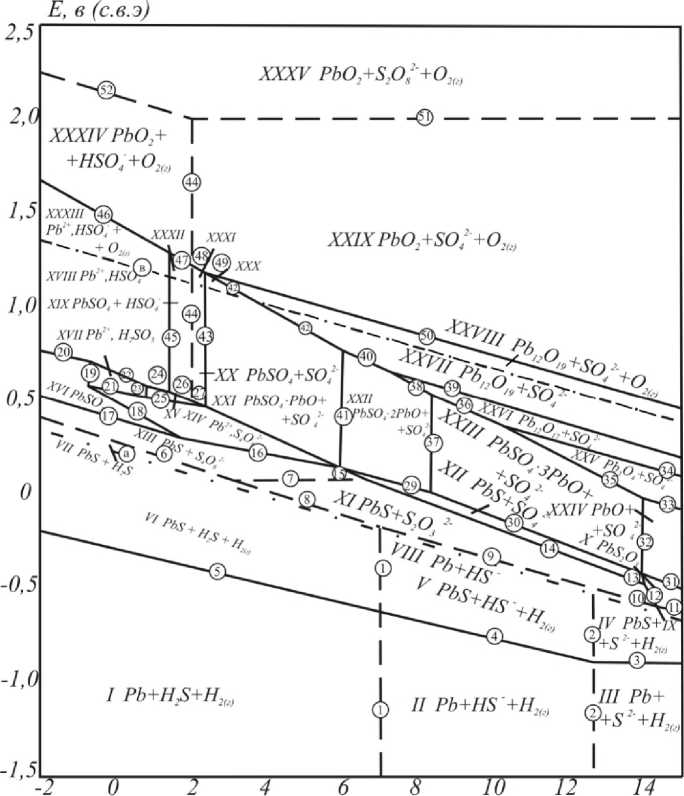
Рис. 1. Диаграмма электрохимического равновесия Е – рН системы Pb – SO 42– – H 2 O при 25 ºС, Р = 1 бар (воздух) и a i = 1 моль/л (негидратированная форма оксидов)
В сульфатсодержащих средах при достаточно отрицательных потенциалах на поверхности свинца может образовываться сульфид свинца PbS во всей области рН. При повышении потенциала в сильнокислых средах присутствует небольшая область активного растворения, а также область существования сульфита свинца PbSO3. Пассивация свинца при анодной поляризации связана с образованием на поверхности в зависимости от рН раствора сульфата свинца PbSO4 в сильнокислых растворах, и смешанных оксидно-сульфатных соединений, образующихся при повышении рН (PbSO4∙PbO; PbSO4∙2PbO; PbSO4∙3PbO). Исключительно оксидная пассивация свин- ца возникает лишь в сильнощелочных средах (рН ≈ 14), а также в щелочных средах при потенциалах положительнее +0,5 В.
На рис. 2. приведена диаграмма электрохимического равновесия олова в сульфатных растворах. На данной диаграмме можно выделить 21 область преобладания. I – Sn (β) + H 2 S + H 2 (г); II – Sn (β) + HS– + H 2 (г); III – Sn (β) + S2– + H 2 (г); IV – SnS + S2– + H 2 (г); V – SnS + HS– + H 2 (г); VI – SnS + H 2 S + H 2 (г); VII – SnO 2 + H 2 S + H 2 (г); VIII – SnO 2 + HS– + H 2 (г); IX – SnO 2 + S2– + H 2 (г); X – SnO 2 + S2–; XI – SnO 2 + HS–; XII – SnO 2 + H 2 S; XIII – SnO 2 + S 4 O 6 2–; XIV – SnO 2 + S 2 O 3 2–; XV – SnO 2 + SO 4 2–; XVI – SnO 2 + HSO 3 –; XVII – SnO 2 + H 2 SO 3 ; XVIII – SnO 2 + HSO 4 –; XIX – SnO 2 + HSO 4 –+ O 2 (г); XX – SnO 2 + SO 4 2–+ O 2 (г); XXI – SnO 2 + S 2 O 8 2– + O 2 (г).
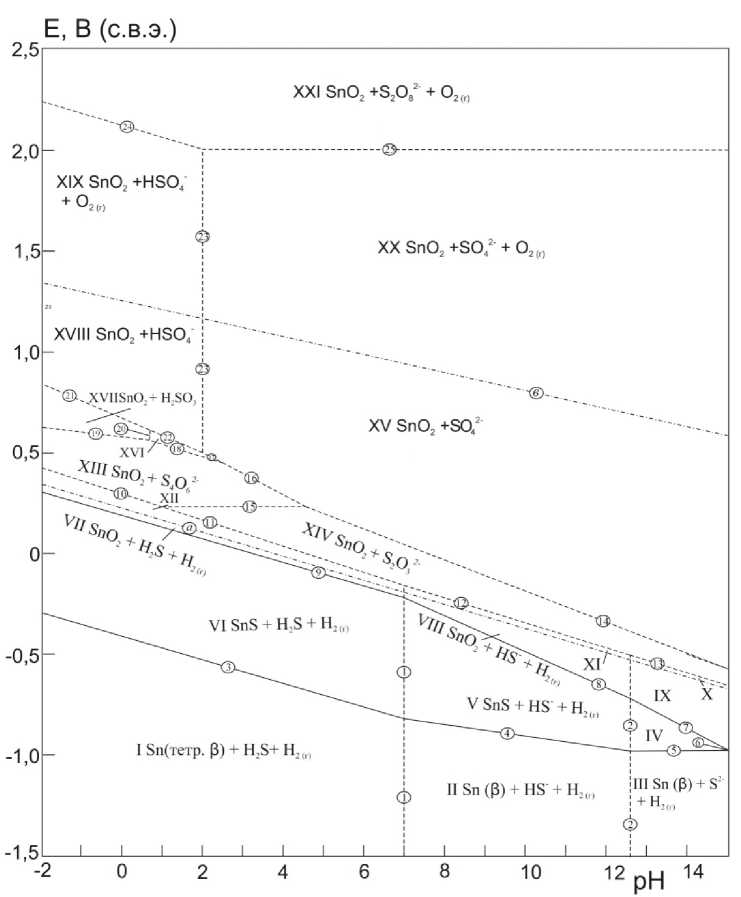
Рис. 2. Диаграмма электрохимического равновесия Е – рН системы Sn – SO 42– – H 2 O при 25 ºС, Р = 1 бар (воздух) и a i = 1 моль/л (негидратированная форма оксидов)
Характерной особенностью коррозионно-электрохимического поведения олова в растворах серной кислоты является также образования сульфида олова SnS при потенциалах ≈ –0,5 В до 0…+0,2 В. При потенциалах выше водородного электрода наблюдается пассивация диоксидом олова SnO 2 вплоть до потенциалов выше +2,0 В. На диаграмме не наблюдается образования таких соединений как сульфиты или сульфаты олова, тем не менее соединения серы претерпевают изменения.
Основные химические и электрохимические равновесия в системе Pb – Sn – SO 4 2– – H 2 O при 25 ºС, давлении 1 бар (воздух) и a i = 1 моль/л, рассчитанные по термодинамическим данным [5], представлены на рис. 3 и в таблице.
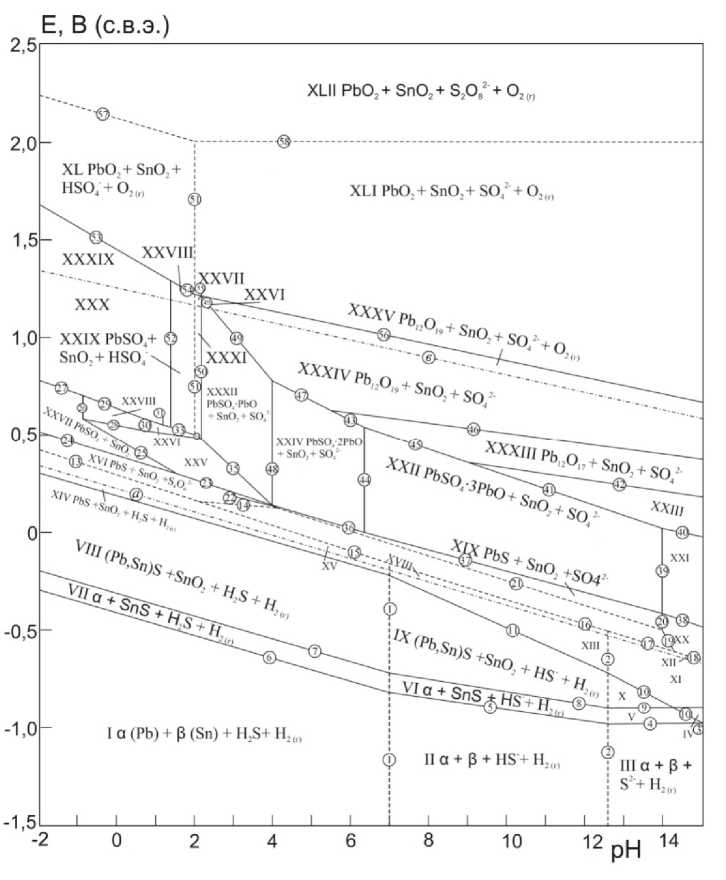
Рис. 3. Диаграмма электрохимического равновесия Е – рН системы Pb –Sn – SO 42– – H 2 O при 25 ºС, Р = 1 бар (воздух) и a i = 1 моль/л (негидратированная форма оксидов)
Основные химические и электрохимические равновесия в системе Pb – Sn – SO 42– – H 2 O при 25 °С, 1 бар (воздух)
|
№ п/п |
Электродная реакция |
Равновесный потенциал, В или рН раствора |
|
a |
2H+ + 2e = H 2 ; P H2 ≈ 5∙10-7 бар |
0,186 – 0,0591рН |
|
b |
О 2 + 4Н+ + 4e = 2H 2 О; P О2 ≈ 0,21 бар |
1,219 – 0,0591рН |
|
1 |
H 2 S ↔ HS– + H+ |
РН = 6,99 + 1g ( a HS - a a H 2 S ) |
|
2 |
HS– ↔ S2– + H+ |
РН = 12,60 + lg ( a 2- att ) S HS |
|
3 |
SnO 2 + 4H+ + 4e = Sn(β) + 2H 2 O; a Sn(β) = 1 |
–0,117 – 0,0591рН |
|
4 |
SnS + 2e = Sn(β) + S2– a Sn(β) = 1 |
-0,998 - 0,02951g a S 2 - |
Продолжение таблицы
|
№ п/п |
Электродная реакция |
Равновесный потенциал, В или рН раствора |
|
5 |
SnS + H+ + 2e = Sn(β) + HS– a Sn(β) = 1 |
–0,626 – 0,0295pH – 0,0295lg a – HS |
|
6 |
SnS + 2H+ + 2e = Sn(β) + H 2 S a Sn(β) = 1 |
–0,419 – 0,0591pH – 0,0295lg a H S |
|
7 |
PbS + 2H+ + 2e = Pb(α) + H 2 S a Pb(α) = 0,97 |
–0,320 – 0,0591pH – 0,0295lg a H S |
|
8 |
PbS + H+ + 2e = Pb(α) + HS– a Pb(α) = 0,97 |
–0,527 – 0,0295pH – 0,0295lg a – HS |
|
9 |
PbS + 2e = Pb(α) + S2– a Pb(α) = 0,97 |
-0,8987 - 0,0295lg a S 2 - |
|
10 |
SnO 2 + S2– + 4H+ + 4e = SnS + 2H 2 O |
-0,764 - 0,1182pH + 0,0295lg a S 2 - |
|
11 |
SnO 2 + HS– + 3H+ + 2e = SnS + 2H 2 O |
0,392 – 0,08865pH + 0,0295lg a – HS |
|
12 |
SnO 2 + H 2 S + 2H+ + 2e = SnS + 2H 2 O |
0,185 – 0,0591pH + 0,0295lg a H S |
|
13 |
S 4 O 6 2– + 20H+ + 18e = 4H 2 S + 6H 2 O |
0,2928 – 0,06567pH + 0,00328lg a a 4 S 4 O 6 H2S |
|
14 |
S 4 O 6 2– + 2e = 2S 2 O 3 2– |
0,08 -0,0295lg ( a S 2O 3 2_/ a S 4o62 _ ) |
|
15 |
S 2 O 3 2– + 10H+ + 8e = 2H 2 S + 3H 2 O |
0,3194 - 0,073875pH + 0,0074lg ( a S^. a h2s ) |
|
16 |
S 2 O 3 2– + 8H+ + 8e = 2HS– + 3H 2 O |
0,216 - 0,0591pH + 0,0074lg ( aq , 2- / a 2 _) S2O 3 HS |
|
17 |
S 2 O 3 2– + 6H+ + 8e = 2S2– + 3H 2 O |
0,030- 0,044325pH + 0,00739lg ( ac . /a 2 2 ) S2O3 S |
|
18 |
PbS 2 O 3 + 6H+ + 8e = PbS + S2– + 3H 2 O |
0,030 - 0,044325pH + 0,00739lg a S 2 - |
|
19 |
PbS 2 O 3 + 6H+ + 8e = 2PbS + S 2 O 3 2– + 3H 2 O |
4,462 - 0,3546pH - 0,0591lg ao .- S2O3 |
|
20 |
PbS+ SO 4 2– + 2H+ = PbS 2 O 3 + H 2 O |
pH = 13,93 + 0,5lg a 2 - SO 4 |
|
21 |
2 SO 4 2–+ 10H+ + 8e = S 2 O 3 2– + 5H 2 O |
0,551 - 0,0739pH + 0,0074lg ( a 2SO 2 - JaS^- ) |
|
22 |
4 SO 4 2– + 20H+ + 14e = S 4 O 6 2–+ 10H 2 O |
0,6185 - 0,0844pH + 0,0042lg ( a4 2- / a , o 2- ) SO4 S4O6 |
|
23 |
4Pb2+ + S 4 O 6 2– + 12H+ + 18e = 4PbS + 6H 2 O |
0,3726 -0,0394pH + 0,00328lg ( a 4p,2+ • a q J Pb S4O6 |
|
24 |
PbSO 3 + 6H+ + 6e = PbS + 3H 2 O |
0,4036 – 0,0591pH |
|
25 |
4PbSO 3 + 12H+ + 6e = S 4 O 6 2– + 4Pb2+ + 6H 2 O |
0,4966 - 0,1182pH + 0,00985lg ( a 4 pb 2 + • a ^O^ - ) |
|
26 |
4PbSO 3 + 2H+ = H 2 SO 3 + Pb2+ |
PH = -0,716 - 0,5lg ( a pb 2 + • a H 2 SO 3 ) |
|
27 |
HSO 4 – + Pb2+ + 2H+ + 3e = PbSO 3 + H 2 O |
0,682 - 0,0394pH + 0,0197lg( a 4 2+ • - . _,) Pb HSO4 |
|
28 |
4H 2 SO 3 + 4H+ + 6e = S 4 O 6 2– + 6H 2 O |
0,553 - 0,0394pH + 0,00985lg ( a 4 h2so3/ a ^O^- ) |
|
29 |
4HSO 4 – + 3H+ + 12e = H 2 SO 3 + H 2 O |
0,553 - 0,0394pH + 0,00985lg ( a 4 h2so3/ a ^O^- ) |
|
30 |
HSO 3 – + H+ = H 2 SO 3 |
PH = 0,715 - lg ( a H 2 SO 3 / a HSO 3- ) |
|
31 |
HSO 4 – + 2H+ + 2e = HSO 3 – + H 2 O |
0,620 -0,0591pH + 0,0295lg ( a HS0 3 -/ a HS0 4 - ) |
|
32 |
4HSO 3 – + 8H+ + 6e = S 4 O 6 2– + 6H 2 O |
0,5565 - 0,04433pH + 0,00985lg ( a 4 HS O - a SO, - ) |
|
33 |
PbSO 4 + 3H++ 2e = 4Pb2+ HSO 3 – + H 2 O |
0,651 - 0,08865pH - 0,0295lg( a ph2+ • a_ n - ) Pb HSO3 |
|
34 |
PbSO 4 + 3H+ + 2e = 4Pb2+ HSO 3 – + H 2 O |
0,651 - 0,08865pH - 0,0295lg( a ph2+ • a_ n - ) Pb HSO3 |
|
35 |
4PbSO 4 ∙PbO + 40H+ + 32e = 5Pb2+ S 4 O 6 2– + 20H 2 O |
0,628 - 0,0739pH - 0,00185lg( a 5.+ • aq .2- ) Pb S4O6 |
Окончание таблицы
|
№ п/п |
Электродная реакция |
Равновесный потенциал, В или рН раствора |
|
36 |
PbSO 4 ∙2PbO + 2 SO 4 2– + 28H+ + 24e = 3PbS + 14H 2 O |
0,5454 - 0,06895pH + 0,00422lg ac „ 2- SO 4 |
|
37 |
PbSO 4 ∙3PbO + 3 SO 4 2–+ 36H+ + 30e = 4PbS + 19H 2 O |
0,5918 - 0,07092pH + 0,0059lg aen 2 - SO 4 |
|
38 |
PbO + 2 SO 4 2–+ 12H++ 8e = PbS 2 O 3 + 6H 2 O |
0,8388 - 0,08865pH + 0,014775lg a en 2- SO4 |
|
39 |
PbSO 4 ∙3PbO + H 2 O = 4PbO + SO 4 2– + 2H+ |
pH = 13,93 + 0,5lg a 2 - SO4 |
|
40 |
PbO + 2H+ + 2e = PbS 2 O 3 + 6H 2 O |
0,804 – 0,0591рН |
|
41 |
4Pb 3 O 4 + 3SO 4 2– + 14H+ + 8e = 3(PbSO 4 ∙3PbO) + 7H 2 O |
1,421 - 0,1034pH + 0,02216lg a en 2- SO4 |
|
42 |
Pb 12 O 17 + 2H+ + 2e = 4Pb 3 O 4 + H 2 O |
0,977 – 0,0591рН |
|
43 |
Pb 12 O 17 + 3SO 4 2– + 14H+ + 10e = 3(PbSO 4 ∙3PbO) + 8H 2 O |
1,332 - 0,09456pH + 0,01773lg a en 2- SO4 |
|
44 |
4(PbSO 4 ∙2PbO) + H 2 O = SO 4 2– + 3(PbSO 4 ∙3PbO) + 2H+ |
pH = 8,34 + 0,5lg a 2 - SO4 |
|
45 |
Pb 12 O 17 + 4SO 4 2– + 18H+ + 10e = 4(PbSO 4 ∙2PbO) + 9H 2 O |
1,4303 - 0,10638pH - 0,0236lg a en 2- SO4 |
|
46 |
Pb 12 O 19 + 4H+ + 4e = Pb 12 O 17 + 2H 2 O |
1,082 – 0,0591рН |
|
47 |
Pb 12 O 19 + 4SO 4 2– + 22H+ + 14e = 4(PbSO 4 ∙2PbO) + 11H 2 O |
1,331 - 0,09287pH - 0,01689lg a en 2- SO4 |
|
48 |
3(PbSO 4 ∙2PbO) + H2O = SO 4 2– + 2(PbSO 4 ∙2PbO) + 2H+ |
pH = 6,04 + 0,5lg a 2 - SO4 |
|
49 |
Pb 12 O 19 + 6SO 4 2– + 26H+ + 14e = 6(PbSO 4 ∙PbO) + 13H 2 O |
1,4323 - 0,109757pH - 0,02533lg a en 2- SO4 |
|
50 |
PbSO 4 + H 2 O = SO 4 2– + PbSO 4 ∙PbO + 2H+ |
pH = 2,41 + 0,5lg a 2 - SO4 |
|
51 |
HSO 4 – = SO 4 2– + H+ |
pH = 2,00 + lg ( a pb 2 +- a H so4 - ) |
|
52 |
PbSO 4 + H+ = HSO 4 – + Pb2+ |
pH = 1,365 - lg ( a рь 2 +- a hso4 - ) |
|
53 |
PbO 2 + 4H+ + 2e = Pb2+ + 2H 2 O |
1,4393 - 0,1182pH - 0,0295lg a p b 2 + |
|
54 |
PbO 2 + HSO 4 – + 3H+ + 2e = Pb2+ + 2H 2 O |
1,399 - 0,08865pH - 0,0295lg a pb 2 + |
|
55 |
PbO 2 + HSO 4 – + 3H+ + 2e = PbSO 4 + 2H 2 O |
1,399 - 0,08865pH + 0,0295lg aue„ - HSO4 |
|
56’ |
Pb 12 O 19 + 12SO 4 2–+ 38H+ + 14e = 12PbSO 4 + 19H 2 O |
1,5543 - 0,1604pH + 0,05067lg ac„ 2- SO4 |
|
56 |
12PbO 2 + 10H++ 10e = Pb 12 O 19 + 5H 2 O |
1,082 – 0,0591рН |
На диаграмме Е – рН присутствуют следующие области преобладания: I – α-фаза (Pb) + +β-фаза (Sn) + H 2 S + H 2 (г); II – α + β + HS– + H 2 (г); III – α + β + S2– + H 2 (г); IV – α + SnO 2 + S2– + H 2 (г); V – α + SnS + S2– + H 2 (г); VI – α + SnS + HS– + H 2 (г); VII – α + SnS + H 2 S + H 2 (г); VIII – (Pb,Sn)S + H 2 S + H 2 (г); IX – (Pb,Sn)S + HS– + H 2 (г); X – (Pb,Sn)S + S2– + H 2 (г); XI – PbS + SnO 2 + S2– + H 2 (г); XII – PbS + SnO 2 + S2–; XIII – PbS + SnO 2 + HS– + H 2 (г); XIV – PbS + SnO 2 + H 2 S + H 2 (г); XV – PbS + SnO 2 + H 2 S; XVI – PbS + SnO 2 + S 4 O 6 2–; XVII – PbS + SnO 2 + S 2 O 3 2–; XVIII – PbS + SnO 2 + S 2 O 3 2– + H 2 (г); XIX – PbS + SnO 2 + SO 4 2–; XX – PbSO 3 + SnO 2 + SO 4 2–; XXI – PbO + SnO 2 + + SO 4 2–; XXII – PbSO 4 ∙3PbO + SnO 2 + SO 4 2–; XXIII – Pb 3 O 4 + SnO 2 + SO 4 2–; XXIV – PbSO 4 ∙2PbO + SnO 2 + SO 4 2–; XXV – SnO 2 + Pb2+,S 4 O 6 2–; XXVI – SnO 2 + Pb2+,HSO 3 –; XXVII – PbSO 3 + SnO 2 ; XXVIII – SnO 2 + Pb2+,H 2 SO 3 ; XXIX – SnO 2 + Pb2+,HSO 4 –; XXX – PbSO 3 + SnO 2 + HSO 4 –; XXXI – PbSO 4 + SnO 2 + SO 4 2–; XXXII – PbSO 4 ∙PbO + SnO 2 + SO 4 2–; XXXIII – Pb 12 O 17 + SnO 2 + SO 4 2–; XXXIV – Pb 12 O 19 + SnO 2 + SO 4 2–; XXXV – Pb 12 O 19 + SnO 2 + SO 4 2– + O 2 (г); XXXVI – PbSO 4 ∙PbO + SnO 2 + SO 4 2– + O 2 (г); XXXVII – PbSO 4 + SnO 2 + SO 4 2– + O 2 (г); XXXVIII – PbSO 4 + SnO 2 + HSO 4 – + O 2 (г); XXXIX – SnO 2 + Pb2+, HSO 4 – + O 2 (г); XL – PbO 2 + SnO 2 + HSO 4 – + O 2 (г); XLI – PbO 2 + SnO 2 + SO 4 2– + O 2 (г); XLII – PbO 2 + SnO 2 + S 2 O 8 2– + O 2 (г).
Согласно данной диаграмме в области иммунности при потенциале ≈ –1,0 В происходит восстановление сульфат ионов до сероводорода в кислой среде. При повышении потенциала олово превращается в сульфид олова SnS, затем образуется смешанный сульфид свинца и олова (Pb, Sn)S. При более положительных потенциалах сульфид олова превращается в диоксид олова SnO2, который встраивается в пассивационную пленку, состоящую из сульфида свинца PbS или сульфа- тов свинца различного состава PbSO4; PbSO4∙PbO. При этом, диоксид олова, обладающий меньшей коррозионной стойкостью в кислых сернокислых средах, очевидно, растворяется и повышает пористость пассивационной пленки на сплавах свинец – олово, тем самым снижая их коррозионную стойкость. Это согласуется с данным, представленными в работах [1, 2]. При проведении рентгенофазового анализа коррозионной пленки, образованной на свинцово-оловянных сплавах при положительных потенциалах, было обнаружено наличие следовых количеств SnO2 в пленке.
Заключение
-
1. Построены диаграммы Е-pH систем Pb – SO 4 2– – H 2 O, Sn – SO 4 2– – H 2 O и сплава Pb – Sn – SO 4 2– – H 2 O при 25 °С.
-
2. Показано, что при саморастворении свинца в кислых сульфатных средах он может подвергаться сульфидной пассивации, а при повышении потенциала – сульфатной пассивации. При увеличении рН возможно образование основных сульфатов с различным содержанием PbO: PbSO 4 ∙nPbO. Олово в кислых сульфатных растворах пассивируется сульфидом SnS и диоксидом олова SnO 2 .
-
3. При коррозии свинцово-оловянных сплавов, согласно диаграмме электрохимического равновесия, в пленке может накапливаться совместно с соединениями свинца диоксид олова, который увеличивает пористость пленки и, соответственно снижает коррозионную стойкость свинцо-во-оловянных сплавов.
Список литературы Особенности влияния сульфат-ионов на коррозионно-электрохимическое поведение свинца, олова и их сплавов. Диаграммы электрохимического равновесия
- Состав и структура пассивирущих слоев на поверхности свинца и многокомпонентных свинцовых сплавов при их анодном окислении в 4,8 М растворе серной кислоты/М.М. Бурашникова, И.В. Зотова, И.А. Казаринов и др.//Электрохимическая энергетика. -2011. -Т. 11, № 4. -С. 213-222.
- Бурашникова, М.М. Механизм анодной пассивации свинцово-оловянных сплавов в растворе серной кислоты/М.М. Бурашникова, И.В. Зотова, И.А. Казаринов//Электрохимическая энергетика. -2013. -Т. 13, № 4. -С. 205-212.
- Тюрин, А.Г. Термодинамика химической и электрохимической устойчивости твердых сплавов железа, хрома и никеля: монография/А.Г. Тюрин. -Челябинск: Изд-во Челяб. гос. ун-та, 2011. -241 с.
- Тюрин, А.Г. Диаграмма электрохимического равновесия стали Ст.3 в сильнокислых сульфатных растворах/А.Г. Тюрин, А. И. Бирюков//Вестник Казанского технологического университета. -Т. 15, № 16. -С. 74-77.
- Справочник по электрохимии/под ред. А.М. Сухотина. -Л.: Химия, 1981. -488 с.


