Особенности выполнения реверсивной артропластики плечевого сустава в условиях дефектов и дефицита костной массы суставной впадины лопатки
Автор: Кесян Г. А., Карапетян Г. С., Шуйский А. А., Уразгильдеев Р. З., Арсеньев И. Г., Кесян О. Г.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Травматология и ортопедия
Статья в выпуске: 3 т.17, 2021 года.
Бесплатный доступ
Цель: разработка и оценка эффективности тактики действий при реверсивной артропластике плечевого сустава в условиях дефектов и дефицита костной массы суставной впадины лопатки. Материал и методы. В отделении ортопедии взрослых ФГБУ «НМИЦ ТО им. Н. Н. Приорова» Минздрава России выполнялось реверсивное эндопротезирование плечевого сустава 6 пациентам с дефицитом костной массы суставной впадины лопатки, которым производилось замещение как краевых (4 пациента), так и обширных костных дефектов (2 пациента). Результаты. За период наблюдения оперированных пациентов в сроки от 6 до 24 месяцев были получены хорошие клинические, рентгенологические и функциональные результаты. Интраи послеоперационных осложнений не было. Заключение. Разработанная методика замещения дефектов суставной впадины лопатки при реверсивном эндопротезировании показал высокую эффективность.
Артропластика, реверсивное эндопротезирование, аутотрансплантат, остеоартроз, омартроз.
Короткий адрес: https://sciup.org/149138133
IDR: 149138133 | УДК: 616–001+616.7+617.3
Features of performing reverse shoulder arthroplasty in conditions of defects and deficiency of bone mass of glenoid cavity of scapula
Objective: development and evaluation of the effectiveness of the tactic of actions for reverse shoulder arthroplasty in conditions of defects and bone mass deficiency of the articular surface of the scapula. Material and Methоds. At the department of adult orthopedics n. a. N. N. Priorov National Research Medical Center Ministry of Health of the Russian Federation, 6 patients with glenoid bone mass deficiency underwent reverse shoulder arthroplasty, which was replaced by both marginal (4 patients) and extensive bone defects (2 patients). Results. During the follow-up period of the operated patients in the period from 6 to 24 months, good clinical, radiological and functional results were obtained. There were no intra- and postoperative complications. Conclusion. The developed method of replacement of glenoid defects in reverse arthroplasty showed high efficiency.
Текст научной статьи Особенности выполнения реверсивной артропластики плечевого сустава в условиях дефектов и дефицита костной массы суставной впадины лопатки
1 Введение. Методом оперативного лечения травм и заболеваний плечевого сустава, сопровождающихся выраженными изменениями анатомии суставных структур, является реверсивное эндопротезирование [1]. Учитывая такие положительные стороны реверсивной артропластики, как смещение центра ротации сустава, улучшение натяжения и тонуса дельтовидной мышцы, показания к проведению такой операции расширяются с течением времени [2].
На основании литературных данных известно, что в 38% случаев травматологи сталкиваются с дефицитом костной массы суставной впадины лопатки при выполнении реверсивного эндопротезирования плечевого сустава [3, 4]. Подобные дефекты суставной впадины лопатки составляют большую сложность для корректной установки метаглена и гленосферы из-за трудностей интраоперационной дифференцировки истинной и ложной плоскости суставной поверхности.
Согласно исследованиям, для таких случаев созданы специальные направляющие устройства, позволяющие устанавливать метаглен в правильном положении по отношению к шейке лопатки [5]. В данных случаях недопустима медиализация гленосфе-ры, кроме того, нежелательно проведение ножки метаглена и фиксирующих винтов через зону дефекта вне костной ткани. Эта ошибка может привести к раннему вывиху эндопротеза. Возможно также нарушение компрессии метаглена к лопатке, нестабильность винтов и миграция лопаточного компонента.
Известны способы компенсации дефицита костной ткани суставной впадины лопатки при помощи костной аутопластики из резецированной головки плеча или аллопластики, использования аугментов и модификации лопаточных компонентов эндопротеза [6]. Многие авторы указывают на то, что наиболее оптимальным костнопластическим материалом являются губчатые аутотрансплантаты, так как губчатая кость обладает высоким потенциалом для сращения и, соответственно, более выраженными остеогенными, остеоиндуктивными и остеокондуктивными свойствами [7, 8]. Учитывая отсутствие общепризнанного четкого алгоритма действий при данных сложных случаях, проблема реверсивного эндопротезирования плечевого сустава при дефектах суставной впадины лопатки является актуальной.
Цель — разработка и оценка эффективности тактики действий при реверсивной артропластике плечевого сустава в условиях дефектов и дефицита костной массы суставной впадины лопатки.
Материал и методы. В отделении ортопедии взрослых ФГБУ «НМИЦ ТО им. Н. Н. Приорова» Минздрава России производилась реверсивная артропластика плечевого сустава 6 пациентам с дефицитом костной массы суставной впадины лопатки, которым для установки метаглена с корректным углом наклона и созданием необходимого уровня латерализации гленосферы требовалось восполнение как краевых (4 пациента), так и обширных костных дефектов (2 пациента). Критериями включения пациентов в исследование были следующие: возраст от 18 и более лет; наличие у пациентов заболеваний, травм плечевого сустава и их последствий с дефектами сустав-
ной впадины лопатки, по общепринятым показаниям нуждающихся в реверсивном эндопротезировании. Критерии исключения пациентов из исследования: гнойно-воспалительные процессы в области плечевого сустава; патологический характер переломов и новообразования плечевого сустава; соматическая патология в стадии обострения и декомпенсации.
В рамках предоперационного обследования и подготовки выполнялись клиническое, рентгенологическое, инструментальное обследования пациента. Оценивался болевой синдром, объем движений в суставе, функциональное состояние дельтовидной мышцы. Проводились рентгенография пораженного сустава, компьютерная томография плечевого сустава с визуализацией суставной впадины и шейки лопатки и трехмерным моделированием. Именно на основании компьютерной томографии производилась оценка объема предполагаемой реконструкции суставной впадины лопатки, которая могла быть в нескольких вариантах.
При краевых дефектах суставной впадины лопатки без медиализации всей суставной поверхности нами производилась их костная аутопластика, фиксация трансплантата с последующим эндопротезированием. Пластика краевых дефектов суставной впадины лопатки выполняли следующим образом. После хирургического доступа к плечевому суставу производили скелетирование суставной впадины, удаляли рубцовые ткани, суставной хрящ. Проводили визуальную, мануальную и инструментальную оценки параметров дефекта и определяли величину потери костной массы суставной впадины. Далее выполняли разрез кожи и подкожно-жировой клетчатки в проекции гребня подвздошной кости. Тупо отсепаровывали мышечные волокна, визуализировали поверхность подвздошной кости, остеотомом производили забор костного аутотрансплантата необходимой величины. Выполняли моделирование трансплантата специальными инструментами. После воссоздания согласно характеру дефекта формы трансплантата осуществляли его имплантацию в зону дефекта. Выполняли остеосинтез трансплантата канюлированными металлическими или биорезорбируемы-ми винтами. Метаглен устанавливали с учетом угла наклона сформированной суставной впадины лопатки и биомеханических данных пациента (таких как наличие кифоза грудного отдела позвоночника и др.). После достижения компрессии и плотного прилегания поверхностей всех элементов системы «лопатка — трансплантат — метаглен» фиксировали метаглен винтами. Принципиальным являлось проведение винтов необходимой длины через всю костную массу шейки лопатки для обеспечения компрессии аутотрансплантата, его стабильности, перестройки и последующей консолидации с костной тканью лопатки. Даже после выполнения замещения небольших дефектов целесообразно выбирать ревизионные метаглены с удлиненной ножкой для их более стабильной фиксации. Основополагающим является попадание длинной ножки метаглена через всю костную массу шейки лопатки.
При наличии массивного дефицита костной массы суставной впадины лопатки и медиализации костной площадки для имплантации метаглена необходимо проведение аутопластики трансплантатом значительного размера. После произведенного хи- рургического доступа к плечевому суставу суставную впадину лопатки обрабатывали фрезой. Рассчитывали толщину трансплантата для необходимой лате-рализации суставной впадины лопатки. Выполняли разрез кожи и подкожно-жировой клетчатки в проекции гребня подвздошной кости. Тупо отсепаровыва-ли мышечные волокна до визуализирования поверхности подвздошной кости, остеотомом выполняли забор костного аутотрансплантата. Производили гемостаз, ушивание раны. Выполняли моделирование трансплантата, выполняли аутопластику концентрическим с ножкой метаглена значительного размера трансплантатом. Причем установку трансплантата производили по направляющей спице, по которой через трансплантат рассверливали канал ножки метаглена. Метаглен устанавливали через центр аутотрансплантата в лопатку с учетом угла наклона суставной впадины и биомеханических данных пациента. Добивались достижения компрессии и плотного прилегания поверхностей всех элементов системы «лопатка — трансплантат — метаглен» по отношению друг к другу на удлиненной ножке метаглена без формирования «зазоров» и пустых пространств. Далее осуществляли проведение фиксирующих метаглен винтов, причем принципиальным являлось использование винтов необходимой длины через костный трансплантат в лопатку для обеспечения его компрессии, стабильности, ремоделирования и последующей консолидации с костной тканью.
Результаты. Проведено наблюдение за пациентами, которым была выполнена костная аутопластика суставной впадины лопатки и последующее реверсивное эндопротезирование в сроки от 6 до 24 месяцев. Получены хорошие клинические, рентгенологические и функциональные результаты. Раны зажили первичным натяжением, послеоперационных гематом, гнойно-воспалительных осложнений не было. Основной критерий — отсутствие вывихов эндопротеза у всех 6 больных на протяжении всего срока наблюдения. По данным компьютерной томографии выявлена перестройка и остеоинтеграция трансплантатов, без признаков нестабильности метаглена с винтами и фиксирующих трансплантат имплантов. Комплекс реабилитационных мероприятий и сроки восстановления движений в оперированном суставе не отличались от таковых при обычном (без костной пластики) реверсивном эндопротезировании.
Клинический пример. Пациент С., 75 лет, обратился в отделение ортопедии взрослых ФГБУ «НМИЦ ТО им. Н. Н. Приорова» Минздрава России с жалобами на боли и нарушение функции правого плечевого сустава. Клинически — выраженное ограничение объема движений, болевой синдром, умеренная гипотрофия дельтовидной мышцы.
В анамнезе — огнестрельное ранение области правого плечевого сустава более 15 лет назад, неоднократные реконструктивные операции на плечевом суставе. По данным рентгенограмм и компьютерной томографии: посттравматический артроз правого плечевого сустава с выраженным «износом» и меди-ализацией суставной впадины лопатки, дефект проксимального отдела плечевой кости (рис. 1).
Выполнена реверсивная артропластика плечевого сустава с замещением значительного костного дефекта суставной впадины трансплантатом из гребня подвздошной кости по ранее описанной методике (рис. 2).
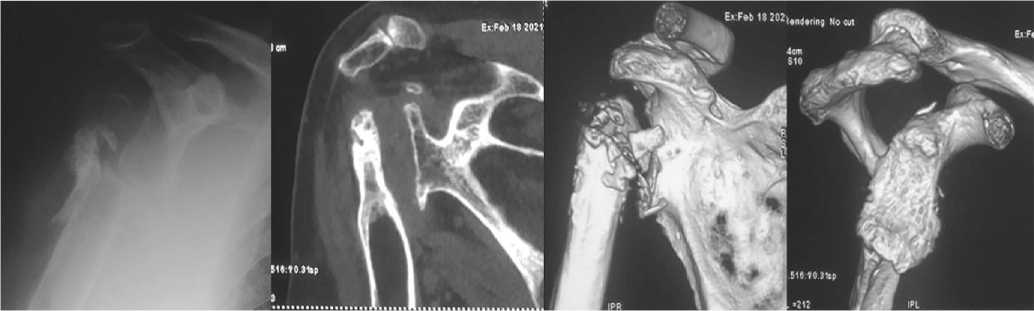
Рис. 1. Пациент С., 75 лет. Рентгенограмма и компьютерная томограмма правого плечевого сустава
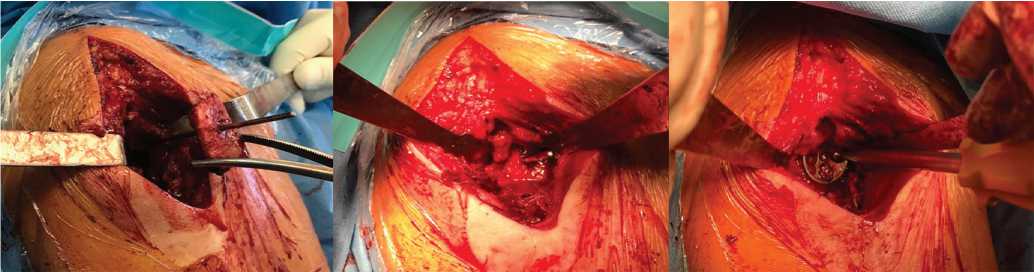
Рис. 2. Имплантация трансплантата по спице, установка метаглена
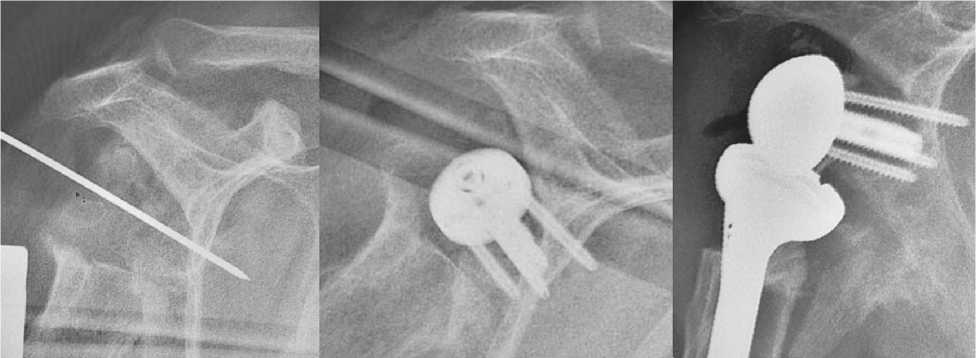
Рис. 3. Поэтапный интраоперационный рентген-контроль
Все этапы операции производятся под рентгенологическим контролем (рис. 3).
В послеоперационный период производилась съемная для реабилитации внешняя иммобилизация оперированной конечности ортезом. Всем пациентам проводился курс реабилитационного лечения, который включал механотерапию и электростимуляцию дельтовидной мышцы на ранних сроках после операции.
Обсуждение. При установке ревизионного лопаточного компонента реверсивного эндопротеза плечевого сустава на медиализированную суставную впадину лопатки происходит медиализация глено-сферы и изменение центра ротации сустава [3]. Это обусловливает развитие осложнений, связанных с нарушением центрации ножки протеза по отношению к гленосфере и отсутствием необходимого натяжения и тонуса дельтовидной мышцы [3]. Данные нарушения биомеханики при реверсивном эндопротезировании приводят к вывихам плечевого компонента [3].
Гребень крыла подвздошной кости в качестве донорской зоны забора трансплантата выбран нами с учетом того, что губчато-кортикальный трансплантат обладает необходимыми механическими свойствами, является оптимальным в плане репаративной регенерации и восстановления костной массы [3, 8]. При замещении значительных, медиализирующих суставную впадину лопатки, дефектов появляется возможность провести стабильную фиксацию губчато-кортикального трансплантата на ножке метаглена с достаточной компрессией при помощи винтов. В похожих условиях губчатый трансплантат из резецированной головки плечевой кости обладает более податливой структурой и не обеспечивает необходимую механическую прочность для латерализации суставной впадины лопатки [6]. Более того, часто на фоне гиповаскулярных и дегенеративно-дистрофических изменений головка плечевой кости вовсе отсутствует. При некоторых заболеваниях и посттравматических изменениях проксимального отдела плечевой кости не удается произвести забор костной ткани и из этой зоны тоже.
Решение проблемы дефицита костной массы суставной впадины лопатки при реконструктивных вмешательствах и эндопротезировании плечевого сустава, разработка тактики действий в зависимости от формы и объема дефекта имеет большую практическую значимость [6].
Заключение. По нашему опыту, в большинстве случаев причиной нестабильности метаглена и вы- вихов эндопротеза являлась некорректная установка лопаточного компонента с нарушением угла установки и офсета гленосферы. Учитывая высокую эффективность предлагаемой тактики действий, используемая методика компенсации дефицита костной ткани лопатки при реверсивном эндопротезировании плечевого сустава может быть рекомендована для внедрения в широкую клиническую практику.
Список литературы Особенности выполнения реверсивной артропластики плечевого сустава в условиях дефектов и дефицита костной массы суставной впадины лопатки
- Frankle M, Marberry S, Pupello D, eds. Reverse shoulder arthroplasty: biomechanics, clinical techniques, and current technologies. Cham-Switzerland: Springer International Publishing, 2016; 486 p.
- Kesyan GA, Urazgil’deev RZ, Karapetyan GS, et al. Reverse shoulder arthroplasty in difficult clinical cases. Bulletin of the Smolensk State Medical Academy 2019; (4): 111–20. Russian (Кесян Г. А., Уразгильдеев Р. З., Карапетян Г. С. и др. Реверсивное эндопротезирование плечевого сустава в сложных клинических случаях. Вестник Смоленской государственной медицинской академии 2019; (4): 111–20).
- Formaini N, Everding N, Levy J. The effect of glenoid bone loss on reverse shoulder arthroplasty baseplate fixation. J Shoulder Elbow Surg 2015; (6): 1–7.
- Kyriacou S, Falworth M. The management of glenoid bone loss in shoulder arthroplasty. J Shoulder Elbow Surg 2018; (6): 21–30.
- Gregori TMS. Shoulder arthroplasty device. Russian Federation patent RF N2569531. 2015 Nov 27. Russian (Грегори Т. М. С. Устройство эндопротезирования плечевого сустава. Патент РФ №2569531. Опубликовано 27.11.2015. Бюллетень № 33).
- Seidl AJ, Williams GR, Boileau P. Challenges in reverse shoulder arthroplasty: addressing glenoid bone loss. Orthopaedics 2016; 39 (1): 14–23.
- Anastasieva EA, Sadovoi MA, Voropaeva AA, Kirilova IA. The use of auto- and allografts foe the replacement of bone defects in resections of bone tumors (literature review). Traumatology and Orthopedics of Russia 2017; (3): 148–55. Russian (Анастасиева Е. А., Садовой М. А., Воропаева А. А., Кирилова И. А. Использование ауто- и аллотрансплантатов для замещения костных дефектов при резекциях опухолей костей (обзор литературы). Травматология и ортопедия России 2017; (3): 148–55).
- Berchenko GN, Kesyan GA, Urazgil’deev RZ, et al. Comparative experimental and morphological study of the influence of some calcium phosphate materials used in traumatological and orthopedic practice on the activation of reparative osteogenesis. Byulleten’ VSNC SO RAMN 2006; (4): 327–32. Russian (Берченко Г. Н., Кесян Г. А., Уразгильдеев Р. З. и др. Сравнительное экспериментально-морфологическое исследование влияния некоторых используемых в травматолого-ортопедической практике кальцийфосфатных материалов на активизацию репаративного остеогенеза. Бюллетень ВСНЦ СО РАМН 2006; (4): 327–32).


