Острейшая стадия инфаркта миокарда: влияние блокады IF на изолированное сердце крыс
Автор: Купцова А.М., Бугров Р.К., Зиятдинова Н.И., Зефиров Т.Л.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Физиология
Статья в выпуске: 3, 2022 года.
Бесплатный доступ
Плотность If в кардиомиоцитах изменяется не только с возрастом, но и при патофизиологической гипертрофии, поэтому исследования патологических состояний на моделях экспериментальных животных позволяют детально изучить роль If в патофизиологических процессах, происходящих в сердце после инфаркта миокарда (ИМ). Цель - изучить влияние блокады If-токов на изолированное сердце крыс с моделью острейшего инфаркта миокарда (ОИМ) и ложнооперированных (ЛО) крыс. Материалы и методы. ИМ воспроизводили путем лигирования левой коронарной артерии. Исследование проводилось на изолированном по Лангендорфу сердце (ADInstruments). В период ОИМ изучали хронотропию, инотропию и ее временные характеристики, кровоснабжение сердца крыс. Результаты. Выявлено, что исходные значения силы сокращения и коронарного потока были достоверно ниже в группе с экспериментальной моделью ОИМ, различий в ЧСС и временных характеристиках силы сокращения не обнаружено. Блокада If (ZD7288, 10-9 М, 10-5 М) уменьшает силу сокращения и коронарный поток изолированного сердца в обеих экспериментальных группах, изменения более выражены в группе ЛО крыс. Блокада If (10-9 M) в группе ЛО крыс приводит к тахикардии, а в группе ОИМ - к брадикардии. ZD7288 (10-5 М) снижает ЧСС в обеих исследуемых группах, но в группе с ОИМ брадикардия была более выраженной. Возможно, полученная динамика выраженности эффектов связана с изменением плотности If в патологическом миокарде. Таким образом, очевидно, что токи If не только участвуют в регуляции различных функций сердца после ИМ, но и меняют свою роль на разных стадиях экспериментального инфаркта миокарда.
Токи, активируемые при гиперполяризации, экспериментальный инфаркт миокарда, изолированное сердце, крыса
Короткий адрес: https://sciup.org/14125349
IDR: 14125349 | УДК: 612.17 | DOI: 10.34014/2227-1848-2022-3-106-119
Acute phase of myocardial infarction: effect of IF-current blockade on isolated rat heart
If-current density in cardiomyocytes changes not only with age, but also with pathophysiological hypertrophy. Thus, studies of pathological conditions in experimental animal models allow us to study If-current role in pathophysiological processes occurring in the heart after myocardial infarction (Ml). The objective of the study is to examine the effect of If-currents blockade on the isolated heart of rats with modelled acute myocardial infarction (AMI) and sham-operated (SO) rats. Materials and Methods. MI was reproduced by the left coronary artery ligation. The study was conducted on a Langendorff-isolated heart (ADInstruments). During AMI, the authors studied chronotropy, inotropy and its temporal characteristics, and blood supply of the rat heart. Results. It was found that the initial values of contractile force and coronary flow were significantly lower in the group with an experimental AMI model. There were no differences in heart rate and temporal characteristics of contractile force. If-current blockade (ZD7288, 10-9 M, 10-5 M) reduced the contractile force and coronary flow of the isolated heart in both experimental groups, the changes were more pronounced in the S O group. If-current blockade (10-9 M) in the S O group led to tachycardia, and in the AMI group - to bradycardia. ZD7288 (10-5 M) reduced heart rate in both groups, but in the AMI group, bradycardia was more pronounced. lt is possible that the obtained dynamics is associated with a change in the if-current density in the dyscrasic myocardium. Thus, it is obvious that If-currents are not only involved in the regulation of various MI heart functions, but their role changes at different stages of experimental myocardial infarction.
Текст научной статьи Острейшая стадия инфаркта миокарда: влияние блокады IF на изолированное сердце крыс
Введение. Ритмические циклы, такие как спонтанные и повторяющиеся паттерны возбуждения в возбудимых клетках, являются важными временными механизмами, которые регулируют различные биологические процессы. Неудивительно, что пейсмекерный ток, также известный как «забавный ток» (If) или ток, активируемый гиперполяризацией, был впервые описан в сердце [1], наиболее надежном ритмическом органе тела. Этот ток, позже также описанный в нервах, оказался опосредованным гиперполяризационно активируемыми ионными каналами, управляемыми циклическими нуклеотидами (HCN-каналы) [1]. HCN-каналы способствуют активности синусного узла и нейронов. В клетках синоатриального узла каналы отвечают за начальную фазу потенциала действия и, следовательно, регулируют скорость возбуждения. HCN-каналы модулируются внутриклеточными циклическими нуклеотидами, включая циклический аденозинмонофосфат (цАМФ). Активность каналов увеличивается в присутствии цАМФ и имеет решающее значение для ускорения частоты сердечных сокращений (ЧСС) при симпатической стимуляции [2]. В нервной системе HCN-каналы участвуют в возбудимости нейронов и сетевой активности [3]. Таким образом, с учетом многочисленных ролей HCN-каналов их дисфункция связана с целым рядом заболеваний [3], например с аритмиями, эпилепсией и невропатической болью, что делает их новыми мишенями для терапевтических исследований [3].
В экспериментальных исследованиях на лабораторных животных показано влияние неселективного блокатора If-токов ZD7288 на показатели работы сердечно-сосудистой системы. Выявлено, что блокада If-токов оказывала влияние как на ЧСС [4], так и на сократимость миокарда [5]. В изолированном сердце с хронической моделью инфаркта миокарда
(ИМ) положительный инотропный эффект возникает при аппликации ZD7288 в концентрациях 10-9 М и 10-7 М, а у здоровых животных положительный инотропный эффект наблюдается только при добавлении минимальной концентрации блокатора [6].
В последние годы в литературе появились данные, свидетельствующие о том, что дисфункциональные HCN-каналы, в частности HCN1 -канал, а также HCN2- и HCN4-каналы, могут играть патогенную роль при эпилепсии, что показано в экспериментальных исследованиях на животных моделях и у пациентов с эпилепсией. В центральной нервной системе изменение Ih-тока может предрасполагать к развитию нейродегенеративных заболеваний, таких как болезнь Паркинсона. Поскольку HCN-каналы широко экспрессируются в периферической нервной системе, их дисфункциональное поведение также может быть связано с патогенезом невропатической боли. С учетом фундаментальной роли HCN-каналов в регуляции спонтанной активности сердечных и нейрональных клеток изучение модуляции их функции в терапевтических целях может быть полезным для коррекции различных патологических состояний [7].
В литературе показано, что плотность If в кардиомиоцитах изменяется не только с возрастом, но и при патофизиологической гипертрофии [8], поэтому исследования патологических состояний на моделях экспериментальных животных позволяют детально изучить патофизиологические процессы, происходящие в миокарде при поражении коронарного русла.
В последние годы в связи с развитием общества, изменением окружающей среды и образа жизни человека увеличилась заболеваемость инфарктом миокарда. ИМ становится одной из основных причин смерти и инвалидности населения [9]. Как независимый фактор риска сердечно-сосудистых заболеваний увеличение ЧСС в покое вызывает смерть от острого инфаркта миокарда [10, 11]. На фоне ИМ происходит увеличение потребления кислорода миокардом, снижение перфузии коронарных артерий, что вызывает ишемию миокарда, рост количества некротических клеток миокарда, снижение сократимости миокарда.
В дальнейшем все это может вызывать ремоделирование миокарда и развитие сердечной недостаточности [12]. Таким образом, активный клинический контроль ЧСС в покое стал одним из наиболее важных методов лечения ИМ [12]. Хотя в-блокаторы используются для замедления ЧCC, такие эффекты, как уменьшение проводимости, снижение силы сокращения и артериального давления и др., а также различные противопоказания следует учитывать при клиническом применении этих препаратов [12].
Селективное снижение ЧСС путем ингибирования If-каналов является одним из современных методов лечения сердечно-сосудистых заболеваний. Так, недавно для клинического применения при лечении хронической сердечной недостаточности был одобрен блокатор HCN-каналов ивабрадин [3]. В инструкции по применению препарата, а также некоторыми исследователями указывается, что ивабрадин может специфически снижать синусовый ритм и замедлять ЧСС без дополнительных эффектов, таких как уменьшение силы сокращения и снижение артериального давления [2, 13]. Кроме того, процесс воздействия на ЧСС другими препаратами, такими как бета-блокаторы, более медленный, поскольку их дозировку необходимо увеличивать постепенно, в то время как ивабрадин позволяет быстрее и эффективнее осуществлять контроль ЧСС без ухудшения сердечной функции [14].
Ивабрадин связывается с каналом If синусового узла, подавляя ток If, уменьшая автономию синусового узла и замедляя ЧСС [1, 15]; замедление ЧСС может продлить диастолический период, увеличить снабжение миокарда кислородом и коронарную перфузию, увеличить сердечный выброс и улучшить сердечную функцию; ЧСС положительно коррелирует с объемом желудочков, а снижение ЧСС может снизить объемную нагрузку желудочков, уменьшить работу миокарда и потребление кислорода, а также улучшить толерантность к физической нагрузке [16, 17]. В то же время, несмотря на перечисленные преимущества, ивабрадин противопоказан для применения при остром инфаркте миокарда.
Цель исследования. Изучить влияние блокады If-токов на изолированное сердце крыс с моделью острейшего инфаркта миокарда и ложнооперированных крыс.
Материалы и методы. Эксперименты выполнены с соблюдением этических норм и правил обращения с лабораторными животными.
В работе использовали беспородных крыс обоего пола в возрасте 4 мес. Непосредственно перед операцией каждое животное взвешивалось. Средняя масса составила 200–250 г.
Крысы были разделены на две группы: 1-я (контроль, n=20) – ложнооперированные животные (ЛО); 2-я (n=20) – крысы с моделью острейшего инфаркта миокарда (ОИМ). Контрольная группа ложнооперированных животных была сформирована для исключения влияния факторов оперативного вмешательства на сердце на результаты исследования.
Методика воспроизведения инфаркта миокарда. Для воспроизведения инфаркта миокарда у экспериментальных животных использовалась классическая модель, разработанная Г. Селье.
Животных обезболивали с помощью эфирного наркоза, помещая под стеклянный колпак. Затем при помощи резиновых лент животное фиксировали на операционном столе. Во время подготовки к торакотомии могла потребоваться дополнительная анестезия. При необходимости над дыхательными путями крысы размещали пропитанный эфиром марлевый тампон. В ходе дальнейшего эксперимента наркоз не применяли.
Для улучшения видения операционного поля использовали ламповое освещение. С грудной клетки животного состригали шерсть, кожу обрабатывали дезинфицирующим раствором. На левой стороне грудной клетки крысы делали разрез кожи. С помощью рано-расширителей разводили в противоположные стороны грудные мышцы. Между V и VI ребрами тонкими ножницами производили поперечный разрез длиной около 15 мм. Теперь воздух поступал в грудную полость, дыхание становилось невозможным, но это не представляло серьезной угрозы для жизни экспериментального животного, поскольку наложение лигатуры занимало около 60–90 с. Манипулируя в операционной ране пинцетом, отводили в сторону легкое и приводили сердце в удобное положение. Затем путем активной компрессии грудной клетки с обеих сторон выводили сердце из грудной полости. Сердце удерживали за желудочки большим и указательным пальцами левой руки. Визуально находили переднюю ветвь левой коронарной артерии. С помощью атравматической иглы и нерассасывающейся нити (Prolene 6/0, Ethicon, США) накладывали лигатуру на 0,5–1 мм ниже ее выхода из-под ушка сердца и трехкратно перевязывали. О правильности наложения лигатуры на коронарную артерию свидетельствовали быстро развивающиеся тахикардия, аритмия и анемия миокарда в области лигатуры. Затем сердце возвращали в грудную полость. Мышцы сдвигали, на кожу накладывали сдавливающий пинцет, а пальцами рук производили надавливания на грудную клетку так, чтобы удалить скопившийся воздух и создать отрицательное давление в грудной полости. Затем кожу зашивали по-лигликолид-ко-лактидом 3/0 («Медтехника») и обрабатывали антисептическим препаратом аримидерм. Сразу после сдвигания мышц и кожи животное начинало самостоятельно дышать. Далее в течение 5 мин после ушивания кожи и начала восстановления дыхания ждали развития острейшей стадии инфаркта миокарда. При необходимости животное дополнительно анестезировали эфиром. Затем грудную клетку вскрывали и готовили препарат изолированного сердца.
Методика приготовления препарата изолированного сердца. Эксперименты ex vivo проводили на установке Лангендорфа (ADInst-ruments, Австралия). Изолированное сердце промывали в охлажденном до +4 °С растворе Кребса – Хензеляйте. Сердце за аорту лигировали на канюле и подавали оксигенированный (95 % О 2 и 5 % СО 2 ) раствор при постоянном гидростатическом давлении 75–80 мм рт. ст. и температуре 37 °С, которые поддерживались в ходе всего эксперимента. Сократительную активность изучали в изоволюмическом режиме с помощью датчика давления и латексного баллончика, заполненного водой и введенного в полость левого желудочка через разрез, сделанный между левым предсердием и левым желудочком. Конечно-диастолическое давление устанавливали на уровне 16–18 мм рт. ст.
Для диагностики развития ОИМ на изолированное сердце накладывали атравматические электроды и записывали электрограмму.
Исследуемые параметры работы изолированного сердца регистрировали и обрабатывали в программе LabChart Pro V8. В ходе эксперимента подсчитывали частоту сердечных сокращений (ЧСС, уд./мин), давление, развиваемое левым желудочком (ДРЛЖ, мм рт. ст.), максимальную скорость сокращения левого желудочка (dP/dt max , мм рт. ст./c), максимальную скорость расслабления левого желудочка (dP/dt min , мм рт. ст./c), длительность сокращения и расслабления левого желудочка (c), время цикла сокращения левого желудочка (c), коронарный поток (КП, мл/мин).
Статистическую обработку полученных результатов проводили в программе Microsoft Excel с использованием однофакторного дис- персионного анализа (ANOVA) и последующим применением апостериорных тестов (Т-тест) для связанных групп, а также использовали парный и непарный t-критерий Стьюдента. Данные представлены в виде среднего значения (М) и ошибки среднего (m). Достоверными считали значения при p<0,05.
Результаты и обсуждение. Согласно данным литературы, ОИМ обычно продолжается от нескольких часов (от 1 до 3 ч) до 1–3 сут и характеризуется развитием повреждения кардиомиоцитов в результате острого нарушения коронарного кровообращения. ЭКГ регистрирует подъем сегмента зубца ST выше изолинии с дугой, обращенной выпуклостью кверху, в виде монофазной кривой, когда сегмент зубца ST сливается с положительным зубцом T [18].
В нашем исследовании на электрограмме изолированного сердца зафиксирована элевация зубца ST выше изолинии (рис. 1).
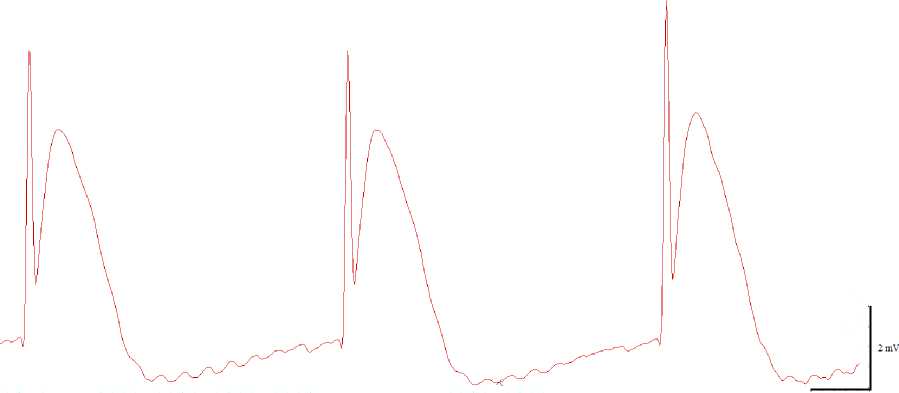
0.5 msec
Рис. 1. Нарушение сердечного ритма на электрограмме изолированного по Лангендорфу сердца с экспериментальной моделью острейшего инфаркта миокарда (оригинальная запись)
Fig. 1. Cardiac arrhythmia on the electrogram of a Langendorff-isolated heart with an experimental model of acute myocardial infarction (original record)
В группе ЛО животных исходное значение ДРЛЖ составило 89,4±6,4 мм рт. ст. В группе крыс с ОИМ исходное значение ДРЛЖ соста- вило 71±10,5 мм рт. ст. и было достоверно ниже, чем у ложнооперированных животных (p<0,05) (рис. 2).
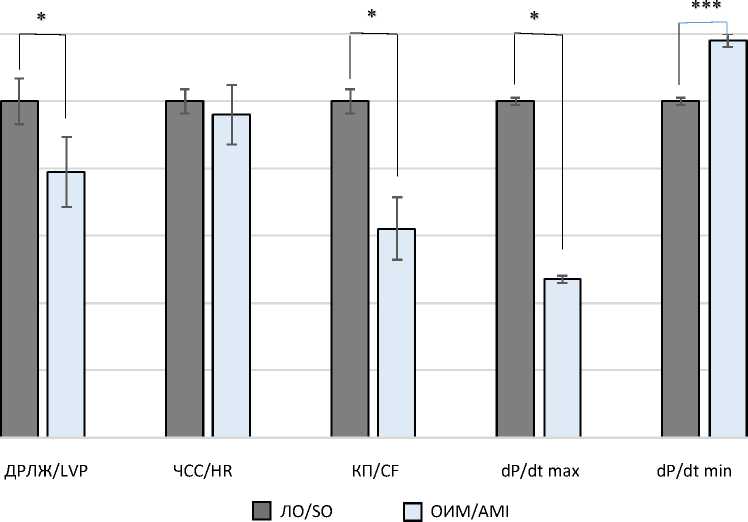
Рис. 2. Сравнение исходных значений ДРЛЖ, ЧСС, КП, dP/dt max и dP/dt min изолированного по Лангендорфу сердца ложнооперированных крыс и крыс с моделью острейшего инфаркта миокарда (различия достоверны по сравнению с группой ЛО: *– p<0,05, *** – p<0,001)
Fig. 2. Initial values of LVP, HR and CF, dP/dt max and dP/dt min of the Langendorff-isolated heart of sham-operated (SO) rats with a model of acute myocardial infarction (* – the differences are significant compared with the SO group (p<0.05);
*** – the differences are significant compared with the SO group (p<0.001))
Значения ЧСС у ложнооперированных крыс и у крыс с моделью ОИМ достоверно не различались: 233,4±3,5 и 224,8±8,8 уд./мин соответственно. Показатель КП изолированного сердца ЛО животных составил 11,7±3,7 мл/мин. В группе крыс с ОИМ он был достоверно ниже и составил 7,3±1,3 мл/мин (p<0,05) (рис. 2).
Максимальная скорость сокращения миокарда левого желудочка у ЛО составила 3691,3±349 мм рт. ст./с, в группе с ОИМ она была достоверно ниже – 1748,1±350 мм рт. ст./с (p<0,05) (рис. 2). Максимальная скорость расслабления миокарда левого желудочка у живот- ных с моделью ОИМ была достоверно выше, чем у ЛО крыс, на 18 % (p<0,001) (рис. 2).
Исходные значения показателя длительности сокращения левого желудочка в группе ЛО животных составляли 0,132±0,004 с, в группе с ОИМ – 0,133±0,007 с (рис. 3). Длительность расслабления миокарда левого желудочка в группе ЛО животных составляла 0,149±0,01 с, в группе ОИМ – 0,148±0,01 с (рис. 3). Длительность цикла сокращения миокарда левого желудочка в группе ЛО животных была равна 0,276±0,003 с, в группе ОИМ – 0,280±0,011 с (рис. 3). Достоверных различий между группами не обнаружено.
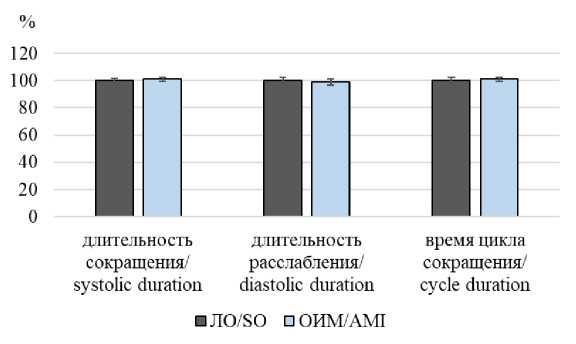
Рис. 3. Сравнение исходных значений времени сокращения, времени расслабления, времени цикла сокращения изолированного по Лангендорфу сердца ложнооперированных крыс и крыс с моделью острейшего инфаркта миокарда
Fig. 3. Initial values of systolic, diastolic, and cycle duration of the Langendorff-isolated heart of sham-operated rats with a model of acute myocardial infarction
Для изучения влияния блокады токов, активируемых при гиперполяризации, в перфузионный раствор добавляли антагонист ZD7288 в концентрациях 10-9 М и 10-5 М. Данные концентрации блокаторов выбраны на основе ранее проведенных исследований, выявивших влияние изучаемых токов на параметры изолированного сердца [19].
При добавлении в перфузионный раствор ZD7288 в концентрации 10-9 М ДРЛЖ в группе ЛО животных снижалось с 88,3±10,5
до 76,7±9,6 мм рт. ст. (p<0,01) к 10-й мин наблюдения. На заключительной минуте эксперимента ДРЛЖ составило 69,1±7,7 мм рт. ст. (p<0,01), т.е. уменьшилось на 22 %. В группе животных с экспериментальной моделью ОИМ ДРЛЖ при аппликации блокатора снижалось с 71±9,9 до 64,2±9 мм рт. ст. (p<0,01) на 5-й мин эксперимента. К 20-й мин экспериментальной записи значения ДРЛЖ снизились до 60,5±8,6 мм рт. ст. (p<0,05), т.е. на 15 % от исходных (рис. 4).
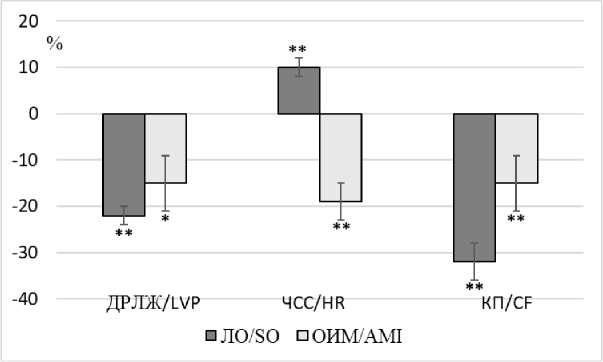
Рис. 4. Влияние ZD7288 (10-9 М) на показатели работы изолированного по Лангендорфу сердца (ДРЛЖ, ЧСС, КП) ложнооперированных крыс и крыс после моделирования ОИМ (ось ординат – показатели работы изолированного сердца, ось абсцисс – изменения по сравнению с исходными значениями (в %): * – р<0,05, ** – р<0,01)
Fig. 4. Effect of ZD7288 (10-9 M) on the Langendorff-isolated heart values (LVP, HR, CF) of sham-operated rats and rats after AMI simulation (Y-axis shows the isolated heart values; X-axis shows the changes compared with the baseline values (%): *p<0.05, **p<0.01)
Показатель dP/dt max в группе ЛО животных до добавления ZD7288 в перфузионный раствор составлял 3921,2±428 мм рт. ст./с, а после аппликации уменьшился до 3640,8±381,7 мм рт. ст./с (p<0.05) на 10-й мин наблюдения. К 20-й мин перфузии изолированного сердца данный показатель уменьшился до 3324,2±264,7 мм рт. ст./с (p<0,01) – на 15 %. При добавлении в перфузионный раствор блокатора If в группе ОИМ значения dP/dt max увеличились с 1870,1±402,4 до 2111,1±457,2 мм рт. ст./с (p<0,05) к 10-й мин эксперимента. На заключительной минуте наблюдения значения dP/dt max левого желудочка увеличились до 2186,9±412,3 мм рт. ст./с (p<0,01) – на 17 %.
Аппликация в перфузионный раствор ZD7288 увеличивала dP/dt min в группе ЛО животных на 16 % (p<0,01) от исходного. В экспериментальной группе с ОИМ данный показатель увеличивался на 15 % (p<0,05) от исходного.
Длительность сокращения миокарда левого желудочка у ЛО животных после аппликации ZD7288 уменьшилась на 6 %: с 0,127±0,005 до 0,120±0,004 с (p<0,01) к 5-й мин эксперимента. Далее длительность сокращения уменьшилась до 0,112±0,008 с (p<0,05). Снижение составило 12 %. В группе с моделью ОИМ изучаемый показатель снизился на 8 %: с 0,129±0,005 до 0,118±0,006 с (p<0,01) к заключительной минуте эксперимента (рис. 5).
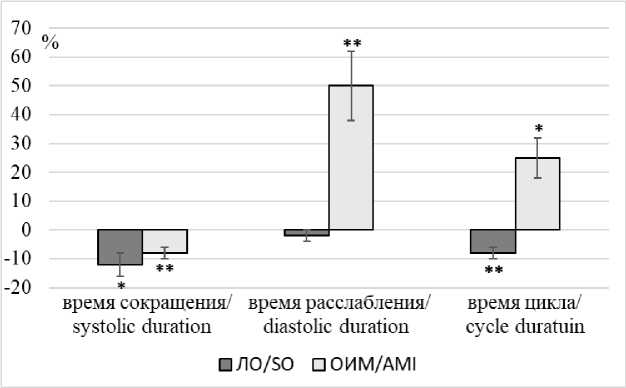
Рис. 5. Влияние ZD7288 (10-9 М) на временные характеристики сокращения изолированного по Лангендорфу сердца ложнооперированных крыс и крыс после моделирования ОИМ (ось ординат – показатели работы изолированного сердца, ось абсцисс – изменения по сравнению с исходными значениями (в %): * – р<0,05, ** – р<0,01)
Fig. 5. Effect of ZD7288 (10-9 M) on the temporal characteristics of contraction of the Langendorff-isolated heart in sham-operated rats and rats after AMI simulation (Y-axis shows the isolated heart values;
X-axis shows the changes compared with the baseline values (%): *p<0.05, **p<0.01)
Длительность расслабления миокарда левого желудочка при аппликации в перфузионный раствор блокатора If в группе ЛО животных уменьшилась с 0,131±0,006 до 0,124±0,003 с (p<0,05) на 5-й мин наблюдения. Далее показатель вернулся к исходному значению и не изменялся до конца эксперимента. В группе с моделью ОИМ длительность расслабления миокарда левого желудочка увеличивалась с 0,148±0,010 до 0,205±0,028 с (p<0,05) на
15-й мин эксперимента. На 20-й мин наблюдения длительность расслабления миокарда левого желудочка возросла до 0,222±0,025 с (p<0,01), увеличение составило 50 % (рис. 5).
Время цикла сокращения левого желудочка изолированного сердца ЛО животных при блокаде If уменьшалось с 0,251±0,004 до 0,231±0,008 с (p<0,01) к 20-й мин эксперимента, уменьшение составило 8 %. В группе с моделью ОИМ время цикла сокращения после блокады If увеличилось на 25 %: с 0,280±0,011 до 0,349±0,031 с (p<0,05) (рис. 5).
При добавлении в перфузионный раствор блокатора токов, активируемых при гиперполяризации, в концентрации 10-5 М ДРЛЖ в группе ЛО уменьшилось на 30 % от исходных значений: с 92,2±3,4 до 82,8±2,5 мм рт. ст. (p<0,01) к 10-й мин эксперимента. На заключительной минуте наблюдения ДРЛЖ уменьшилось до 64,5±5,7 мм рт. ст. (p<0,01). В экспериментальной группе с моделью ОИМ ДРЛЖ уменьшилось на 25 %: с 65±7,2 до 49,4±5,5 мм рт. ст. (p<0,05) на 15-й мин наблюдения. К заключительной минуте эксперимента ДРЛЖ уменьшилось до 48,7±5,4 мм рт. ст. (p<0,05) (рис. 6).
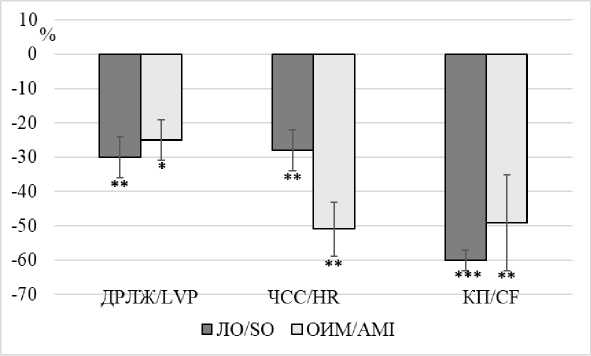
Рис. 6. Влияние ZD7288 (10-5 М) на показатели работы изолированного по Лангендорфу сердца ложнооперированных крыс и крыс после моделирования ОИМ (ось ординат - показатели работы изолированного сердца, ось абсцисс - изменения по сравнению с исходными значениями (в %): * - р<0,05, ** - р<0,01, *** - р<0,001)
Fig. 6. Effect of ZD7288 (10-5 M) on the Langendorff-isolated heart values (LVP, HR, CF) of sham-operated rats and rats after AMI simulation (Y-axis shows the isolated heart values; X-axis shows the changes compared with the baseline values (%): *p<0.05, **p<0.01, ***p<0.001)
ЧСС изолированного сердца ЛО животных после добавления блокатора увеличивалась на 10 %. С 1-й мин наблюдения ЧСС выросла с 241,9±2,6 до 260±2,1 уд./мин (p<0,01). Тахикардия наблюдалась до заключительной 20-й мин эксперимента, когда ЧСС составила 265,1±7,6 уд./мин (p<0,01). Блокада If в группе с ОИМ снижала ЧСС с 224,8±8,3 до 204,1±15,4 уд./мин (p<0,05) к 10-й мин. Брадикардия сохранялась до 20-й мин эксперимента, когда ЧСС снизилась до 182,7±13,2 уд./мин (p<0,01). Снижение составило 19 % (рис. 6).
Показатель КП изолированного сердца в группе ЛО животных уменьшался с 12,8±1,3 до 10,8±1,2 мл/мин (p<0,01) на 5-й мин. Снижение КП наблюдалось до окончания эксперимента и составляло к 20-й мин 8,7±1,1 мл/мин (p<0,01), т.е. показатель уменьшился на 32 %. В экспериментальной группе ОИМ КП уменьшился на 15 %: с 7,3±1,3 до 6,7±1,3 мл/мин (p<0,01) к
5-й мин наблюдения. К 20-й мин эксперимента значение КП составило 6,1±1,4 мл/мин (p<0,01) (рис. 6).
Добавление в перфузионный раствор блокатора ZD7288 (10-5 М) снижало dP/dt max в группе ЛО животных с 3270,7±274,8 до 2968,9±240,6 мм рт. ст./с (p<0,05) к 15-й мин наблюдения. На последней минуте эксперимента dP/dt max снизилась до 2678,5±247,6 мм рт. ст./с (p<0,01), т.е. на 18 %. В группе животных с моделью ОИМ dP/dt max увеличилась на 3 % на 1-й мин эксперимента: с 2309,9±404,1 до 2374,9±412,4 мм рт. ст./с (p<0,01). Далее наблюдали снижение изучаемого показателя до 1622,3±336,3 мм рт. ст./с (p<0,05) на последней 20-й мин эксперимента. Снижение dP/dt max составило 30 % от исходных значений.
После аппликации в перфузионный раствор блокатора If в группе ЛО животных dP/dtmin увеличилась на 25 % (p<0,01) от ис- ходного значения. В экспериментальной группе с моделью ОИМ увеличение dP/dtmin составило 31 % (p<0,05).
Аппликация ZD7288 в перфузионный раствор вызывала брадикардию в обеих изучаемых группах. В группе ЛО животных ЧСС уменьшилась с 216,7±10,7 до 167,3±25,6 уд./мин (p<0,05) к 10-й мин эксперимента, а затем до 157,2±21,1 уд./мин (p<0,01) на 20-й мин. Снижение ЧСС составило 28 % от исходного уровня. В группе животных с моделью ОИМ блокада If уменьшила ЧСС с 208,7±10,9 до 140,3±14,2 уд./мин (p<0,01) к 10-й мин эксперимента. К 20-й мин ЧСС продолжала снижаться до 102,9±8,6 уд./мин (p<0,01). Разница с исходными значениями составила 51 % (рис. 6).
Блокатор токов, активируемых при гиперполяризации, снижал КП изолированного сердца в экспериментальных группах. КП в группе ЛО животных уменьшался с 10±0,3 до 8,7±0,4 мл/мин (p<0,001) к 5-й мин наблюдения. К 20-й мин КП уменьшился до 4±0,2 мл/мин (p<0,001). Снижение КП составило 60 % от исходного уровня. В экспериментальной группе с моделью ОИМ КП уменьшился с 7,2±0,7 до 4,3±0,6 мл/мин (p<0,01) к 5-й мин наблюдения. Затем к 20-й мин КП уменьшился до
3,7±0,6 мл/мин (p<0,01). Снижения КП составило 49 % (рис. 6).
Блокада If вызывала снижение длительности сокращения миокарда левого желудочка в группе ЛО животных с 0,140±0,008 до 0,133±0,006 с (p<0,05) к 5-й мин эксперимента. К 20-й мин длительность сокращения уменьшилась до 0,117±0,004 с (p<0,05) (рис. 7). Уменьшение длительности сокращения составило 17 %. В группе с моделью ОИМ изучаемый показатель увеличился незначительно - на 5 %: с 0,134±0,011 до 0,142±0,006 с на 5-й мин. К заключительной (20-й мин) эксперимента длительность сокращения миокарда левого желудочка составила 0,141±0,003 с (рис. 7).
Длительность расслабления миокарда левого желудочка при аппликации в перфузионный раствор блокатора If в группе ЛО животных увеличивалась на 69 %. Изучаемый показатель вырос с 0,183±0,030 до 0,203±0,031 с (p<0,01) к 5-й мин наблюдения. Затем продолжал увеличиваться и к 20-й мин достигал 0,309±0,044 с (p<0,01). В группе с моделью ОИМ длительность расслабления миокарда левого желудочка увеличивалась на 170 %: с 0,180±0,028 до 0,424±0,077 с (p<0,05) к 15-й мин и до 0,485±0,075 с (p<0,05) на 20-й мин (рис. 7).
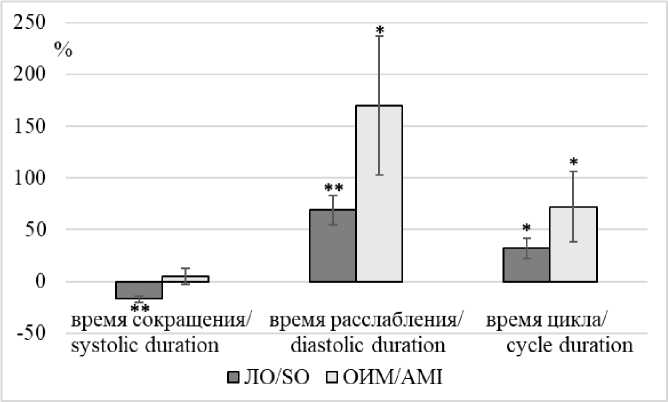
Рис. 7. Влияние ZD7288 (10-5 М) на временные характеристики сокращения изолированного по Лангендорфу сердца ложнооперированных крыс и крыс после моделирования ОИМ (ось ординат - показатели работы изолированного сердца, ось абсцисс - изменения по сравнению с исходными значениями (в %):* - р<0,05, ** - р<0,01)
Fig. 7. Effect of ZD7288 (10 - 5 M) on the temporal characteristics of contraction of the Langendorff-isolated heart of sham-operated rats and rats after AMI simulation (Y-axis shows the isolated heart values;
X-axis shows the changes compared with the baseline values (%): *p<0.05, **p<0.01)
Время цикла сокращения левого желудочка изолированного сердца ЛО животных при блокаде If увеличилось с 0,323±0,037 до 0,424±0,067 с (p<0,05) к 10-й мин наблюдения. Далее время цикла сокращения продолжало расти до 0,427±0,047 с (p<0.05) к заключительной 20-й мин эксперимента. Увеличение составило 32 %. В группе с моделью ОИМ время цикла сокращения после блокады If выросло на 72 %: с 0,324±0,036 до 0,557±0,068 с (p<0,05) к 20-й мин наблюдения (рис. 7).
Заключение. Проведенное исследование выявило, что исходные значения ДРЛЖ, dP/dt max , КП достоверно ниже в группе с экспериментальной моделью ОИМ, различий в ЧСС и временных характеристиках силы сокращения не обнаружено. Возможно, в первые минуты коронарной окклюзии происходит резкое угнетение сократительной функции сердечной мышцы из-за кислородного голодания, нарушения кровоснабжения, влияющего на энергетические ресурсы, чувствительность сердечной мышцы к ионам Ca2+, изменение скорости образования актомиозиновых мостиков и скорости расслабления миоцитов [20]. Однако, по-видимому, перечисленные изменения еще не отражаются на временных показателях сокращения миокарда.
Селективная блокада If (ZD7288, 10-9 М, 10-5 М) уменьшает ДРЛЖ и КП изолированного сердца в обеих экспериментальных группах. Однако в группе ЛО животных уменьшение ДРЛЖ и КП более выраженно по сравнению с группой крыс с моделью ОИМ. В проведенных ранее исследованиях на стадии хронического ИМ блокада If (10-9 М) вызывала положительный инотропный эффект, а максимальная концентрация If уменьшала силу сокращения [6]. На основании полученных дан- ных в экспериментальной модели ИМ у крыс можно сделать вывод, что роль If меняется: он ингибирует давление, развиваемое левым желудочком на начальной стадии ишемии, и усиливает силу сокращения в адаптационный период хронического ИМ. Аппликация ZD7288 оказывает разнонаправленное влияние на ЧСС изолированного сердца в исследуемых группах. Блокада If (10-9 M) в группе ЛО крыс приводит к тахикардии, а в группе ОИМ вызывает брадикардию. ZD7288 в концентрации 10-5 М урежает ЧСС в обеих исследуемых группах, но в группе крыс с ОИМ наблюдается более выраженная брадикардия. Аппликация блокатора (10-9 М, 10-5 М) в обеих исследуемых группах уменьшает время сокращения миокарда. В группе ЛО крыс изменение данного показателя более выражено, чем в группе с ОИМ. Время расслабления после блокады If (10-9 М) в группе ЛО животных не изменялось, а в группе с ОИМ увеличивалось. Аппликация ZD7288 в концентрации 10-5 М увеличивала время расслабления в обеих исследуемых группах, но в группе с ОИМ эффект был более выраженным. Возможно, полученная динамика выраженности эффектов связана с изменением плотности If в патологическом миокарде. Инверсия полученных эффектов может быть связана с участием данных токов в фазе реполяризации потенциала действия в рабочих кардиомиоцитах [21]. Таким образом, очевидно, что токи If не только участвуют в регуляции различных функций сердца после ИМ, но и меняют свою роль на разных стадиях экспериментального инфаркта миокарда.
В дальнейшем необходимо детальное исследование роли If в миокарде с различными патологиями, в т.ч. на разных стадиях развития инфаркта миокарда.
Работа выполнена за счет средств Программы стратегического академического лидерства Казанского (Приволжского) федерального университета (Приоритет-2030).
Список литературы Острейшая стадия инфаркта миокарда: влияние блокады IF на изолированное сердце крыс
- Shi S., WuX. Clinical research progress of ivabradine in cardiovascular disease. Chinese Circulation Journal. 2015; 30: 613-616.
- DiFrancesco D. Funny channels in the control of cardiac rhythm and mode of action of selective blocker. Pharmacol. Res. 2006; 53: 399-406.
- Sartiani L., Mannaioni G., Masi A., Romanelli M.N., Cerbai E. The Hyperpolarization-Activated Cyclic Nucleotide-Gated Channels: from Biophysics to Pharmacology of a Unique Family of Ion Channels. Pharmacol. Rev. 2017; 69: 354-395. DOI: https://doi.org/10.1124/pr.117.014035.
- Zefirov T.L., Ziyatdinova N.I., Zefirov A.L. Autonomic control of cardiac function involves modulation of hyperpolarization activated channels in vitro. Russ. J. Physiol. 2003; 89 (2): 154-160.
- Zefirov T.L., Gibina A.E., Sergejeva A.M., Ziyatdinova N.I., Zefirov A.L. Age-Related Peculiarities of Contractile Activity of Rat Myocardium during Blockade of Hyperpolarization-Activated Currents. Bull. Exp. Biol. Med. 2007; 144 (3): 273-275.
- BugrovR.K., Kuptsova A.M., KhabibrakhmanovI.I., Ziyatdinova N.I., Zefirov T.L. Influence of If-current blockade on rat heart contractility with a model of myocardial infarction. Archivos Venezolanos de Farmacología y Terapéutica. 2020; 37 (7): 817-821.
- Rivolta I., Binda A., Masi A., DiFrancesco J.C. Cardiac and neuronal HCN channelopathies. Pflugers Arch. 2020; 472 (7): 931-951. DOI: 10.1007/s00424-020-02384-3.
- Cerbai E., Pino R., Sartiani L., Mugelli A. Influence of postnatal-development on If occurrence and properties in neonatal rat ventricular myocytes. Cardiovascular Research. 1999; 42: 416-423.
- BoatengS., Sanborn T. Acute myocardial infarction. Dis. Mon. 2013; 59: 83-96.
- Ide T., Ohtani K., Higo T. Ivabradine for the Treatment of Cardiovascular Diseases. Circ. J. 2019; 83: 252-260.
- Sharashova E., Wilsgaard T., Mathiesen E.B. Resting heart rate predicts incident myocardial infarction, atrial fibrillation, ischaemic stroke and death in the general population: the Troms0 Study. J. Epidemiol. Community Health. 2016; 70: 902-909.
- Wang B., ZhangX., Chen J., Chen S., Chen Q., Yang S., Wang Q. Effectiveness and safety of ivabradine in the treatment of acute myocardial infarction: a systematic review and meta-analysis. Ann. Palliat. Med. 2021; 10 (4): 4523-4531. DOI: 10.21037/apm-21-563.
- Swedberg K., Komajda M., Böhm M., Borer J.S., Ford I., Dubost-Brama A., Lerebours G., Tavazzi L. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomized placebo-controlled study. Lancet. 2010; 376: 875-885.
- Fang Y., Debunne M., Vercauteren M., Brakenhielm E., Richard V., Lallemand F., Henry J-P., Mulder P., Thuillez C. Heart rate reduction induced by the if current inhibitor ivabradine improves diastolic function and attenuates cardiac tissue hypoxia. J. Cardiovasc. Pharmacol. 2012; 59: 260-267.
- Li C., Jiang D. Study and progress of ivabradine in cardiovascular diseases. Advances in Cardiovascular Diseases. 2019; 40: 143-145.
- Ramirez-Carracedo R., Tesoro L., Hernandez I., Diez-Mata J., Botana L., Saura M., Sanmartin M., Za-morano J.L., Zaragoza C. Ivabradine-stimulated microvesicle release induces cardiac protection against acute myocardial infarction. Int. J. Mol. Sci. 2020; 21: 6566.
- Brown H., Dfirancesco D., Noble S. How does adrenaline accelerate the heart? Nature. 1979; 280: 235-236.
- Nikulina N.A., Dotsenko E.A., Nerovnya A.M., SalivonchikD.P., Platoshkin E.N., Nikolaeva N.V., Tish-kov S.P. Experimental myocardial infarction in rats: features of modeling and course within the first 48 hours after coronary artery ligation. Problems of health and ecology. 2020; 2 (64): 91-96.
- Купцова А.М., Зиятдинова Н.И., Фасхутдинов Л.И., Биктемирова Р.Г., Зефиров Т.Л. Влияние HCN-каналов на работу изолированного сердца взрослых крыс. Ученые записки Казанского университета. Сер. Естественные науки. 2018; 160 (4): 568-578.
- Катруха И.А. Тропониновый комплекс сердца человека. Структура и функции. Успехи биол. химии. 2013; 53: 149-194.
- Abramochkin D.V., Faskhutdinov L.I., Filatova T.S., Ziyatdinova N.I. Changes in Electrical Activity of Working Myocardium Under Condition of I-f Current Inhibition. Bull. Exp. Biol. Med. 2015; 158 (5): 600-603.


