Острое клеточное отторжение трансплантата почки у пациента африканского происхождения: клиническое наблюдение
Автор: Хубутия М.Ш., Александрова В.О., Балкаров А.Г., Виноградов В.Е., Загородникова Н.В., Сторожев Р.В., Шмарина Н.В., Боровкова Н.В., Дмитриев И.В.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Трансплантация органов и тканей
Статья в выпуске: 2 т.13, 2023 года.
Бесплатный доступ
Этническое происхождение реципиента относится к известным факторам, влияющим на исходы трансплантации почки. В статье представлен первый опыт трансплантации почки пациенту африканского происхождения в НИИ СП им. Н.В. Склифосовского.Материал и методы. Аллогенная трансплантация почечного трансплантата от посмертного донора была выполнена пациенту африканского происхождения мужского пола 60 лет с хронической болезнью почек 5 стадии в исходе гипертонического нефроангиосклероза.Результаты. Ранний послеоперационный период осложнился развитием острого клеточного отторжения трансплантата 1a-b степени по Banff. Проведена противокризовая терапия с некоторым положительным эффектом, однако в отдалённом послеоперационном периоде была отмечена утрата функции почечного трансплантата, и пациент был возвращён на заместительную почечную терапию программным гемодиализом.Заключение. Пациенты африканского происхождения склонны к повышенному риску неблагоприятных исходов вследствие иммунологических причин и нуждаются в более тщательном иммунологическом подборе донорского органа, усиленной схеме иммуносупрессивной терапии и внимательном наблюдении после трансплантации.
Трансплантация почки, пациент африканского происхождения, острый криз отторжения, утрата трансплантата почки
Короткий адрес: https://sciup.org/143180030
IDR: 143180030 | УДК: 616.61-089.843.168:616.155.32 | DOI: 10.20340/vmi-rvz.2023.2.TX.1
Acute cell rejection of a kidney transplant in a patient of African origin: clinical observation
The origin of the recipient is one of the recipient-related factors that statistically significantly affects the outcomes of kidney transplantation, but this factor is not so relevant in our country. The article presents the first experience of kidney transplantation in a patient of African descent at the N.I. N.V. Sklifosovsky.Material and methods. Allogeneic renal graft transplantation from a post-mortem donor was performed in a 60-year-old African male patient with stage 5 chronic kidney disease as a result of hypertensive nephroangiosclerosis.Results. The early postoperative period was complicated by the development of acute cellular graft rejection grade 1a-b according to Banff. Anti-crisis therapy was performed with some positive effect, however, in the late postoperative period, a loss of renal graft function was noted, and the patient was returned to renal replacement therapy with program hemodialysis.Conclusion. Patients of African ancestry are at increased risk of adverse outcomes due to immunological causes and require more careful immunological selection of a donor organ, an enhanced immunosuppressive regimen, and close monitoring after transplantation.
Текст научной статьи Острое клеточное отторжение трансплантата почки у пациента африканского происхождения: клиническое наблюдение
ОРИГИНАЛЬНАЯ СТАТЬЯ ORIGINAL ARTICLE УДК 616.61-089.843.168:616.155.32
Трансплантация почки является оптимальным методом заместительной почечной терапии для большинства пациентов. Это обусловлено значительным улучшением качества и продолжительности жизни по сравнению с пребыванием на диализе [1]. Происхождение реципиентов относится к реци-пиент-обусловленным факторам, статистически значимо влияющим на исходы трансплантации почки. Несмотря на появление новых иммуносупрессивных препаратов и совершенствование диагностики и лечения иммунологических осложнений, пациенты африканского происхождения по-прежнему представляют группу повышенного иммунологического риска [2, 3]. Так, у данной категории реципиентов статистически чаще отмечают развитие эпизодов острого и хронического отторжения, а также частоту утраты трансплантата почки [4, 5]. Численность населения африканского происхождения в России, по данным ряда авторов, варьирует от 40 000 до 70 000 человек, а ведущей причиной терминальной почечной недостаточности у таких пациентов является гипертонический нефроангиосклероз вследствие артериальной гипертензии [2]. В настоящий момент нет официальных данных по пациентам африканского происхождения в Российской Федерации, нуждающихся в заместительной почечной терапии и находящихся в листе ожидания на трансплантацию почки. Из более чем 2000 выполненных трансплантаций почек на базе ГБУЗ «НИИ скорой помощи им. Н.В. Склифосовского ДЗМ» в период с 2008 по 2022 г. только одна была выполнена пациенту африканского происхождения.
Материал и методы
Реципиент. Пациент Н., 1962 года рождения, с клиническим диагнозом: гипертоническая болезнь III стадии, степень 3, риск сердечно-сосудистых осложнений 4. Гипертонический нефроангиосклероз. Хроническая болезнь почек С5Д (заместительная почечная терапия программным гемодиализом с ноября 2020 г.). Нефрогенная суб-компенсированная анемия. Рак предстательной железы (морфологически – аденокарцинома), радикальная простатэктомия в 2021 г.
Анамнез заболевания. Из анамнеза известно, что в 2015 г. была впервые выявлена артериальная гипертензия, тогда же госпитализирован с гипертоническим кризом, отёком лёгких и двусторонней пневмонией. В стационаре проводили гипотензивную и диуретическую терапию. В дальнейшем находился под наблюдением кардиолога. С 2017 г. отметили появление протеинурии, постепенное нарастание уровня азотемии. В ноябре 2020 г. появилась одышка, слабость, некоррегируемия артериальная гипертензия, потеря веса до 10 кг. При госпитализации выявили гиперазотемию и по жизненным показаниями начали лечение программным гемодиализом. В январе
2021 г. имплантировали катетер Тенкхоффа и перевели пациента на перитонеальный диализ. В 2021 г. при обследовании диагностировали рак предстательной железы, провели радикальную простатэктомию, лучевую и химиотерапию не проводили. Отдалённый послеоперационный период осложнился развитием стриктуры уретры, хронической задержкой мочи. В марте 2021 г. в связи с развитием диализного перитонита и стойкого дефицита ультрафильтрации был переведён на лечение программным гемодиализом. 27.10.2021 г. пациент был поставлен в лист ожидания на аллотрансплантацию почки. Анти-HLA антитела до трансплантации по I, II классам – отрицательно, анти-MICA антитела – отрицательно. Типаж реципиента A*24, A*33; B*45; В*78, DRB1*03, DRB1*11.
Донор. Мужчина, возраст 60 лет, индекс массы тела 26,6 кг/м2. У пациента была констатирована смерть головного мозга в исходе острого нарушения мозгового кровообращения по геморрагическому типу. На момент эксплантации креатинин сыворотки крови 93 мкмоль/л, мочевина крови 4,2 ммоль/л. Типаж донора А*01, A*02; В*15, B*35; DRB1*11, DRB1*16.
Иммунологическая совместимость/несовместимость по антигенам системы HLA. Совместимость по антигенам I класса HLA – 0 антигенов, несовместимость – 4 антигена (100 %), совместимость по антигенам II класса HLA – 1 антиген (50 %), несовместимость – 1 антиген (50 %). Общая совместимость по антигенам – 1 антиген (16,7 %), общая несовместимость – 5 антигенов (83,3 %)
Операция. В связи с необратимостью основного заболевания и наличием совместимого почечного трансплантата 17.02.2022 г. выполнили аллогенную гетеротопическую трансплантацию почки от посмертного донора с установкой эпицистостомы.
Иммуносупрессивная терапия. Реципиент получал индукционную иммуносупрессивную терапию поликлональными антителами (антитимоцитарный глобулин, четыре введения, суммарная доза – 1,25 г). Трёхкомпонентная базисная иммуносупрессивная терапия включала такроли-мус пролонгированный, эверолимус и метилпреднизолон.
Особенности послеоперационного периода. Отметили первичную функцию трансплантата почки, немедленное восстановление водовыделительной функции, стабильное снижение показателей азотемии. На 4-е сутки уровень креатинина сыворотки крови составил 281 мкмоль/л, уровень мочевины крови – 15,3 ммоль/л. На 8-е сутки после трансплантации отметили нарастание показателей азотистых шлаков крови: креатинин сыворотки крови – 350 мкмоль/л, мочевина крови – 16,3 ммоль/л. При проведении ультразвукового исследования трансплантата было отмечено увеличение его размеров, признаки отёка паренхимы, резкое повышение индексов сосудистого сопротивления (Ri = 1,0).
Ситуация была расценена как острой – криз отторжения почечного аллотрансплантата (ПАТ). При оценке анти-HLA АТ отметили, что они находились в пределах референтных значений. Провели пульс-терапию глюкокортикостероидами (три введения, суммарная доза 1250 мг) – без эффекта. В связи с продолжающим нарастанием азотемии (креатинин сыворотки крови – 713 мкмоль/л, мочевина крови – 31 ммоль/л), с целью верификации диагноза на 15-е сутки после операции под ультразвуковым наведением выполнили пункционную биопсию ПАТ. Заключение гистологического исследования: острое клеточное отторжение трансплантата 1а-в. Провели противокризовую терапию поликлональными антилимфоцитарными антителами (человеческий иммуноглобулин лошадиный, 14 введений, суммарная доза – 5 г) с положительным эффектом: медленное стабильное снижение показателей креатинина сыворотки крови и мочевины крови: с 924 мкмоль/л и 31 ммоль/л на
18-е сутки после операции до 417 мкмоль/л и 18,6 ммоль/л на 32-е сутки после операции соответственно. В связи с отсутствием дальнейшего снижение показателей азотемии, на 42-е сутки после трансплантации выполнили повторную пункционную биопсию ПАТ. Результат гистологического исследования: острое клеточное отторжение 1а (плазмоклеточный вариант?), острый канальцевый некроз. В дальнейшем отметили снижение показателей азотемии, на 54-е сутки после трансплантации в стабильно-удовлетворительным состоянии пациент был переведён на амбулаторный этап лечения. На момент выписки уровень креатинина сыворотки крови составил 379 мкмоль/л, мочевины крови – 16 ммоль/л. Динамика креатинина сыворотки крови, мочевины крови, содержания анти-HLA антител, концентрации такролимуса и эверолимуса, а также содержания гемоглобина, лейкоцитов и тромбоцитов крови представлены на рисунке 1.
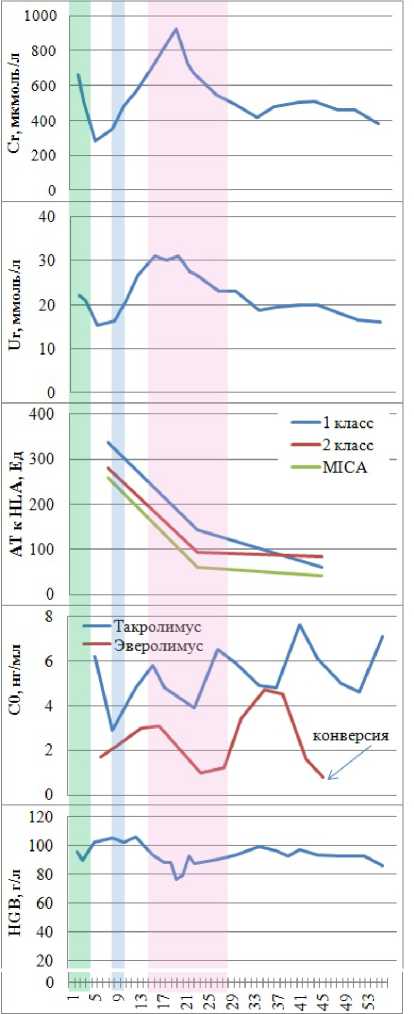
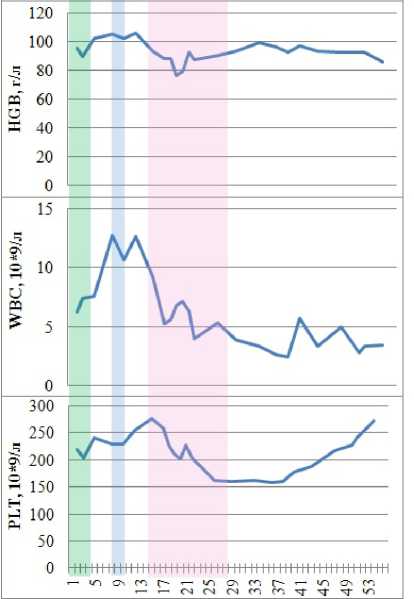
Рисунок 1. Диаграммы, отражающие динамику показателей креатинина сыворотки крови, мочевины крови, уровня анти-HLA антител, содержания гемоглобина, лейкоцитов и тромбоцитов крови: зелёным цветом отмечен период проведения индукционной иммуносупрессивной терапии поликлональными антителами; голубым цветом – период пульс-терапии кортикостероидами; розовым цветом – период противокризовой терапии поликлональными антителами (человеческий иммуноглобулин лошадиный); стрелкой отмечена дата конверсии с эверолимуса на препараты микофеноловой кислоты. По оси Х – дни от выполнения трансплантации
Figure 1. Diagrams showing the dynamics of blood serum creatinine, blood urea, anti-HLA antibody levels, hemoglobin, leukocytes and blood platelets: green color indicates the period of induction immunosuppressive therapy with polyclonal antibodies (human equine immunoglobulin); in blue – the period of pulse therapy with corticosteroids; in pink – the period of anti-crisis therapy with polyclonal antibodies (human equine immunoglobulin); the arrow indicates the date of conversion from evero-limus to mycophenolic acid preparations. On axis X - days from completion of transplantation
В дальнейшем пациент находился на амбулаторном наблюдении специалистов МГНЦ КГБ № 52. Через две недели после выписки пациента госпитализировали с острой задержкой мочи, острым пиелонефритом трансплантата. При поступлении уровень креатинина сыворотки крови – 723 мкмоль/л, мочевина крови – 27 ммоль/л. Проведенная антибактериальная терапия (цефепим+сульбактам, полимиксин В, тилорон) с положительным эффектом. При выписке креатинин сыворотки крови – 551 мкмоль/л, мочевина крови – 6 ммоль/л. В связи с сохраняющейся дисфункцией трансплантата и бесперспективностью в отношении восстановления функции почечного трансплантата в июне 2022 г. пациент был переведён на заместительную почечную терапию программным гемодиализом.
Заключение
Наше наблюдение показывает, что африканское происхождение, очевидно, повышает риск иммунологического конфликта после трансплантации и утрате функции трансплантата почки. Хотя африканское происхождение пациентов не является абсолютным противопоказанием к проведению трансплантации почки, однако такие пациенты нуждаются в более тщательном индивидуальном подборе донорского органа, в усиленной схеме иммуносупрессивной терапии и более тщательном мониторинге иммунологических показателей после трансплантации почки.
Список литературы Острое клеточное отторжение трансплантата почки у пациента африканского происхождения: клиническое наблюдение
- Knechtle SJ, Morris P. Kidney Transplantation - Principles and Practice: Expert Consult. 7th eds. Saunders; 2013.
- Arvelakis A, Lerner S, Wadhera V, Delaney V, Ames S, Benvenisty A, et al. Different outcomes after kidney transplantation between African Americans and Whites: A matter of income? A single-center study. Clin Transplant. 2019;33(11):e13725. PMID: 31585492.
- Schwartz JJ, Wilson S, Shi F, Elsouda D, Undre N, Kumar MSA. Prolonged-Release vs Immediate-Release Tacrolimus Capsules in Black vs White Kidney Transplant Patients: A Post Hoc Analysis of Phase III Data. Transplant Proc. 2018;50(10):3283-3295. PMID: 30577198.
- Feyssa E, Jones-Burton C, Ellison G, Philosophe B, Howell C. Racial/ethnic disparity in kidney transplantation outcomes: influence of donor and recipient characteristics. J Natl Med Assoc. 2009;101(2):111-115. PMID: 19378626.
- Wilkins LJ, Nyame YA, Gan V, Lin S, Greene DJ, Flechner SM et al. A Contemporary Analysis of Outcomes and Modifiable Risk Factors of Ethnic Disparities in Kidney Transplantation. J Natl Med Assoc. 2019;111(2):202-209. PMID: 30409716.


