Острый инфаркт миокарда, осложненный внезапной внегоспитальной сердечной смертью: клинический случай
Автор: Маланин В. А., Шевченко И. И., Иванов Н. М., Веселова В. В., Цурикова А. В.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические случаи
Статья в выпуске: 2 т.38, 2023 года.
Бесплатный доступ
Обоснование. Одним из серьезных осложнений острого инфаркта миокарда (ОИМ) является внегоспитальная сердечная смерть, которая связана с электрической нестабильностью миокарда, желудочковыми нарушениями ритма. Развитие осложнения в присутствии бригады скорой медицинской помощи (СМП) требует немедленного проведения реанимационных мероприятий, включающих базовые реанимационные мероприятия и проведение дефибрилляции.Цель и масштаб исследования. Представлен клинический случай пациентки с ОИМ с подъемом сегмента ST, осложненным рецидивирующей фибрилляцией желудочков, госпитализированной в больницу СМП с возможностью выполнения инвазивных вмешательств.Материал и методы исследования. Проведен анализ анамнестических, электрокардиографических (ЭКГ) данных пациентки, результатов коронароангиографии (КАГ) и стентирования коронарной артерии, эхокардиографического (ЭхоКГ) исследования, холтеровского мониторирования, лабораторных исследований.Результаты. Пациентка П., 81 год, доставлена в больницу СМП через 2 ч 15 мин от начала клиники. На догоспитальном этапе рецидивирующая фибрилляция желудочков, купированная повторными тремя дефибрилляциями. Не контактна, дважды приступы двигательного возбуждения. Консилиумом принято решение о немедленном проведении КАГ с возможным стентированием коронарных артерий. Бедренным доступом справа через 30 мин от госпитализации выполнена КАГ, выявлена полная окклюзия передней межжелудочковой артерии (ПМЖА). Выполнена проводниковая реканализация и стентирование ПМЖА с использованием стента с лекарственным покрытием. В палате интенсивной терапии продолжено капельное введение дофамина, неинвазивная вентиляция легких, введение гепарина, назначена двойная антитромбоцитарная терапия, аторвастатин, амиодарон. С 4-х сут к терапии добавлен бета-блокатор. Проводилась физическая и психологическая реабилитация. Выписана на 15-е сут в удовлетворительном состоянии.Заключение. Внегоспитальная сердечная смерть требует неотложных реанимационных мероприятий (в ряду которых особое место занимает дефибрилляция), а также немедленной госпитализации в кардиологический центр, имеющий возможность осуществления инвазивных вмешательств. Важное значение в лечении пациентов имеет ранняя реабилитация.
Острый инфаркт миокарда, внезапная сердечная смерть, коронароангиография, стентирование, ранняя реабилитация
Короткий адрес: https://sciup.org/149142841
IDR: 149142841 | УДК: 616.127-005.8-036.11-06-036.886 | DOI: 10.29001/2073-8552-2023-38-2-264-274
Acute myocardial infarction complicated by sudden out-of-hospital cardiac arrest: a clinical case
Justification. One of the serious complications of acute myocardial infarction (AMI) is out-of-hospital cardiac arrest, which is associated with electrical instability of the myocardium, ventricular arrhythmias. The development of a complication in the presence of an emergency medical team requires immediate resuscitation measures, including basic resuscitation measures and defibrillation.Aim: To present a clinical case of a patient with AMI with ST segment elevation complicated by recurrent ventricular fibrillation, hospitalized in an emergency hospital with the possibility of performing invasive interventions.Methodology and methods of research. The analysis of anamnesis, electrocardiographic data of the patient, the results of coronary angiography and stenting of the coronary artery, echocardiography examination, Holter monitoring, laboratory studies was carried out.Results. Patient P., female, 81 years old, was taken to the emergency hospital 2 hours and 15 minutes after the start of the clinic. At the prehospital stage, recurrent ventricular fibrillation, stopped by repeated three defibrillations. Non-contact, twice bouts of motor arousal. The council decided to conduct coronary angiography with possible stenting of the coronary arteries immediately. It was performed by femoral access on the right in 30 minutes after hospitalization. Complete occlusion of the anterior interventricular artery was revealed. Conductor recanalization and stenting of permanent residence was performed using a drug-coated stent. In the intensive care unit, drip administration of dopamine, noninvasive ventilation of the lungs, heparin administration were continued; double antiplatelet therapy, atorvastatin, amiodarone were prescribed. Since the fourth day, a beta-blocker has been added to therapy. Physical and psychological rehabilitation was carried out. She was discharged on the 15th day in a satisfactory condition.Conclusion. Out-of-hospital cardiac death requires urgent resuscitation measures, among which defibrillation occupies a special place, as well as immediate hospitalization to a cardiology center with the possibility of performing invasive interventions. Early rehabilitation plays an important role in the treatment of patients.
Текст научной статьи Острый инфаркт миокарда, осложненный внезапной внегоспитальной сердечной смертью: клинический случай
Justification. One of the serious complications of acute myocardial infarction (AMI) is out-of-hospital cardiac arrest, which is associated with electrical instability of the myocardium, ventricular arrhythmias. The development of a complication in the presence of an emergency medical team requires immediate resuscitation measures, including basic resuscitation measures and defibrillation.
Aim: To present a clinical case of a patient with AMI with ST segment elevation complicated by recurrent ventricular fibrillation, hospitalized in an emergency hospital with the possibility of performing invasive interventions.
Methodology and methods of research. The analysis of anamnesis, electrocardiographic data of the patient, the results of coronary angiography and stenting of the coronary artery, echocardiography examination, Holter monitoring, laboratory studies was carried out.
Results. Patient P., female, 81 years old, was taken to the emergency hospital 2 hours and 15 minutes after the start of the clinic. At the prehospital stage, recurrent ventricular fibrillation, stopped by repeated three defibrillations. Non-contact, twice bouts of motor arousal. The council decided to conduct coronary angiography with possible stenting of the coronary arteries immediately. It was performed by femoral access on the right in 30 minutes after hospitalization. Complete occlusion of the anterior interventricular artery was revealed. Conductor recanalization and stenting of permanent residence was performed using a drug-coated stent. In the intensive care unit, drip administration of dopamine, noninvasive ventilation of the lungs, heparin administration were continued; double antiplatelet therapy, atorvastatin, amiodarone were prescribed. Since the fourth day, a beta-blocker has been added to therapy. Physical and psychological rehabilitation was carried out. She was discharged on the 15th day in a satisfactory condition.
Conclusion. Out-of-hospital cardiac death requires urgent resuscitation measures, among which defibrillation occupies a special place, as well as immediate hospitalization to a cardiology center with the possibility of performing invasive interventions. Early rehabilitation plays an important role in the treatment of patients.
Актуальность
Острый инфаркт миокарда (ОИМ) остается актуальной проблемой неотложной кардиологии, что связано, с одной стороны, с необходимостью принимать решения в условиях выраженного временного дефицита, с другой, – с возможным развитием осложнений, которые значительно утяжеляют состояние и во многом определяют прогноз конкретного пациента [1, 2].
Одним из серьезных осложнений ОИМ является вне-госпитальная сердечная смерть, которая развивается в острейшем периоде и связана, по мнению исследователей, с электрической нестабильностью миокарда, приводящей чаще всего к желудочковым нарушениям ритма. Именно подобное течение ОИМ отличается очень высокой летальностью на догоспитальном этапе, протекая зачастую без свидетелей [3].
Развитие осложнения в присутствии бригады скорой медицинской помощи (СМП) требует немедленного проведения реанимационных мероприятий, включающих не только базовые реанимационные мероприятия, но и проведение при необходимости дефибрилляции [4]. В случае эффективных реанимационных мероприятий современные рекомендации считают предпочтительным вариантом немедленную доставку пациента в кардиологический центр, имеющий возможность проведения чрескожных коронарных вмешательств (ЧКВ) [5]. Представляется актуальным разбор клинического случая пациентки с ОИМ с подъемом сегмента ST, осложненным фибрилляцией желудочков, клинической смертью, эффективными реанимационными мероприятиями, госпитализированной в больницу СМП с возможностью выполнения инвазивных вмешательств.
Материал и методы
При подготовке статьи был использован анамнестический метод, данные объективного обследования, включавшие измерение артериального давления (АД), аускультацию сердца и легких с оценкой частоты сердечных сокращений и частоты дыхательных движений. Электрокардиографическое (ЭКГ) исследование было записано с использованием 12-канального электрокардиографа с автоматической интерпретацией и функцией телеметрического контроля КФС-01.001 «Кардиометр-МТ». Восстановление сердечного ритма проводилось при помощи дефибриллятора ДКИ-Н-11. Неинвазивная вентиляция легких осуществлялась аппаратом Philips Respironics Trilogy в режиме CPAP c давлением в дыхательных путях 10 см вод. ст. с помощью лицевой маски. Коронароангиография (КАГ) и стентирование коронарной артерии выполнено в экстренном порядке в отделении рентгеноперационных методов диагностики и лечения, оснащенном ангиографом Phillips Asurion 7М20. Эхокардиографическое (ЭхоКГ) исследование выполнено аппаратами VIVID iq в палате интенсивной терапии и Logic E – в отделении функциональной диагностики. Лабораторные исследования включали общий и биохимический анализ крови, оценку кислотно-щелочного состояния в динамике. Холтеровское мониторирование выполнено на системе «Кардиотехника» в течение 24 ч. При проведении физической реабилитации использовались ступени активности от Ia (строгий постельный режим) до IIIa (палатный режим с самообслуживанием) в зависимости от сроков давности инфаркта и состояния пациентки. При проведении психологической реабилитации применялось несколько методик: тест MiniCog для оценки кратковременной памяти и конструктивного праксиса, шкала нарушения сна, тест умственных способностей Ходкинсона для оценки ориентированности во времени, месте и собственной личности, памяти и общего уровня знаний, а также оценки внимания испытуемого. Для оценки вероятности развития тревоги и депрессии использовалась госпитальная шкала тревоги и депрессии (The Hospital Anxiety and Depression Scale, HADS).
Результаты и обсуждение
Пациентка П., 81 год, доставлена в приемное отделение больницы СМП по скорой помощи в 01 ч 55 мин с направительным диагнозом «Ишемическая болезнь сердца, острый инфаркт миокарда с подъемом ST, кардиогенный шок, фибрилляция желудочков, состояние после дефибрилляции». Со слов врача СМП, вызов принят в 00 ч 25 мин, бригада прибыла в 00 ч 35 мин, повод к вызову – «плохо с сердцем, задыхается». Ухудшение состояния накануне с 23 ч 45 мин, когда появились выраженные жгучие, давящие загрудинные боли с иррадиацией в левую руку и межлопаточную область. Скорую помощь вызвала соседка пациентки. При осмотре врачом СМП состояние тяжелое, кожные покровы влажные, бледные. Тоны сердца глухие, аритмичные. АД – 90/60 мм рт. ст., записана ЭКГ (рис. 1).
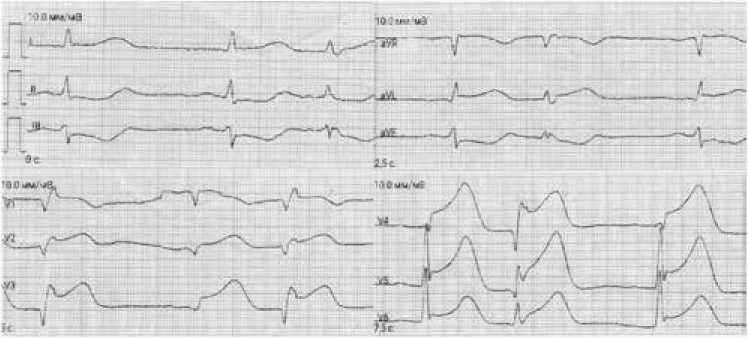
Рис. 1. Электрокардиограмма пациентки П.: синусовый ритм, частота сердечных сокращений – 75 уд/мин, наджелудочковая экстрасистолия, элевация сегмента ST в aVL, V1–V6, депрессия ST во II, III, aVF
Fig. 1. Electrocardiogram of patient P.: sinus rhythm, heart rate 75 beats per minute, supraventricular extrasystole, elevation of ST segment in aVL, V1–V6, depression ST in II, III, aVF
Пациентке установлен периферический катетер, с целью купирования болевого синдрома введен дробно раствор морфина гидрохлорида в дозе 1% – 1 мл в/в, затем нефракционированный гепарин 0,8 мл (4000 ЕД), дана двойная антитромбоцитарная терапия, включающая аспирин 250 мг, клопидогрель 75 мг. Пациентке предложена немедленная госпитализация в больницу СМП, имеющую возможность проведения ЧКВ. При перекладывании для транспортировки у пациентки внезапно возникло хриплое дыхание с последующим транзитор-ным патологическим сгибанием мышц верхних и нижних конечностей, затем остановка дыхательной и сердечной деятельности; пульс, АД не определялись, зрачки на свет не реагировали.
Констатирована клиническая смерть, начаты реанимационные мероприятия, закрытый массаж сердца в соотношении с дыханием 30 : 2, с частотой 100 компрессий в минуту, искусственная вентиляция легких мешком Амбу, введен раствор адреналина 0,1% – 1 мл в/в струй-но. На экране дефибриллятора после наложения элект- родов визуализировалась фибрилляция желудочков. После первого разряда дефибриллятора с энергией 200 Дж фибрилляция желудочков продолжалась (рис. 2а), вновь выполнена серия закрытого массажа сердца и искусственного дыхания, затем был произведен второй разряд с энергией 250 Дж, который также оказался неэффективным. Продолжен закрытый массаж сердца, введен амиодарон 300 мг в/в струйно. Только после третьего разряда дефибриллятора с энергией 250 Дж восстановлен устойчивый сердечный ритм (рис. 2б).
После эффективных реанимационных мероприятий пациентке начато в/в капельное введение дофамина 4% – 5 мл, растворенного в 200 мл 0,9% физиологического раствора со скоростью 20 капель в минуту, через 5 мин – со скоростью 15 капель в минуту. Кроме этого, к лечению добавлено в/в капельное введение амиодарона 300 мг на 200 мл 5% раствора глюкозы, ингаляция кислорода. Во время транспортировки пациентка была неконтактна, некритична, неадекватна, дважды возникали приступы двигательного возбуждения.
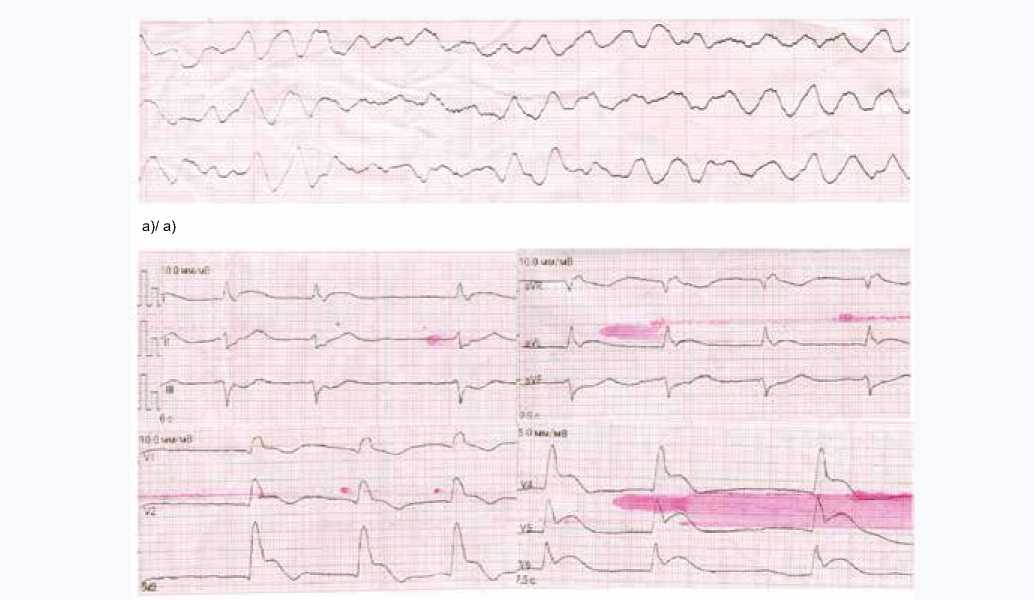
б)/ b)
Рис. 2. Электрокардиограмма пациентки П. во время и после реанимационных мероприятий: а) фрагмент крупноволновой фибрилляции желудочков, б) фибрилляция предсердий, частота сердечных сокращений – 108 уд/мин, элевация сегмента ST в aVL, V1-V6, депрессия ST во II, III, aVF, остро возникшая блокада правой ножки пучка Гиса
Fig. 2. Electrocardiogram of patient P. during and after resuscitation: a) fragment of large-wave ventricular fibrillation, b) atrial fibrillation, heart rate 75 beats per minute, elevation of the ST segment in aVL, V1-V6, depression ST in II, III, aVF, acute right bundle branch block
В противошоковой палате в приемном отделении в 02 ч 00 мин осмотрена совместно дежурными врачами: кардиореаниматологом, врачом эндоваскулярных методов диагностики и лечения, анестезиологом-реаниматологом, невропатологом. Больная жалоб активно не предъявляет, некритична, неадекватна, дезориентирована во времени и пространстве. За время осмотра – дважды двигательное возбуждение с гипертонусом и сгибани- ем конечностей. Дежурным невропатологом состояние расценено как острая постреанимационная энцефалопатия. Кожные покровы чистые, бледные. Тоны сердца глухие, аритмичные, АД – 65/40 мм рт. ст. на фоне инфузии дофамина, сатурация крови (SaO2) – 88%.
Консилиумом в составе дежурного кардиореаниматолога, дежурного врача эндоваскулярных методов диагностики и лечения, дежурного анестезиолога-реани- матолога, дежурного невропатолога принято решение о немедленном проведении КАГ с возможным стентированием коронарных артерий, после чего в сопровождении дежурного кардиореаниматолога в 02 ч 30 мин доставлена в рентгеноперационную.
В операционной продолжено капельное в/в введение дофамина со скоростью 15 мкг/кг/мин, неинвазивная вентиляция легких в режиме CPAP (Continuous Positive Airway Pressure) с помощью лицевой маски с давлением в дыхательных путях 12 см вод. ст., а также ЭКГ-мониторинг и контроль АД. Под местной анестезией бедренным доступом справа в 02 ч 52 мин выполнена КАГ, на серии снимков выявлена полная окклюзия передней межжелудочковой артерии (ПМЖА) на фоне гемодинамически незначимого атеросклероза остальных ветвей левой коронарной артерии (ЛКА) и правой коронарной артерии (ПКА). Отмечалось замедление пассажа контраста по коронарным артериям на фоне низкого АД (рис. 3а). Выполнена проводниковая реканализация и стентирование места окклюзии ПМЖА с использованием стента с лекарственным покрытием. В ПМЖА имплантирован стент «Biomatrix Flex», 2,75 × 18 мм. Конечный результат представлен на коронарограмме (рис. 3б).
В палату интенсивной терапии доставлена в 03 ч 25 мин в сопровождении дежурного кардиореаниматолога. Капельное введение дофамина продолжено со скоростью 15 мкг/кг/мин, продолжена неинвазивная вентиляция легких аппаратом Philips Respironics Trilogy в режиме CPAP c давлением в дыхательных путях 10 см вод. ст. с помощью лицевой маски. Сатурация поддерживалась на уровне 92%. Дополнительно назначено в/в капельное введение гепарина инфузоматом со скоростью 1000 ЕД/ч, назначена двойная антитромбоцитарная терапия (ацекардол – 100 мг и клопидогрель – 75 мг), аторвастатин в дозе 40 мг. Кроме того, пациентка получала в течение трех первых суток амиодарон 600 мг в/в капельно и 600 мг в таблетированной форме, затем 600 мг в таблетированной форме с последующей отменой в палате реабилитации.
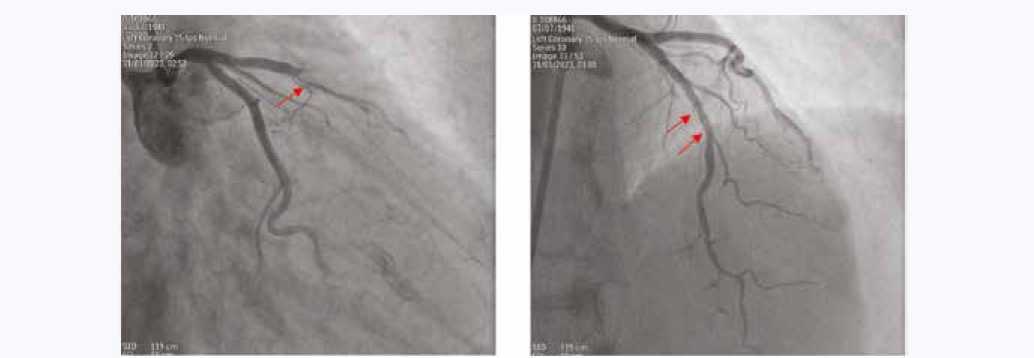
а)/ a) б)/ b)
Рис. 3. а) ангиограмма левой коронарной артерии в правой каудальной проекции, окклюзия передней межжелудочковой артерии (стрелка); б) ангиограмма левой коронарной артерии после имплантации стента в передней межжелудочковой артерии, заполнение дистального русла хорошее и соответствует TIMI III (стрелки)
Fig. 3. a) angiogram of the left coronary artery in the right caudal projection, occlusion of the left anterior descending artery (arrow); b) angiogram of the left coronary artery after implantation of the stent into the left anterior descending artery, filling of the distal bed is good and corresponds to TIMI III (arrows)
Выполнена рентгенография легких: очаговых и инфильтративных изменений не выявлено, легочный рисунок деформирован за счет фиброза, корни не структурны, синусы свободны. Начато мониторирование ЭКГ, проведена оценка сатурации крови. Начиная с 4-х сут, после стабилизации состояния, к терапии добавлен бе- та-блокатор бисопролол в дозе 2,5 мг и ингибитор АПФ лизиноприл в дозе 5 мг в сутки. Анализ крови при госпитализации в 02 ч 37 мин: гемоглобин – 121 г/л, эритроциты – 4,28 × 1012/л, гематокрит 31%, лейкоциты – 29,7 × 109/л, тромбоциты – 187 × 109/л. Динамика клинических и биохимических анализов представлена в таблице 1.
Таблица 1. Динамика клинических и биохимических анализов
Table 1. Dynamics of clinical and biochemical analyses
|
Параметры Parameters |
Референсные значения Reference values |
Через 10 ч After 10 hours |
Через 20 ч After 20 hours |
48 ч 48 hours |
7 дней 7 days |
13 дней 13 days |
|
Общий анализ крови General blood test |
||||||
|
Эритроциты, × 1012/л RBC, 1012/L |
3,5–5,5 |
4,07 |
4,15 |
3,89 |
3,9 |
4,1 |
|
Гемоглобин, г/л Hemoglobin, g/L |
115–165 |
121 |
115 |
112 |
118 |
120 |
Окончание табл. 1
End of table 1
|
Параметры Parameters |
Референсные значения Reference values |
Через 10 ч After 10 hours |
Через 20 ч After 20 hours |
48 ч 48 hours |
7 дней 7 days |
13 дней 13 days |
|
Гематокрит, % Hematocrit, % |
35–55 |
32,9 |
30,3 |
31,7 |
31,3 |
32,4 |
|
Лейкоциты, × 109/л WBC, 109/L |
3,5–10 |
19,1 |
15,1 |
14,4 |
7,4 |
7,6 |
|
Тромбоциты, × 109/л Platelets, 109/L |
100–400 |
150 |
140 |
152 |
180 |
182 |
Биохимический анализ крови Biochemical blood analysis
|
Глюкоза, ммоль/л Glucose, Mmol/L |
3,3–5,5 |
16,8 |
15,2 |
6,4 |
7,3 |
6,4 |
|
АСАТ, ЕД AST Aspartate Aminotransferase, units |
5–40 |
86 |
243 |
75 |
26 |
18 |
|
АЛАТ, ЕД Alanin Aminotransferase, units |
5–40 |
51 |
86 |
47 |
22 |
20 |
|
Мочевина, Ммоль/л Urea, Mmol/L |
2,7–7,3 |
8,4 |
11,1 |
7,8 |
3,8 |
4,6 |
|
Креатинин, мкмоль/л Creatinine, mcmol/L |
44–97 |
94 |
127 |
91 |
68 |
86 |
|
МВ КФК, MB CPK, units |
24 |
74 |
200 |
145 |
18 |
20 |
|
Тропонин I, нг/мл Troponin I, ng/ml |
0,5 |
2,4 |
7,5 |
3,2 |
0,28 |
– |
|
Калий, Ммоль/л Potassium, Mmol/L |
3,5–5,0 |
4,2 |
4,0 |
3,4 |
4,3 |
4,1 |
|
Натрий, Ммоль/л Sodium, Mmol/L |
135–150 |
136 |
138 |
140 |
138 |
136 |
|
Общий холестерин, Ммоль/л Total cholesterol, Mmol/L |
3,3–5,5 |
– |
5,3 |
4,8 |
4,9 |
4,8 |
|
Триглицериды, Ммоль/л Triglycerides, Mmol/L |
1,0–2,29 |
– |
0,81 |
0,9 |
1,0 |
0,8 |
|
ЛПНП, Ммоль/л LDLC, Mmol/L |
09–2,5 |
– |
2,71 |
2,58 |
2,52 |
2,48 |
|
ЛПВП, Ммоль/л HDLC, Mmol/L |
0,9–3,0 |
– |
1,64 |
1,4 |
1,52 |
1,44 |
|
ПТИ, % PI, % |
90–105 |
62 |
70 |
78 |
88 |
92 |
|
АЧТВ, с APTT , sec |
24–34 |
46 |
64 |
62 |
28 |
26 |
|
МНО, ед. INR, units |
0,85–1,15 |
1,78 |
1,78 |
1,3 |
1,15 |
1,1 |
Кислотно-щелочное состояние Acid-base state
|
pH, ед. pH, units |
7,35–7,45 |
7,21 |
– |
7,46 |
7,36 |
– |
|
pCO2, мм рт. ст. pCO2, mm Hg |
36–44 |
51,1 |
– |
39,8 |
42 |
– |
|
pO2, мм рт. ст. pO2, mm Hg |
38–42 |
42 |
– |
40 |
41 |
– |
|
HCO3, Ммоль/л HCO3, Mmol/L |
22–26 |
20,8 |
– |
28,3 |
24 |
– |
|
BE, ммоль/л BE, Mmol/L |
–2…+2 |
–7,5 |
– |
4,2 |
2 |
– |
|
BE ecf., Ммоль/л BE ecf., Mmol/L |
–2,3…+2,3 |
–7,2 |
– |
4,4 |
2 |
– |
Примечание: АСАТ – аспартатаминотрансфераза, АЛАТ – аланинаминотрансфераза, МВ КФК – МВ фракция креатинфосфокиназы, ЛПНП – липопротеиды низкой плотности, ЛПВП – липопротеиды высокой плотности, ПТИ – протромбиновый индекс, АЧТВ – активированное частичное тромбопластиновое время, МНО – международное нормализованное отношение, pH – концентрация ионов водорода, pCO2 – парциальное давление углекислого газа, pO2 – парциальное давление кислорода, HCO3 – бикарбонат, BE – дефицит или избыток буферных оснований, BE ecf. – рассчитанный дефицит или избыток буферных оснований.
Note: RBC – Red blood cells, RBC – Red blood cells, AST – Aspartate Aminotransferase, ALT – Alanin Aminotransferase, МВ CPК – МВ creatine phosphokinase fraction; LDLC – Low-density lipoproteins cholesterol; HDLC – High-density lipoproteins cholesterol, PI – Prothrombin index; APTT – Activated partial thromboplastin time; INR – International normalized ratio; pH – concentration of hydrogen ions; pCO2 – partial pressure of carbon dioxide; pO2 – partial pressure of oxygen, HCO3 – bicarbonate, BE – base excess, BE ecf. – base excess, extracellular fluid.
В блоке интенсивной терапии выполнена ЭхоКГ: конечный диастолический объем (КДО) составил 68 см3, конечный систолический объем (КСО) – 35 см3, ударный объем (УО) – 33 см3, фракция выброса (ФВ) – 48%. Выявлен гипокинез апикальных, переднеперегородочных отделов левого желудочка как в М-режиме (рис. 4а), так и в В-режиме (рис. 4б).
Пациентка переведена из палаты интенсивной терапии в палату реабилитации на 5-е сут после стабили- зации состояния, при этом доза дофамина постепенно снижалась до 10, затем до 5 мкг/кг/мин в течение трех суток. Систолическое АД (САД) стабилизировалось на цифрах 110–115 мм рт. ст., а диастолическое (ДАД) – на цифрах 75–80 мм рт. ст. Диурез восстановлен до уровня 50 мл/ч. В палате реабилитации продолжено введение гепарина п/к по 5000 ЕД каждые 6 ч с увеличением интервала введения до 8, затем 12 ч с последующей отменой.
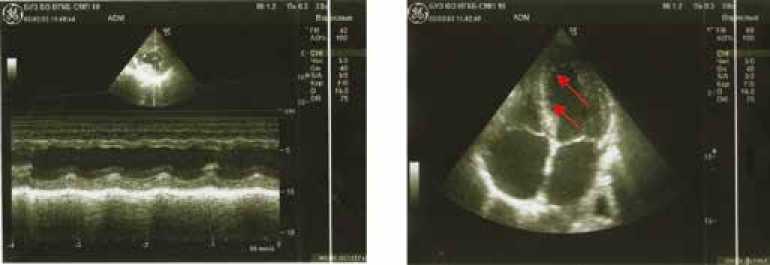
а)/a)
б)/b)
Рис. 4. Эхокардиография пациентки П.: а ) М-режим, парастернальная позиция, длинная ось левого желудочка, гипокинез переднеперегородочных отделов левого желудочка (стрелки); б ) апикальная четырехкамерная позиция, В-режим, гипокинез переднеперегородочных отделов левого желудочка (стрелки)
Fig. 4. Echocardiography of the patient P.: a ) M-mode, parasternal long-axis-view, long axis of the left ventricle, hypokinesis of the anteroseptal segments of the left ventricle (arrows); b ) apical four-chamber position, B-mode, hypokinesis of the anteroseptal segments of the left ventricle (arrows)
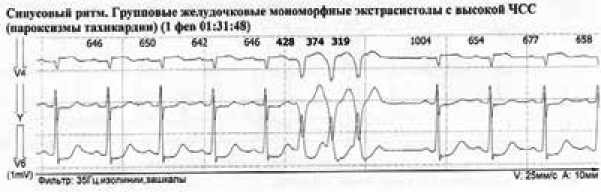
Холтеровское мониторирование выполнено в палате реабилитации в течение 22 ч 23 мин, при этом средняя частота сердечных сокращений составила 86 уд/мин днем, 93 уд/мин ночью. В течение мониторирования наблюдался синусовый ритм с частотой 89 уд/мин (от 74 до 112). Атриовентрикулярное проведение в норме. Зарегистрирована желудочковая эктопическая активность в виде одиночной, парной и групповой экстрасистол в среднем количестве 45 в час, эпизоды желудочкового мономорфного ускоренного ритма (3 эпизода), пароксизмы желудочковой мономорфной тахикардии (3 эпизода) общей длительностью 23 с, пароксизм желудочковой полиморфной тахикардии длительностью 1 с (рис. 5а).
Желудочковые нарушения ритма соответствуют 5-му классу аритмий в градации по Ryan. Средний корригированный интервал QT за сутки – 461 мс, зарегистрировано значительное удлинение корригированного интервала QT от 450 до 501 мс в течение 13 ч 59 мин. ЭКГ при выписке с трактовкой изменений представлена на рисунке 5 б .
а)/a)
б)/b)
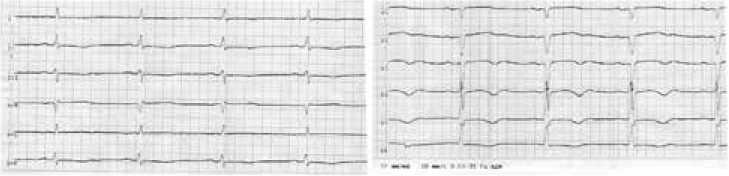
Рис. 5. а ) Холтеровское мониторирование, частота сердечных сокращений – 110 уд/мин, желудочковая экстрасистолия; б ) электрокардиограмма при выписке: синусовый ритм, зубец Т± в отведении V3, зубец Т отрицательный в отведении I–III, aVF, V4–V6, в отведении V1-V3 форма комплекса QS, длительность интервала QT – 480 мс
Fig. 5 . a ) Holter monitoring, heart rate 75 beats per minute, ventricular extrasystole; b ) ECG at discharge: sinus rhythm, T-wave ± in lead V3, negative T-wave in I–III, aVF, V4–V6, QS-pattern in V1–V3, the duration of the QT interval – 480 ms
Важное место в ведении пациентки занимала не только адекватная медикаментозная терапия, но и физическая и психологическая реабилитация, которые осуществлялись лечащим врачом кардиореаниматологом совместно с врачом-реабилитологом и клиническим психологом отделения ранней реабилитации. При проведении физической реабилитации использовались ступени активности от Ia (строгий постельный режим) до IIIa (палатный режим с самообслуживанием) в зависимости от сроков давности инфаркта и состояния пациентки [6, 7]. САД и ДАД, частота дыхания и частота пульса, а также самочувствие пациентки являлись критерием адекватности проведения дыхательной гимнастики и физической реабилитации в целом (табл. 2).
Таблица. 2. Динамика параметров пациентки П. во время физической реабилитации
Table 2. Dynamics of parameters of the patient P. during physical rehabilitation
|
Параметры Parameters |
Дни в стационаре Days in the hospital |
||||||||||
|
2 |
3 |
4 |
7 |
8 |
9 |
10 |
11 |
14 |
15 |
||
|
Срок ОИМ Term of AMI |
3 |
4 |
5 |
8 |
9 |
10 |
11 |
12 |
15 |
16 |
|
|
Ступень активности Activity stage |
Iа |
Iа |
Iб |
IIа |
IIа |
IIб |
IIб |
IIIа |
IIIа |
IIIа |
|
|
Пульс Pulse |
До before |
64 |
63 |
77 |
78 |
80 |
80 |
76 |
72 |
74 |
78 |
|
После after |
62 |
70 |
81 |
82 |
84 |
86 |
80 |
76 |
78 |
82 |
|
|
ЧДД |
до before |
20 |
19 |
18 |
17 |
16 |
16 |
17 |
16 |
16 |
16 |
|
FRM |
после after |
21 |
20 |
19 |
18 |
17 |
18 |
18 |
17 |
17 |
17 |
|
САД SBP |
До |
90 |
95 |
100 |
105 |
105 |
110 |
105 |
110 |
115 |
115 |
|
ДАД DBP |
before |
60 |
70 |
70 |
80 |
75 |
80 |
80 |
80 |
80 |
80 |
|
САД SBP |
после after |
90 |
90 |
95 |
100 |
105 |
110 |
105 |
110 |
115 |
115 |
|
ДАД DBP |
60 |
70 |
70 |
80 |
80 |
80 |
80 |
80 |
80 |
80 |
|
Примечание: САД – систолическое артериальное давление, мм рт. ст., ДАД – диастолическое артериальное давление, мм рт. ст., ЧДД – частота дыхательных движений в минуту
Note: SBP – systolic blood pressure, mm Hg; DBP – diastolic blood pressure, mm Hg; FRM – frequency of respiratory movements per minute.
При проведении психологической реабилитации использовалось несколько методик: тест Mini-Cog для оценки кратковременной памяти (из трех слов) и конструктивного праксиса (задание на изображение часов), общее количество баллов от 0 до 5, при этом при наборе от 0 до 3 баллов вероятность тяжелых когнитивных нарушений высокая. Шкала нарушения сна с оценкой от 0 баллов – отсутствие диссомнии до 3 баллов и более, когда необходима консультация сомнолога.
Тест умственных способностей Ходкинсона оценивает ориентированность во времени, месте и собственной личности, память и общий уровень знаний, а также внимание испытуемого. Сумма 10 баллов за 10 вопросов является нормой. Для оценки вероятности развития тре- воги и депрессии использовалась госпитальная шкала тревоги и депрессии (The Hospital Anxiety and Depression Scale, HADS), при этом оценка от 0 до 7 баллов – норма, 8–10 баллов – субклиническая депрессия / тревога и 11 баллов и более – клинически выраженная тревога / депрессия [7] (табл. 3).
По результатам предварительного тестирования выявлена антероградная амнезия. В течение первых двух дней пациентка постоянно задавала одни и те же вопросы, о чем практически сразу же забывала. Анализ данных таблицы показывает, что в психологическом плане первые несколько дней после восстановления сознания сопровождались выраженной тревогой и депрессией, а также снижением когнитивных функций.
Таблица 3. Психологическая реабилитация
Table 3. Psychological rehabilitation
|
Дни Days |
Шкала сна Sleep scale |
Тест Mini Cog Mini Cog Test |
Тест Ходкинсона Hodkinson ‘s Test |
HADS |
|
|
Тревога Anxiety |
Депрессия Depression |
||||
|
1 |
– |
– |
– |
– |
– |
|
2 |
1 |
1 |
2 |
10 |
7 |
|
4 |
1 |
3 |
3 |
10 |
6 |
|
8 |
1 |
4 |
7 |
5 |
3 |
|
11 |
0 |
5 |
10 |
1 |
0 |
|
14 |
0 |
5 |
10 |
1 |
0 |
Примечание: HADS – The Hospital Anxiety and Depression Scale – госпитальная шкала тревоги и депрессии.
Note: HADS – The Hospital Anxiety and Depression Scale.
Ежедневные беседы с пациенткой лечащего врача, реабилитолога и психолога были направлены на повышение адаптационных возможностей пациентки, формирование и усиление мотивации к лечению, коррекцию психоэмоционального состояния. Последовательная психологическая реабилитация позволила значительно улучшить ее психологическое состояние к моменту выписки из стационара.
Обсуждение
У пациентки П. развившийся ОИМ с подъемом сегмента ST осложнился рецидивирующей фибрилляцией желудочков на догоспитальном этапе. По современным данным, подобное осложнение встречается в 5–10% случаев [1, 2], что значительно осложняет прогноз, и госпитальная летальность достигает 37,7% [1]. Еще одной особенностью нашей пациентки является то, что она проживает в пригороде, в сельской местности, в 20 км от больницы СМП города и обслуживается скорой помощью местной районной больницы. Время приезда скорой помощи составило около 10 мин, что, несомненно, сыграло большую положительную роль. Данные современных источников подчеркивают, что в аналогичных случаях время приезда СМП может быть на 16,7 мин больше, чем в условиях города [6].
Важными аспектами оказания помощи больным ОИМ являются своевременное обращение за медицинской помощью и время до первого медицинского контакта. В нашем случае СМП сработала очень оперативно, чего не скажешь о пациентке, которая обратилась за медицинской помощью только через 40 мин от начала клиники. Позднее обращение пациентов за медицинской помощью является самостоятельной проблемой, повышает риск развития осложнений, ведет к ухудшению прогноза. Возможные пути решения – повышение осведомленности пациентов о клинике, симптомах ОИМ, мерах первой помощи, что будет способствовать своевременному обращению и улучшит качество ведения пациентов с ОИМ, прежде всего на догоспитальном этапе [7]. Нашей пациентке повезло, что пароксизм фибрилляции желудочков случился в присутствии бригады СМП, и ей сразу были проведены реанимационные мероприятия, включавшие не только базовые мероприятия, но и дефибрилляцию. Именно своевременное проведение реанимационных мероприятий и дефибрилляции является важным условием улучшения прогноза у данной категории пациентов [7, 8].
Возникшая острая постреанимационная энцефалопатия была обусловлена гипоксией головного мозга и благополучно разрешилась в течение суток. Уровень сознания при поступлении – кома, по шкале Глазго 6 баллов, через 6 ч – сопор (10 баллов), через 12 ч – оглушение (13 баллов), через 18 ч – ясное сознание [9, 10]. Важное место в ведении пациентки занимала не только адекватная медикаментозная терапия, но и физическая и психологическая реабилитация, которые осуществлялись лечащим врачом кардиореаниматологом совместно с врачом-реа-билитологом и клиническим психологом отделения ранней реабилитации [11, 12].
При госпитализации уже в противошоковой палате активно обсуждался и решался вопрос о проведении КАГ. Современные клинические рекомендации однозначно рекомендуют после успешных реанимационных мероприятий в данной ситуации как можно более оперативное выполнение инвазивных коронарных вмешательств
[5, 13]. Время от начала клиники до открытия коронарной артерии у нашей пациентки составило 3 ч 15 мин.
Учитывая низкое АД, в операционной продолжено в/в капельное введение раствора дофамина в инотропной дозе 15 мкг/кг/мин. Послеоперационное лечение и наблюдение продолжено в блоке интенсивной терапии, учитывая нестабильность гемодинамики и необходимость контроля витальных функций. Болевой синдром не рецидивировал, но АД оставалось низким (65–70 мм рт. ст.), что потребовало продолжения введения раствора дофамина. К концу первых суток пребывания в блоке интенсивной терапии АД стабилизировалось на уровне 90/60 мм рт. ст., восстановился диурез на уровне 30 мл/ч.
В последующие двое суток доза дофамина уменьшена до почечной 3 мг/кг/мин, затем отменена, так как диурез составил 50 мл/ч. Инотропная поддержка является важным компонентом в комплексной терапии кардиогенного шока, возникшего на фоне ОИМ и клинической смерти [14]. В течение 3 дней в блоке интенсивной терапии продолжалась неинвазивная вспомогательная вентиляция в режиме CPAP с давлением в дыхательных путях 10 см вод. ст., что связано с дыхательным ацидозом (pH 7,21) (см. табл. 1), при этом сатурация крови сохранялась на уровне 92–94%.
Метаболический ацидоз (BE – 7,2) не потребовал дополнительных мероприятий и разрешился по мере стабилизации гемодинамики. Транзиторный лейкоцитоз при госпитализации не мог быть объяснен возможной пневмонией, так как на рентгенограмме очаговых и инфильтративных изменений не выявлено. На наш взгляд, повышение уровня лейкоцитов связано с перенесенной клинической смертью и проведенными реанимационными мероприятиями.
На 5-е сут пациентка переведена в палату реабилитации. Выполнено холтеровское мониторирование, которое выявило значимые желудочковые нарушения ритма, которые соответствовали 5-му классу по Ryan [7]. Подобные нарушения ритма явились, на наш взгляд, следствием неблагоприятного течения ОИМ, осложнившегося электрической нестабильностью, рецидивирующей фибрилляцией желудочков и клинической смертью. При выполнении ЭхоКГ перед выпиской не выявлено существенной положительной динамики. Адаптивное ремоделирование миокарда привело к росту КДО до 92 см3 (+24 см3), КСО до 51 см3 (+6 см3), а также УО до 41 см3 (+8 см3), в то же время ФВ снизилась до 44% (–4%). Сохранился гипокинез апикальных, переднеперегородочных отделов и верхушки.
Выписана в удовлетворительном состоянии на 15-е сут, при выписке рекомендовано наблюдение у терапевта и кардиолога по месту жительства. Обязательным является прием двойной антиагрегантной терапии: ацекардола и клопидогреля, а также бета-адреноблокаторов, ингибиторов ангиотензинпревращающего фермента, антагонистов минералокортикоидных рецепторов. Учитывая данные ЭхоКГ и холтеровского мониторирования, рекомендовано при стабильном состоянии выполнение контрольных исследований, а при ухудшении состояния обязательное ЭКГ-исследование, определение маркеров повреждения, при необходимости – повторная госпитализация.
Заключение
Внегоспитальная сердечная смерть требует проведения неотложных реанимационных мероприятий, в ряду которых особое место занимает дефибрилляция.
Пациентам с осложненным течением ОИМ на догоспитальном этапе необходима немедленная госпитализация в кардиологический центр, имеющий возможность осуществления инвазивных вмешательств. КАГ и возможное стентирование должны сопровождаться обязательным мониторированием гемодинамики. Патологическое ремоделирование, связанное с ОИМ, препятствует быстрому восстановлению систолической функции миокарда. Важное место в госпитальном лечении пациентов занимает физическая и психологическая реабилитация. Диспансерное наблюдение у кардиолога и терапевта с обязательным регулярным ЭКГ-контролем, ЭхоКГ-иссле-дованием является обязательным условием постгоспитальной реабилитации.
Список литературы Острый инфаркт миокарда, осложненный внезапной внегоспитальной сердечной смертью: клинический случай
- Karam N., Bataille S., Marijon E., Tafflet M., Benamer H., Caussin C. et al. Incidence, mortality, and outcome-predictors of sudden cardiac arrest complicating myocardial infarction prior to hospital admission. Circ. Cardiovasc. Interv. 2019;12(1):e007081. https://doi.org/10.1161/CIRCINTERVENTIONS.118.007081.
- Kragholm K., Lu D., Chiswell K., Al-Khalidi H.R., Roettig M.L., Roe M. et al. Improvement in care and outcomes for emergency medical service-transported patients with ST-elevation myocardial infarction (STEMI) with and without prehospital cardiac arrest: A mission: Lifeline Stemi Accelerator Study. J. Am. Heart Assoc. 2017;6(10):e005717. https://doi.org/10.1161/JAHA.117.005717.
- Ashburn N.P., Snavely A.C., Angi R.M., Scheidler J.F., Crowe R.P., McGinnis H.D. et al. Prehospital time for patients with acute cardiac complaints: A rural health disparity. Am. J. Emerg. Med. 2022;52:64-68. https://doi.org/10.1016/j.ajem.2021.11.038.
- Sonoda T., Wada H., Ogita M., Takahashi D., Nishio R., Yasuda K. et al. Clinical features and predictors of outcome in patients with acute myocardial infarction complicated by out-of-hospital cardiac arrest. BMC Cardiovasc. Disord. 2022;22(1):185. https://doi.org/10.1186/s12872-022-02628-3.
- Рекомендации ЕОК по ведению пациентов с острым инфарктом миокарда с подъемом сегмента ST, 2017. Ассоциация специалистов по острой сердечно-сосудистой помощи, Европейская ассоциация по превентивной кардиологии, Европейская ассоциация специалистов по методам визуализации сердечно-сосудистой системы, Европейская Ассоциация по чрескожным коронарным вмешательствам, Европейская Ассоциация по сердечному ритму, Ассоциация специалистов по сердечной недостаточности. Российский кардиологический журнал. 2018;23(5):103-158. https://doi.org/10.15829/ 15-60-4071-2018-5-103-158.
- Stopyra J.P., Crowe R.P., Snavely A.C., Supples M.W., Page N., Smith Z. et al. Prehospital time disparities for rural patients with suspected STEMI.Prehosp. Emerg. Care.2022:1-8. https://doi.org/10.1080/10903127.2022.2061660.
- Желудочковые нарушения ритма. Желудочковая тахикардия и внезапная смерть. Клинические рекомендации, 2020. Российское кардиологическое общество (РКО). При участии: Всероссийского научного общества специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции (ВНОА); Всероссийской общественной организации «Ассоциация детских кардиологов России»; Общества холтеровского мониторирования и неинвазивной электрокардиологии. Российский кардиологический журнал. 2021;26(7):4600. https://doi.org/10.15829/ 15-60-4071-2021-4600.
- Sawyer K.N., Camp-Rogers T.R., Kotini-Shah P., Del Rios M., Gossip M.R., Moitra V.K. et al.; American Heart Association Emergency Cardiovascular Care Committee; Council on Cardiovascular and Stroke Nursing; Council on Genomic and Precision Medicine; Council on Quality of Care and Outcomes Research; and Stroke Council. Sudden cardiac arrest survivorship: A scientific statement from the American Heart Association. Circulation. 2020;141(12):e654-e685. https://doi.org/10.1161/CIR.0000000000000747.
- Заболотских И.Б., Проценко Д.Н., Лебединский К.М. Интенсивная терапия. Национальное руководство. Том 1. М.: ГЭОТАР-Медиа; 2022:1152.
- Марино П.Л. Интенсивная терапия. Пер. с англ. под ред. А.И. Ярошецкого. М.: ГЭОТАР-Медиа; 2022:1152.
- Аронов Д.М. Кардиореабилитация и вторичная профилактика. М.: ГЭОТАР-Медиа; 2021:464.
- Реабилитация в отделениях реанимации и интенсивной терапии (РеабИТ). Методические рекомендации Союза реабилитологов России и Федерации анестезиологии и реаниматологии. Вестник интенсивной терапии им. А.И. Салтанова. 2022,2:7-40. https://doi.org/10.21320/1818-474X-2022-2-7-40.
- Рекомендации ESC/EACTS по реваскуляризации миокарда, 2018. Рабочая группа по реваскуляризации миокарда Европейского общества кардиологов (ESC) и Европейской ассоциации кардио-торакальных хирургов (EACTS). Разработаны с участием Европейской ассоциации по чрескожным сердечно-сосудистым вмешательствам (EAPCI). Российский кардиологический журнал. 2019;24(8):151-226. https://doi.org/10.15829/15-60-4071-2019-8-151-226.
- Григорьев Е.В., Баутин А.Е., Киров Д.Л., Шушкевич Д.Л., Корнелюк Р.А. Кардиогенный шок при остром коронарном синдроме: современное состояние проблемы диагностики и интенсивной терапии. Вестник интенсивной терапии им. А.И. Салтанова. https://doi.org/;2:73-85.DOI: 10.21320/1818-474X-2020-2-73-85.


