Отдаленные результаты гибридного кардиохирургического шунтирования и эндоваскулярного стентирования пациентов с наследственной гиперхолестеринемией и стенокардией напряжения
Автор: Суковатых Б.С., Сидоров Д.В., Боломатов Н.В., Середицкий А.В., Вишневский В.И., Альянов А.Л., Карасев А.Ю., Швец Д.А., Слетова А.М., Гаврилина А.В., Орлова А.Ю.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.19, 2024 года.
Бесплатный доступ
Цель исследования. Сравнение результатов коронарного стентирования и коронарного шунтирования пациентов с наследственной гиперхолестеринемией и стенокардией.Материалы и методы. Проведен анализ результатов лечения 100 пациентов с наследственной гиперхолестеринемией и стенокардией напряжения. В рамках предоперационной подготовки, все пациенты были классифицированы по шкале SYNTAX Score - во всех случаях выявлена умеренная тяжесть поражения. На основании этого, перед 2-м этапом хирургического лечения, рандомизированно, все пациенты были разделены на 2 равные группы: в 1 группу вошли пациенты, которым была выполнена эндоваскулярная реваскуляризация пораженной коронарной артерии в качестве 2-го этапа оперативного лечения; во 2 группу вошли пациенты, которым в качестве 2-го этапа реваскуляризации выполнено коронарное шунтирование (КШ).Результаты. Результаты эндоваскулярного стентирования и кардиохирургического шунтирования демонстрируют практически идентичные результаты спустя 12 месяцев после проведенного хирургического лечения и пациентов с умеренной тяжестью поражения по шкале SYNTAX Score. Качество жизни пациентов, перенесших стентирование коронарных артерий, намного превышают аналогичные показатели больных, подвергшихся открытому кардиохирургическому вмешательству
Аорто-коронарное шунтирование, наследственная гиперхолестеринемия, стент, коронарное стентирование, стенокардия напряжения
Короткий адрес: https://sciup.org/140307881
IDR: 140307881 | DOI: 10.25881/20728255_2024_19_3_44
Long-term results of hybrid cardiac bypass and endovascular stenting in patients with hereditary hypercholesterinemia and angina
Purpose of the study. Comparison of the results of coronary stenting and coronary bypass surgery in patients with hereditary hypercholesterolemia and angina pectoris.
Текст научной статьи Отдаленные результаты гибридного кардиохирургического шунтирования и эндоваскулярного стентирования пациентов с наследственной гиперхолестеринемией и стенокардией напряжения
погибают более 360 000 пациентов [1; 2]. В нашей стране болезни сердца по-прежнему являются лидирующей причиной смертности населения на протяжении многих десятилетий: в 2018 г. более 80% из них были связаны с ИБС [3].
Восстановление проходимости пораженной коронарной артерии, по-прежнему является наиболее результативным способом улучшения прогноза и качества жизни

Суковатых Б.С., Сидоров Д.В., Боломатов Н.В. и др.
ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ ГИБРИДНОГО КАРДИОХИРУРГИЧЕСКОГО ШУНТИРОВАНИЯ И ЭНДОВАСКУЛЯРНОГО СТЕНТИРОВАНИЯ ПАЦИЕНТОВ С НАСЛЕДСТВЕННОЙ ГИПЕРХОЛЕСТЕРИНЕМИЕЙ И СТЕНОКАРДИЕЙ НАПРЯЖЕНИЯ пациентов. При этом золотым стандартом хирургической помощи этой категории больных, остается коронарное шунтирование (КШ): в нашей стране выполняется около 40 000 вмешательств в год [1–3].
Благодаря огромному скачку в развитии технологий внутрисосудистые операции стали еще более эффективными и доступными. Это привело к тому, что рентгенэн-доваскулярные диагностика и лечение прочно заняли свою нишу на одной ступени с «открытым» хирургическим лечением и не уступают ему по эффективности и количеству возможных осложнений [4].
В последние годы была разработана гибридная методика реваскуляризации миокарда, которая, с одной стороны объединяет преимущества обоих методов реваскуляризации, а с другой стороны – нивелирует их недостатки. Методика может выполняться как одномоментно, так и в два этапа. При этом первым этапом можно выполнить, как и эндоваскулярный этап реваскуляризации, так и коронарное шунтирование. К сожалению, до сих пор остается нерешенным вопрос о чередовании того или иного этапа хирургического лечения, а также сроках его выполнения. Только проведение крупных рандомизированных исследований позволит определить роль гибридной хирургии среди остальных методик реваскуляризации миокарда [5].
В настоящее время, с целью определения показаний к тому или иному способу реваскуляризации используют шкалу SYNTAX Score (SS). После внесения всех поражений рассчитывается суммарный балл: SS<23 – считается низкой тяжестью поражения, таким пациентам возможно выполнить реваскуляризацию эндоваскулярными методиками; SS = 23–32 – характеризуется средним уровнем поражения, у таких пациентов выполнение КШ/ ЧКВ демонстрируют идентичные результаты, поэтому у данной группы больных возможно проведение как одного, так и другого вида операций и в каждом конкретном случае решение принимается индивидуально. SS>33 характеризуется высокой тяжестью поражения, поэтому преимущество остается за КШ [6; 7].
Помимо ангиографических критериев, не стоит недооценивать значимость клинических факторов, таких как функциональный класс стенокардии, коморбид-ный фон. Особое место отводится группе пациентов, страдающих наследственной (семейной) гиперхолестеринемией (СГХС) – наследственным аутосомно-доминантным нарушением метаболизма липопротеинов (ЛП), характеризующееся высоким содержанием в плазме крови ЛП низкой плотности (ЛПНП), раннему атеросклеротическому поражению сосудов, (в том числе – диффузному), и сердечно-сосудистым событиям в молодом возрасте. Особенно важно отметить, что при диффузном атероматозе зачастую поражается дистальное русло венечных артерий, что, в свою очередь, ограничивает перспективность ЧКВ и КШ вследствие снижения их эффективности и высокого риска периоперационных осложнений [8].
По данным ряда наблюдений, проведенных на моно-и дизиготных близнецах и в семьях пациентов с ИБС, роль наследственной предрасположенности в развитии ИБС, варьирует от 30 до 80%. Заболевание, как правило, возникает вследствие мутации нескольких генов: гена рецептора к ЛПНП – LDLR, гена аполипопротеина В-100, гена PCSK9, кодирующего конвертазу. Изменения в этих генах имеют доминантный тип наследования и проявляются клинически как гетеро- и гомозиготные формы СГХС, а изменения в гене LDLRAP1 имеют рецессивный тип наследования и клинически проявляются только как гомозиготная форма СГХС [9–11]. По последним данным, в целом распространенность СГХС в мире составляет 1 на 220 человек, в Западной Сибири — еще выше — 1 на 108 человек. [14; 15]. Гетерозиготная форма СГХС считается одним из самых частых наследственных заболеваний с частотой 1 случай на 200 в открытой популяции. Гомозиготная форма СГХС является не только более тяжелой, но и значительно более редкой – 1 случай на 1 млн. населения [10; 11].
Цель исследования
Сравнение результатов коронарного стентирования и КШ пациентов с наследственной гиперхолестеринемией и стенокардией.
Материалы и методы
Проведен анализ хирургического лечения и послеоперационного наблюдения 100 пациентов со стабильной стенокардией напряжения и наследственной гиперхолестеринемией. Семейное заболевание было диагностировано по следующим критериям:
-
• данные анамнеза: все, без исключения, пациенты подтверждают факт перенесенного острого инфаркта у ближайших родственников в возрасте 50–60 лет; 5 (5%) больных отмечали наличие сухожильных ксантом у своих ближайших родственников;
-
• результаты осмотра: у 9 больных (у 5 пациентов в 1-й группе и у 4 больных из 2-й группы) были обнаружены сухожильные ксантомы;
-
• средние показатели ХС-ЛПНП, на момент включения в исследование, у всех больных составили 5,9±1,1 ммоль/л.
Все наблюдаемые пациенты ранее были госпитализированы в ЧКВ-центр по поводу острого коронарного синдрома: по данным первичной коронароангиографии (КАГ) всех больных было выявлено многососудистое поражение коронарных артерий, и принято решение об этапном вмешательстве на коронарных артериях. В качестве 1-го этапа реваскуляризации пациентам незамедлительно было выполнено стентирование симптом-зависимой артерии. По стабилизации состояния, всем больным, в кратчайшие сроки был выполнен 2-й этап реваскуляризации. В рамках предоперационной подготовки, для определения дальнейшей тактики хирургического лечения, все пациенты были классифицированы

по шкале SYNTAX Score – во всех случаях выявлена умеренная тяжесть поражения. На основании этого, перед 2-м этапом хирургического лечения, рандомизированно, все пациенты были разделены на 2 равные группы: · в 1 группу вошли пациенты, которым была выполнена эндоваскулярная реваскуляризация пораженной коронарной артерии в качестве 2-го этапа оперативного лечения в условиях отделений рентгенохирургических методов диагностики и лечения (РХМДиЛ) Орловской областной клинической больницы и Курской городской клинической больницы скорой медицинской помощи;
-
· во 2 группу вошли пациенты, которым в качестве 2-го этапа реваскуляризации выполнено КШ в различных медицинских учреждениях Российской Федерации.
Первичные результаты эффективности проводимого лечения оценивались на 5–10 сутки после операции и включали в себя оценку скорости кровотока в реваскуля-ризированной артерии, анализ сердечной деятельности по данным ЭКГ, ЭХО-КГ, холтеровского мониторирования, анализировались показатели липидограммы. Скорость кровотока у пациентов, подвергшихся эндоваскулярному лечению, определялась согласно методике оценки количества кадров (TFC – TIMI frame count или «количество временных кадров»): ее суть заключается в подсчете количества ангиографических кадров, где происходит «тугое» заполнение венечной артерии. Нормальные показатели для TFC – менее 20 кадров (то есть в норме артерия полностью заполняется контрастным веществом к 20-му кадру по данным КАГ), замедленный кровоток – от 20-го до 40-го кадра, а в случае возникновения синдрома noreflow – TFC более 40 кадров. Необходимо отметить, что поскольку передняя межжелудочковая артерия (ПМЖВ), как правило, длиннее, чем остальные венечные артерии, то для нее значения TFC до 40-го кадра считаются нормальными. Оценка кровотока у пациентов, подвергшихся КШ, производилась на основании интраоперационной шунтографии. При этом за эталонные значения, ввиду отсутствия международного согласительного документа, принимались параметры, встречающиеся в литературе: значение средней объемной скорости кровотока (Qmean или MGF), более 20 мл/мин. в позиции внутренней грудной артерии, и более 30–40 мл/мин. у венозных шунтов, индекс пульсации (PI) не выше 5,0 (в идеале – от 1 до 3); процент диастолического объемного наполнения (DF) – более 50% MGF [16].
Окончательные результаты исследования оценивались через 12 месяцев после выписки пациента из стационара и включали в себя результаты ЭКГ, ЭХО КГ, Холтеровского мониторирования, показатели липидограммы, при необходимости (наличие у пациентов симптомов стенокардии или выявленные «новые» признаки ишемии миокарда по данным инструментального обследования) – повторная диагностическая КАГ.
Для оценки качества жизни пациентов, в том числе и после проведенного хирургического лечения, широкое распространение получил опросник SF-36 [12; 13]. Он содержит 36 пунктов, они сгруппированы в восемь шкал: 1) физическое функционирование (Physical Functioning
-
— PF) – данный параметр отражает степень ограничения выполнения физических нагрузок (самообслуживание, ходьба, подъем по лестнице, и т.д.). Чем ниже показатель, тем больше ограничена физическая активность пациента состоянием его здоровья;
-
2) ролевое функционирование, обусловленное физическим состоянием деятельность (Role-Physical Functioning — RP) – оценка влияния физического состояния на выполнение каждодневных обязанностей. Снижение показателя свидетельствует об ограничения повседневной активности пациента его физическим состоянием;
-
3) интенсивность боли (Bodily pain — BP – оценка ее воздействия на возможность выполнять ежедневную работу (в том числе – по дому). Сниженный показатель говорит об ограничении активности пациента;
-
4) общее состояние здоровья (General Health — GH) – параметр оценки пациентом своего состояния здоровья, а также перспектив от проводимого лечения. Чем ниже показатель, тем хуже пациент оценивает исследуемые параметры;
-
5) жизненная активность (Vitality — VT) – данный параметр позволяет пациенту оценить ощущение полноты сил и энергии, или же, наоборот: ослабленным и истощенным. Низкие баллы говорят о выраженном утомлении пациента и снижении его жизненной активности;
-
6) социальное функционирование (Social Functioning — SF) – данный параметр характеризует ограничение социальной активности пациента его физическим или же эмоциональным состоянием. Низкие показатели говорят о выраженном ограничении социальной коммуникации пациента из-за его физического и эмоционального состояния;
-
7) эмоциональное состояние (Role-Emotional — RE) – данный параметр позволяет оценить уровень эмоционального статуса пациента, при котором его состояние мешает повседневной деятельности (включая большие затраты времени на выполнение той или иной работы, уменьшение объема выполненной работы, снижение ее качества и т.д.). Низкий показатель расценивается как ограничение при выполнении повседневной работы из-за снижения эмоционального статуса больного;
-
8) психическое здоровье (Mental Health — MH) – данный параметр позволяет оценить настроение пациента (в том числе наличие у больного депрессии, тревоги, а также общий показатель положительных эмоций). Снижение показателя говорит о наличии депрессивных, тревожных переживаний и психическом неблагополучии.
Показатели каждой шкалы варьируют между 0 и 100, где 100 представляет полное здоровье [17].

Суковатых Б.С., Сидоров Д.В., Боломатов Н.В. и др.
ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ ГИБРИДНОГО КАРДИОХИРУРГИЧЕСКОГО ШУНТИРОВАНИЯ И ЭНДОВАСКУЛЯРНОГО СТЕНТИРОВАНИЯ ПАЦИЕНТОВ С НАСЛЕДСТВЕННОЙ ГИПЕРХОЛЕСТЕРИНЕМИЕЙ И СТЕНОКАРДИЕЙ НАПРЯЖЕНИЯ
Табл. 1. Основные характеристики и наличие сопутствующих заболеваний
|
Параметры |
1 группа n = 50 |
2 группа n= 50 |
Значение Р |
|
Возраст, лет |
65,4±7,2 |
66,1±6,4 |
р = 0,546 |
|
Возраст более 60 лет |
37 (74%) |
34 (68%) |
р = 0,615 |
|
Мужчины |
33 (66%) |
36 (72%) |
р = 0,584 |
|
Курение |
40 (80%) |
39 (78%) |
р = 0,715 |
|
Злоупотребление алкоголем |
20 (40%) |
22 (44%) |
р = 0,694 |
|
Показатели индекса массы тела (ИМТ) |
26,4±3,2 |
25,8±4,3 |
р = 0,527 |
|
Количество баллов по шкале Syntax Score (SS) |
25,8±1,7 |
27,4±1,3 |
р = 0,594 |
|
Показатели ФВ ЛЖ, % |
53,2±5,1 |
54,2±3,4 |
р = 0,867 |
|
Триглицериды (ТГ) |
2,2±0,3 ммоль/л |
1,9±0,4 ммоль/л |
р = 0,538 |
|
Липопротеины низкой плотности (ЛПНП) |
3,1±1,4 ммоль/л |
3,4±1,1 ммоль/л |
р = 0,531 |
|
Холестерин не-ЛВП |
2.5±1,1 ммоль/л |
2,3±1,2 ммоль/л |
р = 0,507 |
|
Длина пораженного сегмента артерии, мм |
40,3±2,4 |
39,7±3,7 |
р = 0,915 |
|
Частота бифуркационных поражений |
26 (52%) |
28 (56%) |
р = 0,862 |
|
Хроническая сердечная недостаточность (ХСН) |
10 (20%) |
12 (24%) |
р = 0,964 |
|
Гипертоническая болезнь (ГБ) |
23 (46%) |
21 (42%) |
р = 0,735 |
|
Предшествующий инфаркт миокарда |
50 (100%) |
50 (100%) |
р = 0,211 |
|
Сахарный диабет (СД) |
I Тип – 11 (22%) пациентов II тип – 15 (30%) больных |
I Тип – 10 (20%) пациентов II тип – 14 (28%) больных |
р = 0,623 р = 0,712 |
|
Хроническая болезнь почек (ХБП) |
7 (14%) |
5 (10%) |
р = 0,817 |
|
Онкопатология |
2 (4%) |
3 (6%) |
р = 0,764 |
|
Язвенная болезнь |
5 (10%) |
3(6%) |
р = 0,829 |
|
Хроническая обструктивная болезнь легких (ХОБЛ) |
4 (8%) |
2 (4%) |
р = 0,846 |
|
Бронхиальная астма (БА) |
1 (2%) |
0 |
р = 0,998 |
|
Острое нарушение мозгового кровообращения (ОНМК) |
3 (6%) |
2 (4%) |
р = 0,878 |
|
Заболевание щитовидной железы |
2 (4%) |
1 (2%) |
р = 0,856 |
|
Психотические расстройства |
2 (4%) |
3 (6%) |
р = 0,911 |
Примечание : в таблице представлены основные клинические параметры обследуемых пациентов: статистической разницы в обеих группах не выявлено.
Статистическую обработку материала проводили с использованием методов однофакторного дисперсного и корреляционного анализа. Вычисляли средние величины количественных показателей, стандартные ошибки и критерий согласия Пирсона ( χ 2). Полученные данные представлены в виде M±SD. Существенность различий средних величин оценивали с помощью t-критерия Стьюдента. Различия считали статистически значимыми при р<0,05.
Результаты
Основные характеристики и наличие сопутствующих заболеваний в обеих группах пациентов представлены в таблице 1.
Результаты интраоперационной оценки скорости кровотока, после проведенного стентирования коронарной артерии представлены в таблице 2, а после выполненного КШ – таблица 3.
Как видно из таблицы 2, у всех пациентов удалось восстановить антеградный кровоток. У 3 (6%) больных интраоперационно возник феномен slow-reflow.
С целью профилактики тромботических осложнений, были использованы блокаторы IIB–IIIA рецепторов тромбоцитов, а у 1 больного – тромбоаспирация в дополнении к уже введенному препарату. В обоих случаях был достигнут удовлетворительный ангиографический результат.
Табл. 2. Анализ интенсивности коронарного кровотока по шкале TFC после проведенной эндоваскулярной реваскуляризации
|
Параметры |
1 группа n = 50 |
|
Удовлетворительная скорость кровотока – до 20 кадров |
47 (94%) |
|
Замедленный кровоток (синдром slow-reflow) – 20–40 кадров |
3 (6%) |
|
Невосстановленный кровоток (синдром no-reflow) – более 40 кадров |
0 |
Примечание : у большинства пациентов удалось восстановить удовлетворительный кровоток сразу после имплантации стентов. У 3(6%) пациентов, после имплантации стентов, возник синдром slow-reflow на фоне вазоспазма: после введения 1 ml – 0,001% раствора нитроглицерина спастическая реакция была купирована, скорость кровотока была восстановлена.

Таблица 3 демонстрирует удовлетворительные показатели интенсивности кровотока по аорто-, мамморо-коронарным шунтам после проведенной кардиохирургической реваскуляризации.
В раннем послеоперационном периоде летальных исходов и повторных экстренных вмешательств не зафиксировано. У 7 (2 больных в 1-й группе и 5 – во 2-й группе) пациентов зарегистрированы эпизоды мерцательной аритмии, которые были купированы назначенной консервативной терапией.
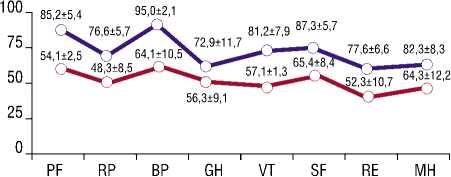
Перед выпиской из стационара для пациентов группы 1 и после выписки из стационара и по прибытию по месту проживания у пациентов группы 2, у всех пациентов была проведена оценка качества жизни при помощи опросника MOS SF-36 v.2 (График 1).
График 1 демонстрирует улучшение качества жизни пациентов после проведенного эндоваскулярного лечения, по сравнению с пациентами, подвергшимися КШ, что, по всей вероятности, объясняется малотравма-тичностью оперативного лечения, более низкой продолжительностью операции и ранним периодом активации больного, в то время как «открытая» реваскуляризация значительно превышает все указанные параметры.
Спустя 6 месяцев после проведенного хирургического лечения все пациенты были приглашены на контрольный осмотр к кардиологу. Повторное экстренное вмешательство было выполнено 2 (2%) больным, по 1 больному в каждой из групп из-за вновь возникшего стойкого болевого синдрома, признаков ишемии миокарда по данным ЭКГ: у пациента в 1-й группе был выявлен тромбоз стентированного сегмента, была выполнена реваскуляризация с положительной динамикой. У больного из 2-й группы, по результатам шунтографии, кондуиты полностью проходимы, реваскуляризация пациенту не потребовалась. У оставшихся пациентов ухудшения состояния не наблюдалось. В обеих группах пациентов, летальных случаев зарегистрировано не было.
Спустя 12 месяцев после проведенной операций достоверного различия в группах не получено (Табл. 4).
Среди всех наблюдаемых пациентов, летальных случаев зарегистрировано не было. Повторное экстренное вмешательство, суммарно за 12 месяцев было выполнено 3 (3%) больным: с момента предыдущего осмотра во 2-й группе был прооперирован еще один пациент. По данным КАГ, все шунты оставались проходимы, реваскуляризация не потребовалась. У 2 пациентов, по 1-му больному в каждой из групп, вновь были зарегистрированы симптомы нестабильной стенокардии. Пациентам была выполнена КАГ: у пациента из 1-й группы выявлен гемодинамически значимые рестеноз, выявлена реваскуляризация с положительной динамикой. У больного из 2-й группы был выявлен гемодинамически значимый стеноз коронарного шунта, выполнено стентирование с положительной динамикой.
У всех наблюдаемых пациентов была проведена повторная оценка качества жизни согласно опроснику
Табл. 3. Средние показатели интенсивности кровотока по коронарным шунтам по данным ультразвуковой флуометрии
|
Параметры |
2 группа n = 50 |
|
Средняя объемная скорость кровотока (Qmean или MGF), мл/ мин. |
41±3 мл/ мин. |
|
Индекс пульсации (PI) |
2,3±0,7 |
|
Процент диастолического объемного наполнения (DF), % |
72±5% |
Примечание : по данным УЗ-исследования, у всех пациентов определялся удовлетворительный кровоток по шунтам.
1 группа
График 1. Оценка качества жизни пациентов после проведенного 2-го этапа хирургического лечения в раннем послеоперационном периоде при помощи опросника MOS SF-36 (p<0,000001). У пациентов из 1 группы отмечается достоверное увеличе-ние всех анализируемых параметров: показатель PF выше на 36,5%; RP – на 36,9%; BP – на 32,5%; GH – на 22,7%; VT – на 29,6%; SF – 25%; RE – 32,6%; MH – 21,8%.
Табл. 4. Основные показатели неблагоприятных событий спустя 12 месяцев после проведенного хирургического лечения
|
Параметры |
1 группа n = 50 |
2 группа n = 50 |
Значение Р |
|
Летальный исход |
0 |
0 |
|
|
Повторное экстренное вмешательство |
1 (2%) |
2 (4%) |
р = 0,831 |
|
Повторная экстренная реваскуляризация |
1 (2%) |
0 |
р = 0,974 |
|
Вновь возникшие симптомы нестабильной стенокардии: |
1 (2%) |
1 (2%) |
р = 0,898 |
|
а) Результаты ЭКГ |
Ухудшение питания миокарда |
Ухудшение питания миокарда |
р = 0,911 |
|
б) Результаты ЭХО-КГ |
ФВ 41% |
ФВ 36% |
р = 0,455 |
|
в) Результаты ХМ-ЭКГ |
Положительная велоэргоме-трическая проба |
Положительная велоэрго-метрическая проба |
р = 0,487 |
|
Реваскуляризация после верификации ишемии |
1 (2%) |
1 (2%) |
р = 0,792 |
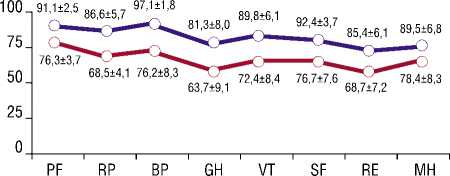
SF-36, и полученные параметры были сравнены с предыдущими показателями (График 2).
Спустя 12 месяцев пациенты в обеих группах отмечают улучшение своего самочувствия по сравнению с состоянием здоровья на момент выписки. Обращает на себя внимание более выраженная тенденция к увеличению показателей у пациентов во 2-й группе, чем в 1-й группе в сравнении с аналогичными параметрами на момент
Суковатых Б.С., Сидоров Д.В., Боломатов Н.В. и др.
ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ ГИБРИДНОГО КАРДИОХИРУРГИЧЕСКОГО ШУНТИРОВАНИЯ И ЭНДОВАСКУЛЯРНОГО СТЕНТИРОВАНИЯ ПАЦИЕНТОВ С НАСЛЕДСТВЕННОЙ ГИПЕРХОЛЕСТЕРИНЕМИЕЙ И СТЕНОКАРДИЕЙ НАПРЯЖЕНИЯ
—2— 1 группа —С— 2 группа
График 2. Сравнительный анализ качества жизни пациентов в раннем послеоперационном периоде и спустя 12 месяцев после операции при по-мощи опросника MOS SF-36 (p<0,000001). В обеих группах отмечается увеличение показателей, отражающих качество жизни больных, причем показатели пациентов из 1-й группы превышают таковые больных из 2-й группы: PF выше на 16,2%; RP – на 20,7%; BP – на 21,5%; GH – на 21,6%; VT – на 19,3%; SF – на 16,9%; RE – на 19,5%; MH – 12,4%.
выписки из стационара: показатель PF во 2-й группе увеличился на 29%, в 1-й группе – на 6,4%; RP – на 29,4 и 11,3; BP – на 15,8 и 2,1; GH – на 11,6 и 10,3; VT – на 21,1 и 9,5; SF – на 14,7 и 5,5; RE – на 23,8 и 9,1; MH – 17,9 и 8%, соответственно. Однако, несмотря на это, качество жизни пациентов из группы эндоваскулярного стентирования превышает таковое по сравнению с пациентами из группы коронарного шунтирования. Данная картина, по всей вероятности, объясняется видом перенесенной операции и особенностями периода восстановления после хирургического лечения.
Обсуждение
В настоящее время ИБС является наиболее распространенным заболеванием сердца и сосудов во всех развитых странах мира. Наиболее результативным способом улучшения прогноза больных с ИБС является реваскуляризация пораженной коронарной артерии. КШ остается золотым стандартом медицинской помощи для этой группы пациентов. Однако, технологический прогресс последних десятилетий, позволил рентгенэн-доваскулярным диагностике и лечению прочно занять свое место, как неотъемлемая помощь при лечении сердечно-сосудистых заболеваний. В настоящее время ни у кого не вызывает сомнений, что ЧКВ является методикой выбора при лечении ИБС.
Результаты нашего исследования говорят об одинаковой эффективности обоих методик реваскуляризации. Однако показатели опросника SF-36 демонстрируют более выраженное увеличение показателей качества жизни больных из группы эндоваскулярного стентирования по сравнению с аналогичными значениями у пациентов из группы кардиохирургического шунтирования, что, по всей вероятности, объясняется тяжестью открытой операции и особенностями периода восстановления.
При выполнении нашего исследования, определяя показания к тому или иному способу хирургического лечения, мы использовали шкалу SYNTAX Score. Однако, помимо преимуществ, данная шкала имеет и свои не- достатки: она содержит в себе лишь ангиографические критерии пораженной артерии (наличие извитости и/ или кальциноза артерии, протяженность поражения, наличие тромботических масс в просвете сосуда и т.д.) и совершенно не учитывает клинические характеристики больного, что самым непосредственным образом влияет как на успех реваскуляризации, так и качество жизни пациента после перенесенного оперативного лечения [18]. Принимая во внимание увеличение количества пациентов пожилого возраста с большим количеством коморбидной патологии, выбор способа оперативного лечения должен основываться не только на ангиографических критериях, но также и на клинических данных пациента [19].
В попытке нивелирования подобных недочетов, шкала Syntax Score была модифицирована, и на ее основе создана шкала Syntax Score II [20]. В нее вошли, помимо ангиографической оценки степени поражения, рассчитанного в первой версии Syntax Score, 6 клинических параметров: возраст пациента, пол, скорость клубочковой фильтрации (СКФ), фракция выброса (ФВ) ЛЖ, наличие обструктивной болезни легких (ХОБЛ) и поражения периферических артерий. Кроме того, в шкале SS II существует возможность прогнозирования возможного летального исхода в течение 4-х лет с момента выполнения как эндоваскулярной интервенции, так и открытой операции (в шкале SS I существует возможность прогнозирования риска только лишь для КШ) [21]. За последние годы в литературе появляется все больше публикаций об успешном применении шкалы риска SS II: так, C. Campos и соавт. в своей работе продемонстрировали, что SS II является более точным инструментом для выбора хирургической тактики у пациентов с трехсосудистым поражением коронарных артерий. Кроме того, было доказано соответствие заключений «Heart Team» с результатами расчета по шкале SS II [22].
Однако, на наш взгляд, не следует останавливаться на достигнутом: шкалу SS II следует и дальше развивать и совершенствовать, включать в нее новые параметры и характеристики. В частности, у пациентов с умеренным риском поражения венечных артерий (когда можно выполнить как эндоваскулярную интервенцию, так и открытую операцию) следует обговаривать с пациентами и с его родственниками все возможные риски, а также вероятность их развития при той или иной методике хирургической операции, чтобы дать возможность пациенту выбрать метод лечения, а результаты этого выбора следует указывать в качестве отдельного параметра. Кроме того следует отмечать готовность хирургической службы выполнить определенный вид вмешательства (наличие необходимых расходных материалов, уровень подготовки оперирующих хирургов и т.д.). Эти, а также ряд других параметров целесообразно использовать в последующих версия шкалы Syntax Score, что позволит улучшить качество хирургической помощи пациентам, повысит уровень жизнь больных, а само лечение сделает более пациентоориентированным.
Выводы
-
1. Основные показатели неблагоприятных событий после эндоваскулярного стентирования и КШ демонстрируют аналогичные результаты спустя 12 месяцев после проведенного хирургического лечения и пациентов с умеренной тяжестью поражения по шкале SYNTAX Score.
-
2. Спустя 12 месяцев после перенесенного хирургического лечения самочувствие пациентов достоверно лучше в группе коронарного стентирования: PF выше на 16,2%; RP – на 20,7%; BP – на 21,5%; GH – на 21,6%; VT – на 19,3%; SF – на 16,9%; RE – на 19,5%; MH – 12,4%.
-
3. Целесообразно и дальше модифицировать шкалу SYNTAX Score для полноты оценки клинического статуса пациента и выбора оптимального варианта реваскуляризации.
Список литературы Отдаленные результаты гибридного кардиохирургического шунтирования и эндоваскулярного стентирования пациентов с наследственной гиперхолестеринемией и стенокардией напряжения
- Hillis LD, Smith PK, Anderson JL, Bittl JA, Bridges CR, et al. 2011 ACCF/AHA Guideline for Coronary Artery Bypass Graft Surgery: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation. 2011; 124: e652–735. doi: 10.1161/CIR.0b013e31823c074e.
- Мамутов Р.Ш., Мавлянова Д.А., Мамараджабова Д.А. Сборник клинических протоколов по диагностике, лечению и профилактике сердечно-сосудистых заболеваний для врачей районных и городских медицинских объединений. – Ташкент, 2015.
- Кардиоваскулярная профилактика 2022. Российские национальные рекомендации. С. 8. doi: 10.15829/1560-4071-2023-5452.
- Хоролец Е.В., Шлык С.В. Возможности реперфузионной терапии пациентов с острым инфарктом миокарда // Consilium Medicum. – 2020. – Т.22. – №5. – С.87-91. doi: 10.26442/20751753.2020.5.200182.
- Holzhey DM, Jacobs S, Morchalski M, et al. Minimally invasive hybrid coronary artery revascularization. Ann. Thorac. Surg. 2008, 86, 1856-1860. doi: 10.1016/j.athoracsur.2008.08.034.
- Mohr FW, Morice MC, Kappetein AP, Feldman TE, Ståhle E, Colombo A, et al. Coronary artery bypass graft surgery versus percutaneous coronary intervention in patients with three-vessel disease and left main coronary disease: 5-year follow-up of the randomised, clinical SYNTAX trial. Lancet. 2013; 381(9867): 629-38. doi: 10.1016/S0140-6736(13)60141-5.
- Григорьев В.С., Петросян К.В., Абросимов А.В., Анатомическая шкала оценки риска SYNTAX Score – инструмент определения тяжести поражения коронарного русла и прогнозирования исходов эндоваскулярных вмешательств // Креативная кардиология. – 2019. – №13(2). doi: 10.24022/ 1997-3187-2019-13-2-159-172.
- Shuhaiber JH, Evans AN, Massad MG, Geha AS. Mechanisms and future directions for prevention of vein graft failure in coronary bypass surgery. European Journal of Cardiothoracic Surgery. 2002; 22: 387-396. doi: 10.1016/s10107940(02)002531.
- Ежов М.В., Сергиенко И.В., Рожкова Т.А. и соавт. Российские рекомендации по диагностике и лечению семейной гиперхолестеринемии // Атеросклероз и дислипидемии. – 2016. – №4. – С.21-29. doi: 10.20969/ВСКМ.2017.10(2).72-79.
- Кухарчук В.В., Малышев П.П., Мешков А.Н. Семейная гиперхолестеринемия: современные аспекты диагностики, профилактики и терапии // Кардиология. – 2009. – №49(1). – С.76-83. doi: 10.1161/ATVBAHA.113.301218.
- Catapano AL, Graham I, De Backer G, et al. ESC/EAS Guidelines for the Management of Dyslipidaemias: The Task Force for the Management of Dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS) Developed with the special contribution of the European Assocciation for Cardiovascular Prevention & Rehabilitation (EACPR). Eur Heart J 2016. doi: 10.1093/eurheartj/ehz455.
- Ware JE, Snow KK, Kosinski M, Gandek B. SF-36 Health Survey. Manual and interpretation guide. The Health Institute, New England Medical Center. Boston, Mass. 1993.
- Ware JE, Kosinski M, Keller SD. SF-36 Physical and Mental Health Summary Scales: A User`s Manual. The Health Institute, New England Medical Center. Boston, Mass. 1994.
- Ershova AI, Meshkov AN, Bazhan SS, et al. The prevalence of familial hypercholesterolemia in the West Siberian region of the Russian federation: A substudy of the ESSE-RF. PLoS One. 2017; 12(7): 1-10. doi: 10.1371/ journal.pone.0181148.
- Sturm AC, Knowles JW, Gidding SS, et al. Clinical Genetic Testing for Familial Hypercholesterolemia: JACC Scientific Expert Panel. J Am Coll Cardiol. 2018; 72(6): 662-80. doi: 10.1016/j.jacc.2018.05.044.
- Потеев М.А., Якубов Р.А. Интраоперационный менеджмент при коронарном шунтировании: флоуметрия как способ контроля качества // Практическая медицина. – 2017. – №4(105). – С.15-20.
- Недошивин А.О., Кутузова А.Э., Петрова Н.Н. и др. Исследование качества жизни и психологического статуса больных с хронической сердечной недостаточностью // Сердечная недостаточность. – 2000. – Т.1. – №4.
- Thuijs D, Kappetein AP, Serruys PW, et. al. Percutaneous coronary intervention versus coronary artery bypass grafting in patients with three-vessel or left main coronary artery disease: 10-year follow-up of the multicentre randomised controlled SYNTAX trial// Lancet (London, England). 2020; 394(10206): 1325-1334. doi: 10. 1016/S0140-6736(19)31997-X.
- Takahashi K, Serruys PW, Fuster V, et al. Redevelopment and validation of the SYNTAX score II to individualise decision making between percutaneous and surgical revascularisation in patients with complex coronary artery disease: secondary analysis of the multicentre randomised controlled SYNTAXES trial with external cohort validation. Lancet. 2020; 396: 1399-1412. doi: 10.1016/S0140-6736(20)32114-0.
- Farooq V, van Klaveren D, Steyerberg EW, et.al. Anatomical and clinical characteristics to guide decision making between coronary artery bypass surgery and percutaneous coronary intervention for individual patients: development and validation of SYNTAX score II. The Lancet. 2013; 381 (9867): 639-650. doi: 10.1016/S0140-6736(13)60108-7.
- Алекян Б.Г., Карапетян Н.Г., Кравченко В.В. и др. Роль шкалы SYNTAX Score II в принятия решений «сердечной командой» о методе лечения пациентов со сложными поражениями коронарных артерий. Обзор литературы // Кардиологический вестник. – 2019. – №3(14). – С.17. doi: 10.36396/Ms. 2019.14.03.003.
- Campos CM, Stanetic BM, Farooq V, Walsh S, et al. Risk stratification in 3 vessel coronary artery disease: Applying the SYNTAX Score II in the Heart Team Discussion of the SYNTAX II trial. Catheterization and Cardiovascular Interventions. 2015; 86(6): е229-е238. doi: 10.1002/ccd.25907.


