Отдаленные результаты лечения пациентов с переломами позвонков в шейном отделе позвоночника с применением коралл-основанного остеозамещающего материала «BoneMedik-s»
Автор: Аганесов А.Г., Хейло А.Л., Микаелян К.П., Галян Т.Н., Постников Юрий Владимирович
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.10, 2015 года.
Бесплатный доступ
Представлены ближайшие и отдаленные результаты хирургического лечения 39 пациентов с переломами шейного отдела позвоночника с применением кораллоснованного остеозамещающего материала, проведенного с 2010 по 2012 годы, период наблюдения составил от 2,8 до 4 лет. Пациентам после проведения декомпрессивного этапа операции осуществлялось заполнение дефекта костной ткани остеозамещающим материалом, фиксация пластиной. Для оценки остеоинтеграции и деградации использованного материала применялась компьютерная томография. Во всех случаях нами наблюдался плотный контакт реципиент-кость, плотность костной ткани в зоне контакта соответствовала критериям выраженной остеоинтеграции (разница плотности кости в зоне контакта имплантат-кость составляла 3-7%), отсутствовали зоны просветления в местах контакта имплантат-кость, однако при длительном наблюдении (в среднем 3,2 года) у пациентов не было обнаружено полной деградации материала.
Остеозамещаюшие материалы, хирургия позвоночника, спинальная травма, спондилодез, плотность костной ткани, коралл-основанные материалы
Короткий адрес: https://sciup.org/140188488
IDR: 140188488 | УДК: 616.711.8-001.5:616-089.819.843-079.7
Long-term results of treatment of patients with fractures of cervical spine vertebrae with the use of coral-based bone substitute material «BoneMedik-s»
This study represents short- and long-term results of surgical treatment of 39 patients with fractures of cervical spine vertebrae with the use of coral-based bone substitute material, performed between 2010 and 2012. Mean observation time was 3,2 years (2.8-4.0). During the surgery, after decompression of spinal cord, bony defect has been filled with bone substitute material, and then bones have been fixated with metal plate. Computer tomography was used to evaluate osseointegration and biodegradation. In every case we have observed tight donor-recipient bone contact, bone density in contact zone matched the criteria of marked osseointegration ( difference between density in contact zone and appropriate zone of adjacent vertebrae was 3-7%), there were no zones of clarification between bone and substitute material, but even after long-term observation we could not mark full biodegradation of this material.
Текст научной статьи Отдаленные результаты лечения пациентов с переломами позвонков в шейном отделе позвоночника с применением коралл-основанного остеозамещающего материала «BoneMedik-s»
Ежегодно в мире проводится более 2 млн операций с применением костной пластики, что является второй по частоте операцией по пересадке тканей после переливания компонентов крови[12]. В настоящее время стандартом для подобных вмешательств считается применение аутокости. Но существуют некоторые ограничения: объем материала и требования к его механической прочности. Более того взятие аутокости связано с несколькими осложнениями: болезненность в области забора, косметические дефекты, гематомы, инфекция, переломы донорской кости, повреждение нервов и артерий [3]. Иногда использовать собственный материал пациента не представляется возможным ввиду возраста пациента или сопутствующей патологии. Поэтому врачи все чаще отходят от ее применения и ищут другие материалы для трансплантации.
Существует несколько вариантов замены аутокости: аллотрансплантаты, ксенотрансплантаты, синтетические полимеры, биоорганические материалы, керамические заменители костной ткани, композитные материалы [9].
Идеальный остеозамещающий материал должен обладать остеоиндуктивными и остеокондуктивнами свойствами, не только замещать собой кость, но и интегрироваться в кость реципиента [5, 8]. Способность материалов к подобным процессам определяется их физико-химическими свойствами, биоактивностью или биоинертностью, то есть способностью материала сохранять постоянство своей структуры и состава[5]. Для усиления остеоиндуктивных свойств материала часто применяется обогащение костными морфогенными белками (BMP-2, BMP-7) и иными факторами роста, стволовыми клетками [2, 9]. Кроме того, поскольку остеозамещающие материалы должны находиться в теле реципиента длительное время, необходимо чтобы они не вызывали иммунного ответа [7].
Всем этим требованиям отвечает аутокость, но в свете указанных выше ограничений, применяются и иные способы заполнения дефектов.
Аллотрансплантаты, как правило, обладают высокой прочностью и остеокондуктивностью, но слабыми остео-индуктивными свойствами в связи со способами обработки и подготовки к внедрению в место дефекта. Кроме того они крайне медленно остеоинтегрируются, и при их использовании существует риск заражения реципиента некоторыми заболеваниями донора, реакции отторжения трансплантата, хронического гранулематозного воспаления [13, 16].
В качестве ксенотрансплантатов применяют свиную или коровью кость, кораллы [9]. В настоящий момент данные по использованию ксенотрансплантатов противоречивы, хотя некоторые исследователи сообщали

Аганесов А.Г., Хейло А.Л., Микаелян К.П., Галян Т.Н., Постников Ю.В.
ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ПЕРЕЛОМАМИ ПОЗВОНКОВ В ШЕЙНОМ ОТДЕЛЕ ПОЗВОНОЧНИКА С ПРИМЕНЕНИЕМ КОРАЛЛ-ОСНОВАННОГО ОСТЕОЗАМЕЩАЮЩЕГО МАТЕРИАЛА «BONEMEDIK-S»
о хороших результатах, в клинической практике такие имплантаты применяются редко в связи с опасениями передачи человеку зоонозных инфекций (свиного эндогенного ретровируса или коровьей губчатой энцефалопатии) [8, 15, 16].
Синтетические остеозамещающие материалы, такие как полилактат, полиактид-полигликолид, полиметилметакрилат и иные в настоящее время используются в основном как дополнительные материалы, позволяющие увеличить размер трансплантата [18]. В чистом виде не обладают остеоиндуктивными свойствами; имеют минимальные способности к деградации. Также они применяются для вертебропластики при остеопорозе или опухолевом поражении позвонков [17].
Биоорганические материалы, например, деминерализованный костный матрикс, как правило, обладают хорошими остеоиндуктивными свойствами, но недостаточной механической прочностью. Поэтому его применяют либо как наполнитель, либо вместе с дополнительным материалом (сульфатом кальция и др.) [9].
Керамические остеозамещающие материалы представляют собой смесь из гидроксиапатита и трикальций фосфата. Гидроксиапатит является относительно инертным веществом, которое резорбируется крайне медленно, трикальций фосфат, наоборот, резорбируется в среднем в течение 6 недель. Как правило, керамические имплантаты содержат оба варианта этих фосфатов кальция в соотоношении от 4:6 до 6:4 [9]. Эти материалы широко применяются в современной практике и доступны в виде мелкодисперсных порошков, гранулятов и блоков [2].
Коралл-основанные материалы преимущественно состоят из карбонатов и фторидов кальция, в отличие от человеческой кости, в основном состоящей из гидроксиапатита, фосфатов и карбонатов кальция, однако такая форма легко резорбируется организмом [9]. Для изменения состава таких трансплантатов применяют гидротермическую обработку, в результате получают не-резорбируемый трансплантат с гидроксиапатитом [11]. Некоторые исследователи сообщают об обнадеживающих результатах в раннем послеоперационном периоде [1].
На сегодняшний день наиболее актуальной теорией остеоинтеграции является теория ретракции кровяного свёртка. Процесс остеоинтеграции имплантата состоит из трех стадий:
– остеокондукция, заключающаяся в привлечении и миграции остеобластов на поверхность имплантата, через остаток кровяного свёртка, сформированного вокруг имплантата;
– минерализация костного матрикса, заключающаяся в инициировании образования костного матрикса. В этой фазе параллельно протекают процессы контактного и дистантного остеогенеза;
– ремоделирование кости: длительный процесс, са-моподдерживающийся циклами резорбции и образования кости, стабилизация которого достигается приблизительно через 18 месяцев после операции.
Оптимальным исследованием, показывающим остеоинтеграцию имплантата, является рентгеновская компьютерная томография, так как она обеспечивает возможность проведения точных измерений, позволяет оценить область имплантации в 3-х проекциях: аксиальной, фронтальной и сагиттальной, дает возможность определить плотность костной ткани [4].
Материалы и методы
В клинике с 2010 по 2012 год было проведено 40 оперативных вмешательств, направленных на достижение спондилодеза у пациентов с различными травмами шейного отдела позвоночника. В качестве остеокондуктивного материала был применен препарат «Bonemedik-S» в виде блоков. Он представляет собой ко-ралл-основанный трабекулярный (поры размером около 400 мкм) гидроксиапатитовый (не менее 95%) остеозамещающий материал с небольшим (до 1%) включением кремния в состав, применяемый для заполнения дефектов костной ткани. Средний возраст пациента составил 40 лет (24–73), среднее время наблюдения составило 3,2 года (от 2,3 до 4-х лет). Все пациенты были разделены на несколько групп: мужчины (25 человек) и женщины (15 человек), и пациенты в возрасте до 45 (20 и 5, соответственно) и после 45 лет (5 и 10, соответственно). В дальнейшем 1-го пациента из группы мужчин после 45 лет были вынуждены исключить в связи с тем, что в раннем послеоперационном периоде пациент упал, произошла миграция пластины, и пациенту было выполнено повторное вмешательство с переустановкой фиксатора и заменой остеозаменителя. Для рентгенологической оценки деградации материала и его биоинтеграции применена компьютерная томография.
Большинство пациентов оперировались по поводу осложненных переломов в шейном отделе позвоночника со стенозом позвоночного канала до 30%, сопровождаемым неврологическим дефицитом и мышечно-тоническим синдромом. Для лечения выбрано оперативное вмешательство, направленное на декомпрессию позвоночного канала, установку коралл-основанного остеозамещающего материала в месте дефекта после корпор- или дискэктомии, достижение переднего спондилодеза с фиксацией пластиной. В раннем послеоперационном периоде у всех пациентов отмечено облегчение или купирование симптоматики. Средняя продолжительность койко-дня составила 7 ± 3 дней у всех групп пациентов.
Осложнений, связанных с оперативным вмешательством или остеозамещающим материалом, отмечено не было. Средняя продолжительность наблюдения составила 3,2 года.( от 2,8 до 4,02) (табл. 1). Пациентам проводилось рентгенологическое обследование через 6 недель, 6 и 12 месяцев, два года спустя и далее каждый год КТ.
На компьютерных томограммах всех пациентов (рис. 1) наблюдалась картина частичной деградации материала и качественной остеоинтеграции (рис. 1, 2, 3).

Аганесов А.Г., Хейло А.Л., Микаелян К.П., Галян Т.Н., Постников Ю.В.
ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ПЕРЕЛОМАМИ ПОЗВОНКОВ В ШЕЙНОМ ОТДЕЛЕ ПОЗВОНОЧНИКА С ПРИМЕНЕНИЕМ КОРАЛЛ-ОСНОВАННОГО ОСТЕОЗАМЕЩАЮЩЕГО МАТЕРИАЛА «BONEMEDIK-S»
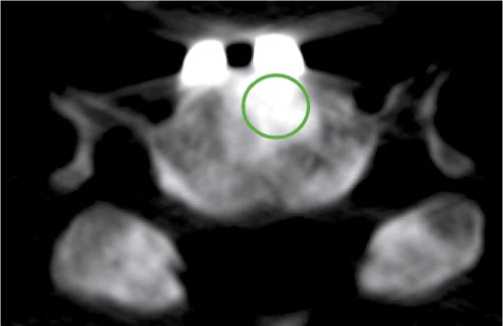
Рис. 1. Женщина 46 лет, 2,9 лет с момента операции. Аксиальный срез. Кругом обведена зона имплантации. На снимке видны четкие границы имплантата, различие в рентгенологической плотности имплантата и нативной кости
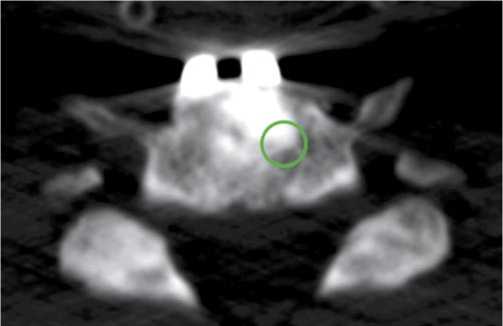
Рис. 2. Женщина 46 лет, 2,9 лет с момента операции. Аксиальный срез. Зона контакта имплантата и кости реципиента. Виден плотный контакт остеозамещающего материала и ткани реципиента, отсутствие просветлений по всем периметру имплантата
Tабл. 1. Распределение пациентов по группам
|
Пол |
Мужчины |
Женщины |
||
|
возраст (год) |
< 45 |
> 45 |
< 45 |
> 45 |
|
Срок наблюдения (год) |
3,04 ± 0,37 |
3,63 ± 0,39 |
2,82 ± 0,33 |
3,21 ± 0,34 |
Tабл. 2. Распределение костной плотности по группам
|
Пол |
Мужчины |
Женщины |
||
|
возраст (год) |
< 45 |
> 45 |
< 45 |
> 45 |
|
Плотность костной ткани в месте имплантации (HU) |
969 ± 335 |
820 ± 221 |
821 ± 209 |
837 ± 235 |
|
Плотность костной ткани в зоне контакта имплантат-кость(HU) |
580 ± 177 |
595 ± 181 |
576 ± 176 |
540 ± 168 |
|
Плотность костной ткани в соседнем позвонке (имплантационная зона)(HU) |
532 ± 162 |
547 ± 180 |
530 ± 166 |
487 ± 155 |
|
Плотность костной ткани в соседнем позвонке (зона контакта имлпнатат-кость)(HU) |
540 ± 168 |
560 ± 187 |
556 ± 237 |
509 ± 161 |
|
Разница HU (%) (имплантат) |
82 % |
50 % |
55 % |
71 % |
|
Разница HU (%) (зона контакта имплантат-кость) |
7 % |
6 % |
3 % |
6 % |
Для оценки остеоинтеграции плотность костной ткани в зоне контакта имплантат-реципиент сравнивалась с плотностью костной ткани аналогичной области соседнего позвонка, определялось соответствие критериям остеоинтеграции: определяется четкий контакт имплантата с костью реципиента, отсутствие просветлений в зоне перехода имплантат-реципиент диаметром болee 2 мм [4]. Для оценки деградации имплантированного остеозамещающего материала сравнивалась плотность ткани
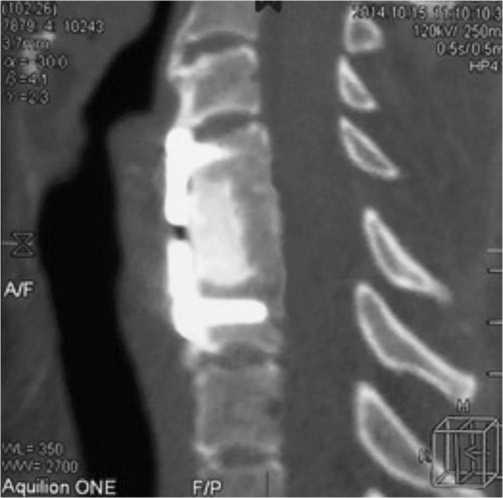
Рис. 3. Женщина 46 лет, 2,9 лет с момента операции. Сагиттальный срез. На снимке четко видно положение имплантата в кости пациента, различие в плотности нативной кости и остеозамещающего материала в области установленного имплантата и аналогичной области соседнего позвонка.
Так как в литературе нами не было обнаружено четких критериев перестройки имплантированного материала, было решено принять отличие плотности костной ткани в месте имплантации до 30% за выраженную деградацию, от 30 до 49% за удовлетворительно выраженные процессы деградации, и более 50% за низкую степень деградации.
В результате исследования нами получены следующие данные (табл. 2). Данные костной плотности измерены в единицах Хаунсфилда, представлены средние значения с квадратичными отклонениями в каждой группе.

Аганесов А.Г., Хейло А.Л., Микаелян К.П., Галян Т.Н., Постников Ю.В.
ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ПЕРЕЛОМАМИ ПОЗВОНКОВ В ШЕЙНОМ ОТДЕЛЕ ПОЗВОНОЧНИКА С ПРИМЕНЕНИЕМ КОРАЛЛ-ОСНОВАННОГО ОСТЕОЗАМЕЩАЮЩЕГО МАТЕРИАЛА «BONEMEDIK-S»
Выводы
В зоне контакта имлантат-кость нами не было отмечено случаев остеолиза, склерозирования контактной поверхности кости реципиента, миграции имплантатов. При длительном наблюдении (в среднем 3,2 года, от 2,8 до 4) у пациентов не было обнаружено полной деградации материала.
Во всех наблюдениях был обнаружен плотный контакт реципиент-кость, плотность костной ткани в зоне контакта соответствовала критериям выраженной остеоинтеграции (разница плотности кости в зоне контакта имплантат-кость составляла 3–7%).
У всех больных после декомпрессивного этапа и установки остеозамещающего материала был достигнут спондилодез. За все время исследования (от 2,8 до 4 лет) не возникло осложнений, связанных с оперативным вмешательством или с остеозамещающим материалом.
Применение материала на основе коралла «Bonemedik-S» для замещения костных дефектов при оперативных вмешательствах на шейном отделе позвоночника эффективно и безопасно.
Список литературы Отдаленные результаты лечения пациентов с переломами позвонков в шейном отделе позвоночника с применением коралл-основанного остеозамещающего материала «BoneMedik-s»
- Аганесов А.Г., Месхи К.Т. Современный синтетический заменитель костной ткани в хирургии шейного отдела позвоночника. Журнал Вестник Травматологии и Ортопедии им. Н.Н. Приорова, 2012, №2, С. 16-19.
- Ардашев И.П. Современное состояние вопроса о костнопластических материалах, стимулирующих остеогенез./И.П. Ардашев, С.В. Черницов, И.Ю. Веретельникова, А.А. Гришанов, М.С. Шпаковский.//Вестник новых медицинских технологий. -2011. -Т. XVIII, №4. -C. 161-165.
- Берченко Г.Н. Синтетические кальций-фосфатные материалы в травматологии и ортопедии, «Применение искусственных кальциево-фосфатных биоматериалов в травматологии и ортопедии» сборник работ Всероссийской научно-практической конференции. М., 2010. -С. 3-5.
- Воробьев А.А., Шемонаев В.И., Михальченко Д.В., Величко А.С. Современные методы оценки остеоинтеграции дентальных внутрикостных имплантатов (литературный обзор)//Актуальные вопросы экспериментальной, клинической и профилактической стоматологии: сборник научных трудов Волгоградского государственного медицинского университета. -Волгоград: ООО «Бланк», 2008. (Выпуск № 1, Т. 65).
- Кирилова И.А. Различные виды костно-пластических материалов для восстановления костной структуры/И.А. Кирилова, В.Т. Подорожная, И.П. Ардашев, С.В. Черницов//Политравма. -№4. -2008. -С. 60-64.
- Кирилова И.А. Новые виды материалов для костной палстики в свете современных представлений о костных трансплантатах/И.А. Кирилова, Н.Г. Фомичев, В.Т. Подорожная. Хирургия позвоночника. -2007. -№2. -С. 66-70.
- Корж Н.А. Роль биологической фиксации и остеоинтеграции в реконструкции кости. Н.А. Корж, Д.А. Кладченко, С.В. Малышкин.//Ортопедия, травматология и протезирование. -2005. -№4. -С. 118-127.
- Окропиридзе Г.Г. Оценка антимикробной активности биокомпозиционных материалов. Г.Г. Окропиридзе, Т.Я. Пхакадзе. Биоматериалы. -2005. -№3. -С. 2-3.
- Campana V. Bone substitutes in orthopaedic surgery: from basic science to clinical practice/V. Campana, G. Milano • E. Pagano, M. Barba, C. Cicione, G. Salonna, W. Lattanzi, G. Logroscino//J Mater Sci: Mater Med (2014) 25: 2445-2461.
- Charalambides C., Beer M., Cobb A.G. Poor results after augmenting autograft with xenograft (Surgibone) in hip revision surgery: a report of 27 cases. Acta Orthop. 2005; 76(4): 544-9.
- Dumitrescu A.L. Bone grafts and bone graft substitutes in periodontal therapy. In: Chemicals in surgical periodontal therapy. Berlin: Springer; 2011. p. 92.
- Faour O., Dimitriou R., Cousins C.A., Giannoudis P.V. The use of bone graft substitutes in large cancellous voids: any specific needs? Injury. 2011; 42(Suppl 2): 87-90.
- Khan SN, Cammisa FPJ, Sandhu HS, Diwan AD, Girardi FP, Lane JM. The biology of bone grafting. J Am Acad Orthop Surg. 2005; 13(1): 77-86.
- Laurencin CT, El-Amin SF. Xenotransplantation in orthopaedic surgery. J Am Acad Orthop Surg. 2008;16(1):4-8.
- Lofgren H, Johannsson V, Olsson T, Ryd L, Levander B. Rigid fusion after cloward operation for cervical disc disease using autograft, allograft, or xenograft: a randomized study with radiostereometric and clinical follow-up assessment. Spine. 2000; 25(15): 1908.
- Manyalich M, Navarro A, Koller J, Loty B, de Guerra A, Cornu O, Vabels G, Fornasari P, Costa A, Siska I, et al. European quality system for tissue banking. Transplant Proc. 2009; 41(6): 2035-43.
- Nandi SK, Roy S, Mukherjee P, Kundu B. Orthopaedic applications of bone graft & graft substitutes: a review. Indian J Med Res. 2010; 132: 15-30.
- Palussie're J, Berge J, Gangi A, et al. Clinical results of an open prospective study of a bis-GMA composite in percutaneous vertebral augmentation. Eur Spine J. 2005; 14: 982-91.


