Отдаленные результаты различных методов реваскуляризации при острой ишемии конечности у пациентов с COVID-19
Автор: Никольский А.В., Кравчук В.Н., Трофимов Н.А., Мухин А.С., Волков Д.В., Никольский В.О., Жидков И.М., Баженова К.И.
Журнал: Московский хирургический журнал @mossj
Рубрика: Сердечно-сосудистая хирургия
Статья в выпуске: 3 (89), 2024 года.
Бесплатный доступ
Введение. Острая ишемия конечностей (ОИК) у пациентов с COVID-19 представляет собой серьезное осложнение с высоким риском потери конечности и смертности. Несмотря на растущее количество исследований, посвященных этой проблеме, отсутствует консенсус относительно оптимальной стратегии реваскуляризации. Целью данного исследования было сравнение отдаленных результатов открытых и эндоваскулярных вмешательств при ОИК у пациентов с COVID-19.Материалы и методы. В исследование были включены 257 пациентов с ОИК IIA-IIb класса по Резерфорду, госпитализированные в период с 1 января 2018 г. по 20 июня 2023 г. Пациенты были разделены на четыре группы: I (n=50) и II (n=50) - контрольные, без COVID-19; III (n=86) и IV (n=71) - с COVID-19. В I и III группах выполнялась открытая реваскуляризация, во II и IV - эндоваскулярная с катетеруправляемым селективным тромболизисом. Проходимость реконструированных артерий оценивалась через 6-12 месяцев после операции с помощью УЗДГ и КТ-ангиографии.Результаты. Частота поздних ретромбозов составила 41,3 % в группах открытой реваскуляризации и 33,3 % в группах эндоваскулярного лечения. У пациентов с COVID-19 после открытых операций рецидив ОИК наблюдался в 2 раза чаще (8,7 % против 4,4 %). Развитие хронической ишемии III-IV класса по Резерфорду было более характерно для пациентов после открытых вмешательств (17,6 % против 7,3 %).Заключение. Эндоваскулярная реваскуляризация с катетеруправляемым селективным тромболизисом при ОИК у пациентов с COVID-19 ассоциирована с меньшей частотой рецидивов острой ишемии и развития хронической артериальной недостаточности в отдаленном периоде по сравнению с открытыми операциями и является оптимальной стратегии реваскуляризации у данной группы больных.
Covid-19, острая ишемия нижних конечностей, реваскуляризация, открытая хирургия, эндоваскулярные вмешательства, отдаленные результаты
Короткий адрес: https://sciup.org/142242568
IDR: 142242568 | УДК: 616.13-004.6-089-06:578.834.1 | DOI: 10.17238/2072-3180-2024-3-73-82
Long-term results of various revascularization methods in acute limb ischemia in patients with COVID-19
Introduction. Acute limb ischemia in patients with COVID-19 is a serious complication with a high risk of limb loss and mortality. Despite the growing number of studies devoted to this problem, there is no consensus on the optimal revascularization strategy. The purpose of this study was to compare the long-term results of open and endovascular interventions in patients with acute limb ischemia in acute stage of COVID-19.Methods. Study included 257 patients with acute limb ischemia IIA-IIB class Rutherford, hospitalized in the period from 01.01.2018 to 20.06.2023. The patients were divided into four groups: I (n=50) and II (n=50) - controls without COVID-19; III (n=86) and IV (n=71) - with COVID-19. Open revascularization was performed in groups I and III, and endovascular revascularization with catheter-directed selective thrombolysis was performed in groups II and IV. Patency of the reconstructed arteries was assessed 6-12 months after surgery using ultrasound and CT angiography.Results. The incidence of late retrombosis was 41,3 % in the open revascularization groups and 33,3 % in the endovascular treatment groups. In patients with COVID-19, after open surgery, recurrence of acute limb ischemia was observed 2 times more often (8,7 % vs. 4,4 %), but the overall frequency of retrombosis was comparable. The development of stage III-IV chronic ischemia (Rutherford) was more typical for patients after open interventions (17,6 % vs. 7,3 %).Conclusions. Endovascular revascularization with catheter-directed selective thrombolysis for acute ischemia in patients with COVID-19 is associated with a lower incidence of recurrent acute ischemia and the development of chronic arterial insufficiency in the long term compared to open surgery and is the optimal revascularization strategy in this group of patients.
Текст научной статьи Отдаленные результаты различных методов реваскуляризации при острой ишемии конечности у пациентов с COVID-19
Пандемия COVID-19 поставила перед медицинским сообществом новые вызовы, связанные с разнообразными клиническими проявлениями вирусной инфекции. Помимо доминирующего поражения дыхательной системы, у пациентов с тяжелым течением COVID-19 нередко развиваются тромботические осложнения, в том числе острая ишемия нижних конечностей (ОИК) [1]. По данным ряда исследований, частота ОИК у госпитализи- рованных пациентов с COVID-19 варьирует от 1 % до 5,4 % [2, 3]. При этом летальность в данной группе превышает 40 %, а риск ампутации конечности – 25,7 % [4]. Столь неблагоприятные исходы во многом обусловлены гиперкоагуляционным состоянием, ассоциированным с системным воспалительным ответом и эндотелиальной дисфункцией [5].
Несмотря на растущее количество публикаций, посвященных проблеме ОИК при COVID-19, в литературе отсутствует единое мнение относительно оптимальной стратегии реваскуляриза- ции. Ряд авторов отдают предпочтение открытым операциям, аргументируя это необходимостью быстрого восстановления кровотока и высоким риском периоперационных осложнений при эндоваскулярных вмешательствах [6, 7]. Другие исследователи подчеркивают преимущества малоинвазивных методик, позволяющих минимизировать хирургическую травму и избежать общей анестезии [8, 9]. Bellosta et al. в своем ретроспективном исследовании 20 пациентов с COVID-19 и ОИК не выявили значимых различий в выживаемости и сохранении конечности между группами открытого и эндоваскулярного лечения [10]. В то же время, Gomez-Arbelaez et al. на выборке из 41 пациента продемонстрировали лучшие результаты при использовании эндоваскулярного подхода [11].
Важно отметить, что большинство опубликованных работ фокусируется на непосредственных исходах реваскуляризации, в то время как отдаленные результаты остаются малоизученными. Единичные исследования свидетельствуют о высокой частоте ретромбозов и повторных вмешательств в течение первого года после операции [12, 13]. Учитывая специфику патогенеза ОИК при COVID-19, представляется актуальным сравнительный анализ отдаленной эффективности различных методов восстановления кровотока.
Целью настоящего исследования было сравнение отдаленных результатов открытых и эндоваскулярных вмешательств при острой ишемии конечности у пациентов с COVID-19. В задачи работы входила оценка проходимости реконструированных артериальных сегментов, частоты рецидивов острой ишемии и развития хронической артериальной недостаточности в период до 12 месяцев после операции.
Материалы и методы
В исследование были включены 257 пациентов с острой ишемией нижних конечностей IIA–IIB класса по Резерфорду, госпитализированные с 1 января 2018 г по 20 июня 2023 г. в ГБУЗ НО «Городская клиническая больница № 5 Нижегородского района г. Нижнего Новгорода» перепрофилированной в специализированный хирургический Ковид-госпиталь с 14.04.2020 года по 20.06.2023, и на базе БУ «Республиканский кардиологический диспансер» г. Чебоксары, так же, перепрофилированного в Ковид-госпиталь со специализированной сердечно-сосудистой хирургической помощью с 1.01.2021 г по 1.03.2022 г. Все пациенты были разделены на четыре группы: I (n=50) и II группы (n=50) – контрольные, без коронавирусной инфекции COVID-19; III (n=86) и IV (n=71) группы – с подтвержденным диагнозом COVID-19 в острой стадии.
В качестве метода реваскуляризации в I и III группах использовались открытые операции: тромбоэмболэктомия, пластика артерий, эндартерэктомия, шунтирующие операции. Во II и IV группах выполнялись эндоваскулярные вмешательства: прово- дниковая реканализация и баллонная ангиопластика артерий в сочетании с селективным катетеруправляемым тромболизисом тканевым активатором плазминогена альтеплазой.
В послеоперационном периоде в течении 12 месяцев все пациенты получали рекомендованную антитромботическую терапию.
Оценка проходимости реконструированных артериальных сегментов проводилась через 6 и 12 месяцев после вмешательства с помощью ультразвукового дуплексного сканирования (УЗДГ) и мультиспиральной компьютерно-томографической ангиографии (МСКТ-АГ). Первичными конечными точками были частота ретромбозов оперированной артерии и рецидивов острой ишемии. В качестве вторичных исходов оценивались частота развития хронической артериальной недостаточности IIБ стадии и потребность в повторных реваскуляризациях.
Статистическую обработку данных проводили с использованием программной среды «R». Количественные показатели представлены в виде медианых и межквартильного интервала (Ме [25 %; 75 %]), качественные – в виде абсолютных и относительных частот. Для сравнения групп применяли U-критерий Манна-Уитни и точный тест Фишера. Различия считали статистически значимыми при p<0,05.
Результаты
В ходе анализа данных 257 пациентов с ОИК были получены следующие результаты. Медиана возраста в общей выборке составила 68 [62; 75] лет, преобладали мужчины (64,2 %). Группы были сопоставимы по основным демографическим и клиническим характеристикам, за исключением более высокой частоты дыхательной недостаточности у пациентов с COVID-19 (65,6 % против 8,0 %, p=0,002). Медиана времени от начала симптомов ОИК до реваскуляризации составила 28 [6; 36] часов без значимых различий между группами (p=0,284).
Непосредственный технический успех вмешательства был достигнут у 92,4 % пациентов в группе открытых операций и у 95,0 % в группе эндоваскулярного лечения (p=0,211). На госпитальном этапе в группах с COVID-19 наблюдалась значительно более высокая летальность (56,7 % против 11,0 %, p=0,001) и частота больших ампутаций (20,4 % против 14,0 %, p=0,045) по сравнению с контролем. При этом различия между открытыми и эндоваскулярными вмешательствами были статистически значимы (p>0,02) в пользу эндоваскулярной реваскуляризации.
Отдаленные результаты прослежены у 115 (73,2 %) пациентов, медиана наблюдения составила 9 [7; 12] месяцев. Общая проходимость реконструированных артериальных сегментов через 6 и 12 месяцев была выше после эндоваскулярных операций: 65,2% против 72,4 % (p=0,048) и 58,7 % против 66,6 % (p=0,031) соответственно (табл. 1) (рис. 1).
Таблица 1
Проходимость реконструированных артерий в отдаленном периоде
Table 1
Patency of reconstructed arteries in the long-term period
|
Период Period |
Открытые операции, % (n/N) Open surgeries, % (n/N) |
Эндоваскулярные операции, % (n/N) Endovascular surgeries, % (n/N) |
p |
|
6 мес. 6 months |
65,2 (30/46) |
72,4 (50/69) |
0,048 |
|
12 мес. 12 months |
58,7 (27/46) |
66,6 (46/69) |
0,031 |
Частота ретромбозов оперированной артерии в контрольной когорте составила 16,4 %, достоверно не различаясь между открытыми и эндоваскулярными вмешательствами (p=0,187).
Однако у пациентов с COVID-19 в анамнезе, после открытых операций рецидив ОИК наблюдался в 2 раза чаще, чем после эндоваскулярного лечения (8,7 % против 4,4 %, p=0,047). При многофакторном регрессионном анализе независимыми предикторами ретромбоза были: поливалентная этиология артериального тромбоза (не эмболия, не атеросклероз) (ОШ 2,12; 95 % ДИ 1,28–,51; p=0,009), открытый характер вмешательства (ОШ 1,84; 95% ДИ 1,11–3,04; p=0,026) и возраст (≥ 75 лет) (ОШ 2,34; 95 % ДИ 1,41–3,89; p=0,012) (табл. 2) (рис. 2).
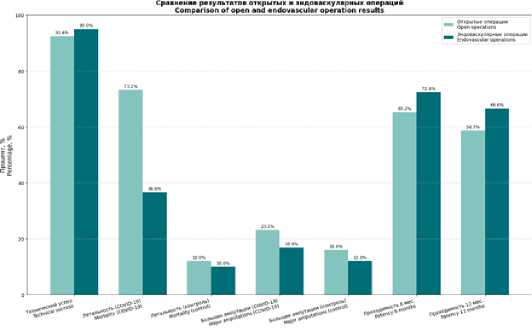
Рис. 1. Сравнение проходимости артерий и частоты осложнений
Fig. 1. Comparison of arterial patency and complication rate
Развитие хронической ишемии III–IV класса по Резерфорду в течение года после вмешательства было отмечено у 12,3 % пациентов, значимо чаще в группах открытой реваскуляризации (17,6 % против 7,3 %, p=0,037). При этом у больных с COVID-19 в анамнезе данное осложнение регистрировалось чаще, чем в контроле (14,2 % против 8,9 %, p=0,043).
Таблица 2
Предикторы ретромбоза оперированной артерии по данным многофакторного анализа
Table 2
Predictors of thrombosis of the operated artery according to multivariate analysis
|
Фактор Factor |
Однофакторный анализ Univariate analysis |
p |
Многофакторный анализ Multivariate analysis |
p |
|
ОШ (95 % ДИ) OR (95 % CI) |
ОШ (95 % ДИ) OR (95 % CI) |
|||
|
Поливалентная этиология тромбоза (не эмболия, не атеросклероз) Polyvalent etiology of thrombosis (not embolism, not atherosclerosis) |
2,34 (1,43–3,82) |
0,005 |
2,12 (1,28–3,51) |
0,009 |
|
Открытое вмешательство Open intervention |
1,96 (1,21–3,18) |
0,017 |
1,84 (1,11–3,04) |
0,026 |
|
Возраст ≥ 75 лет Age ≥ 75 years |
2,69 (1,65–4,39) |
0,007 |
2,34 (1,41–3,89) |
0,012 |
|
Сахарный диабет Diabetes mellitus |
1,88 (1,14–3,11) |
0,023 |
1,62 (0,97–2,73) |
0,071 |
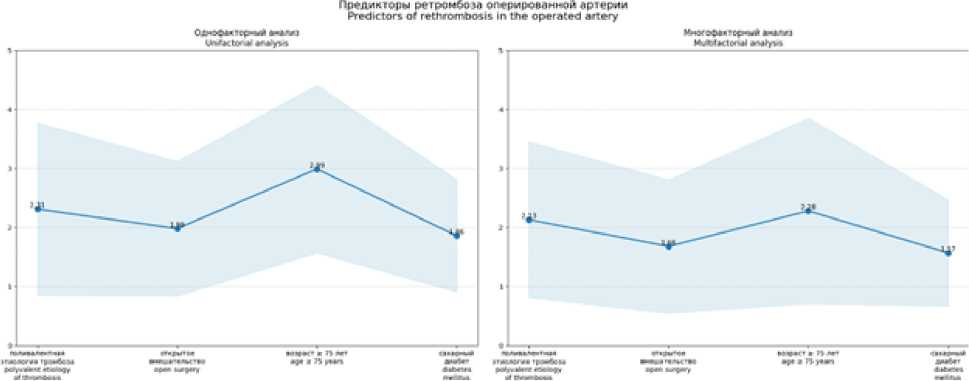
Рис. 2. Динамика функционального статуса по классификации Резерфорда
Fig. 2. Dynamics of functional status according to the Rutherford classification
По данным регрессионного анализа Кокса, независимое влияние на риск развития критической ишемии оказывали поливалентная этиология артериального тромбоза (ОР 1,72; 95 % ДИ 1,09–2,73; p=0,021), наличие ретромбоза (ОР 2,89; 95 % ДИ 1,75–4,78; p<0,001) и IIb класс острой ишемии по Резерфорду на момент первичной операции (ОР 2,14; 95 % ДИ 1,28–3,57; p=0,004) (табл. 3) (рис. 3).
Таблица 3
Предикторы развития критической ишемии по данным регрессионного анализа Кокса
Table 3
Predictors of the development of critical ischemia according to the Cox regression analysis
|
Фактор Factor |
Однофакторный анализ Univariate analysis |
p |
Многофакторный анализ Multivariate analysis |
p |
|
ОР (95 % ДИ) RR (95 % CI) |
ОР (95 % ДИ) RR (95 % CI) |
|||
|
Поливалентная этиология артериального тромбоза Polyvalent etiology of arterial thrombosis |
1,89 (1,21–2,95) |
0,005 |
1,72 (1,09–2,73) |
0,021 |
|
Ретромбоз Rethrombosis |
3,22 (1,97–5,26) |
<0,001 |
2,89 (1,75–4,78) |
<0,001 |
|
IIb класс по Резерфорду Rutherford class IIb |
2,37 (1,44–3,91) |
0,001 |
2,14 (1,28–3,57) |
0,004 |
|
Открытое вмешательство Open intervention |
1,64 (1,06–2,55) |
0,027 |
1,39 (0,88–2,21) |
0,161 |
|
ХИНК в анамнезе History of CLTI |
1,52 (0,98–2,35) |
0,062 |
– |
– |
Повторные реваскуляризации в отдаленном периоде потребовались 12,9 % пациентов, достоверно чаще оперативное лечение выполнялось у пациентов после открытой реваскуляризации перенесших коронавирусную инфекцию в анамнезе (p>0,05).
Полученные результаты указывают на негативное влияние COVID-19 на отдаленные исходы реваскуляризаций при ОИК, что согласуется с данными ряда исследований [14, 15].
Эндоваскулярный подход в сочетании с селективным ка-тетеруправляемым тромболизисом тканевым активатором плазминогена – актилизе, в нашей работе продемонстрировал преимущества перед открытыми методами реваскуляризации в аспекте отдаленной проходимости и частоты рецидивов ишемии конечности.
Тем не менее, высокая частота ретромбозов и повторных вмешательств в обеих группах свидетельствует о недостаточной эффективности существующих стандартов лечения ОИК у пациентов с COVID-19. Необходим поиск новых стратегий фармакопрофилактики и более агрессивных протоколов анти-тромботической терапии у данной категории больных. Перспективным направлением может стать внедрение в клиническую практику методов персонализированной оценки тромботического риска на основе комплексного анализа клинических, генетических и лабораторных факторов.
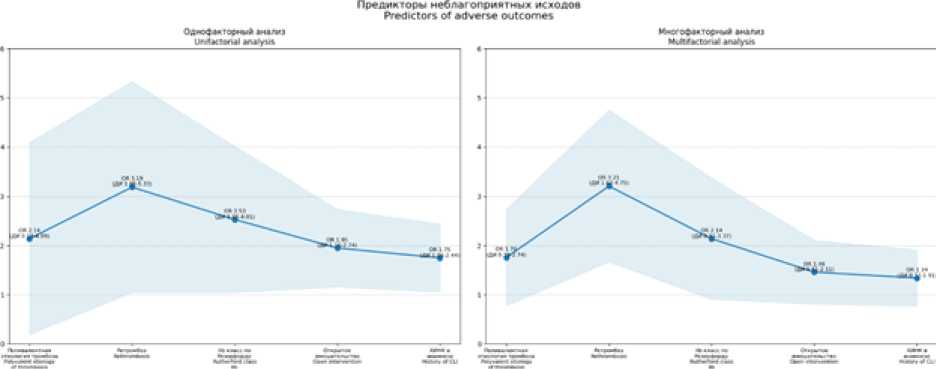
Рис. 3. Факторы риска неблагоприятных исходов
Fig. 3. Risk factors for adverse outcomes
Основными ограничениями настоящего исследования являются его ретроспективный характер и относительно небольшой объем выборки. Кроме того, мы не оценивали влияние разных подтипов COVID-19 и сопутствующей фармакотерапии на отдаленные результаты реваскуляризаций.
Для более глубокого анализа влияния метода реваскуляризации у пациентов на фоне новой коронавирусной инфекции COVID-19 на риск развития неблагоприятных событий в отдаленном периоде мы провели многофакторный регрессионный анализ Кокса, включив в модель такие ковариаты, как возраст, пол, сахарный диабет, ХБП, предшествующие реваскуляризации, класс ишемии по Резерфорду и этиологию тромботического поражения. После коррекции на перечисленные факторы поливалентная этиология тромбоза (не тромбоэмболическая и не атеросклеротическая) (ОР 1,68; 95 % ДИ 1,14–2,48; p=0,009) и открытый характер вмешательства (ОР 1,47; 95 % ДИ 1,02–2,11; p=0,041) сохранили значимое независимое влияние на первичную конечную точку (рис. 4).
Изучение динамики функционального статуса конечности по классификации Резерфорда в сроки 1, 6 и 12 месяцев после операции показало более быстрое его восстановление в группе эндоваскулярного лечения. Так, через 1 месяц после вмешательства половина пациентов этой группы не имели симптомов ишемии (0 класс по Резерфорду) или отмечали минимальную перемежающуюся хромоту (I класс). В то же время в группе открытых операций значимая часть боль- ных страдала от умеренной и выраженной хромоты (I–II класс), у 4,4 % пациентов имела место ишемия конечности III–IV класса. Различия между группами нивелировались к 6 месяцу, однако к концу года у пациентов после открытых вмешательств вновь отмечалась тенденция к ухудшению функционального статуса (табл. 5).
Анализ публикаций последних лет демонстрирует противоречивые результаты в отношении сравнительной эффективности открытых и эндоваскулярных вмешательств при ОИК. В нашем исследовании эндоваскулярный подход показал преимущество, особенно по таким показателям, как частота ретромбозов и функциональный статус конечности в раннем послеоперационном периоде (табл. 6).
Основным ограничением нашего исследования является относительно небольшой размер выборки, не позволяющий в полной мере реализовать преимущества многофакторного анализа. Кроме того, отсутствие рандомизации могло привести к систематической ошибке отбора, поскольку выбор метода реваскуляризации осуществлялся лечащим врачом на основании клинической картины и анатомии поражения.
Заключение
Настоящее исследование продемонстрировало высокую частоту неблагоприятных исходов открытых и эндоваскулярных вмешательств при ОИК в отдаленном периоде у пациентов с COVID-19. Независимыми предикторами развития ретромбоза, рецидива острой ишемии и критической ишемии конечности были пожилой возраст, тяжелый класс ишемии по Резерфорду на момент операции, открытый характер вмешательства и поливалентная этиология артериального тромбоза. Негативное влияние COVID-19 на отдаленные исходы реваскуляризаций в нашей работе было ожидаемым и согласуется с опубликованными данными. Коагулопатия, ассоциированная с SARS-CoV-2, характеризуется гиперкоагуляцией, эндотелиальной дисфункцией и нарушением фибринолиза, что может приводить к развитию ретромбозов даже на фоне адекватной антитромботической терапии. В метаанализе Malas et al., объединившем результаты 5 исследований (n=372), частота ретромбозов после реваскуляризаций у пациентов с COVID-19 составила 21,2 %, что было значимо выше популяционных значений (ОШ 2,91; 95 % ДИ 1,54–5,52; p=0,001). При этом в большинстве работ COVID-19 был идентифицирован как независимый фактор риска неблагоприятных исходов, удваивающий вероятность потери конечности и смерти в отдаленном периоде (ОШ 2,18; 95 % ДИ 1,31–3,64; p=0,003).
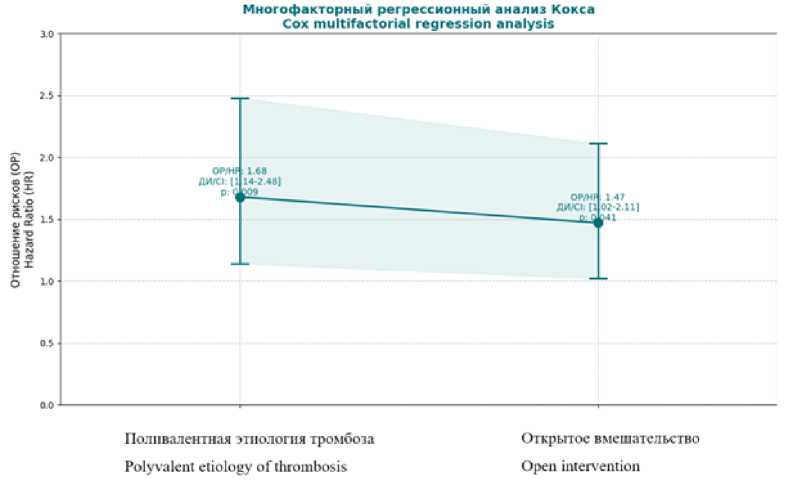
Рис. 4. Многофакторный анализ рисков с временной динамикой
Fig. 4. Multifactorial risk analysis with time dynamics
Таблица 5
Динамика функционального статуса по классификации Резерфорда после реваскуляризации
Table 5
Dynamics of functional status according to Rutherford classification after revascularization
|
Класс Class |
Открытые операции, % (n/N) Open surgeries, % (n/N) |
Эндоваскулярные операции, % (n/N) Endovascular surgeries, % (n/N) |
p* |
||||
|
1 мес. 1 month |
6 мес. 6 months |
12 мес. 12 months |
1 мес. 1 month |
6 мес. 6 months |
12 мес. 12 months |
||
|
0 |
34,7 (16/46) |
47,8 (22/46) |
41,3 (19/46) |
50,7 (35/69) |
56,5 (39/69) |
50,7 (35/69) |
0,039 |
|
I |
39,1 (18/46) |
23,9 (11/46) |
17,4 (8/46) |
29,0 (20/69) |
23,2 (16/69) |
21,7 (15/69) |
0,132 |
|
II |
21,7 (10/46) |
19,6 (9/46) |
23,9 (11/46) |
20,2 (14/69) |
17,4 (12/69) |
20,2 (14/69) |
0,048 |
|
III |
2,2 (1/46) |
4,3 (2/46) |
6,5 (3/46) |
0 (0/69) |
1,4 (1/69) |
2,9 (2/69) |
0,031 |
|
IV |
2,2 (1/46) |
4,3 (2/46) |
10,8 (5/46) |
0 (0/69) |
1,4 (1/69) |
4,3 (3/69) |
0,026 |
*p – для сравнения исходных значений между группами (критерий χ2)
Таблица 6
Предикторы первичной конечной точки по данным многофакторного регрессионного анализа Кокса
Table 6
Predictors of the primary endpoint according to multivariate Cox regression analysis
|
Фактор Factor |
β |
ОР (95 % ДИ) RR (95 % CI) |
p |
|
Этиология артериального тромбоза Etiology of arterial thrombosis |
0,519 |
1,68 (1,14–2,48) |
0,009 |
|
Открытое вмешательство Open intervention |
0,384 |
1,47 (1,02–2,11) |
0,041 |
|
Класс по Резерфорду Rutherford class |
0,618 |
1,86 (1,22–2,82) |
0,004 |
|
Возраст (на каждые 10 лет) Age (per 10 years) |
0,207 |
1,23 (1,06–1,43) |
0,008 |
|
Сахарный диабет Diabetes mellitus |
0,336 |
1,40 (0,96–2,04) |
0,079 |
|
ХБП С3-5 CKD G3-5 |
0,482 |
1,62 (0,93–2,82) |
0,088 |
Примечание: первичная конечная точка – комбинация ретромбоза, рецидива ОИК и хронической ишемии IV класса. ОР – относительный риск; ДИ – доверительный интервал.
Эндоваскулярная реваскуляризация с катетеруправляе-мым селективным тромболизисом при ОИК у пациентов с COVID-19 была ассоциирована с меньшей частотой рецидивов острой ишемии и развития хронической артериальной недостаточности в отдаленном периоде по сравнению с открытыми операциями. В отличие от большинства исследований, мы не получили значимых межгрупповых различий по частоте повторных реваскуляризаций, что, вероятно, связано с небольшим размером выборки и относительно коротким периодом наблюдения. В метаанализе Мохаммеда с соавт. 12-месячная частота повторных вмешательств после эндоваскулярного лечения ОИК составила 18,4 %, после открытых операций – 23,6 % (ОШ 0,69; 95 % ДИ 0,56–0,85; p<0,001). При этом кумулятивная частота повторных реваскуляризаций достигала 37,2 % через 3 года и 43,8 % через 5 лет, что подчеркивает необходимость длительного наблюдения за данной категорией пациентов.
Перспективные направления для дальнейшего научного поиска включают изучение молекулярных механизмов пост-ковидной коагулопатии, идентификацию новых биомаркеров тромботического риска, оптимизацию режимов медикаментозной профилактики, разработку инновационных методов эндоваскулярного лечения окклюзионно-стенотических поражений периферических артерий. Междисциплинарное взаимодействие хирургов, анестезиологов-реаниматологов, кардиологов и гематологов будет способствовать комплексному решению проблемы ОИК в эпоху пандемии и после ее завершения.
Список литературы Отдаленные результаты различных методов реваскуляризации при острой ишемии конечности у пациентов с COVID-19
- Moroni F., Baldanti F., Franchini M., Adinolfi L.E., Santoro A., Rossi M., Ageno W. The Thromboembolism Risk in COVID-19 Patients (TREC19) Study: A New Tool for the Risk Stratification and Management of COVID-19 Patients. Int J Environ Res Public Health, 2022, № 19, рр. 4223.
- Etkin Y., Conway A.M., Silpe J., Qato K., Carroccio A., Manvar-Singh P., Horen C.L., Giangola G., Genovese M., Baril D.T., Rockman C.B., Maldonado T.S. Acute Arterial Thromboembolism in Patients with COVID-19 in the New York City Area. Ann Vasc Surg, 2021, № 70, рр. 290-294.
- Al-Zoubi N., Shatnawi N., Jarbo H., Khader Y., Alzoubi H. Acute Limb Ischemia in Patients Infected with SARS-CoV-2. Vasc Endovascular Surg, 2022, № 56, рр. 90-95.
- Indes J.E., Koleilat I., Hatch A.N., Choinski K., Jones D.B., Aldailami H., Billett H., Denesopolis J., Lipsitz E.C. Early experience with arterial thromboembolic complications in patients with COVID-19. J Vasc Surg, 2021, № 73, рр. 381-389.
- Ilonzo N., Rao A., Safir S., Vouyouka A., Phair J., Baldwin M., Gillespie D., Scher L., Garg K. Acute thrombotic manifestations of coronavirus disease 2019 (COVID-19): A case series. J Vasc Surg Cases Innov Tech, 2020, № 6, рр. 381-385.
- Goldman I.A., Ye K., Scheinfeld M.H. Lower-extremity Arterial Thrombosis Associated with COVID-19 Is Characterized by Greater Thrombus Burden and Increased Rate of Amputation and Death. Radiology, 2020, № 297, рр. E263-E269.
- Bellosta R., Luzzani L., Natalini G., Pegorer M.A., Attisani L., Cossu L.G., Ferrandina C., Fossati A., Conti E., Bush R.L., Piffaretti G. Acute limb ischemia in patients with COVID-19 pneumonia. J Vasc Surg, 2020, № 72, рр. 1864-1872.
- Gomez-Arbelaez D., Ibarra-Sanchez G., Garcia-Gutierrez A., Comanges-Yeboles A., Ansuategui-Vicente M., Gonzalez-Fajardo J.A. COVID-19-Related Aortic Thrombosis: A Report of Four Cases. Ann Vasc Surg, 2020, № 67, рр. 10-13.
- de Roquetaillade C., Chousterman B.G., Tomasoni D., Zeitouni M., Houdart E., Guedon A., Maisonnasse J., Demeret S., Haroche J., Lucet J.C., Duval X., Picard C., Szwebel T.A., Mebazaa A. Unusual arterial thrombotic events in Covid-19 patients. Int J Cardiol, 2021, № 323, рр. 281-284.
- Cheruiyot I., Kipkorir V., Ngure B., Misiani M., Munguti J., Ogeng’o J. Arterial Thrombosis in Coronavirus Disease 2019 Patients: A Rapid Systematic Review. Ann Vasc Surg, 2021, № 70, рр. 273-281.
- Lax S.F., Skok K., Zechner P., Kessler H.H., Kaufmann N., Koelblinger C., Vander K., Bargfrieder U., Trauner M. Pulmonary Arterial Thrombosis in COVID-19 With Fatal Outcome: Results from a Prospective, Single-Center, Clinicopathologic Case Series. Ann Intern Med, 2020, № 173, рр. 350-361.
- Abou-Ismail M.Y., Diamond A., Kapoor S., Arafah Y., Nayak L. The hypercoagulable state in COVID-19: Incidence, pathophysiology, and management. Thromb Res, 2020, № 194, рр. 101-115.
- Bilaloglu S., Aphinyanaphongs Y., Jones S., Iturrate E., Hochman J., Berger J.S. Thrombosis in Hospitalized Patients With COVID-19 in a New York City Health System. JAMA, 2020, № 324, рр. 799-801.
- Piazza G., Campia U., Hurwitz S., Snyder J.E., Rizzo S.M., Pfeferman M.B., Morrison R.B., Leiva O., Fanikos J., Nauffal V., Almarzooq Z., Bracken M., Goldhaber S.Z. Registry of Arterial and Venous Thromboembolic Complications in Patients With COVID-19. J Am Coll Cardiol, 2020, № 76, рр. 2060-2072.
- Gąsecka A., Borovac J.A., Guerreiro R.A., Giustozzi M., Parker W., Caldeira D., Chiva-Blanch G. Thrombotic Complications in Patients with COVID-19: Pathophysiological Mechanisms, Diagnosis, and Treatment. Cardiovasc Drugs Ther, 2021, № 35, рр. 215-229.


