Отдалённые результаты операции «замороженный хобот слона»: 10-летний опыт центра
Автор: Чарчян Э.Р., Брешенков Д.Г., Чакал Д.А., Генс А.П., Степаненко А.Б., Абугов С.А., Белов Ю.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Сердечно-сосудистая хирургия
Статья в выпуске: 3 (93), 2025 года.
Бесплатный доступ
Введение. Операция «замороженный хобот слона» (ЗХС) – широко используемый метод при лечении распространенных. форм заболеваний грудной аорты. Несмотря на популярность, доступность методики и значительные преимущества над менее радикальными операциями, сохраняется высокий риск дистальных аортальных осложнений, требующих повторных вмешательств. Цель. Оценить ранние и отдаленные результаты операции ЗХС, частоту и структуру повторных вмешательств, а также факторы риска, ассоциированные с реинтервенциями. Материалы и методы. Проведено ретроспективное одноцентровое обсервационное когортное исследование 347 пациентов, оперированных с использованием методики ЗХС с 2014 по 2025 год. Использовались различные гибридные протезы, включая новый отечественный расслоение специфический гибридный протез «Мягкий хобот слона». Анализ выживаемости и факторов риска выполнен с использованием методов Каплана-Мейера и многофакторного логистического регрессионного анализа. Результаты. Средний возраст пациентов составил 52,8±11,5 года, 71 % – мужчины. Десятилетняя выживаемость составила 78 %. Повторные вмешательства потребовались у 13,5 % пациентов, из них 11,2 % – дистальные реинтервенции, 1,7 % – проксимальные. Основной причиной внеплановых реинтервенций (n=19, 5,5 %) являлось отрицательное ремоделирование, которое в 58 % случаев развивалось на фоне новой дистальной стент-графт-индуцированной фенестрации (ДСИФ), тогда как плановые этапные вмешательства потребовались в 20 случаях (5,7 %). Плановые открытые вмешательства сопровождались более высокой 7-летней выживаемостью (90 %) по сравнению с эндоваскулярными (60 %). Наличие синдрома дисплазии соединительной ткани было независимым предиктором риска повторных вмешательств (HR 4,11; p=0,002). Заключение. Операция ЗХС остаётся золотым стандартом в лечении распространенных заболеваний грудной аорты, обеспечивая высокую выживаемость в отдаленном периоде. Исследование показало, что открытая хирургия после ЗХС обеспечивает лучшие долгосрочные результаты в сравнении эндоваскулярными вмешательствами. Пациенты с дисплазией соединительной ткани требуют динамичного МСКТ-контроля. Оптимизация хирургической стратегии и активное послеоперационное наблюдение остаются ключевыми факторами успешного лечения и профилактики поздних осложнений.
Гибридная хирургия, стент-графт, гибридный протез, расслоение аорты, аневризма аорты
Короткий адрес: https://sciup.org/142245630
IDR: 142245630 | УДК: 616.132-007.64 | DOI: 10.17238/2072-3180-2025-3-56-67
Long-term results of the frozen elephant trunk procedure: 10-year experience of a single center
Background. The frozen elephant trunk (FET) procedure is a widely used method for treating extensive thoracic aortic diseases. Despite its significant advantages, a high risk of distal aortic complications requiring reintervention remains. Objectives. To evaluate outcomes of the FET procedure, the frequency and nature of reinterventions, and risk factors associated with reoperations. Materials and methods. We performed a retrospective single-center observational study of 347 patients who underwent FET from 2014 to 2025. Various hybrid prostheses were used, including the Russian dissection-specific stent-graft “Soft Elephant Trunk.” Survival and risk factor analyses were performed using Kaplan–Meier and multivariate logistic regression. Results. The mean patient age was 52,8±11,5 years, with 71 % male. Ten-year survival was 78 %. Reinterventions were required in 13,5 % of patients, including 11,2 % distal and 1,7 % proximal reinterventions. The main cause of unplanned reinterventions (n=19, 5,5 %) was negative remodeling, which in 58 % of cases of new distal stent graft-induced new entry (dSINE), whereas staged reinterventions were performed in 20 cases (5,7 %). Open surgical reinterventions were associated with higher 7-year survival (90 %) compared to endovascular treatments (60 %). Connective tissue disorder was an independent predictor of reintervention risk (HR 4,11, p=0,002). Conclusions. The FET procedure remains the gold standard for treating extensive thoracic aortic disease, ensuring high long-term survival. Our study showed that open surgery after FET provides better long-term results compared to endovascular interventions. Connective tissue disorders require dynamic CT follow-up. Optimization of surgical strategy, and active postoperative monitoring remain key factors in successful treatment and prevention of complications.
Текст научной статьи Отдалённые результаты операции «замороженный хобот слона»: 10-летний опыт центра
Операция «замороженный хобот слона» (ЗХС), предложенная Kato еще в 1995 году, является одной из ключевых и популярных методик в хирургии расслоения аорты [1]. Основная идея этой методики заключается в одномоментной коррекции распространенной патологии дуги и нисходящего отдела [2]. За последние десятилетия операция ЗХС стала золотым стандартом при лечении как острых, так и хронических расслоений аорты А и В типа по Стэнфорду, а также торакоабдоминальных аневризм аорты (ТААА). Несмотря на неоспоримые преимущества методики, в виде индукции тромбоза ложного канала (ЛК) на уровне стент-графта и потенциальное положительное ремоделирование (ПР), связанное с этим, сохраняется риск дистальных аортальных событий, требующих повторного вмешательства. В ряде публикаций сообщается о высокой частоте реинтервенций на дистальной аорте, достигающей 60–80% в течение первых 5 лет наблюдения [3–5]. Этот факт ставит под сомнение предполагаемую универсальность подхода «ЗХС при расслоении – один этап» и требует более тщательной оценки долгосрочных результатов [6].
Целью настоящего исследования стало определение результатов операции ЗХС, частоты и структуры проксимальных и дистальных повторных вмешательств, а также выявление факторов риска, ассоциированных с реинтервенциями.
Материалы и методы
Проведено ретроспективное одноцентровое обсервационное когортное исследование, включившее пациентов, перенёсших операцию ЗХС в ГНЦ ФГБНУ «РНЦХ им. акад. Б.В. Петровского» в период с 2014 по 2025 год. В исследование были включены 347 пациентов, независимо от этиологии патологии (острое/ хроническое расслоение аорты А и В типа, аневризма, shaggy aorta и др.). Все вмешательства выполнялись с использованием гибридных протезов, включая Thoraflex Hybrid (Vascutek, Шотландия), E-Vita Open Plus (Jotec, Германия), «Мягкий хобот слона» (МедИнж, Пенза, Россия), Braile (Braile, Бразилия), Valiant Thoracic (Medtronic, США). Исследование “Ретроспективный анализ результатов гибридной хирургии грудной аорты аорты (Гибрид-Р)” одобрено локальным этическим комитетом 24.01.2025 (протокол заседания ЛЭК № 1 от 24.01.2025).
Критерии включения:
– выполнение операции ЗХС;
– возраст старше 18 лет;
-
– наличие доступных клинических данных и контрольных МСКТ минимум через 6 месяцев после операции;
– возможность использования нескольких типов гибридных протезов на основании оценки анатомических и клинических данных.
Критерии исключения:
-
– отказ от участия в исследовании.
Хирургическая техника
До 2014 года в нашем центре применялась преимущественно гибридная методика, получивший название «русский гибрид», включающая классическую технику «хобот слона» с последующим этапом ЭЛАГА. С 2014 года в нашем центре впервые в РФ начато активное использование современных фабричных гибридных протезов: первыми имплантированными изделиями стали Thoraflex Hybrid и E-Vita Open Plus. Начиная с 2019 года, в нашей практике внедрён и активно используется отечественный расслоение-специфический гибридный протез – «Мягкий хобот слона» (МедИнж, Пенза, Россия). Концепция этого гибридного протеза аорты основана на прогрессивном снижении радиальной жёсткости за счёт постепенного уменьшения толщины нитино-ловых колец. Дистальное кольцо имеет Z-образную форму ни-тинолового кольца и снижает жёсткость на 50 % по сравнению с первым кольцом. Кроме того, дистальный край снабжён сосудистым безнитиноловым сегментом длиной 2 см с девятью платиновыми рентгенконтрастными метками. Такая конструкция предотвращает жесткое давление на интиму и, тем самым, снижает риск развития новой дистальной стент-графт-индуцированной фенестрации (ДСИФ). Важным дополнением является общая длина протеза (200 мм) и отсутствие шовного кольца, что позволяет безопасно имплантировать его ниже уровня Th8 и эффективно закрывать возможные дистальные фенестрации, что положительно влияет на ремоделирование аорты [3, 7–9].
Пациенты были разделены на группы в зависимости от типа реинтервенции (эндоваскулярное лечение аневризм грудной аорты (ЭЛАГА) или открытая хирургия, а также в зависимости от этапного или экстренного характера вмешательств. Повторные вмешательства классифицировались как дистальные (ЭЛАГА, протезирование TAA, протезирование брюшной аорты (БА) и др.) и проксимальные (рестернотомия, репротезирование дуги).
Для оценки выживаемости и свободы от повторных вмешательств использовался анализ по методу Каплана-Мейера с использованием лог-рангового теста для сравнения кривых. Факторы риска, ассоциированные с повторными вмешательствами, определялись с помощью многофакторного логистического регрессионного анализа с расчётом отношения шансов (ОШ) и 95 % доверительных интервалов (ДИ).
Результаты
В исследование были включены 347 пациентов, перенёсших операцию ЗХС в период с 2014 по 2025 гг. Средний возраст когорты составил 52,8 ± 11,5 лет, преобладали пациенты мужского пола (71 %). Расслоение аорты А типа по Стэнфорду было показанием к операции у 58,7 % пациентов, в основном в хронической стадии (41,6 %). Расслоение аорты В типа по Стэнфорду встречалось реже (21,3 %), и также преимущественно в хронической стадии (78,4 %). Большая половина когорты пациентов была оперирована с использованием расслоение-специфического гибридного протеза аорты «Мягкий хобот слона» (МедИнж, Пенза, Россия). Повторные вмешательства на аорте выполнялись в 47 случаях (13,5 %) пациентов, а дисплазия соединительной ткани была верифицирована у 11 % пациентов (табл. 1).
Таблица 1
Предоперационная характеристика пациентов
Preoperative patients characteristics
Table 1
|
Характеристика Characteristic |
N, Me (Q1; Q3), Mean (SD) |
|
Возраст, лет Age, years |
52,8 (11,5) |
|
Мужской пол, n (%) Male sex, n (%) |
247 (71,1) |
|
Индекс массы тела, кг/м2 Body mass index, kg/m² |
28,25 (4,5) |
|
Аневризма торакоабдоминальной аорты, n (%) Thoracoabdominal aortic aneurysm, n (%) |
62 (17,8) |
|
Shaggy аорта, n (%) |
7 (2) |
|
Расслоение аорты А типа по Стэнфорду, n(%) Stanford Type A aortic dissection, n (%) |
204 (58,7) |
|
- Острая стадия, n (%) Acute phase, n (%) |
70 (34,3) |
|
- Подострая стадия, n (%) Subacute phase, n (%) |
49 (24) |
|
- Хроническая стадия, n (%) Chronic phase, n (%) |
85 (41,6) |
Продолжение Таблицы 1
|
Расслоение аорты В типа по Стэнфорду, n (%) Stanford Type B aortic dissection, n (%)
Acute phase, n (%)
Subacute phase, n (%)
Chronic phase, n (%) |
74 (21,3) 3 (4) 13 (17,5) 58 (78,4) |
|
Тип гибридного протеза аорты, n Type of hybrid aortic prosthesis, n
Stent-graft “Soft Elephant Trunk”, n (%)
|
52 (17) 21 (10,6) 2 (0,5) 247 (66) 25 (8,3) |
|
Повторные вмешательство на аорте, n (%) Redo aortic repair |
47 (13,5) |
|
Наследственная дисплазия соединительной ткани, n (%) Hereditary connective tissue disorder, n (%)
Marfan syndrome, n (%)
|
38 (10,9) 21 (55,3) 2 (5,2) 1 (0,3) 1 (0,3) 13 (34,2) |
|
Артериальная гипертензия, n (%) Hypertension, n (%) |
286 (82,4) |
|
Ишемическая болезнь сердца, n (%) Coronary artery disease, n (%) |
65 (18,7) |
|
Фракция выброса, % Ejection fraction, % |
59,5 (7,5) |
|
ОНМК в анамнезе, n (%) History of stroke, n (%) |
33 (9,5) |
|
Хроническая обструктивная болезнь лёгких, n (%) Chronic obstructive pulmonary disease, n (%) |
21 (6) |
|
Сахарный диабет, n (%) Diabetes mellitus, n (%) |
17 (4,8) |
|
Фибрилляция предсердий, n (%) Atrial fibrillation, n (%) |
36 (10,4) |
|
Хроническая болезнь почек, n (%) Chronic kidney disease, n (%) |
80 (23) |
*ОНМК – острое нарушение мозгового кровообращения, Me – median, SD – standard deviation
Классический вариант гибридной операции по «замороженный хобот слона» с использованием гибридного протеза выполнялся в превалирующем количестве случаев (83,2 %), тогда как гибридные подходы с применением ЭЛАГА были реализованы в 16,8 % случаев и являются на данном этапе историческим вариантом, и в настоящее время не используются. Средний диаметр гибридного протеза составил 28 (26; 30) мм, а длина имплантируемой части 150 (140; 180) мм. Протезирование дуги чаще проводилась с применением многобраншевых протезов (55 %), в то время как имплантация ветвей на единой площадке – в 45 % случаев. Для артериальной канюляции чаще всего использовалась правая подключичная артерия (65 %), также в примерно одинаковой частоте использовались ОБА, аорта и ОСА в зависимости от анатомии расслоения аорты. Мини-инвазивное вмешательство с использованием министернотомии выполнялось у 5,4 % пациентов. Средняя продолжительность искусственного кровообращения (ИК) составила 160 (134; 192) мин, ишемии миокарда (ИМ) – 94 (77; 118) мин, циркуляторного ареста (ЦА) – 32 (28; 39) мин при стандартной температуре 28 °C. Средний объем интраоперационной кровопотери в среднем составил 1000 (700; 1500) мл. Частота ре-эксплораций по поводу кровотечения – 6,3 %. В послеоперационном периоде параплегия зафиксирована в 0,5 % случаев, парапарез – в 3,7 % из которых более 50 % восстановилось в госпитальном периоде, ОНМК – 4 %. Средняя длительность ИВЛ составила 9 (7; 13) часов, пребывания в ОРИТ – 2 (1; 4) суток, а госпитализация – 10 (8; 14) суток. Госпитальная летальность составила 4,3 %. Средний срок наблюдения составил 60 месяцев (34,3–85,8 мес.) (табл. 2). Отдаленная выживаемость через 10-лет после операции составила 78 %.
Таблица 2
Ранние результаты операций
Overall results
Table 2
|
Характеристика Characteristic |
N (%), Me (Q1; Q3), Mean (SD) |
|
Тип гибридной операции: Type of hybrid repair:
Frozen Elephant Trunk, n (%)
|
322 (92,7) 25 (7,2) |
|
Размер протеза, мм Prosthesis size, mm |
28 (26; 30) |
|
Длина эндоваскулярной части, мм Endovascular part length, mm |
150 (140; 180) |
Продолжение Таблицы 2
|
Реконструкция брахиоцефальных ветвей, n (%) Branches repair, n (%)
Island technique, n (%)
Selective repair, n (%) |
156 (45) 191 (55) |
|
Артериальная канюляция, n (%): Arterial cannulation site, n (%)
Aorta, n (%)
Femoral artery, n (%)
Right subclavian artery, n (%)
Innominate artery, n (%)
Common carotid artery, n (%) |
60 (17,3) 20 (5,8) 227 (65) 10 (2,8) 30 (8,6) |
|
Сочетанные операции, n (%): Concomitant procedures, n (%)
Mitral valve repair, n (%)
Tricuspid valve repair, n (%)
Coronary artery bypass grafting, n (%) |
28 (8) 10 (2,8) 58 (16,7) |
|
Время ИК, мин Cardiopulmonary bypass time, min |
160 (134; 192) |
|
Время пережатия аорты, мин Aortic cross-clump time, min |
94 (77; 118) |
|
Время циркуляторного ареста, мин Circulatory arrest time, min |
32 (28; 39) |
|
Температура, °С Temperature, °C |
28 (28; 28) |
|
Кровопотеря, мл Blood loss, ml |
1,000 (700; 1500) |
|
Мини-стернотомия, n (%) Mini-sternotomy, n (%) |
19 (5,4) |
|
Ре-эксплорация по причине кровотечения, n (%) Re-exploration for bleeding, n (%) |
22 (6,3) |
|
Параплегия, n (%) Paraplegia, n (%) |
2 (0,5) |
|
Парапарез, n (%) Paraparesis, n (%) |
13 (3,7) |
|
Время ИВЛ, ч Ventilation time, h |
9 (7; 13) |
|
Время в ОРИТ, сутки ICU stay, days |
2 (1; 4) |
|
Время в стационаре, сутки Hospital stay, days |
10 (8; 14) |
|
Срок наблюдения, мес. Follow-up duration, months |
60 (34,3–85,8) |
|
ОНМК, n (%) Stroke, n (%) |
14 (4) |
|
Госпитальная летальность, n (%) Hospital mortality, n (%) |
15 (4,3) |
|
Отдаленная 10-летняя выживаемость, % Ten-year survival, % |
78 |
*ИВЛ – искусственная вентиляция лёгких, ИК – искусственное кровообращение, ОБА – общая бедренная артерия, ОНМК – острое нарушение мозгового кровообращения, ОРИТ – отделение реанимации и интенсивной терапии, ОСА – общая сонная артерия, ЦА – циркуляторный арест, ЧЗДА – частичная замена дуги аорты, ЭЛАГА – эндопротезирование нисходящей грудной аорты, Me – median, SD – standard deviation, TEVAR – thoracic endovascular aortic repair.
Проксимальные и дистальные реоперации
Повторные вмешательства на проксимальной аорте проводились реже (всего у 6 пациентов, что составило 1,7 %), при этом госпитальная летальность составила, а отдаленная 50 %, что еще раз подчеркивает как техническую сложность реинтервенций в этом сегменте, так и тяжелый соматический статус пациентов (табл. 3). В 1-ом случае у пациента на 3-й месяц после операции развилась аорто-пищеводная фистула в области дистального анастомоза аорты с гибридным протезом, что потребовало радикального удаления протеза корня, дуги и НГА с асцендо-абдоминальное шунтирование гомографтом (рис. 1).
Плановые (этапные) реоперации потребовались 20 пациентам (5,8 %), тогда как внеплановые вмешательства – 25 (7,2 %) Характеристика плановых и экстренных вмешательств в зависимости от сегмента представлены на рисунке 2.
Дистальные реоперации встречались в 39 случаев – 11,2 % (рис. 3). В этой подгруппе у 20 пациентов (5,7 % из общей когорты) вмешательства несли плановый этапный характер. В 8 случаях (40 %) выполнено открытое протезирование то-е ракоабдоминальной аорты (TAA), в 10 (50 %) – ЭЛАГА, в 2 (10 %) – протезирование брюшной аорты. Отрицательное ремоделирование, как причина повторной операции, зафиксировано у 19 пациентов (5,4 % из общей когорты). У 11 из них (58 %) развитие этого осложнения произошло на фоне формирования ДСИФ, что вновь подчёркивает важную роль этого механизма в прогрессии аневризматической болезни и отрицательного ремоделирования заболевания. В этой группе открытая реконструкция TAA была проведена у 10 пациентов (53 %). Таким образом, почти каждая вторая операция на тора- коабдоминальном сегменте проводилась при наличии новой ДСИФ, особенно у пациентов с дисплазией соединительной ткани.
Таблица 3
Проксимальные реоперации после операции ЗХС
Proximal reoperations after Frozen Elephant Trunk procedure
Table 3
|
Причина Cause |
N |
Реоперация Reoperation |
Летальность Mortality |
|
Ложная аневризма в области проксимального анастомоза протезо-коронарного шунта False aneurysm at the site of proximal anastomosis of prosthetic-coronary bypass graft |
3 |
|
2 живы 2 alive 1 лет. исход через 3 года 1 death after 3 years |
|
Дегенерация двустворчатого аортального клапана Aortic valve replacement due to degeneration of a bicuspid aortic valve |
1 |
Протезирование аортального клапана Aortic valve replacement |
Жива Alive |
|
Ложная аневризма ВА и корня аорты на фоне инфекции протеза аорты False aneurysm of the ascending aorta and aortic root due to aortic graft infection |
1 |
Репротезирование гомографтом + омен-топластика Redo aortic arch replacement using homograft |
Госпитальная летальность In-hospital mortality |
|
Аорто-пищеводный свищ (инфекция протеза аорты) Aorto-esophageal fistula (infected prosthetic graft of the aortic arch) |
1 |
Асцендо-абдоминальное шунтирование гомографтом Ascending-to-abdominal aorta bypass using homograft |
Летальность через 5 мес Death after 5 months |
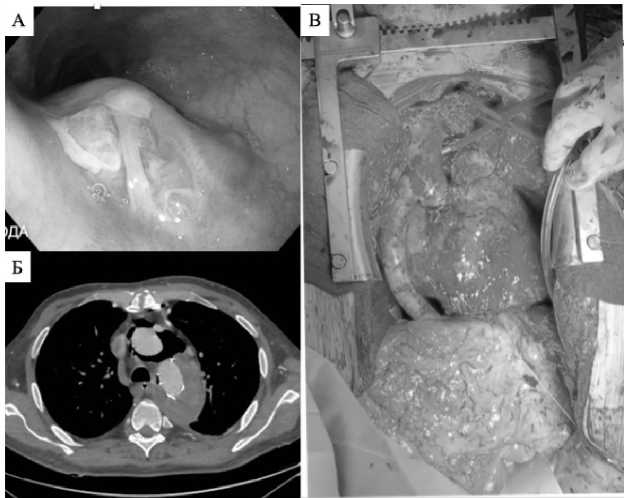
Рис. 1. Случай инфекции гибридного протеза у пациента после ЗХС с образованием аорто-пищеводной фистулы. А – аорто-пищеводный свищ; Б – МСКТ-диагностика инфекции протеза дуги аорты – парапротезный газ; В – выполненное асцендо-абдоминальное шунтирование гомографтом Fig. 1. Case of FET infection with aorto-esophageal fistula. A – aorto-esophageal fistula; B – CT infection view– paraprothetic gas; C – ascending-to-abdominal aortic bypass using homograft
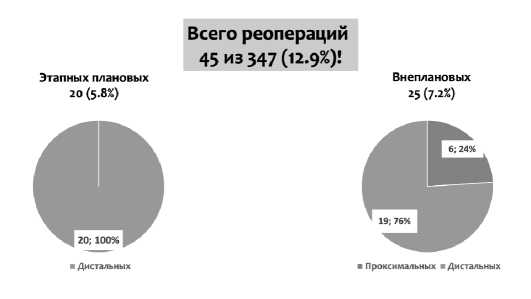
Рис. 2. Диаграмма распределения реопераций после ЗХС
Fig. 2 . Distribution of reoperations after FET
Всего 39 случаев - 11.2%

Рис. 3. Характеристика распределения повторных дистальных реопераций. ПБА – протезирование брюшной аорты, ТАА – торакоабдоминальный отдел аорты, ЭЛАГА – эндоваскулярное лечение аневризмы грудной аорты Fig. 3. Characteristics of the distal aortic reoperations. PBA – abdominal aortic prosthetics, TAA – thoracoabdominal aorta, ELAGA – endovascular treatment of thoracic aortic aneurysm
Таким образом отрытое протезирование дистальной аорты перенесло 20 пациентов (18 с протезированием ТААА и 2 пациента с протезированием брюшной аорты). Наши данные показали хорошие ранние и отдаленные результаты открытой хирургии после ЗХС (табл. 4). Это подчёркивает более благоприятный прогноз у пациентов, перенесших плановые открытые вмешательства, особенно при наличии дисплазии соединительной ткани.
При сравнении отдаленных результатов после различных типов реинтервенций 7-летняя выживаемость после ЭЛАГА составила (60 %), тогда как после открытого вмешательства (90 %). Кумулятивная функция риска также показала более высокий риск летального исхода после ЭЛАГА в качестве реинтервенции – 50 % через 7 лет (рис. 4).
Анализ выживаемости в зависимости от характера вмешательства (плановое, внеплановое) показал отсутствие значимых различий среди пациентов, перенёсших плановые (7-летняя выживаемость составила 80 %) и экстренные повторные вмешательства (с отрицательным ремоделированием аорты 7-летняя выживаемость – 75 %). Кумулятивный риск летальности был выше в подгруппе с плановыми вмешательствами, особенно в первые 3 года наблюдения, что подчёркивает неблагоприятный прогноз, связанный с синдромом мега-аорты (рис. 5).
Таблица 4
Результаты открытой хирургии дистальной аорты после ЗХС
Table 4
Results of open thoracoabdominal surgery of the distal aorta after FET
|
Характеристика Characteristic |
N, Me (Q1; Q3), Mean (SD) |
% |
|
Этапные операции, n Staged procedures, n |
10 |
52,6 |
|
ДСИФ, n dSINE, n |
6 |
31,6 |
|
Время до реоперации, мес. Time to reoperation, months |
14 (11; 22) |
|
|
Протезирование ТАА Extent II, n TAA replacement Extent II, n |
2 |
10,5 |
|
Протезирование ТАА Extent III, n TAA replacement Extent III, n |
15 |
78,9 |
|
Протезирование брюшной аорты, n Abdominal aortic replacement, n |
2 |
10,5 |
|
Методика Crawford, n Crawford technique, n |
6 |
31,6 |
|
Методика Coselli, n Coselli technique, n |
4 |
21,1 |
|
Метод «кнопки» , n Button technique, n |
7 |
36,8 |
|
Бифуркационнное аорто-подвздошное протезирование, n Bifurcated aorto-iliac prosthetic repair, n |
11 |
57,9 |
|
Кровопотеря, мл Blood loss, ml |
1100 (1000; 1450) |
|
|
Окклюзия баллоном, n Balloon occlusion, n |
2 |
10,5 |
|
Висцеральная перфузия, n Visceral perfusion, n |
16 |
84,2 |
|
День в ОРИТ, день ICU stay, days |
1 (1; 2,5) |
|
|
Госпитальная летальность, n Hospital mortality, n |
0 |
0 |
|
Острое почечное повреждение, n Acute kidney injury, n |
3 |
15,8 |
|
Временный диализ, n Temporary dialysis, n |
1 |
5,3 |
|
Дыхательная недостаточность, n Respiratory failure , n |
2 |
10,5 |
|
Параплегия, n Paraplegia, n |
0 |
0 |
|
Парапарез, n Paraparesis, n |
1 |
5,3 |
|
Ре-эксплорация по причине кровотечения, n Re-exploration for bleeding, n |
1 |
5,3 |
|
Парез кишечника, n Intestinal paresis, n |
0 |
0 |
|
Реоперации после, n Reoperations after, n |
0 |
0 |
|
Отдаленная летальность, n Late mortality, n |
1 |
5,3 |
|
Койко-день в стационаре, дней Hospital stay, days |
12,21 (2,3) |
|
|
Время наблюдения после, мес. Follow-up after reoperation, months |
35,42 (27,6) |
*ДСИФ – дистальная стент-графт-индуцированная фенестрация, ОРИТ – от-С деление реанимации и интенсивной терапии, ТАА – торакоабдоминальный отдел аорты, dSINE – distal stent-graft induced new entry, ICU – intensive care unit, Me – median, SD – standard deviation
Анализ факторов риска реопераций
Проведение многофакторного анализа позволило выделить независимые предикторы повторных вмешательств (табл. 5). Наличие СТД является наиболее значимым предиктором: у пациентов с СТД риск повторного вмешательства был выше в 4 раза как в однофакторной (HR = 4,20; 95% ДИ: 2,02–8,72; p<0,001), так и в многофакторной модели (HR = 4,11; 95% ДИ: 1,69–10,01; p=0,002). Повторная операция на аорте в анамнезе также ассоциировалась с повышенным риском (HR = 2,81; 95% ДИ: 1,34–5,91; p=0,006), однако в многофакторном анализе достигала лишь тренда к значимости (HR = 2,39; p=0,063). Такие переменные, как стадия расслоения, пол и возраст, не показали статистически значимого влияния на риск реопераций
Результаты нашего 10-летнего опыта выполнения операции ЗХС подтверждают её эффективность как метода радикального одномоментного лечения сложных распространенных форм расслоения и аневризм грудной аорты [10–12]. Тем не менее, несмотря на высокую общую выживаемость (более 75 % на 10-летнем интервале), частота дистальных осложнений, включая отрицательное ремоделирование и развитие ДСИФ, остаётся значимой проблемой и требует дальнейшего совершенствования подходов к лечению и наблюдению за данной когортой пациентов.
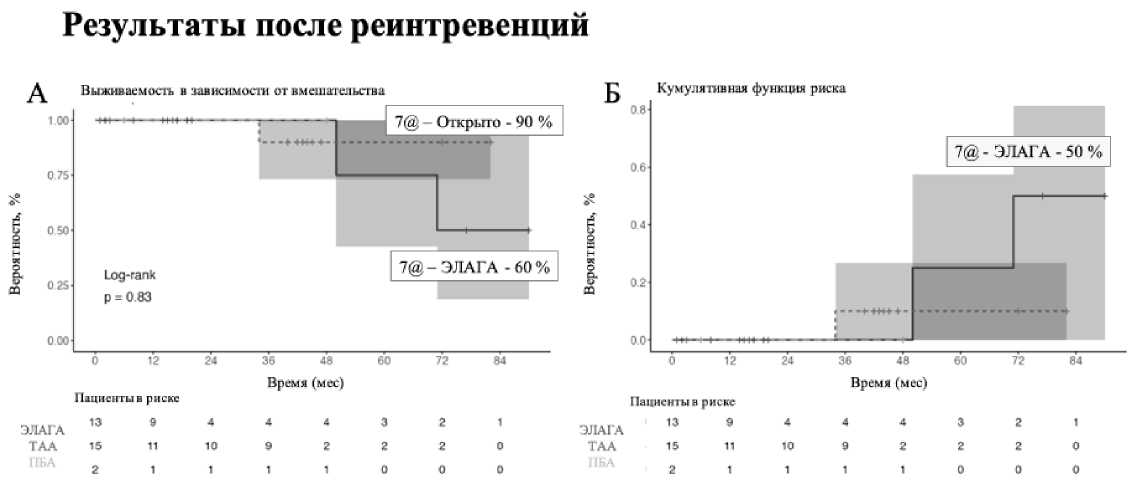
Рис. 4. Выживаемость после реопераций в зависимости от типа вмешательства. А – Отдаленная выживаемость в зависимости от типа вмешательств; Б – Кумулятивная функция риска летального исхода после реинтервенций. ПБА – протезирование брюшной аорты, ТАА – торакоабдоминальная аорта, ЭЛАГА – эндоваскулярное лечения аневризмы грудной аорты
Fig. 4. Follow survival after reoperations depending on the type of reintervention. A – Follow up survival depending on the type of intervention; B – Cumulative risk function of death after reinterventions. PBA – abdominal aortic prosthetics, TAA – thoracoabdominal aorta, ELAGA – endovascular treatment of thoracic aortic aneurysm
Результаты после реинтревенций
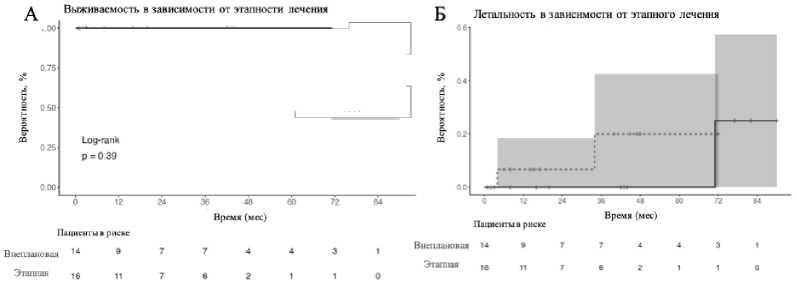
Рис. 5. Выживаемость после реопераций в зависимости от характера вмешательства. А – Отдаленная выживаемость в зависимости от характера вмешательств; Б – Кумулятивная функция риска летального исхода после реинтервенций
Fig. 5. Survival after reoperations depending on the staging of the intervention. A – Long-term survival depending on the staging of interventions; B – Cumulative hazard function of mortality after reinterventions

Таблица 5
Анализ факторов риска реопераций на аорте после ЗХС
Table 5
Risk factor analysis for aortic reoperations after FET procedure
|
Фактор риска Risk factor |
Сумма Total |
HR (однофакторный) HR (univariable) |
HR (многофакторный) HR (multivariable) |
|
|
Соединительно-тканная дисплазия, n (%) Connective tissue disorder, n (%) |
НЕТ NO |
211 (86,5) |
– |
– |
|
ДА, n (%) YES, n (%) |
33 (13,5) |
4.20 (2,02–8,72, p<0,001) ** |
4,11 (1,69–10,01, p=0,002) ** |
|
|
Повторная операция на аорте, n (%) Previous aortic surgery, n (%) |
НЕТ NO |
205 (84) |
– |
– |
|
ДА YES |
39 (16) |
2.81 (1,34–5,91, p=0,006) * |
2,39 (0,96–5,97, p=0,063) * |
|
|
Аневризмa, n (%) Aneurysm, n (%) |
52 (21,3) |
– |
– |
|
|
Стадия расслоения, n (%) Dissection phase, n (%) |
Острая Acute |
55 (22,5) |
0,65 (0,18–2,30, p=0,5) |
0,89 (0,23–3,46, p=0,867) |
|
Подострая Subacute |
41 (16,8) |
1.53 (0,52–4,44, p=0,438) |
1,84 (0,59–5,8, p=0,296) |
|
|
Хроническая Chronic, |
96 (39,3) |
1,03 (0,39–2,76, p=0,947) |
0,65 (0,23–1,83, p=0,418) |
|
|
Пол, n (%) Sex, n (%) |
Женский Female |
72 (29,5) |
– |
– |
|
Мужской Male |
172 (70,5) |
1,8 (0,69–4,70, p=0,233) |
2,16 (0,78–6,02, p=0,139) |
|
|
Возраст, лет Age, years |
Mean (SD) |
53,8 (12,5) |
0,98 (0,96–1,01, p=0,188) |
1,01 (0,98–1,05, p=0,418) |
*HR – hazard ratio, SD – standard deviation
Обсуждение
Анализ подгрупп показал, что около 13,5 % пациентов потребовали повторного вмешательства, причём почти половина из них – по поводу отрицательного ремоделирования дистальной аорты. Как видно на представленных графиках Каплана-Мейера (рис. 5), при сравнении плановых и внеплановых повторных вмешательств не выявлено статистически значимых различий в долгосрочной выживаемости (лог-ранк, p = 0,39). Однако при оценке типа повторного вмешательства было отмечено увеличение риска летального исхода в группе эндоваскулярных повторных операций, которые сопровождались более низкой 7-летней выживаемостью (60 % против 90 %). Современная стратегия этапного лечения, особенно с применением открытых реконструкций торакоабдоминального сегмента, позволяет добиться высокой выживаемости и минимальной летальности [13]. Несмотря на более высокий интраоперационный риск при открытом протезировании, открытые вмешательства обеспечивают стабильный результат, особенно у пациентов с СТД и пациентов молодого возраста. Это подчёркивает необходимость персонализированного подхода при выборе метода повторного лечения.
Отрицательное ремоделирование и ДСИФ, как показал наш анализ, нередко развиваются в течение первых 2–3 лет наблюдения, особенно у пациентов с СТД и при использовании неспецифических для расслоения гибридных протезов аорты. Основные работы, представленные в современной литературе, также подчёркивают роль дистальной механической травмы интимы как основного триггера поздних осложнений [8, 14, 15].
Внедрение в клиническую практику принципиально новых расслоение-специфических гибридных протезов с мягким дистальным концом, в частности, отечественного гибридного протеза «Мягкого хобота слона», позволяет снижать риск возникновения ДСИФ и тем самым отрицательного ремоделирования, как это продемонстрировано и в нашем исследовании. Тем не менее, даже при использовании этих протезов у ряда пациентов высокого риска сохраняется необходимость в дистальных реинтервенциях, что требует активного послеоперационного мониторинга.
Заключение
Операция ЗХС остаётся золотым стандартом в лечении распространенных заболеваний грудной аорты, обеспечивая высокую выживаемость в отдаленном периоде. Однако дистальные осложнения, включая отрицательное ремоделирование и ДСИФ, сохраняют свою актуальность и требуют активного изучения. Результатом данной работы стали следующие тезисы: 1) операция ЗХС имеет удовлетворительные ранние и отдаленные результаты, и может активно применяться в опытных центра у пациентов со сложной патологией дуги и НГА, 2) использование расслоение-специфических стент- графтов снижает частоту ДСИФ, 3) открытые вмешательства при повторных операциях обеспечивают лучшие долгосрочные результаты по сравнению с эндоваскулярными методами, 4) пациенты с СТД требуют особо тщательного наблюдения и раннего этапного вмешательства, 5) Ключевыми факторами успешного лечения и профилактики поздних осложнений являются индивидуализированный подход к выбору протеза, оптимизация хирургической стратегии и активное послеоперационное наблюдение.
Оптимизация хирургической стратегии, индивидуализация выбора протеза и активное послеоперационное наблюдение остаются ключевыми факторами успешного лечения и профилактики поздних осложнений после ЗХС.


