Отдельные клинико-биологические особенности злокачественных опухолей головного мозга у детей
Автор: Моргун А.В., Черепанов С.М., Малютин О.А., Борисова М.В., Таранушенко Т.Е., Салмина А.Б.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 1 (49), 2012 года.
Бесплатный доступ
При изучении прогностического значения маркеров апоптоза, пролиферации и химиорезистентности при опухолях ЦНС у детей оценивали динамическое изменение этих показателей после химиотерапии. Установлена значимость экспрессии Р-гликопротеина и показателя пролиферации (Ki-67) в прогнозе опухолей ЦНС. Обнаружены гендерные отличия при развитии химиорезистентности опухолей. Обозначена возрастная группа с высокими показателями маркера пролиферации при отсутствии отличий по половому признаку.
Злокачественные опухоли головного мозга, детская онкология, прогноз течения заболевания
Короткий адрес: https://sciup.org/14056179
IDR: 14056179 | УДК: 616.831-006.6-053-036
Clinical features and biological markers of brain tumors in children
When studying prognostic markers of apoptosis, proliferation and chemoresistance for CNS tumors in children, changes in these parameters after chemotherapy were assessed. P-glycoprotein expression and proliferation marker (Ki-67) were found to be significant for prognosis of CNS tumors. Gender distinctions in the development of tumor chemoresistance were found. Age group with high level of proliferation marker without distinctions by sex characteristics was identified.
Текст научной статьи Отдельные клинико-биологические особенности злокачественных опухолей головного мозга у детей
В последние десятилетия отмечается тенденция роста заболеваемости злокачественными заболеваниями как в целом в популяции, так и у детей. В России уровень онкологической заболеваемости детского населения составляет 9,5–15 на 100000 [1]. Опухоли центральной нервной системы (ЦНС) в детском возрасте являются одними из самых частых злокачественных новообразований, они занимают 2-е ранговое место после лейкозов. Несмотря на возросшую радикальность удаления опухолей головного мозга (ОГМ) и достижения в разработке новых более эффективных химиопрепаратов, частота рецидивов ОГМ у детей остается достаточно высокой – 7–35 % [10].
В настоящее время информация о прогностической значимости различных молекул, экспрессирующихся при опухолевой прогрессии, весьма противоречива [5]. Предполагается, что одним из значимых прогностических маркеров может являться уровень апоптоза в опухолевой ткани, так как низкий уровень спонтанного или индуцированного апоптоза опухолевых клеток является основой прогрессирования опухоли [11]. Другим прогностическим маркером опухолевой прогрессии может быть показатель пролиферации. Есть работы, показывающие связь между уровнем апоптоза, показателями пролиферации и степенью злокачественности опухолей головного мозга [7]. Особое место в развитии рецидивов и метастазов отводится химиорезистентности, которую предлагается учитывать как важный прогностический фактор. Одним из важнейших механизмов химиорезистентности опухолевой клетки является гиперэкспрессия белков, ответственных за экструзию цитостатиков из клетки, например Р-гликопротеина (Pgp).
В настоящее время результаты исследований по рассматриваемой проблеме не имеют единой интерпретации, большинство опубликованных работ носят преимущественно эксперименталь- ный характер, а публикации, посвященные оценке состояния апоптоза, пролиферации и химиорезистентности при опухолях центральной нервной системы у детей с их оценкой на фоне химиотерапии, практически отсутствуют.
Цель исследования – изучить молекулярные механизмы опухолевой прогрессии (эффективность апоптоза, пролиферативная активность, экспрессия маркера лекарственной устойчивости) при опухолях головного мозга у детей.
Материал и методы
Объект исследования – 37 пациентов Красноярской краевой детской больницы, которые находись в онкогематологическом отделении с морфологически верифицированным диагнозом: опухоль головного мозга. Средний возраст больных – 9,9 ± 0,7 года. Все опухоли носили злокачественный характер: астроцитомы – 22, медуллобластомы – 8, глиобластомы – 7. Всем больным был выполнен диагностический стандарт, включающий в себя: сбор анамнеза, физикальный осмотр, клинический анализ крови, общий анализ мочи, биохимический анализ крови, КТ головного мозга в аксиальной проекции с контрастом до и после оперативного лечения, МРТ в 3 проекциях. Химиотерапия осуществлялась по стандартным протоколам (М-2000, HIT91\HIT2000 для медуллобластом, лучевая терапии параллельно с темозоломидом, PCV в лечении злокачественных глиом, также использовалась схема введения винкристина на фоне лучевой терапии). Течение расценивалось как неблагоприятное при рецидиве опухоли, смерти пациента, развитии метастазов. Изучались препараты опухолевой ткани, полученные интраоперационно до и после химиотерапии.
Для регистрации апоптоза клеток головного мозга использовался метод TUNEL (Apoptag Direct Detection kit, Immunotech, France) согласно протоколу производителя в депарафинизированных срезах. Подсчитывалось общее количество TUNEL+ клеток не менее чем в 20 полях зрения (×900) с последующим расчетом апоптозного индекса (АИ) (АИ – доля TUNEL+ клеток, выраженная в процентах от общего количества клеток). За низкий уровень апоптоза принимались значения от 0 до 5 %, умеренный – от 5,1 до 10 %, АИ выше 10,1 % расценивался как высокий. Определение экспрессии антигенов Ki-67 (показатель пролиферативной активности) и Р-гликопротеина (маркер лекарственной устойчивости) проводилось двойным непрямым методом иммуноферментного окрашивания. Для определения Ki-67 использовались первичные моноклональные антитела MIB-1 (DAKO, Дания). Антителами для Р-гликопротеина были первичные мышиные антитела JSB1 (No-vocastra, Англия). В качестве вторичных антител использовались ФИТЦ-меченые антимышиные моноклональные антитела. Иммуногистохимические исследования проводились по стандартной методике в депарафинизированных срезах. Для каждого образца готовился негативный контроль. Образцы опухоли расценивались как отрицательные при отсутствии окраски. Для определения выраженности пролиферативной активности рассчитывался пролиферативный индекс (ПИ – доля Ki-67+ клеток, выраженная в процентах от общего количества клеток) Положительные результаты для Р-гликопротеина ранжировались следующим образом: слабое окрашивание менее 10 % клеток – низкая экспрессия, слабое окрашивание более 10 % – умеренная, сильно выраженное окрашивание более 10 % – выраженная. На основании результатов окраски повышенным уровнем считались образцы с умеренной и выраженной окраской.
Для статистического анализа результатов использовался точный критерий Фишера, критерий Уилкоксона, кривая Kaplan–Meier и логранговый критерий. Расчеты проводились с помощью программы StatPlus 2005, Primer of Biostatics, версия 4.03.
Результаты и обсуждение
Из 37 человек с опухолями головного мозга, вошедших в исследование, мальчиков 25 (67,6 %), девочек 12 (32,4 %). Манифестация заболевания наступала у большинства детей данной группы в возрасте 11–17 лет – 19 из 37 пациентов (51,4 %). При изучении локализации опухолевого процесса установлено, что преимущественной областью поражения был мозжечок – в 40,5 % случаев и полушария мозга – в 27 %, реже опухоль располагалась в лобной (18,9 %) и височной (13,5 %) долях. Ведущими клиническими симптомокомплексами, сопутствующими злокачественным новообразованиям мозга, были цефалгия (70,3 %), астенический синдром (70,3 %), неврологические проявления (51,3 %), зрительные нарушения (10,8 %). Указанные проявления по частоте встречаемости соответствуют литературным данным [2–4].
На следующем этапе работы исследовались молекулярные маркеры опухолевой прогрессии в образцах злокачественной ткани и проводилось сопоставление полученных результатов с особенностями клинического течения болезни, с результатами лечения и исходами заболевания пациентов c онкологическими заболеваниями головного мозга. Установлено отсутствие гендерных и возрастных отличий в уровнях апоптоза (таблица). При оценке исходных значений апоптотической активности отмечена некоторая тенденция к увеличению данного показателя у умерших детей. Наряду с этим имеются достоверно более высокие значения АИ у детей с метастазированием и прогрессированием опухолей головного мозга (р<0,05). На фоне проведенного лечения зарегистрировано увеличение АИ, что отмечают и другие авторы [6, 9]. Не обнаружено статистически значимых различий уровня запрограммированной клеточной гибели у выживших и умерших детей, при сохранении тенденции к более высокой выраженности апоптоза у умерших детей. Важно отметить, что у детей с метастазами до и после терапии уровень апоптоза был значительно выше, чем у детей без метастазирования опухоли. Высокие значения АИ являются фактором развития неблагоприятных исходов, что противоречит общепринятому мнению об ассоциации высоких значений апоптоза с благоприятными исходами опухолей головного мозга [8].
Исследования исходной выраженности экспрессии Ki-67 в образцах опухолей головного мозга не обнаружили гендерных и возрастных различий пролиферативной активности у детей с данной патологией (таблица). Однако отмечается тенденция к более высоким значениям указанного параметра в подгруппах умерших мальчиков и при метастазировании опухоли. На фоне проведенной терапии установлено изменение пролиферативной активности в опухолевой ткани со снижением ПИ в возрастной группе 11–17 лет. Важно, что высокая пролиферативная активность наблюдается у умерших детей по сравнению с выжившими пациентами и в случаях метастазирования опухоли (р<0,05). На фоне терапии в подгруппе умерших детей и при метастазирующих опухолях ПИ не имел существенной динамики и был высоким. В ходе работы нами установлено влияние экспрессии антигена Ki-67 на длительность бессобытийной выживаемости (рис. 1): при высоком уровне пролиферативной активности время бессобытийной выживаемости было короче, чем при низких значениях ПИ (р<0,05).
При анализе особенностей лекарственной устойчивости у детей с ОГМ выявлено наличие гендерных различий (р<0,05) исходных показателей экспрессии Р-гликопротеина (таблица). Для пациентов мужского пола характерна низкая, а для женского пола – высокая экспрессия исследуемого антигена. Установлено достоверное (р<0,05) преобладание экспрессии Pgp в подгруппе умерших детей. Отмечена тенденция к повышению указанного параметра при метастазировании опухоли.
Таблица
|
Группы больных |
АИ |
ПИ |
Pgp |
|||
|
До терапии |
После терапии |
До терапии |
После терапии |
До терапии |
После терапии |
|
|
Мальчики |
17,3 ± 3 |
18,4 ± 3,2 |
12,2 ± 2,5 |
8,3 ± 1,9* |
9,5 ± 1,3 # |
9,8 ± 1,4 # |
|
Девочки |
13,5 ± 4,2 |
15 ± 3,8* |
6,3 ± 0,7 |
4,1 ± 0,9* |
15 ± 1,9 # |
15,3 ± 2,3 # |
|
Все дети |
16,6 ± 2,4 |
17,9 ± 2,5* |
10 ± 1,7 |
6,9 ± 1,3* |
11,3 ± 1,1 |
11,6 ± 1,3 |
|
3–6 лет |
13,2 ± 3,5 |
14,9 ± 3,9 |
11,1 ± 3,8 |
7,5 ± 3,1* |
13 ± 2,1 |
12 ± 2,4 |
|
7–10 лет |
16,8 ± 6,3 |
18,6 ± 6,4* |
6 ± 1,1 |
5 ± 1,4 |
7,2 ± 2 |
7,2 ± 1,6 |
|
11–17 лет |
18,2 ± 3,7 |
19,5 ± 3,4 |
10,7 ± 2,3 |
7,2 ± 1,8* |
11,7 ± 1,5 |
12,7 ± 1,8 |
|
0–10 лет |
15,1 ± 3,3 |
17,1 ± 3,6 |
9,3 ± 2,5 |
6,6 ± 2,1 |
10,9 ± 1,6 |
10,3 ± 1,7 |
|
Живые |
13,7 ± 3,2 |
14 ± 3,5 |
6,2 ± 0,7 |
7,1 ± 1 # |
10,5 ± 1,1 # |
10,6 ± 1,2 # |
|
Умершие |
18,1 ± 3,2 |
19,9 ± 3,4 |
13,6 ± 6,7 |
13,6 ± 1,6 # |
20,7 ± 3,2 # |
22,3 ± 3,5 # |
|
Метастазы |
27 ± 3,7 # |
28,5 ± 3,8 |
15,8 ± 5,5 |
17,8 ± 5,9 # |
15,6 ± 5,5 |
17,8 ± 6 |
|
Без метастазов |
15,4 ± 2,7 # |
17,1 ± 2,9* |
9,4 ± 1,7 |
6,8 ± 1,4 # * |
10,8 ± 1 |
10,8 ± 1,2 |
Примечание: * – различия статистически значимы между показателями в одной подгруппе до и после терапии (р<0,05); # – различия статистически значимы между подгруппами: мальчики/девочки; живые/умершие; с метастазами/без метастазов (р<0,05).
СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2012. №1 (49)
Иммуногистохимическое исследование образцов опухолей головного мозга (М ± δ)
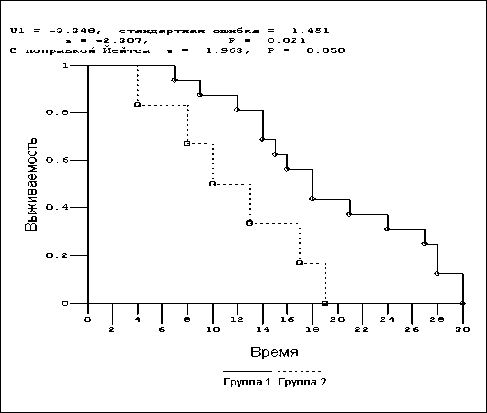
Рис. 1. Показатели бессобытийной выживаемости детей с опухолями головного мозга в зависимости от уровня пролиферации опухолевых клеток. Примечание: группа 1 – опухоли с низким уровнем пролиферации; группа 2 – опухоли с высоким уровнем пролиферации
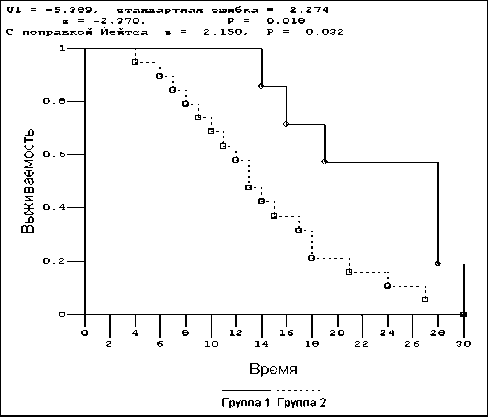
Рис. 2. Показатели бессобытийной выживаемости детей с опухолями головного мозга в зависимости от уровня экспрессии Pgp в опухолевых клетках.
Примечание: группа 1 – опухоли с низким уровнем экспрессии Pgp; группа 2 – опухоли с высоким уровнем экспрессии Pgp
Изменения экспрессии Pgp на фоне химиотерапии отсутствовали во всех рассматриваемых подгруппах с сохранением указанных выше тенденций и умеренным повышением экспрессии Рgp в подгруппах умерших, а также при метастазировании опухолей. Мы доказали влияние уровня экспрессии Рgp на длительность бессобытийной выживаемости (рис. 2). Для высокой экспрессии Р-гликопротеина характерно более короткое время бессобытийной выживаемости (p<0,05).
Заключение
Результаты исследования опухолевого материала до начала химиотерапии показали увеличенные значения АИ при метастазах опухоли, отсутствие гендерных и возрастных различий в выраженности апоптоза и пролиферативной активности, высокую экспрессию Р-гликопротеина у девочек и умерших детей со злокачественными новообразованиями головного мозга. На фоне лечения отмечено отсутствие динамики Р-гликопротеина, увеличение апоптотического индекса (преимущественно у девочек и в возрастной подгруппе 7–10 лет), снижение пролиферативной активности во всех рассматриваемых подгруппах при более высоких значениях указанного показателя у умерших детей и при метастазировании опухоли. Представленные данные выявили прямую взаимосвязь выражен- ности апоптоза с частотой метастазирования, причастность пролиферативной активности опухоли к бессобытийной выживаемости детей в возрастных подгруппах 3–6 лет и 11–17 лет, а также отсутствие динамики маркера лекарственной устойчивости на фоне терапии при установленном влиянии экспрессии Pgp на выживаемость пациентов со злокачественными новообразованиями головного мозга.


