«Открытый живот» в лечении вторичного перитонита и абдоминального сепсиса: лимитирующие факторы
Автор: Щеголев А.А., Товмасян Р.С., Маркаров А.Э., Чевокин А.Ю., Васильев М.В., Плотников В.В., Мурадян Т.Г.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 2 (92), 2025 года.
Бесплатный доступ
Введение. Несмотря на отсутствие исследований с высоким уровнем доказательности относительно эффективности вакуумной лапаростомии при тяжёлых формах вторичного перитонита, в настоящее время в практической хирургии накоплен значительный опыт применения данной хирургической стратегии, а имеющиеся результаты дают возможность проанализировать возможные противопоказания и факторы риска применения данной методики. Цель исследования. Детализировать противопоказания к вакуум-ассистированной лапаростомии при хирургическом лечении вторичного перитонита, осложнённого абдоминальным сепсисом. Материалы и методы исследования. Изучены результаты лечения 84 больных абдоминальным сепсисом, в лечении которых применялись вакуум-ассистированные лапаростомы (ВАЛС). У всех больных абдоминальный сепсис был следствием вторичного перитонита, источником которого были дефекты различных отделов желудочно-кишечного тракта (ЖКТ). У подавляющего большинства больных (85,7 %) на момент стартового хирургического вмешательства был диагностирован септический шок, абсолютное большинство больных (81 %) были оперированы позже 24 часов от момента заболевания. Изучена корреляция результатов лечения в зависимости от исходной локализации источника перитонита. Результаты лечения. Общая летальность в исследовании составила 38 %. В группе больных с локализацией источника перитонита в тонкой кишке летальность составила 52,8 %. В группе больных с источником перитонита в других отделах ЖКТ летальность составила 27 %. Разница летальности в группах была достоверной (р<0,05). Успешность первичного фасциального закрытия (ПФЗ) также достоверно отличалась в группах (31,3 % против 82,5 %, р<0,05). Заключение. Есть основания полагать, что при наличии ушитых зон или участков десерозации тонкой кишки при вторичном перитоните необходимо либо вовсе отказаться от использования ВАЛС, либо использовать редуцированные варианты вакуумных повязок, в которых предусмотрено воздействие отрицательного давления только в пределах лапаротомной раны с изоляцией зоны отрицательного давления от свободной брюшной полости синтетическими протезами, фиксированными к фасциальным краям раны.
Абдоминальный сепсис, вакуум-ассистированная лапаростома, «замороженный» живот, кишечные свищи, «открытый живот», перитонит, фасциальное закрытие живота
Короткий адрес: https://sciup.org/142244466
IDR: 142244466 | УДК: 616.381-002 | DOI: 10.17238/2072-3180-2025-2-27-33
"Open abdomen" in the treatment of secondary peritonitis and abdominal sepsis: limiting factors
Introduction. Despite the lack of studies with a high level of evidence regarding the effectiveness of VAC-laparostomy in severe forms of secondary peritonitis, significant experience in the application of this surgical strategy has been accumulated in practical surgery, and the accumulated results make it possible to analyze possible contraindications and risk factors for the use of this technique. The purpose of the study. To detail contraindications to vacuum-assisted laparotomy in the surgical treatment of secondary peritonitis complicated by abdominal sepsis. Materials and methods of research. The results of treatment of 84 patients with abdominal sepsis treated with vacuum-assisted laparostomy (VALS) were analyzed. In all patients, abdominal sepsis was the result of secondary peritonitis, the source of which was defects in various parts of the gastrointestinal tract (GIT). Most patients (85,7 %) were diagnosed with septic shock at the time of initial surgery, and many patients (81 %) underwent surgery later than 24 hours after the onset of the disease. The correlation of treatment results what depending on the initial localization of the source of peritonitis. Treatment results. The overall mortality rate in the study was 38 %. In the group of patients with localization of the source of peritonitis in the small intestine, mortality was 52,8 %. In the group of patients with the source of peritonitis in other parts of the gastrointestinal tract, mortality was 27 %. The difference in mortality in the groups was significant (p<0,05). The success rate of primary fascial closure (PFC) was also significantly different in the groups (31,3 % vs. 82,5 %, p<0,05). Conclusion. There is reason to believe that in the presence of sutured areas or areas of damage to the serous membrane of the small intestine in secondary peritonitis, it is necessary either to completely abandon the use of VALS, or to use reduced versions of vacuum dressings, which provide for the effect of negative pressure only within the laparotomy wound with isolation of the negative pressure zone from the free abdominal cavity with synthetic prostheses fixed to the fascial edges of the wound.
Текст научной статьи «Открытый живот» в лечении вторичного перитонита и абдоминального сепсиса: лимитирующие факторы
За последние несколько лет в литературе сформировалось довольно устойчивое понятие так называемого «открытого живота» (ОЖ), которое подразумевает использование различных вариантов вакуум-ассистированных лапаростом (ВАЛС) при внутрибрюшных катастрофах. Не вызывает сомнения основное показание к ОЖ: максимально эффективное снижение внутрибрюшного давления в случаях интраабдоминальной гипертензии (ИАГ) и абдоминального компартмент - синдрома (АКС). Большинство авторов также едины во мнении относительно ВАЛС в качестве оптимального способа временного закрытия живота в случаях damage-control (DC) и необходимости second-look (SL) релапаротомий [1 - 2].
Что касается применения ОЖ конкретно при абдоминальном сепсисе (АС), то в настоящее время, достоверных результатов, свидетельствующих о снижении летальности при АС с применением данной стратегии в больших выборках, пока не получено [3–7].
С другой стороны, прослеживается тенденция, отчетливо сформировавшаяся за последние несколько лет: акцент востребованности стратегии ОЖ при внутрибрюшных катастрофах смещается от травмы к АС. За последние 5 лет, количество публикаций по использованию стратегии ОЖ при травме резко снизилось, а при АС, наоборот, значительно возросло [8]. На наш взгляд, это связано с двумя причинами: рутинным освоением навыков рестриктивного типа интенсивной терапии при тяжёлой травме и снижением количества лапаротомий, в целом. Более того, применение ОЖ при травме в настоящее время в наибольшей степени связано с повреждением полых органов (контроль контаминации и инфекции, в отличие от контроля кровотечения при травме паренхиматозных органов и сосудов). Что касается показаний к ОЖ при АС, то здесь наблюдается постепенное смещение акцентов от «местных» критериев в брюшной полости к параметрам общего состояния пациента. В этом смысле показания к ОЖ при АС в настоящее время, в основном, ассоциируются с септическим шоком (SCIAS - severe complicated intra-abdominal sepsis) [9-11].
Материалы и методы
В работе проанализированы результаты лечения 84 больных абдоминальным сепсисом, в лечении которых применялась стратегия «открытого живота». Все больные проходили лечение в университетской хирургической клинике РНИМУ имени Н. И. Пирогова (руководитель клиники и заведующий кафедрой - д. м. н. профессор Щеголев А. А.) на базе городской клинической больницы имени Ф.И. Иноземцева ДЗ г. Москвы
(главный врач - Маркаров А. Э.) в период с 2016 по 2023 гг. Этиологически у всех больных АС был следствием вторичного перитонита, источником которого были дефекты различных отделов желудочно-кишечного тракта (ЖКТ). Пациенты были рандомизированы по полу, возрасту, сопутствующей патологии, тяжести перитонита (Мангеймский индекс перитонита - МИП) и степени органной недостаточности на момент стартовой операции, определяемой по шкале SOFA. Средний возраст больных составил 63,8±11,5 лет; гендерное деление: 40 мужчин, 44 женщин.
Критериями включения в исследование были: наличие абдоминального сепсиса по критериям протокола Сепсис-3 и использование ВАЛС. Критерий исключения был только один – смерть в течение 48 часов от момента поступления в стационар.
У подавляющего большинства больных на момент стартового хирургического вмешательства был диагностирован септический шок (72 больных – 85,7 % от общего числа наблюдений). Также у подавляющего числа больных стартовая операция была выполнена в срок более 24 часов от момента манифестации перитонита (68 больных – 81 %). Среднее значение МИП в общей группе составило 33,45±2,45. Среднее значение SOFA на момент стартовой операции в общей группе составило 3,98±1,56.
Решение об использовании ВАЛС в каждом конкретном случае принималось оперирующим хирургом лично, либо в ходе интраоперационного консилиума с руководителем хирургической клиники. Показаниями для выбора стратегии ОЖ были: септический шок, в том числе сокращённая лапаротомия из-за нестабильной гемодинамики, высокий риск развития абдоминального компартмент-синдрома (АКС), необходимость повторной оценки жизнеспособности кишечника и восстановления непрерывности желудочно-кишечного тракта, флегмона лапаротомной раны.
Стратегия ОЖ предусматривала наложение ВАЛС во время стартового хирургического вмешательства в традиционном исполнении с широкой инкорпорацией компонентов вакуумной повязки в брюшную полость без фасциальной тяги. Сразу после стабилизации состояния больного и достижения устойчивого хирургического контроля источника перитонита переходили к модификациям ВАЛС с фасциальным вытяжением посредством эластомеров и синтетических сеток под контролем внутрибрюшного давления (ВБД) либо выполнялось одномоментное полноценное фасциальное ушивание лапаротомной раны наглухо.
Конечной целью стратегии ОЖ всегда было стремление к первичному фасциальному закрытию живота. Удовлетворительным результатом считалось также кожное закрытие лапаротомной раны.
Неудовлетворительными результатами считали:
-
1. Летальный исход
-
2. «Замороженный живот» ( тип 3 по классификации Бьорк )
-
3. Кишечные свищи ( тип 4 по классификации Бьорк )
Целью данной работы было изучение эффективности лечения абдоминального сепсиса с использованием стратегии ОЖ в целом и выявление тех факторов риска, которые в наибольшей степени коррелировали с неудовлетворительными результатами лечения.
По данным литературы общеизвестны главные факторы, которые достоверно коррелируют с неудовлетворительными результатами лечения тяжелых форм вторичного перитонита и АС. Таковыми являются: наличие или отсутствие септического шока, давность перитонита более 24 часов от момента стартовой операции, локализация источника перитонита в ЖКТ.
Поскольку в настоящую работу исходно вошли пациенты с самыми тяжелыми характеристиками вторичного (перфорационного) перитонита и абдоминального сепсиса, а именно: подавляющее большинство пациентов находились в септическом шоке и были оперированы позднее 24 часов от начала перитонита, то наши основные усилия были направлены на выявление других отрицательных прогностических критериев выживаемости. В частности, в работе изучена зависимость результатов лечения вторичного перитонита и АС с использованием стратегии ОЖ в зависимости от локализации (уровня) источника перитонита в желудочно-кишечном тракте.
Исходя их поставленных целей выбран следующий дизайн исследования. В таблице 1 приведено распределение больных по первичному источнику перитонита.
Таблица 1
Первичный источник перитонита
The source of peritonitis
Table 1
|
Локализация источника перитонита Localization of the source of peritonitis |
Количество больных (n) Quantity of patients (n) |
|
|
Первичные операции Primary operations |
||
|
Желудок и 12-перстная кишка Stomach and duodenum |
4 |
|
|
Тонкая кишка Small bowel |
26 |
|
|
Ободочная кишка Large bowel |
Опухолевые Neoplastic |
18 |
|
Неопухолевые Non-cancerous |
8 |
|
|
Послеоперационные перитониты Postoperative peritonitis |
||
|
Желудок и 12-перстная кишка Stomach and duodenum |
2 |
|
Продолжение Таблицы 1
|
Тонкая кишка Small bowel |
10 |
|
Ободочная кишка Large bowel |
16 |
|
Всего: Total: |
84 |
На промежуточных этапах исследования была обнаружена отчётливая корреляция неудовлетворительных результатов с локализацией источника перитонита в тонкой кишке. Для проверки данной гипотезы все больные, вошедшие в исследование, были разделены на 2 группы по первичной локализации источника перитонит:
-
I. Тонкая кишка - 36 больных
-
II. Другие отделы ЖКТ - 48 больных
Группы были однородны по полу возрасту, давности перитонита, тяжести перитонита по МИП и органной недостаточности по SOFA.
Далее в каждой группе были исследована частота каждого из основных критериев неудовлетворительных результатов лечения (летальность, частота развития «замороженного живота», кишечные свищи типа Бьорк 4). В качестве критерия хорошего результата лечения изучена частота первичного фасциального закрытия в каждой группе.
Дизайн исследования: ретроспективное рандомизированное клиническое.
Результаты
Общая летальность в исследовании составила 38 % (32 пациента). В I группе (источник перитонита в тонкой кишке) летальность составила 19 больных (52,8 %), во II группе (больные с источником перитонита НЕ в тонкой кишке) летальность составила 13 больных (27 %). Разница летальности в группах была достоверной (р<0,05).
Попытка первичного фасциального закрытия (ПФЗ) предпринята у 56 пациентов. При этом успешность ПФЗ в целом в исследовании составила 71,4 % (40 больных). Успешность ПФЗ в I группе составила 5 из 16 наблюдений (31,3 %). Аналогичный показатель во II группе - составил 33 из 40 больных (82,5 %). Разница результатов в группах достоверна (р<0,05).
Частота развития «замороженного живота» в исследовании составила 3,57 % (3 случая). При этом все 3 случая развития «замороженного живота» отмечались в I группе (8,3 %), в этой же группе отмечено 2 случая формирования кишечных свищей типа Бьорк 4 (5,6 %). Любопытно, что во II группе случаев «замороженного живота» и кишечных свищей типа Бьорк 4 не отмечено (0 %). Разница результатов по данному показателю в группах недостоверна (р > 0,05). Сравнительные результаты лечения в группах представлены на рисунке 1.
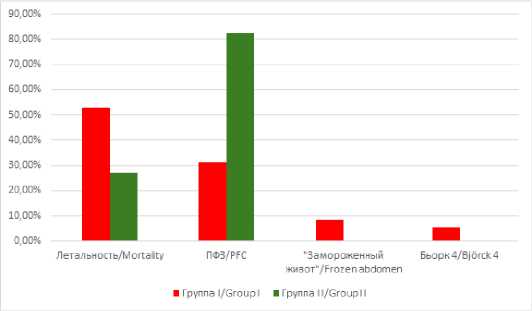
Рис. 1. Результаты лечения
Fig. 1. Treatment results
Обсуждение
С одной стороны, полученные результаты созвучны результатам наиболее известных исследований по стратификации тяжёлых форм перитонита, осложненных абдоминальным сепсисом, в которых выявлен повышенный риск летального исхода, связанный с локализацией источника перитонита в тонкой кишке. Это, безусловно, широко известное исследование «WISS Study», посвященное валидации шкалы тяжести сепсиса всемирного общества неотложных хирургов (SSS WSES) и нисколько не теряющий своей актуальности уже более 30 лет Мангеймский индекс перитонита [12, 13]. В первой системе пункт валидации, посвященный тонкой кишке как источнику перитонита, оценивается максимально высоко (3 балла), во второй — внеободочным источникам перитонита присвоен также высокий балл (4 балла) в отношении летального исхода.
С другой стороны, наше исследование интересно тем, что в него вошли больные с исключительно тяжёлыми формами перитонита неаппендикулярного генеза: практически у всех больных отмечался септический шок и хирургическое вмешательство было выполнено после 24 часов с начала перитонита. Это так называемая категория больных, которая в зарубежной литературе описывается термином SCIAS (severe complicated intraabdominal infections, COOL-trial) [2]. В нашей работе получен сопоставимый с данными литературы уровень общей летальности (38 %), но выявленные результаты свидетельствуют о наличии повышенного риска летального исхода при локализации источника перитонита в тонкой кишке, несмотря на использование методики ОЖ.
Эти результаты могут свидетельствовать о следующем. Методика ОЖ за счет декомпрессивного и форсированного деконтаминационного эффекта довольно успешно справляется с перитонитами нетонкокишечной этиологии, поскольку при локализации дефекта в ободочной кишке проблемная зона кишечника может быть относительно безболезненно и эффективно «выключена» обструктивным стомированием.
Что же может быть лимитирующим патогенетическим фактором меньшей эффективности ВАЛС при локализации дефекта в тонкой кишке? На наш взгляд, имеют значение 2 фактора.
Во-первых, при локализации дефекта в тонкой кишке традиционное исполнение ВАЛС не может вывести этот участок из-под опасного влияния вакуума, а попытка «выключить» дефект тонкой кишки посредством высокой илеостомии зачастую непродуктивна и сопряжена с высоким риском некор-регируемых патофизиологических последствий.
Во-вторых, в условиях септического шока и «капиллярной утечки» стенка тонкой кишки в наибольшей степени страдает из-за дисциркуляции и нарушения спланхнического кровотока в условиях так называемого энтерального дистресс-синдрома. Вкупе с анатомической особенностью наибольшего предлежания петель тонкой кишки к лапаротомной ране это создает тупиковую ситуацию с применением вакуума: с одной стороны нужна декомпрессия и форсированная деконтаминация брюшной полости, с другой стороны - использование вакуума становится крайне опасным в условиях отека, «мацерации» и дисциркуляции кишечной стенки с наличием ушитых дефектов или десерозаций. Попытки ряда авторов для этих целей использовать большой сальник в качестве изолирующей про-тективной субстанции от негативного влияния вакуума, на наш взгляд, малопродуктивны, хотя сколько-нибудь доказательных суждений на это счёт по известным причинам в настоящее время быть не может.
Что может быть перспективным решением вышеизложенных проблем, связанных с поражением тонкой кишки? Мы полагаем, что перспективным направлением дальнейшего поиска хирургических решений лечения абдоминального сепсиса и септического шока в стадии «капиллярной утечки» и значимого висцерального отека помимо успехов интенсивной терапии может быть смещение акцентов в сторону редуцированных вариантов ВАЛС, которые не предусматривают широкую инкорпорацию компонентов в брюшную полость и ограничиваются зоной отрицательного давления исключительно в лапаротомной ране. Эти варианты ВАЛС в качестве висцеральной защитной субстанции в дне раны должны иметь композитный сетчатый протез нужного размера для обеспечения ключевых задач: декомпрессии брюшной полости за счет обеспечения адекватного диастаза мышечно-фасциальных краев и одновременной дозированной фасциальной тяги в лапаротомной ране. В за- висимости от особенностей клинического случая и наличия или отсутствия слабых мест ЖКТ данный протез может быть перфорированным и неперфорированным.
Выводы
-
1. Во всех случаях интраабдоминальных катастроф с ушитым источником перитонита в тонкой кишке, а также с наличием потенциальных зон «слабости» стенки тонкой кишки имеется обоснованный риск применения ВАЛС в традиционном исполнении.
-
2. Наличие таких условий в брюшной полости требует либо полного отказа от использования вакуумной лапаростомы, либо поиска компромиссных технических решений, предусматривающих полную изоляцию ушитых или десерозированных участков тонкой кишки от зоны воздействия отрицательного давления
-
3. Редуцированные варианты ВАЛС, предусматривающие использование отрицательного давления лишь в пределах ла-паротомной раны с отграничением брюшной полости синтетическим протезом, фиксированным к фасциальным краям раны, по-видимому, могут быть перспективным вариантом временного закрытия живота у данной категории больных.


