Отравление животных этиленгликолем. Диагностика и методы идентификации
Автор: Дроздова Т.С., Кашин А.С.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Ветеринария
Статья в выпуске: 4, 2012 года.
Бесплатный доступ
В статье представлен редкий случай отравления собаки этиленгликолем - главным компонентом антифризов, антиобледенителей, гидравлических жидкостей. Разработаны комплексные методы идентификации при отравлении собак этиленгликолем. Методы исследования проводили в два этапа: первый - скрининговый (качественные реакции и тонкослойная хроматография), второй - арбитражный (использование метода газожидкостной хроматографии).
Исследование, отравление, этиленгликоль, метод, качественное и количественное определение, реакции
Короткий адрес: https://sciup.org/14082308
IDR: 14082308 | УДК: 619:615.9
Animal ethylene glycol poisoning. Diagnostics and identification methods
Rare occurrence of dog poisoning by ethylene glycol which is the main component of antifreezes, anti-icers, hydraulic liquids is given in the article. Complex techniques for identification in case dog ethylene glycol poisoning are developed. The research techniques have been conducted in two stages: the first is screening (qualitative reactions and thin-layer chromatography); the second is arbitration (use of the gas-liquid chromatography technique).
Текст научной статьи Отравление животных этиленгликолем. Диагностика и методы идентификации
Введение. Этиленгликоль – бесцветная сиропообразная жидкость, сладковатого вкуса, без запаха. Температура кипения 197,4 0С. Хорошо растворяется в спирте, воде, ацетоне, плохо – в эфире и жирах. Водные растворы этиленгликоля замерзают при температуре -65 0С [4].
Этиленгликоль применяют во многих отраслях промышленности: химической, фармацевтической, парфюмерной, автомобильной, авиационной, электротехнической, текстильной, нефтегазовой и других. В ограниченных масштабах этиленгликоль также применяют как растворитель печатных и некоторых других красок, в производстве чернил и паст для шариковых ручек, в органическом синтезе [3].
Одной из основных областей применения этиленгликоля и его производных (целлозольфы, карбитолы) является производство незамерзающих жидкостей в виде 35–40 %-го водного раствора, таких как антифризы, тормозные и технические жидкости [3,4].
Отравление этиленгликолем, как правило, происходит при пероральном приеме. Ингаляционные отравления этиленгликолем из-за малой летучести не встречаются [4,5].
Токсическое действие этиленгликоля и его эфиров во многом определяется процессами его биотрансформации и токсичностью метаболитов [7].
Если в первую фазу не удалось предотвратить интоксикацию, этиленгликоль метаболизируется в печени ферментом алкогольдегидрогеназой с образованием нескольких веществ, вызывающих развитие ацидоза и повреждающих почки. Метаболитами этиленгликоля являются гликолевый альдегид, гликолевая кислота, глиоксиловая кислота и щавелевая кислота. Гликолевый альдегид угнетает ЦНС, усиливает метаболический ацидоз и анионную разницу. Другие метаболиты ответственны за повреждение почек. Так, щавелевая кислота, взаимодействуя с ионами кальция, образует в почечных канальцах кристаллы оксалата кальция. И хотя повреждения, которые они вызывают, сравнительно невелики, без соответствующего лечения в течение 1–4 дней развивается анурическая форма острой почечной недостаточности [5, 9].
В механизме токсического действия этиленгликоля большую роль играют его гидрофильные свойства. Этиленгиколь и продукты его метаболизма являются осмотически активными веществами и вызывают гидропические изменения клеток. Проникая в клетку, молекула этиленгликоля увлекает за собой цитоплазматическую жидкость, нарушая клеточную структуру вплоть до ее гибели. Возникает резкая гидропическая дистрофия с образованием так называемых клеток-пузырей, что приводит к гибели клеток. Этот процесс наблюдается в эпителии проксимальных отделов почечных канальцев, где происходит реабсорбция жидкости, что является одной из причин развития почечной недостаточности [9, 10].
Отравление этиленгликолем характеризуется фазностью развития патологического процесса, в ней выделяют следующие периоды: начальный (опьянения с возбуждением); скрытый (мнимого благополучия); выраженных проявлений (а – преимущественно мозговых нарушений; б – преимущественно поражения внутренних органов: печени и почек); восстановления и последствий. Начальные проявления напоминают симптомы при алкогольной интоксикации: депрессия, атаксия, рвота. К сожалению, такая симптоматика появляется только через несколько часов после попадания этиленгликоля в организм и часто остается незамеченной владельцем животного. При достаточно большом количестве принятого внутрь яда в течение последующих 12 ч развиваются полиурия, полидипсия и дегидратация организма. Эти симптомы характерны для начинающейся олигурической острой почечной недостаточности. У кошек почечная недостаточность возникает в первые 12 – 24 ч. К неспецифическим проявлениям отравления относятся: изъязвление слизистой оболочки полости рта, гиперсаливация, рвота, олигурия с изостенурией и возникновение анурии в течение 4 дней. При поступлении большого количества этиленгликоля быстро развивается кома, животное погибает в течение нескольких часов , в первую очередь из-за угнетающего действия вещества на ЦНС [3, 11].
Относительно смертельной дозы этиленгликоля в литературе нет единого мнения. Значительное влияние на выраженность токсического эффекта оказывают общее состояние организма и индивидуальные особенности животного. Большинство смертельных отравлений у собак вызывается приемом 4,4–4,6 г/кг этиленгликоля; кошки более чувствительны, и смертельная доза для них составляет только 2,0 г/кг; для кроликов – 5,0 г/кг; для морских свинок – 6,6 – 11,1 г/кг; для крыс, по данным разных авторов, – от 7,5 до 13,0 г/ кг, для мышей – 8,0 г/кг [6, 10].
Материалы и методы исследований . В химико-токсикологическом отделе Красноярской краевой ветеринарной лаборатории нами зарегистрирован (2011 г.) случай отравления собаки этиленгликолем.
Анамнез: кобель, возраст 3 года; спустя примерно 9 часов после кормления у собаки появились признаки болезни: рвота, миоклонус, атаксия, очаговые конвульсии, ступор, кома и смерть. Как пояснил владелец, вода для приготовления корма для собаки хранилась в канистрах из-под антифриза.
После смерти собака была доставлена в ветеринарную лабораторию для установления причин смерти.
При вскрытии наблюдали следующую патологоанатомическую картину: острый катаральногеморрагический энтерит кишечника. Печень кровенаполнена, увеличена, на разрезах имела «мускатный» вид, в ней были выражены признаки дистрофии. В почках наблюдается гидропическая дистрофия эпителия извитых канальцев, сильное кровенаполнение мозгового слоя (граница между слоями четко выражена). Паралич сердца. Множественные кровоизлияния в головном мозге, который приобрел синеватый цвет, кровенаполнение сосудов головного мозга.
Для исследования был отобран патологический материал: головной мозг, почка, печень, желудок с содержимым, моча.
Исследования проводились по общетоксикологическим показателям: реакция с групповым реактивом Драгендорфа при анализе на алкалоиды, реакция на количественное определение поваренной соли аргентометрическим методом, исследование на определение нитратов и нитритов фотометрическим методом, качественное и количественное определение этиленгликоля, гистологическое исследование срезов головного мозга, общий анализ мочи [8].
Выделение из биологического материала этиленгликоля для качественного определения основано на использовании бензола как селективного переносчика этиленгликоля из объектов в дистиллят. Бензол совместно с парами и небольшим количеством водяного пара переносится в дистиллят. Вода, которая перегоняется при этом, практически содержит весь этиленгликоль. На исследование был отобран желудок с содержимым, в котором после острого отравления содержится больше этиленгликоля, чем в других органах [7, 11].
Для качественного обнаружения этиленгликоля применяли цветные и микрокристаллоскопические реакции, в частности реакцию окисления этиленгликоля перйодатом калия и обнаружение образующегося формальдегида. Эта реакция основана на окислении этиленгликоля перйодатом натрия или калия. В результате указанной реакции образуется формальдегид, который можно обнаружить при помощи фуксинсернистой кислоты [2].
При выполнении этой реакции избыток ионов перйодата калия связывали раствором сернистой кислоты, а затем прибавляли фуксинсернистую кислоту. Реакцию формальдегида с фуксинсернистой кислотой осуществляли по схеме: к 3–5 мл дистиллята прибавляли 5 капель 12 %-го раствора серной кислоты, 5 капель 5 %-го раствора перйодата калия в 5 %-м растворе серной кислоты и взбалтывали. Через 5 мин прибавляли 3–5 капель раствора сернистой кислоты, а затем 4 капли раствора фуксинсернистой кислоты.
Появление красно-фиолетовой или розовой окраски через 3–20 мин свидетельствует о наличии этиленгликоля [11].
Окисление этиленгликоля азотной кислотой и обнаружение щавелевой кислоты проводили при многократном выпаривании этиленгликоля с азотной кислотой, в результате чего образуется щавелевая кислота, которая с солями кальция образует кристаллы оксалата кальция, имеющие характерную форму. Эти кристаллы в ряде случаев появляются через 2–3 суток [4].
Параллельно проводили реакцию с сульфатом меди: от прибавления сульфата меди и щелочи к этиленгликолю образуется соединение, имеющее синюю окраску. К 2–3 мл исследуемого раствора прибавляли 1–2 мл 10 %-го раствора гидроксида натрия и несколько капель 10 %-го раствора сульфата меди. Появление голубой окраски указывает на наличие этиленгликоля в растворе [6, 11].
Выделение из биологического материала этиленгликоля для полуколичественного определения: 20,0 г печени и почек настаивали в ацетоне дважды, объединяли извлечения, прибавляли 0,5 г активированного угля, фильтровали, затем упаривали при 60 0 С до 1–2 мл [8].
Полуколичественное определение проводили методом тонкослойной хроматографии (ТСХ): 0,2 мл извлечения наносили на хроматографическую пластину «Сорбфил» в виде точки, последующую каплю наносили после испарения предыдущей. На расстоянии 2 см от точки исследуемого извлечения наносили 0,02 мл раствора сравнения – этиленгликоля. Пластинку хроматографировали в системе растворителей: хлоро-форм-ацетон-этанол (4:4:1). Затем ее высушивали до удаления запаха растворителей и проявляли (последовательно): 0,1 %-м раствором перйодата калия, после высушивания – 0,1 %-м раствором бензидина. При наличии этиленгликоля наблюдали пятно белого цвета на серо-синем фоне в области стандарта и исследуемого извлечения (Rf 0,4) [8,11].
Количественное определение проводили методом газожидкостной хроматографии: 3 мкл извлечения (пробоподготовка, как для ТСХ) вводили в газожидкостный хроматограф «Кристалл-2000». Условия хроматографирования: колонка HP FFAP 50m·0,32mm·0/52mkm, газ-носитель азот, детектор ионизационнопламенный, Т инжектора =210 0 С, Т детектора =210 0 С, Т колонки изменяется от 100 до 2000С (5 мин – изотерма, затем – со скоростью 15 0 С/мин). Далее идентифицировали пик на хроматограмме.
Общий анализ мочи включает оценку физико-химических характеристик мочи и микроскопию осадка.
Оценка физико-химических характеристик мочи проводилась по общепринятой схеме.
Микроскопия осадка является неотъемлемой и важной частью общеклинических исследований при отравлении этиленгликолем. Принцип метода заключается в микроскопическом исследовании нативных препаратов мочевого осадка, полученного при центрифугировании мочи. Приготовление препарата: в центрифужную пробирку помещали мочу после тщательного ее перемешивания. Центрифугировали в течение 5 мин при скорости 2000 об/мин. Затем быстрым наклоном пробирки сливали прозрачный верхний слой, а оставшийся осадок переносили пипеткой с тонко оттянутым концом на середину предметного стекла и покрывали покровным, затем проводили микроскопию осадка [5].
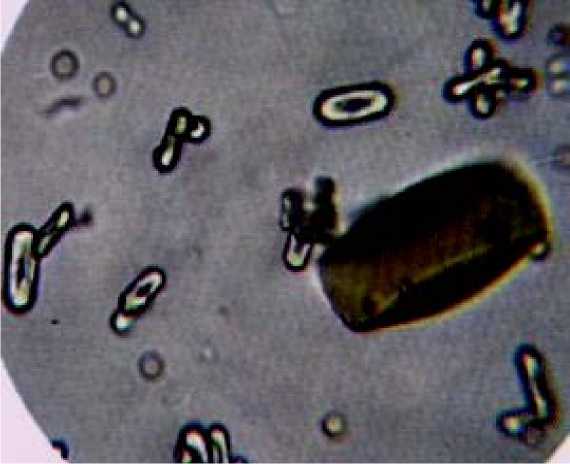
Рис. 1. Кристаллы оксалата кальция в моче
При гистологическом исследовании головного мозга наблюдали следующее: венозное полнокровие (стаз эритроцитов в капиллярах), множественные диапедезные кровоизлияния и очаги некроза в нефроглии (рис . 2).
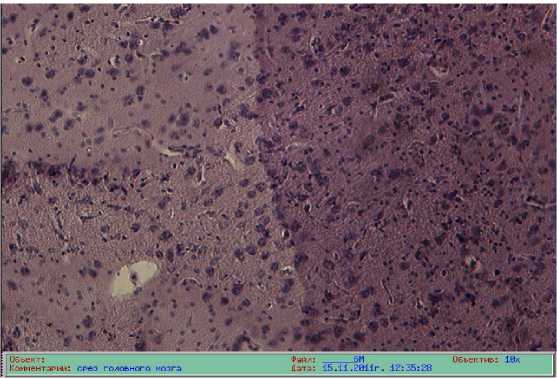
Рис. 2. Гистологический срез головного мозга собаки
При проведении качественной реакции с азотной кислотой микроскопически были обнаружены кристаллы оксалата кальция (рис. 3).

Рис. 3. Окисление этиленгликоля азотной кислотой и обнаружение щавелевой кислоты
При реакции с сульфатом меди появление голубой окраски также свидетельствовало о наличии этиленгликоля.
При тонкослойной хроматографии наблюдали пятно белого цвета на серо-синем фоне в области стандарта и исследуемого извлечения.
При газожидкостной хроматографии этиленгликоль был идентифицирован путем обнаружения пика на хроматограмме (время удержания этиленгликоля 8,68 мин) , количество этиленгликоля составило 116 мг/кг (рис . 4).
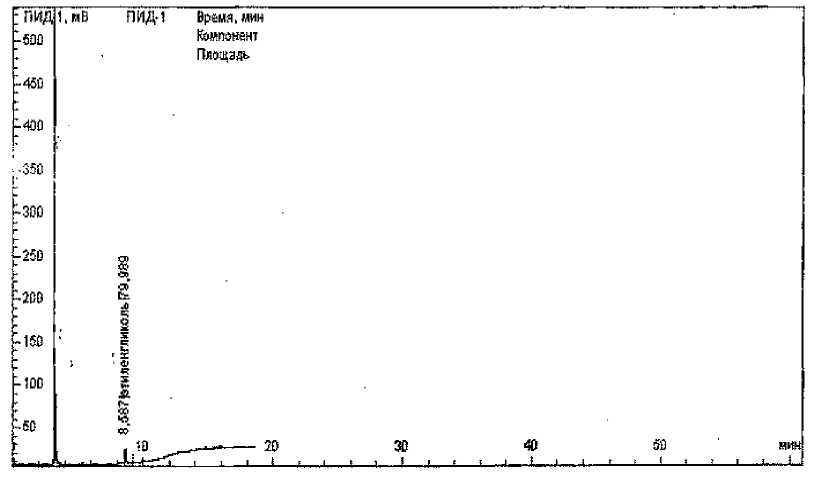
Рис . 4. Хроматограмма выделения этиленгликоля из почек
Для подтверждения была использована абсолютная градуировка (рис . 5).
; ПИД-1. мВ
ПИД-1 Время, МИН
Компонент Площадь
-<100
-3500
-3000*
-2500
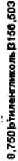
-2000
-1500
-woo
-500
Рис. 5. Абсолютная градуировка этиленгликоля в пробе
Совпадение формы пика и времени удержания при использовании абсолютной градуировки является подтверждением присутствия данного токсиканта в пробе.
Выводы
-
1. Выбор совокупности методов определения этиленгликоля должен являться алгоритмом проведения той или иной экспертизы и предполагать применение методов, основанных на разных физикохимических принципах.
-
2. Первым этапом химико-токсикологического анализа на определение этиленгликоля является анализ первичной информации (анамнеза) и результатов вскрытия.
-
3. Стратегия проведения химико-токсикологического анализа на определение этиленгликоля выстраивается в зависимости от особенностей направленного или ненаправленного исследования.
-
4. Для качественного определения этиленгликоля используют такие методы, как реакция образования формальдегида, цветные реакции с сульфатом меди, обнаружение кристаллов оксалата кальция. Эти методы позволяют очень грубо оценить градацию содержания этиленгликоля в пробе и могут дать недостоверный результат в зависимости от общего его содержания.
-
5. Тонкослойная хроматография является одним из основных методов определения этиленгликоля. Хроматографические зоны этиленгликоля легко извлекаются с пластин, что позволяет дополнять уже имеющуюся информацию о данном веществе результатами исследований другими методами. Заключение о присутствии этиленгликоля дается на основе значения Rf, равном 0,4, а также при сравнении окрасок хроматографических зон исследуемого вещества и использованного аналитического образца сравнения (этиленгликоля).
-
6. Количественный анализ определения этиленгликоля позволяет с гарантированной требуемой точностью определить в образце количественное содержание этиленгликоля, которое составило 116 мг/кг.
-
7. Газовая хроматография – один из самых современных методов идентификации этиленгликоля. При использовании данного метода достигается экспрессность, точность, необходимый предел обнаружения, кроме того, метод значительно более удобен и эффективен. При количественной оценке результатов разделения методом газовой хроматографии большое значение имеет форма пика и время удержания.


