Отсутствие взаимодействия тамоксифена с ASP351 и PHE404 эстрогенового рецептора может приводить к раку эндометрия
Автор: Шкиль Д.О., Алашеев А.Ю., Асаинов Д.Т., Петерсен Е.В., Максимов Ф.Е.
Журнал: Труды Московского физико-технического института @trudy-mipt
Рубрика: Информатика и управление
Статья в выпуске: 4 (64) т.16, 2024 года.
Бесплатный доступ
Рак молочной железы остается наиболее распространенным видом рака среди женщин, и в значительном числе случаев его прогрессирование обусловлено влиянием эстрогеновых рецепторов. Тамоксифен, являясь селективным модулятором эстрогеновых рецепторов, широко используется в адъювантной терапии, особенно у женщин в пременопаузе. Однако его применение связано с повышенным риском рака эндометрия, что ограничивает его применение. В этом исследовании были проведены молекулярные динамические моделирования комплексов тамоксифена и ралоксифена с эстрогеновым рецептором альфа. Анализ был сосредоточен на взаимодействиях с критическими аминокислотными остатками в активном центре рецептора. Результаты показывают, что ослабленное связывание тамоксифена с этими остатками может лежать в основе его связи с ER-зависимым раком эндометрия.
Рак груди, эстрогеновый рецептор, тамоксифен, рак эндометрия, молекулярная динамика
Короткий адрес: https://sciup.org/142243839
IDR: 142243839 | УДК: 577.32,
Weakened binding of tamoxifen to critical amino acid residues on the estrogen receptor as a potential driver of uterine cancer
Breast cancer remains the most common cancer among women, and in a significant number of cases its progression is due to the influence of estrogen receptors. Tamoxifen, being a selective estrogen receptor modulator, is widely used in adjuvant therapy, especially in premenopausal women. However, its use is associated with an increased risk of endometrial cancer, which limits its use. In this study, molecular dynamics simulations of tamoxifen and raloxifene complexes with estrogen receptor alpha were performed. The analysis focused on interactions with critical amino acid residues within the receptor’s active site. The results indicate that weakened binding of tamoxifen to these residues may underlie its association with ER-dependent uterine cancer.
Текст научной статьи Отсутствие взаимодействия тамоксифена с ASP351 и PHE404 эстрогенового рецептора может приводить к раку эндометрия
Рак молочной железы — наиболее распространённое онкологическое заболевание среди женщин в мире и второе по частоте среди всех видов рака, включая мужчин. Это также ведущая причина смертности от рака среди женщин [1]. Примерно 70-80% случаев рака молочной железы связаны с положительным статусом гормональных рецепторов [2], таких
-
(с) Шкиль Д. О., Алашеев А.Ю., Асаинов Д. Т., Петерсен Е.В., Максимов Ф.Е., 2024
-
(с) Федеральное государственное автономное образовательное учреждение высшего образования «Московский физико-технический институт (пациопальпый исследовательский университет)», 2024
-
2. Результаты и обсуждение
как рецепторы эстрогена и прогестерона, которые стимулируют рост опухолевых клеток под воздействием стероидных гормонов [3]. Адъювантная антигормональная терапия гормонозависимого рака молочной железы включает три подхода: блокаду эстрогеновых рецепторов с использованием избирательных модуляторов рецепторов эстрогена (например, тамоксифена или торемифена); деградацию рецепторов через препараты, такие как фул-вестрант или элацестрант; и ингибирование синтеза эстрогенов при помощи ингибиторов ароматазы, таких как анастрозол и летрозол [4] (рис. 1). У женщин в пременопаузе стандартом первой линии терапии является тамоксифен [5], в то время как в постменопаузе предпочтение отдают ингибиторам ароматазы [6]. Эти подходы имеют свои особенности. Тамоксифен, будучи избирательным модулятором эстрогеновых рецепторов, действует как антагонист в тканях груди, но стимулирует рецепторы в костях, эндометрии и других органах. У женщин в постменопаузе это может повышать риск развития рака эндометрия [7], поэтому он чаще используется у пациенток в пременопаузе [6]. Ингибиторы ароматазы, подавляя синтез эстрогенов, лишают раковые клетки стимула к росту, что приводит к их гибели. Однако дефицит эстрогенов может способствовать развитию остеопороза [9]. Тем не менее ингибиторы ароматазы доказали эффективность в снижении риска рецидива у женщин в постменопаузе [8]. Пациентки могли бы получить преимущество от костнозащитных свойств модуляторов рецепторов эстрогена, если бы такие препараты были безопасны для эндометрия [10]. Изучались альтернативные модуляторы с целью улучшения профиля безопасности. Ралоксифен снижает риск тромбоэмболий и катаракты по сравнению с тамоксифеном, обеспечивая аналогичное снижение риска инвазивного рака молочной железы у женщин в постменопаузе с высоким риском. Однако вероятность неинвазивного рака при этом несколько выше [11]. Также отмечено значительное снижение частоты рака эндометрия [11].
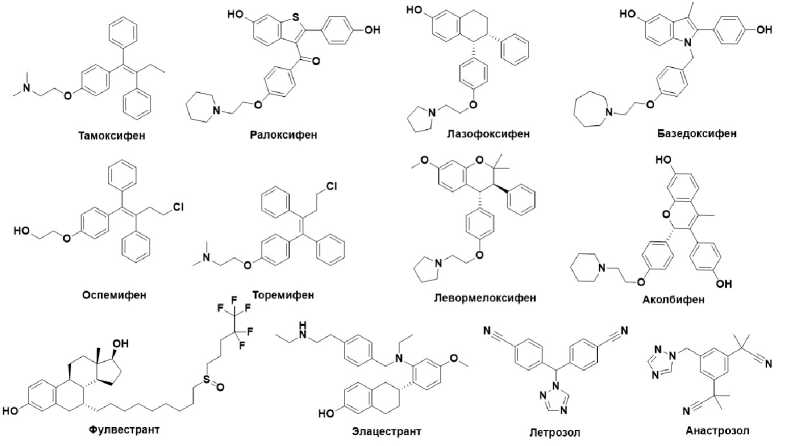
Рис. 1. Адъювантная антигормональная терапия гормопозависимого рака молочной железы
Лазофоксифен доказал эффективность в снижении риска переломов, сердечнососудистых заболеваний и рака молочной железы, но сопровождался повышенным риском тромбоэмболий [12]. Его влияние на эндометрий было сопоставимо с плацебо [12]. Базедоксифен имеет аналогичный профиль безопасности, снижая частоту остеопороза и рака молочной железы без увеличения риска рака эндометрия [13]. Оспемифен также безопасен для эндометрия у женщин в постменопаузе [14]. Торемифен, модифицированный аналог тамоксифена, применяется для лечения метастатического рака молочной железы (одобрен только в США), но, как и тамоксифен, увеличивает риск рака эндометрия [15]. Различия в профилях безопасности модуляторов, вероятно, связаны с их хи- мической структурой и особенностями взаимодействия с рецепторами в различных тканях. В рамках исследования выполнены молекулярно-динамические симуляции комплексов 4-гидрокситамоксифена (активный метаболит тамоксифена) и ралоксифена с рецептором эстрогена альфа. Целью работы было выявление возможных причин развития рака эндометрия путем анализа структурных особенностей этих молекул.
Для 4-гидрокситамоксифена характерен значительный вклад водородных связей с Glu353, а также заметное взаимодействие с Thr347 (рис. 2). Связывание с Asp351 присутствует, однако выражено слабо и имеет преимущественно ионный характер. Важно отметить существенный вклад гидрофобных взаимодействий с Phe404, Met388 и Leu525, что подчеркивает их роль в стабилизации комплекса.
Protein-Ligand Contacts
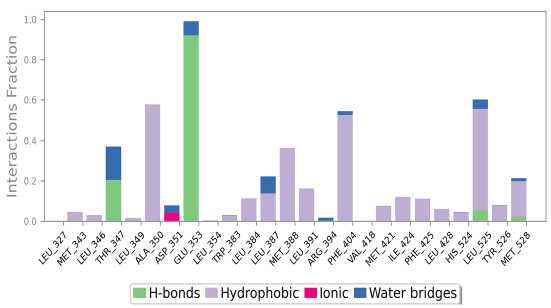
Рис. 2. Профиль белок-лигандного взаимодействия для эстрогенового рецептора и 4-гидрокситамоксифена (PDB ID:2JFD)
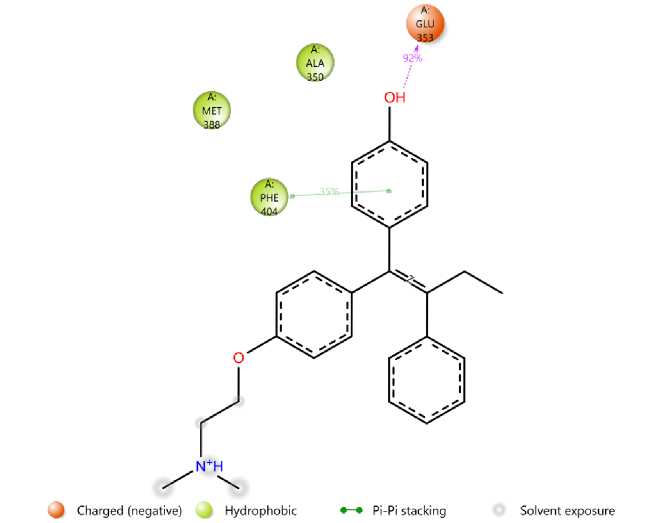
Рис. 3. Основное окружение 4-гидрокситамоксифена внутри эстрогенового рецептора
При анализе взаимодействий 4-гидрокситамоксифена с учетом только тех контактов, которые сохраняются в течение не менее 30% траектории, становится очевидным, что основными являются взаимодействия с Glu353 и Phe404 (рис. 3). Остаток Glu353 образует устойчивую водородную связь с гидроксильной группой тамоксифена, что способствует стабилизации лиганда в активном центре. Взаимодействие с Phe404 осуществляется за счет тг-тг стекинга между ароматическим кольцом Phe404 и одним из колец трифенилэтиле- нового ядра 4-гидрокситамоксифена, что играет ключевую ролв в обеспечении прочного и специфичного связывания. Аминогруппа 4-гидрокситамоксифена, находящаяся вблизи Asp351, по-видимому, не образует прочных контактов с этим остатком, что может быть связано с отсутствием благоприятных условий для устойчивого ионного взаимодействия.
Protein-Ligand Contacts
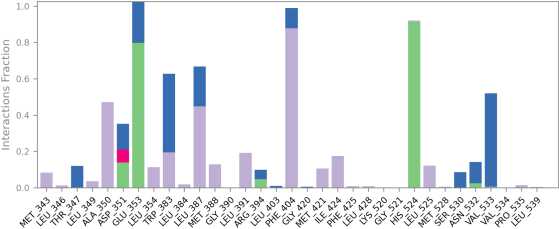
H-bonds Hydrophobic I Ionic I Water bridges I Halogen bonds
Рис. 4. Профиль белок-лигандного взаимодействия для эстрогенового рецептора и ралоксифена (PDB ID:7KBS)
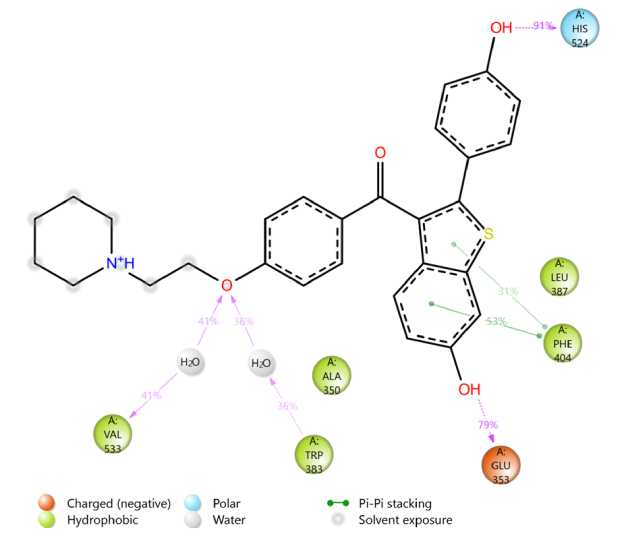
Рис. 5. Основное окружение ралоксифена внутри эстрогенового рецептора
Для ралоксифена, согласно полученным данным, основными взаимодействиями с белком являются водородные связи и гидрофобные взаимодействия (рис. 4). Остаток Glu353 формирует стабильную водородную связь с гидроксильной группой ралоксифена, что подчеркивает его важность в стабилизации комплекса. Значительный вклад также наблюдается со стороны His524, который формирует прочные водородные связи с молекулой лиганда, что способствует усилению связывания. Phe404 демонстрирует существенное гидрофобное взаимодействие с ароматической частью ралоксифена, что подтверждает его роль в стабилизации лиганда за счет я-я стекинга. В то же время остаток Asp351 демонстрирует устойчивую связь смешанного характера. Кроме того, важным вкладом являются водные мостики, которые наблюдаются для Leu387 и Phe404, что дополнительно стабилизирует структуру комплекса. Гидрофобные взаимодействия с остатками, такими как Leu525 и Met388, усиливают взаимодействие с гидрофобными частями ралоксифена. Таким образом, взаимодействия с Glu353, His524, Asp351 и Phe404 являются ключевыми для стабилизации комплекса ралоксифена с белком, дополняемыми гидрофобными контактами и водивши мостиками.
На рисунке 5 представлено окружение ралоксифена в комплексе с рецептором. Ключевыми взаимодействиями являются водородная связв с Glu353, образуемая гидроксильной группой ралоксифена, которая играет важнейшую роль в стабилизации лиганда в активном центре белка, и водородная связь с His524 — уникальный фармакофор ралоксифена, отсутствующий у 4-гидрокситамоксифена. Эта связь является одним из наиболее стабильных контактов, обеспечивающих дополнительную фиксацию лиганда. Гидрофобные взаимодействия с Phe404 и Leu387 значительно укрепляют комплекс за счет взаимодействий с ароматической системой ралоксифена, при этом тг-тг стекинг с Phe404 дополнительно усиливает эти гидрофобные взаимодействия, подчеркивая ключевую роль данного остатка.
Комплексы рецептор-лиганд были извлечены из базы данных белковых структур RCSB PDB и предварительно обработаны в соответствии со стандартными протоколами. Для подготовки систем к молекулярно-динамическому моделированию (МД) комплексы были сольватированы с использованием модуля System Builder программного пакета Desmond. Каждая система была помещена в прямоугольную периодическую ячейку, заполненную молекулами воды модели TIP3P, с границами, отстоящими на 12 А от ближайших атомов белка. Для воспроизведения физиологических условий и обеспечения нейтральности заряда системы были добавлены ионы натрия и хлорида до концентрации 0,145 М. Перед основным этапом моделирования производилась минимизация энергии и короткие релаксационные прогоны МД, чтобы устранить стерические столкновения и стабилизировать системы. Эти этапы проводились в соответствии с протоколами по умолчанию Desmond. Моделирование каждой системы проводилось в течение 50 наносекунд с шагом интегрирования 2 фемтосекунды. Координаты атомов сохранялись каждые 2 пикосекунды для последующего анализа траекторий.
Для ралоксифена и 4-гидрокситамоксифена ключевой контакт с Glu353 играет важнейшую роль в стабилизации комплекса. Однако у ралоксифена дополнительно наблюдается устойчивая связь с His524, которая также может усиливать антагонистический эффект. Пока не ясно, является ли эта связь отличительной чертой хемотипа ралоксифена или же она напрямую связана с антагонистической активностью. В случае Asp351 и Phe404 у 4-гидрокситамоксифена эти взаимодействия также присутствуют, но в слабой степени, в то время как у ралоксифена они значительно усилены. Это приводит нас к гипотезе, что недостаточная степень взаимодействия с Asp351 и Phe404 может быть связана с развитием рака эндометрия при использовании 4-гидрокситамоксифена. Таким образом, более детальное изучение механизма связывания и специфичности этих взаимодействий может пролить свет на различия в активности двух соединений. В дальнейшем планируется продолжить изучение селективных модуляторов эстрогеновых рецепторов с целью сбора статистики, чтобы оценить, насколько значимыми являются различия во взаимодействиях с ключевыми аминокислотными остатками, и их влияние на антагонистическую активность.
Работа выполнена при поддержке Минобрнауки РФ, проект № 1024081900029-8.
Список литературы Отсутствие взаимодействия тамоксифена с ASP351 и PHE404 эстрогенового рецептора может приводить к раку эндометрия
- WHO International Agency for Research on Cancer. https://gco.iarc.fr/en.
- Joe B.N. Clinical Features, Diagnosis, and Staging of Newly Diagnosed Breast Cancer. URL: https://www.uptodate.com/contents/clinical-features-diagnosis-and-stagingof-newly-diagnosed-breast-cancer.
- Anderson W.F., Chatterjee N., Ershler W.B., Brawley O.W. Estrogen Receptor Breast Cancer Phenotypes in the Surveillance, Epidemiology, and End Results Database // Breast Cancer Research and Treatment. 2002. V. 76. P. 27–36. DOI:10.1023/A:1020299707510.
- Trayes K.P., Cokenakes S.E.H. Breast Cancer Treatment // American Family Physician. 2021. V. 104. P. 171–178.
- Fisher B., Costantino J.P., Wickerham D.L., Cecchini R.S., Cronin W.M., Robidoux A., Bevers T.B., Kavanah M.T., Atkins J.N., Margolese R.G., et al. Tamoxifen for the Prevention of Breast Cancer: Current Status of the National Surgical Adjuvant Breast and Bowel Project P-1 Study // Journal of the National Cancer Institute. 2005. V. 97. P. 1652–1662. DOI:10.1093/jnci/dji372.
- Buzdar A.U., Hortobagyi G. Update on Endocrine Therapy for Breast Cancer // Clinical Cancer Research. 1998. V. 4. P. 527–534.
- Maximov P.Y., Lee T.M., Jordan V.C. The Discovery and Development of Selective Estrogen Receptor Modulators (SERMs) for Clinical Practice // Current Clinical Pharmacology. 2013. V. 8. P. 135–155. DOI:0.2174/1574884711308020006.
- Aromatase Inhibitors versus Tamoxifen in Early Breast Cancer: Patient-Level Meta-Analysis of the Randomised Trials. The Lancet // 2015. V. 386. P. 1341–1352. DOI:10.1016/S0140-6736(15)61074-1.
- Tseng O.L., Spinelli J.J., Gotay C.C., Ho W.Y., McBride M.L., Dawes M.G. Aromatase Inhibitors Are Associated with a Higher Fracture Risk than Tamoxifen: A Systematic Review and Meta-Analysis // Therapeutic Advances in Musculoskeletal Disease. 2018. V. 10. P. 71–90. DOI:10.1177/1759720X18759291.
- Jordan V.C. SERMs: Meeting the Promise of Multifunctional Medicines // Journal of the National Cancer Institute. 2007. V. 99. P. 350–356. DOI:10.1093/jnci/djk062.
- Vogel V.G. Effects of Tamoxifen vs Raloxifene on the Risk of Developing Invasive Breast Cancer and Other Disease Outcomes: The NSABP Study of Tamoxifen and Raloxifene (STAR) P-2 Trial // JAMA. 2006. V. 295. P. 2727. DOI:10.1001/jama.295.23.joc60074.
- Cummings S.R., Ensrud K., Delmas P.D., LaCroix A.Z., Vukicevic S., Reid D.M., Goldstein S., Sriram U., Lee A., Thompson J. [ et al.]. Lasofoxifene in Postmenopausal Women with Osteoporosis // New England Journal of Medicine. 2010. V. 362. P. 686–696. DOI:10.1056/NEJMoa0808692.
- Archer D.F., Pinkerton J.V., Utian W.H., Menegoci J.C., de Villiers T.J., Yuen C.K., Levine A.B., Chines A.A., Constantine G.D. Bazedoxifene, a Selective Estrogen Receptor Modulator // Menopause. 2009. V. 16. P. 1109–1115. DOI:10.1097/gme.0b013e3181a818db.
- Constantine G.D., Goldstein S.R., Archer D.F. Endometrial Safety of Ospemifene // Menopause. 2015. V. 22. P. 36–43. DOI:0.1097/GME.0000000000000275.
- Zhou W.-B., Ding Q., Chen L., Liu X.-A., Wang S. Toremifene Is an Effective and Safe Alternative to Tamoxifen in Adjuvant Endocrine Therapy for Breast Cancer: Results of Four Randomized Trials // Breast Cancer Research and Treatment. 2011. V. 128. P. 625–631. DOI:10.1007/s10549-011-1556-5.


