Палочково-колбочковая дистрофия с мутацией в гене GUCY2D (клинический случай)
Автор: Зольникова И.В., Кадышев В.В., Зинченко Р.А., Егорова И.В.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Дерматовенерология
Статья в выпуске: 4 т.14, 2018 года.
Бесплатный доступ
Приводится клинический случай палочково-колбочковой дистрофии (беспигментной формы пигментного ретинита) при мутации в гене GUCY2D. Мутации в гене GUCY2D являются частой причиной амавроза Лебера (LCA1, OMIM 204000), обнаружены при центральной ареолярной хориоидальной дистрофии 1 (CACD1, OMIM 215500); мутации в гетерозиготном, компаунд- гетерозиготном и гомозиготном состоянии описаны при колбочковой дистрофии CORD6 (OMIM 601777), однако при палочково-колбочковой дистрофии не описаны. У пациента с жалобами на нарушение зрения в темноте установлено снижение остроты зрения с максимальной коррекцией до 0,7 на правом и 0,9 на левом глазу. По данным максимальной электроретинографии (ЭРГ) выявлено снижение функции периферической сетчатки. Высокочастотная ритмическая ЭРГ с частотой стимуляции 30Гц и макулярная ЭРГ были в пределах нормы. У пациента выявлен не описанный ранее как патогенный вариант нуклеотидной последовательности в экзоне 11 гена GUCY2D (chrl 7:7916486G>A), приводящий к образованию миссенс-мутации (p.Gly727Ser, NM_000180.3) в гетерозиготном состоянии. Таким образом, впервые выявлены генофенотипические ассоциации палочково-колбочковой дегенерации с ранее неизвестными патологическими последовательностями в гене GUCY2D.
Ассоциация генотипа и фенотипа, палочково-колбочковая дистрофия, электроретинограмма
Короткий адрес: https://sciup.org/149135228
IDR: 149135228 | УДК: 617.735-007.23
Rod-cone dystrophy with mutation in GUCY2D gene (clinical case)
The cinical case of rod-cone dystrophy (retinitis pigmentosa sine pigmento) in a patient with mutation in GUCY2D gene is described Mutations in GUCY2D gene are the common cause of Leber Congenital Amaurosis (LCA1, OMIM 204000), central areolarchoroidal dystrophy (CACD1 OMIM 215500), mutations in heterozygous, compound heterozygous and homozygous state are described in cone dystrophy CORD6 (OMIM 601777), but have not been described in rod-cone dystrophy. In patient who complained of nictalopia decrease of the best corrected visual acuity to 0.7 OD and 0.9 OS was revealed. Maximal electroretinogram was subnormal, which indicated decrease in the function of peripheral retina. 30 Hz flicker and macular ERG were within normal range. Not described previously as pathogenic variant of nucleotide sequence in exon 11 of GUCY2D gene (chrl 7:7916486G>A), causing missense mutation (p. Gly727Ser, NM_000180.3) in heterozygous state in patient was revealed. Thus we are first to describe genotype-phenotype associations of rod-cone degeneration with mentioned above pathological in GUCY2D gene.
Текст научной статьи Палочково-колбочковая дистрофия с мутацией в гене GUCY2D (клинический случай)
-
1 В ФГБУ «Московский НИИ глазных болезней им. Гельмгольца» Минздрава России обратился пациент К. 1983 г.р. с жалобами на никталопию. При осмотре острота зрения с максимальной коррекцией составила OD 0,7 c sph- 2,75D cyl- 0,5D ax 180° и OS 0,9 c sph –2,75D cyl –0,5D ax 180°. Передний отрезок спокойный. На глазном дне выявлена восковидная бледность диска зрительного нерва (ДЗН) и сужение ретинальных артерий, на периферии сетчатки отсутствовала пигментация в виде «костных телец».
Электроретинографические исследования проводились на электроретинографе фирмы МБН (Россия). На правом глазу амплитуда а-волны составила 36,7 мкВ, латентность а-волны 32,5 мс, амплитуда b-волны 166 мкВ, латентность b-волны 63,7 мкВ. На левом глазу амплитуда а-волны составила 50,5 мкВ, латентность а-волны 29,5 мс, амплитуда b-волны 192 мкВ, латентность b-волны 60 мкВ. Следователь- но, максимальная ганцфельд ЭРГ на обоих глазах была субнормальна (норма амплитуды b-волны составляет 250–450 мкВ), что свидетельствовало о снижении функции наружных и средних слоев периферической сетчатки (рис. 1).
Амплитуда высокочастотной ритмической ЭРГ на 30 Гц была в норме и составила 20,7 мкВ на правом и 24,2 мкВ на левом глазу (при норме 20–50 мкВ), что свидетельствовало о сохранении функции колбочковой системы сетчатки. Электроретинографические кривые представлены нa рис. 2.
Макулярная ЭРГ (МЭРГ) на красный стимул оставалась в пределах нормы, что свидетельствовало о нормальной функции наружных и средних слоев сетчатки в фовеа. На правом глазу амплитуда а-волны МЭРГ составила 5,1 мкВ, латентность а-волны 25 мс, амплитуда b-волны 19,8 мкВ, латентность b-волны 52,9 мкВ. На левом глазу амплитуда а-волны соста-
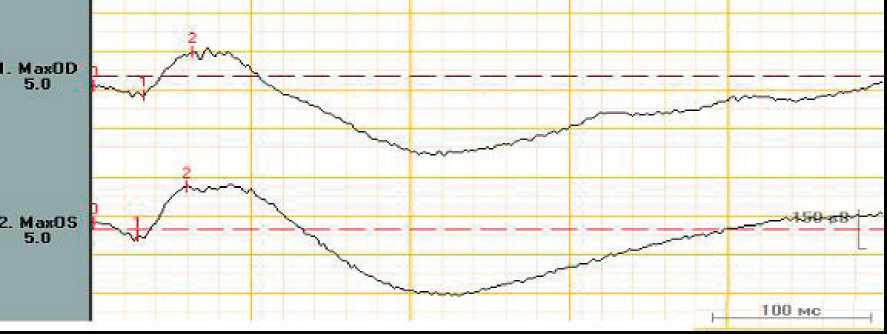
Рис. 1. Максимальная ЭРГ правого и левого глаз
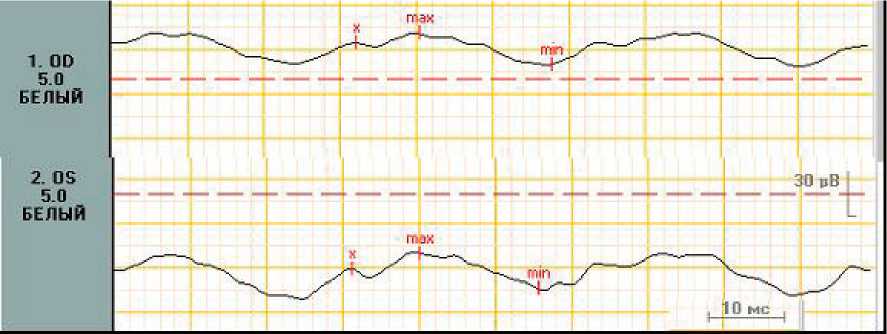
Рис. 2. Высокочастотная ритмическая ЭРГ на стимул с частотой 30 Гц правого и левого глаз
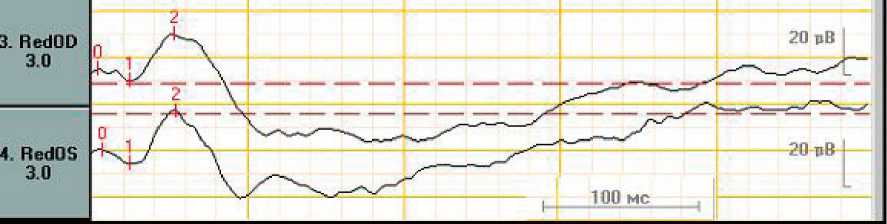
Рис. 3. Макулярная хроматическая ЭРГ на красный стимул правого и левого глаз
вила 5,98 мкВ, латентность а-волны 25 мс, амплитуда b-волны 22,5 мкВ, латентность b-волны 54,5 мкВ (рис. 3).
Таким образом, данные электрофизиологических исследований указывали на вовлечение периферической сетчатки. У пациента на основании клинических и электрофизиологических данных диагностирована палочково-колбочковая дистрофия. Для установления клинико-генетической формы пигментного ретинита пациент направлен в ФГБНУ «Медико-генетический научный центр», где ему было назначено проведение молекулярно-генетических исследований.
При использовании метода секвенирования следующего поколения (NGS) выявлен не описанный ранее как патогенный вариант нуклеотидной последовательности в экзоне 11 гена GUCY2D (chr17:7916486G>A), приводящий к образованию миссенс-мутации (p.Gly727Ser, NM_000180.3) в гетерозиготном состоянии. Частота выявленного варианта нуклеотидной последовательности в контрольной выборке The Genome Aggregation Database (gnomAD) составляет 0,04%. Алгоритмы предсказания патогенности SIFT, Provean, PolyPhen2, Mutation Taster оценивают выявленный вариант нуклеотидной последовательности как патогенный.
Палочково-колбочковая дегенерация представляет собой беспигментную форму пигментного ретинита [1–2]. GUCY2D (OMIM 600179) — мембранная гу-анилатциклаза 2D (guanylate cyclase 2d, membrane), ген которой локализован на 17p13.1 [3]. Колбочково-палочковая дистрофия 6 (СORD6, OMIM 601777) с аутосомно-рецессивным (АР) и аутосомно-доминантным типом наследования была описана Kelsell et al. [3]. Чаще всего гомозиготные мутации в гене
GUCY2D вызывают врожденный амавроз Лебера 1-го типа (Leber congenital amaurosis-1, LCA1; OMIM 204000) [4]. В базе данных OMIM описаны и другие заболевания, вызванные мутацией в гене GUCY2D. Например, центральная ареолярная хороидальная дистрофия 1 (CACD1, OMIM 215500) с АР типом наследования описана в семье, где была обнаружена миссенс-мутация в гене GUCY2D [5]. На сегодняшний день мутации в гене GUCY2D , в частности при амаврозе Лебера, ассоциированном с этим геном, подлежат генной терапии, эффективность и безопасность которой еще оценивается в клинических испытаниях [6, 7].
Таким образом, впервые в российской популяции описаны генофенотипические ассоциации клинической картины палочково-колбочковой дегенерации (беспигментной формы пигментного ретинита) с ранее неизвестными патологическими последовательностями в гене GUCY2D (p.Gly727Ser, NM_000180.3).
Список литературы Палочково-колбочковая дистрофия с мутацией в гене GUCY2D (клинический случай)
- Пигментный ретинит или тапеторетинальная абиотрофия. В кн: Шамшинова A.M. Наследственные и врожденные заболевания сетчатки и зрительного нерва. М.: Медицина, 2001; с. 134-51
- Шамшинова A.M., Зольникова И.В. Молекулярные основы наследственных дегенерации сетчатки. Медицинская генетика 2004; (4): 160-9
- Kelsell RE, Evans К, Gregory CY, et al. Localisation of a gene for dominant cone-rod dystrophy (CORD6) to chromosome 17p. Hum Molec Genet 1997; (6): 597-600
- Boye SE. A Mini-review: Animal Models of GUCY2D Leber Congenital Amaurosis (LCA1). Adv Exp Med Biol 2016; (854): 253-8
- Hughes AE, Meng W, Lotery AJ, et al. A novel GUCY2D mutation, V933A, causes central areolar choroidal dystrophy. IOVS 2012; (53): 4748-53
- Jacobson SG, Cideciyan AV, Sumaroka A,.et al. Defining Outcomes for Clinical Trials of Leber Congenital Amaurosis Caused by GUCY2D Mutations. Am J Ophthalmol 2017; (177): 44-57
- McCullough KT, Boye SL, Fajardo D, et al. Somatic gene editing of GUCY2D byAAV-CRISPR/Cas9 alters retinal structure and function in mouse and macaque. Hum Gene Ther 2018 Oct 25


