Параметры окислительного стресса и эндогенной интоксикации при экспериментальном моделировании деструктивного холецистита
Автор: Беков Т.А., Уметалиев Ю.К.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Медицинские науки
Статья в выпуске: 2 т.12, 2026 года.
Бесплатный доступ
Острый деструктивный холецистит (ОДХ) остается серьезной проблемой абдоминальной хирургии с высоким уровнем осложнений и летальности. Традиционный взгляд на его патогенез как на следствие обструкции и инфекции является недостаточным. Современные данные указывают на ключевую роль системных нарушений, в частности, окислительного стресса и эндогенной интоксикации, однако их временная динамика и взаимосвязь при ОДХ изучены недостаточно. Цель - комплексное исследование временной динамики параметров окислительного стресса (ОС) и эндогенной интоксикации (ЭИ) в условиях экспериментального моделирования деструктивного холецистита. Эксперимент проведен на 60 кроликах-самцах с моделью ОДХ, созданной путем лигатуры пузырного протока и введения бактериальной суспензии. Животные были разделены на 5 групп в зависимости от срока забора материала (исходно, 2, 5, 7, 10 сутки). В мембранах эритроцитов и плазме крови определяли маркеры перекисного окисления липидов (ПОЛ) – диеновые конъюгаты (ДК), кетодиены (КТ), малоновый диальдегид (МДА); активность антиоксидантной системы (АОС) – общую антиокислительную активность (АОА) и каталазу; маркеры ЭИ – концентрацию среднемолекулярных пептидов (СМП) и активность фосфолипазы А2; а также фосфолипидный состав мембран эритроцитов. Результаты: Выявлена прогрессирующая активация ПОЛ: к 7-м суткам уровень ДК, КТ и МДА достоверно увеличился в 2,9; 5,4 и 3,7 раза соответственно относительно исходного уровня (p<0,001). К 5-м суткам зафиксировано истощение АОС – снижение АОА плазмы и активности каталазы (p<0,05), достигшее максимума к 7-м суткам (снижение в 3 раза, p<0,001). Параллельно нарастала ЭИ: концентрация СМП к 7-м суткам увеличилась в 2 раза (p<0,001), а активность фосфолипазы А2 – в 5 раз (p<0,001). Установлены сильные положительные корреляции между маркерами ПОЛ, СМП и активностью фосфолипазы (r=0,63-0,78). Развитие экспериментального деструктивного холецистита характеризуется стадийным формированием порочного круга, инициируемого окислительным стрессом, который приводит к истощению антиоксидантной системы, активации фосфолипазы А2, глубокому нарушению структуры клеточных мембран и нарастанию эндогенной интоксикации.
Окислительный стресс, эндогенная интоксикация, деструктивный холецистит, перекисное окисление липидов, антиоксидантная система, фосфолипаза A2, среднемолекулярные пептиды
Короткий адрес: https://sciup.org/14134456
IDR: 14134456 | УДК: 616.36-002-092.9/577.3/616-092.9 | DOI: 10.33619/2414-2948/123/44
Parameters of Oxidative Stress and Endogenous Intoxication in Experimental Modeling of Destructive Cholecystitis
Acute destructive cholecystitis (ADC) remains a serious problem in abdominal surgery with high rates of complications and mortality. The traditional view of its pathogenesis as a consequence of obstruction and infection is insufficient. Modern data point to the key role of systemic disorders, particularly oxidative stress and endogenous intoxication, but their temporal dynamics and interrelationship in ADC are poorly understood. A comprehensive study of the temporal dynamics of oxidative stress (OS) and endogenous intoxication (EI) parameters in an experimental model of destructive cholecystitis. The experiment was conducted on 60 male rabbits with an ADC model created by ligation of the cystic duct and injection of a bacterial suspension. The animals were divided into 5 groups according to the sampling time point (baseline, 2, 5, 7, 10 days). Markers of lipid peroxidation (LPO) – diene conjugates (DC), ketodienes (KD), malondialdehyde (MDA); activity of the antioxidant system (AOS) – total antioxidant activity (TAA) and catalase; markers of EI – concentration of middle molecular weight peptides (MMWP) and phospholipase A2 activity; as well as the phospholipid composition of erythrocyte membranes were determined in erythrocyte membranes and blood plasma. A progressive activation of LPO was revealed: by day 7, the levels of DC, KD and MDA significantly increased by 2.9, 5.4 and 3.7 times, respectively, compared to the baseline (p<0.001). By day 5, depletion of the AOS was recorded – a decrease in plasma TAA and catalase activity (p<0.05), reaching a maximum by day 7 (a 3-fold decrease, p<0.001). EI increased in parallel: the concentration of MMWP doubled by day 7 (p<0.001), and phospholipase A2 activity increased 5-fold (p<0.001). Strong positive correlations were established between LPO markers, MMWP and phospholipase A2 activity (r=0.63-0.78). The development of experimental destructive cholecystitis is characterized by a staged formation of a vicious cycle initiated by oxidative stress, which leads to depletion of the antioxidant system, activation of phospholipase A2, profound disruption of cell membrane structure, and an increase in endogenous intoxication.
Текст научной статьи Параметры окислительного стресса и эндогенной интоксикации при экспериментальном моделировании деструктивного холецистита
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 616.36-002-092.9/577.3/616-092.9
Острый деструктивный холецистит (ОДХ) остается одной из наиболее актуальных и проблем современной неотложной хирургии органов брюшной полости. Несмотря на значительный прогресс в диагностических и лечебных технологиях, частота его осложненных форм, таких как эмпиема, гангрена, перфорация желчного пузыря с развитием разлитого перитонита и сепсиса, продолжает оставаться высокой, достигая по данным различных авторов 15-25% [1].
Высокая летальность, особенно в группах пациентов пожилого и старческого возраста с отягощенным коморбидным фоном, диктует необходимость более глубокого изучения патогенетических механизмов, лежащих в основе деструкции стенки желчного пузыря. Традиционный взгляд на патогенез ОДХ как на следствие механической обструкции пузырного протока и инфекционного фактора в настоящее время представляется явно недостаточным. Современные исследования убедительно демонстрируют, что ключевую роль в запуске и прогрессировании деструктивных изменений играют системные нарушения на молекулярно-клеточном уровне, среди которых центральное место занимают дисбаланс про-и антиоксидантных систем с развитием окислительного стресса и накопление продуктов эндогенной интоксикации, формирующие порочный круг, усугубляющий течение заболевания [2, 3].
В последние годы накоплен значительный объем данных, свидетельствующих о критической роли окислительного стресса (ОС) в патогенезе широкого спектра воспалительных и деструктивных заболеваний желудочно-кишечного тракта. Окислительный стресс, определяемый как нарушение равновесия между генерацией активных форм кислорода (АФК) и активностью антиоксидантной системы (АОС), приводит к пероксидации липидов клеточных мембран, денатурации белков и фрагментации ДНК, что в конечном итоге инициирует апоптоз и некроз клеток [4].
Применительно к ОДХ, исследования последних лет показывают, что уже на ранних стадиях обструкции желчевыводящих путей происходит массивная активация нейтрофилов и макрофагов в стенке пузыря, которые в процессе «респираторного взрыва» генерируют огромное количество супероксид-аниона, перекиси водорода и гипохлорита [5].
В исследовании Li et al. (2022) было продемонстрировано, что в образцах ткани желчного пузыря пациентов с флегмонозной и гангренозной формами холецистита уровень малонового диальдегида (МДА) – ключевого маркера липопероксидации – превышал таковой у пациентов с катаральным холециститом в 3,5 и 5,8 раза соответственно, при параллельном снижении активности супероксиддисмутазы (СОД) и глутатионпероксидазы (GPx) [6].
Эти данные напрямую указывают на корреляцию между интенсивностью окислительного стресса и тяжестью морфологических повреждений. Особый интерес представляет изучение роли митохондриальной дисфункции в генезе ОС при холецистите. Работа Chen et al. (2023) на модели холестатического повреждения печени показала, что нарушение оттока желчи приводит к накоплению гидрофобных желчных кислот внутри гепатоцитов, что, в свою очередь, индуцирует открытие митохондриальной поры проницаемости и деполяризацию мембранного потенциала, сопровождающуюся массивным выбросом АФК [7]. Логично предположить, что аналогичные процессы происходят и в эпителиоцитах желчного пузыря, находящихся в условиях постоянного контакта с агрессивным содержимым. Более того, выявили значительное повышение уровня 8-окси-2'-дезоксигуанозина (8-OHdG) – маркера окислительного повреждения ДНК – не только в ткани пузыря, но и в плазме крови больных ОДХ, что свидетельствует о системном характере окислительного стресса и его потенциале в качестве прогностического биомаркера [8].
Однако, несмотря на убедительные доказательства участия ОС в деструкции стенки желчного пузыря, остаются недостаточно изученными временная динамика этих процессов на доклинической стадии, а также их взаимосвязь с другими патогенетическими звеньями, в частности, с синдромом эндогенной интоксикации (ЭИ). Синдром эндогенной интоксикации является неотъемлемым компонентом патогенеза любого тяжелого воспалительного процесса и рассматривается как универсальный патогенетический фактор полиорганной дисфункции. При ОДХ его развитие обусловлено резорбцией из воспаленного и некротизированного желчного пузыря в системный кровоток бактериальных эндотоксинов, продуктов протеолиза, активных медиаторов воспаления, а также веществ, образующихся в результате нарушения детоксикационной функции печени и кишечной барьерной функции [9].
Классическими маркерами ЭИ служат молекулы средней молекулярной массы (МСММ), отражающие уровень низкомолекулярных пептидов и олигонуклеотидов в плазме, а также уровень билирубина, мочевины, креатинина и активность ферментов, таких как щелочная фосфатаза и γ-глутамилтрансфераза [10].
Была установлена прямая корреляционная связь между концентрацией МСММ в плазме крови и индексом тяжести по шкале APACHE-II у пациентов с гнойным холециститом, что подтверждает диагностическую и прогностическую ценность данного показателя [11].
Важнейшим аспектом, связывающим окислительный стресс и эндогенную интоксикацию, является концепция «оксидазной» гипотезы интоксикации. Продукты липопероксидации, в частности, МДА и 4-гидроксиноненал, обладают выраженной токсичностью, способны инактивировать ключевые ферменты и выступать в роли эндогенных сенситизаторов, потенцируя повреждающее действие бактериальных липополисахаридов [12].
Это создает порочный круг: АФК повреждают клетки, что ведет к выходу их содержимого и накоплению токсинов, которые, в свою очередь, активируют лейкоциты и эндотелий, стимулируя дальнейшую продукцию АФК. При обструкции желчных путей происходит значительное повышение уровня вторичных желчных кислот, таких как дезоксихолевая и литохолевая, которые не только сами по себе обладают детергентными свойствами, повреждая мембраны клеток, но и индуцируют окислительный стресс через активацию NADPH-оксидазного комплекса [13].
Таким образом, ОС и ЭИ представляют собой не два параллельных процесса, а тесно интегрированную патогенетическую систему, взаимно отягощающую течение ОДХ.
Перспективным направлением является изучение роли нарушения микробиоты кишечника и увеличения проницаемости кишечной стенки (феномена «дырявого кишечника») в усугублении ЭИ при холецистите. Холестаз, неизбежно сопровождающий ОДХ, приводит к избыточному бактериальному росту в тонкой кишке и транслокации микробных патогенов и их токсинов через кишечный барьер в портальный кровоток [14].
Это дополнительно увеличивает токсическую нагрузку на печень, которая в условиях воспаления и ишемии не справляется с функцией детоксикации. Более того, бактериальные липополисахариды являются мощными индукторами синтеза провоспалительных цитокинов (ФНО-α, ИЛ-1β, ИЛ-6), которые сами по себе способны стимулировать продукцию АФК в митохондриях гладкомышечных клеток и фибробластов стенки желчного пузыря, усиливая деструкцию [15].
Данный цитокиновый каскад является еще одним связующим звеном между интоксикацией и оксидативным повреждением. Несмотря на очевидную клиническую значимость, комплексное экспериментальное изучение динамики параметров окислительного стресса и эндогенной интоксикации именно при деструктивном холецистите остается фрагментарным. Большинство существующих работ либо сфокусированы на клинических аспектах, либо проводятся на моделях холестаза без учета фазы острого гнойнонекротического воспаления [16].
В этом контексте проведение целенаправленного экспериментального исследования с моделированием ОДХ представляется крайне востребованным. Современные модели, такие как лигирование пузырного протока с введением бактериальной суспензии или наложение лигатуры на шейку желчного пузыря с частичной окклюзией сосудов, позволяют с высокой воспроизводимостью получить стадийную картину развития деструкции, аналогичную таковой у человека [17, 18].
Это открывает возможность для точного временного мониторинга маркеров ОС (активность СОД, каталазы, GPx, уровень МДА, восстановленного и окисленного глутатиона) и ЭИ (уровень МСММ, содержание полиненайтриновых лимфоцитов, концентрация оксида азота, уровень среднемолекулярных пептидов) в гомогенатах ткани желчного пузыря, сыворотке крови и гепатоцитах. Актуальность такого комплексного подхода подчеркивается и развитием фармакотерапии, направленной на коррекцию выявленных нарушений. Понимание временных закономерностей в развитии ОС и ЭИ позволит определить «терапевтическое окно» для применения антиоксидантов (мелатонин, альфа-липоевая кислота, N-ацетилцистеин) и энтеросорбентов [19, 20].
Ряд исследований последних лет демонстрирует эффективность комбинированного применения антиоксидантов и методов экстракорпоральной детоксикации при перитоните и панкреонекрозе [21, 22].
Введение мексидола на фоне экспериментального перитонита не только снижало уровень МДА и повышало активность СОД в тканях, но и значимо уменьшало концентрацию МСММ в плазме, что свидетельствует о сочетанном позитивном воздействии на оба патогенетических звена [23].
Подобная стратегия может оказаться высокоэффективной и в лечении тяжелых форм ОДХ, однако для ее разработки необходима надежная экспериментальная база, устанавливающая четкие причинно-следственные связи и временну́ю динамику изучаемых процессов. Изучение параметров окислительного стресса и эндогенной интоксикации в условиях контролируемого экспериментального моделирования деструктивного холецистита является высокоактуальной и своевременной задачей. Полученные данные позволят не только расширить существующие представления о патогенезе этого жизнеугрожающего состояния, но и заложить научную основу для разработки новых патогенетически обоснованных схем терапии, направленных на разрыв порочного круга «оксидативный стресс – эндогенная интоксикация – деструкция ткани», что в конечном итоге будет способствовать снижению частоты осложнений и летальности при данной патологии.
Материалы и методы
Настоящее экспериментальное исследование было проведено на 60 половозрелых кроликах-самцах породы «Шиншилла» со средней массой тела 3,0–3,5 кг. Все животные содержались в стандартных виварийных условиях при контролируемой температуре (22±2°C) и 12-часовом цикле свет/темнота, с свободным доступом к воде и стандартному комбикорму. Эксперимент проводился в строгом соответствии с международными принципами обращения с лабораторными животными (Директива EU 2010/63/EU) и был одобрен Этическим комитетом учреждения.
Моделирование острого деструктивного холецистита (ОДХ) осуществлялось путем лигатуры пузырного протока с последующим введением в просвет желчного пузыря суспензии аутохтонной микрофлоры, выделенной из кишечника животных, в концентрации 1x10^9 КОЕ/мл. Данная методика позволяет воспроизводить стадийное развитие гнойновоспалительного процесса, аналогичное таковому у человека. Животные были рандомизированы на 5 экспериментальных групп (n=12 в каждой) в соответствии со сроком забора материала: исходные данные (интактные животные), 2, 5, 7 и 10 сутки после операции.
Забор биологического материала (кровь, ткань желчного пузыря) проводился под общей анестезией (внутримышечное введение кетамина 40 мг/кг и ксилазина 5 мг/кг) путем тотальной кровепотери из яремной вены. Для биохимических исследований кровь собирали в вакутейнеры с ЭДТА, плазму и мембраны эритроцитов выделяли путем ступенчатого центрифугирования при 1500 g и 10000 g соответственно. Мембраны эритроцитов лизировали в гипотоническом буфере и использовали для дальнейших анализов.
Оценка интенсивности процессов перекисного окисления липидов (ПОЛ) в мембранах эритроцитов проводилась по содержанию первичных (диеновые конъюгаты, ДК) и вторичных (кетодиены, КТ) продуктов, а также конечного продукта – малонового диальдегида (МДА). Концентрацию ДК и КТ определяли спектрофотометрически в гептановом экстракте при длинах волн 232 нм и 278 нм соответственно, выражая в нмоль/мг белка. Уровень МДА оценивали в реакции с тиобарбитуровой кислотой и регистрировали на спектрофотометре при 532 нм, результаты выражали в Ед/мл.
Антиоксидантный статус оценивали в плазме крови. Общую антиокислительную активность (АОА) плазмы определяли методом хемилюминесцентного ингибирования, индуцируя свечение люминол-перекисной системой. Активность ключевого фермента антиоксидантной защиты – каталазы – измеряли спектрофотометрически по скорости разложения перекиси водорода при 410 нм. Для оценки степени эндогенной интоксикации использовали два ключевых параметра. Концентрацию среднемолекулярных пептидов (СМП) в плазме крови определяли методом трёхфазной депротеинизации с последующей спектрофотометрией в ультрафиолетовом диапазоне (λ=254 нм и 280 нм). Активность фосфолипазы А2 в гемолизате эритроцитов измеряли флуориметрическим методом с использованием 1-ацил-2-(12-борапирен-11-ил-додеканоил)-sn-глицеро-3-фосфохолина в качестве субстрата.
Фосфолипидный состав мембран эритроцитов анализировали методом тонкослойной хроматографии на пластинах «Sorbfil». Липиды экстрагировали смесью хлороформ-метанол (2:1), разделяли в системе растворителей хлороформ-метанол-вода-аммиак (120:75:6:2). После визуализации в йодных парах и идентификации по стандартам проводили денситометрию и рассчитывали процентное содержание фосфатидилхолина (ФХ), фосфатидилсерина (ФС), фосфатидилэтаноламина (ФЭА), сфингомиелина (СФМ) и лизофосфатидилхолина (ЛФХ). На основании полученных данных вычисляли коэффициент (ФС+ФЭА)/(СФМ+ФХ), характеризующий проницаемость мембран.
Статистическую обработку данных проводили с использованием пакета прикладных программ «Statistica 10.0». Все количественные показатели представлены как M ± m, где M – выборочное среднее, m – стандартная ошибка среднего. Нормальность распределения проверяли критерием Шапиро-Уилка. Для сравнения групп использовали однофакторный дисперсионный анализ (ANOVA) с последующим тестом Тьюки для множественных сравнений. Для оценки корреляционных связей применяли коэффициент корреляции Пирсона. Различия считались статистически значимыми при p < 0,05.
Результаты исследования
Анализ данных, представленных в таблице 1, демонстрирует прогрессирующую активацию процессов пероксидации липидов (ПОЛ) в мембранах эритроцитов в динамике экспериментального моделирования деструктивного холецистита. Уже на 2 сутки эксперимента наблюдается статистически значимое увеличение концентрации как первичных (диеновые конъюгаты, ДК), так и вторичных (кетодиены, КТ, малоновый диальдегид, МДА) продуктов липопероксидации относительно исходных значений (p<0,05-0,01). Количественная оценка выявила диспропорциональный рост исследуемых маркеров: концентрация ДК повысилась на 27%, тогда как уровень КТ и МДА возрос на 100% и 50% соответственно, что указывает на интенсификацию процессов свободнорадикального окисления уже на начальной стадии воспалительного процесса.
К 5 суткам эксперимента регистрируется дальнейшее усугубление окислительной модификации липидов. Уровень ДК достигает значений, почти в 2 раза превышающих исходные (p<0,01), а концентрация КТ увеличивается в 3 раза (p<0,001). В отличие от этих показателей, содержание МДА стабилизируется, не демонстрируя статистически значимого прироста по сравнению с показателями 2-х суток (p>0,05), что может свидетельствовать о временной стабилизации процессов деградации полиненасыщенных жирных кислот или активации механизмов утилизации альдегидных продуктов.
Наиболее выраженная активация липопероксидации отмечается на 7 сутки эксперимента, о чем свидетельствует достоверное увеличение концентрации всех исследуемых маркеров ПОЛ как относительно исходного уровня (p<0,001), так и по сравнению с предыдущими временными точками (p<0,05–0,01). К 10 суткам эксперимента интенсивность процессов ПОЛ сохраняется на максимальном уровне, достигая пиковых значений относительно контрольной группы (p<0,001).
Таблица 1
ПОКАЗАТЕЛИ ПРОДУКТОВ ПОЛ В МЕМБРАНАХ ЭРИТРОЦИТОВ
ПРИ РАЗВИТИИ ДЕСТРУКТИВНОГО ХОЛЕЦИСТИТА У КРОЛИКОВ
|
Период обследования |
n |
Показатель |
ДК, нмоль/мг белка |
КТ, нмоль/мг белка |
МДА, Ед/мл |
|
Исходные показатели |
12 |
M±m |
0,28±0,02 |
0,10±0,01 |
0,125±0,031 |
|
На 2-е сутки |
12 |
M±m |
0,38±0,04 |
0,20±0,02 |
0,221±0,05 |
|
P (2–1) |
< 0,05 |
< 0,01 |
< 0,05 |
||
|
На 5-е сутки |
12 |
M±m |
0,53±0,06 |
0,33±0,03 |
0,262±0,057 |
|
P (3–1) |
< 0,01 |
< 0,001 |
< 0,05 |
||
|
P (3–2) |
< 0,05 |
< 0,05 |
> 0,05 |
||
|
На 7-е сутки |
12 |
M±m |
0,804±0,071 |
0,54±0,034 |
0,461±0,061 |
|
P (4–1) |
< 0,001 |
< 0,001 |
< 0,001 |
||
|
P (4–2) |
< 0,01 |
< 0,001 |
< 0,05 |
||
|
P (4–3) |
< 0,05 |
< 0,01 |
< 0,05 |
||
|
На 10-е сутки |
12 |
M±m |
0,841±0,072 |
0,58±0,041 |
0,488±0,062 |
|
P (5–1) |
< 0,001 |
< 0,001 |
< 0,001 |
||
|
P (5–2) |
< 0,01 |
< 0,01 |
< 0,05 |
||
|
P (5–3) |
< 0,05 |
< 0,05 |
< 0,05 |
||
|
P (5–4) |
> 0,05 |
> 0,05 |
> 0,05 |
Полученная динамика маркеров окислительного стресса коррелирует с морфофункциональными стадиями развития гнойно-воспалительного процесса в желчном пузыре. Инфицирование полости желчного пузыря бактериальной флорой инициирует каскад свободнорадикальных реакций, приводящий к кумуляции в клеточных мембранах промежуточных (ДК) и конечных (КТ, МДА) продуктов пероксидации липидов, что является одним из ключевых патогенетических механизмов деструкции ткани. Особое патогенетическое значение имеет малоновый диальдегид – реактивный альдегид, образующийся при неферментативном распаде полиненасыщенных жирных кислот, в том числе арахидоновой. Способность МДА вступать в реакции с нуклеиновыми кислотами, фосфолипидами и аминокислотами обуславливает его цитотоксические свойства, а его накопление служит интегральным маркером развития оксидативного стресса.
Выявленная активация процессов липопероксидации находится в тесной взаимосвязи с функциональным состоянием системы антиоксидантной защиты, степень угнетения которой коррелирует с выраженностью клеточных воспалительных реакций. Таким образом, установленная временная динамика маркеров ПОЛ объективно отражает этапность развития окислительного стресса при экспериментальном деструктивном холецистите.
Анализ состояния антиоксидантной системы (АОЗ) в ходе эксперимента выявил характерную динамику исследуемых параметров (Рисунок 1.). На вторые сутки моделирования патологического процесса в желчном пузыре уровень общей антиокислительной активности (АОА) плазмы крови статистически не отличался от исходных значений (p>0,05), тогда как активность ключевого фермента антиоксидантной защиты - каталазы - демонстрировала достоверное повышение (p<0,05). К пятым суткам эксперимента наблюдалось значимое снижение АОА плазмы как относительно исходного уровня, так и по сравнению с показателями вторых суток (p<0,05).
Наиболее выраженные изменения зарегистрированы на седьмые сутки эксперимента, когда отмечалось резкое угнетение активности АОЗ, проявляющееся снижением как общей АОА плазмы, так и активности каталазы приблизительно в 3 раза относительно исходных показателей и значений вторых суток (p<0,001). Данная негативная динамиция сохранялась и на десятые сутки эксперимента (p<0,001).
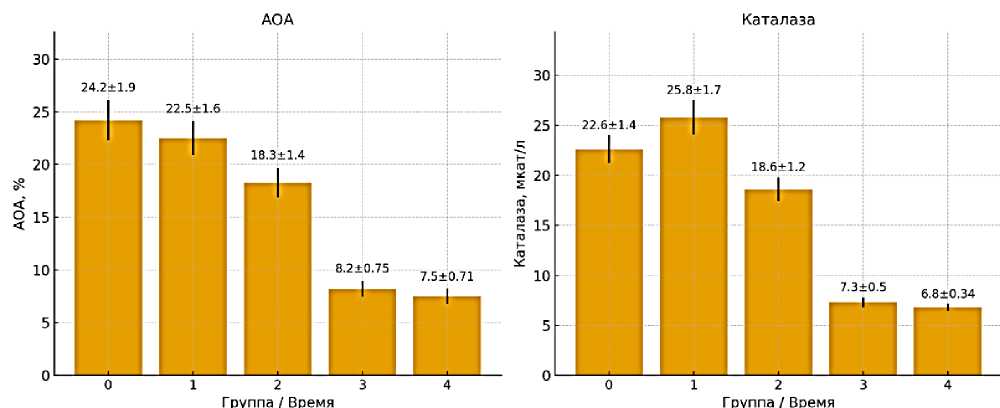
Рисунок 1. Показатели системы АОЗ в плазме крови в процессе динамики моделирования деструктивного холецистита у животных
Согласно данным, представленным на Рисунке 2, динамика концентрации среднемолекулярных пептидов (СМП) в плазме крови имела выраженный прогрессирующий характер.
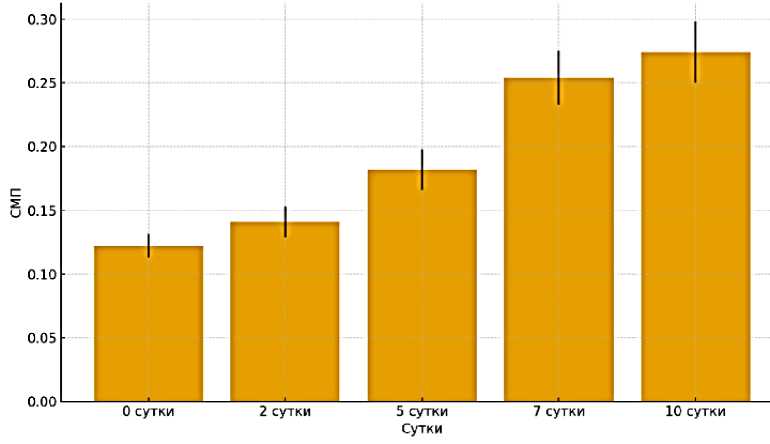
Рисунок 2. Показатели концентрации СМП в плазме крови при моделировании деструктивного холецистита у животных
На вторые сутки экспериментального моделирования деструктивного холецистита содержание СМП не претерпело статистически значимых изменений по сравнению с исходными значениями (p>0,05). Однако к пятым суткам наблюдения зафиксировано достоверное возрастание данного показателя как относительно исходного уровня, так и в сравнении со значениями вторых суток (p<0,05).
К седьмым суткам эксперимента концентрация СМП достигла значений, вдвое превышающих исходный уровень (p<0,001), а также значительно превзошла показатели третьих и пятых суток исследования (p < 0,001). На десятые сутки эксперимента продолжилось прогрессирующее накопление СМП в плазме крови, о чем свидетельствует дальнейший достоверный рост их концентрации относительно всех предшествующих этапов эксперимента (p<0,001).
Анализ динамики активности фосфолипазы выявил прогрессирующий характер её активации в ходе эксперимента (Рисунок 3). Статистически значимое увеличение ферментативной активности по сравнению с исходными значениями регистрируется уже на третьи сутки эксперимента (p<0,05). К пятым суткам наблюдения отмечается дальнейшее достоверное усиление фосфолипазной активности как относительно исходного уровня (p<0,01), так и по сравнению с показателями третьих суток (p<0,05).
Наиболее выраженная активация фермента зафиксирована на седьмые сутки эксперимента, когда значения активности фосфолипазы превысили исходный показатель в 5 раз (p < 0,001), значения третьих суток - в 3 раза (p < 0,001) и показатели пятых суток - в 2 раза (p < 0,001). Полученные данные свидетельствуют о стабильном сохранении значительно повышенной активности фосфолипазы вплоть до десятых суток эксперимента (p < 0,001), что демонстрирует устойчивый характер активации данного фермента в условиях моделирования воспалительного процесса в желчном пузыре.
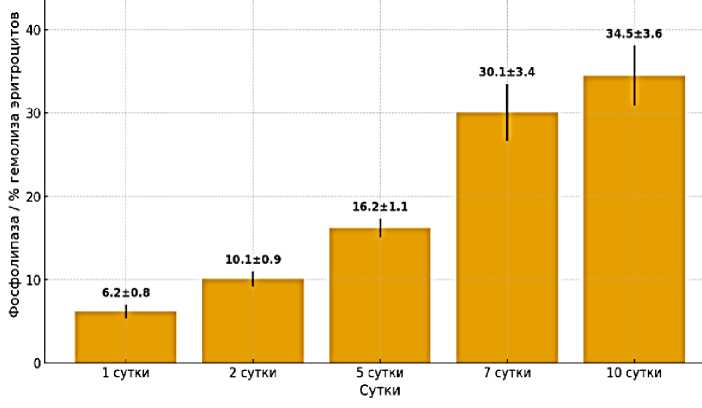
Рисунок 3. Показатели активности фосфолипазы в эритроцитах при моделировании деструктивного холецистита у животных
В рамках настоящего исследования проведен детальный анализ динамики фосфолипидного состава мембран эритроцитов в условиях экспериментального моделирования деструктивного холецистита. Как следует из данных Таблицы 2, на 2 сутки эксперимента зарегистрировано статистически значимое снижение концентрации фосфатидилхолина (ФХ) (p<0,05) и повышение уровня фосфатидилсерина (ФС) (p<0,01) относительно исходных значений, в то время как содержание лизофосфатидилхолина (ЛФХ), сфингомиелина (СФМ) и фосфатидилэтаноламина (ФЭА) оставалось в пределах физиологической нормы (p>0,05). Указанные изменения обусловили достоверное увеличение коэффициента соотношения легкоокисляемых (ФС, ФЭА) и трудноокисляемых (СФМ, ФХ) фракций фосфолипидов (p<0,01).
К 5 суткам эксперимента отмечено прогрессирование нарушений фосфолипидного спектра мембран эритроцитов, проявляющееся значительным увеличением содержания ЛФХ как относительно исходного уровня, так и по сравнению с показателями 2 суток (p<0,01), а также дальнейшим ростом концентрации ФС (p<0,01) при одновременном выраженном снижении уровня ФХ (p < 0,05-0,01). Содержание СФМ и ФЭА сохранялось без существенных изменений (p>0,05), в то время как фосфолипидный коэффициент оставался статистически значимо повышенным (p<0,05).
На 7 сутки эксперимента, соответствующие пику развития деструктивного холецистита, наблюдалось сохранение выявленной ранее тенденции с дополнительным значительным нарастанием концентрации ЛФХ относительно всех предшествующих временных точек исследования (p<0,05-0,001). К 10 суткам эксперимента соотношение фосфолипидных фракций принципиально не отличалось от показателей 7 суток (p<0,05-0,001).
Таблица 2
ФОСФОЛИПИДНЫЙ СОСТАВ МЕМБРАН ЭРИТРОЦИТОВ
У КРОЛИКОВ ПРИ МОДЕЛИРОВАНИИ ДЕСТРУКТИВНОГО ХОЛЕЦИСТИТА
|
Периоды обследования |
Стат. показатели |
ЛФХ, % |
СФМ, % |
ФХ, % |
ФС, % |
ФЭА, % |
ФС+ФЭА СФМ+ФХ |
|
Исходные |
М±m |
6,1 + 0,402 |
24,5 + 1,25 |
28,3 + 1,66 |
19,4 + 1,11 |
21,3 + 1,32 |
0,77 + 0,054 |
|
показатели |
|||||||
|
На 2 сутки |
P 2-1 |
7,5 + 0,65 |
21,4 + 1,6 |
24,2 + 1,47 |
23,9 + 1,2 |
23,0 + 1,5 |
1,128 + 0,062 |
|
>0,05 |
>0,05 |
<0,05 |
<0,05 |
>0,05 |
<0,01 |
||
|
На 5 сутки |
P 3-1 |
13,6 + 0,707 |
20,6 + 1,33 |
19,5 + 0,908 |
26,4 + 1,72 |
21,6 + 1,82 |
1,201 + 0,071 |
|
P 3-2 |
<0,01 |
>0,05 |
<0,01 |
<0,01 |
>0,05 |
<0,01 |
|
|
<0,01 |
>0,05 |
<0,05 |
>0,05 |
>0,05 |
>0,05 |
||
|
На 7 сутки |
P 4-1 |
17,9 + 0,804 |
19,8 + 0,76 |
18,7 + 0,614 |
23,7 + 1,56 |
20,5 + 1,28 |
1,381 + 0,078 |
|
P 4-2 |
<0,001 |
>0,05 |
<0,001 |
<0,05 |
>0,05 |
<0,01 |
|
|
P 4-3 |
<0,001 |
>0,05 |
<0,01 |
>0,05 |
>0,05 |
<0,05 |
|
|
<0,05 |
>0,05 |
>0,05 |
>0,05 |
>0,05 |
>0,05 |
||
|
На 10 сутки |
P 5-1 |
18,3 + 0,774 |
18,6 + 0,612 |
18,3 + 0,591 |
24,1 + 1,81 |
21,4 + 1,61 |
1,233 + 0,069 |
|
P 5-2 |
<0,001 |
>0,05 |
<0,01 |
<0,05 |
>0,05 |
<0,01 |
|
|
P 5-3 |
<0,001 |
>0,05 |
<0,05 |
>0,05 |
>0,05 |
>0,05 |
|
|
P 5-4 |
<0,05 |
>0,05 |
>0,05 |
>0,05 |
>0,05 |
>0,05 |
|
|
>0,05 |
>0,05 |
>0,05 |
>0,05 |
>0,05 |
>0,05 |
Полученные данные свидетельствуют о глубокой структурной перестройке клеточных мембран в условиях моделирования гнойно-воспалительного процесса в желчном пузыре. Выявленные изменения фосфолипидного состава представляют собой интегральный ответ биологических мембран на развитие оксидативного стресса и эндотоксикоза. Снижение концентрации ФХ в мембранных комплексах указывает на угнетение процессов его ресинтеза, что приводит к ослаблению антиоксидантных свойств данного фосфолипида и снижению резистентности клеточных структур к повреждающему действию активированных процессов перекисного окисления липидов и эндогенной фосфолипазы. Патогенетической основой уменьшения содержания ФХ является нарушение процессов трансметилирования ФЭА и конверсии ФХ из ненасыщенной формы в насыщенную. Одновременное накопление ЛФХ в мембранах эритроцитов связано с дисбалансом реакций ацилирования и подавлением активности лизолецитин-ацилтрансферазы, а также может быть следствием блокады метаболических путей трансформации ФХ и изменения механизмов его элиминации из организма.
Обсуждение полученных результатов
Проведенное экспериментальное исследование выявило комплекс взаимосвязанных патобиохимических сдвигов, развивающихся при моделировании деструктивного холецистита и формирующих единый патогенетический контур. Полученные данные убедительно демонстрируют, что в основе деструкции стенки желчного пузыря лежит не просто локальное воспаление, а системный каскад реакций, инициируемых оксидативным стрессом и усугубляемых эндогенной интоксикацией.
Ключевым звеном в запуске патологического процесса является активация свободнорадикального окисления. Выявленная прогрессирующая динамика маркеров ПОЛ — нарастание концентрации диеновых конъюгатов, кетодиенов и малонового диальдегида в мембранах эритроцитов — свидетельствует о персистирующем оксидативном стрессе. Особое значение имеет накопление МДА, являющегося не просто конечным продуктом липопероксидации, но и высокоактивным токсичным соединением, способным инициировать дальнейшее повреждение за счет взаимодействия с белками и нуклеиновыми кислотами. Достижение максимальных значений всех изучаемых маркеров ПОЛ к 7-10 суткам эксперимента коррелирует с пиком морфологических проявлений деструкции, что подтверждает их роль в прямом цитолитическом повреждении.
Важнейшим аспектом патогенеза является дисбаланс в системе антиоксидантной защиты. Обнаруженная на 2 сутки компенсаторная активация каталазы оказалась недолговечной и к 5-7 суткам сменилась критическим угнетением как ферментативного звена (каталаза), так и общей антиокислительной активности плазмы. Истощение АОЗ создает благоприятные условия для неконтролируемой пролонгации реакций свободнорадикального окисления, формируя порочный круг: продукты ПОЛ еще больше подавляют активность ключевых антиоксидантных ферментов.
Полученные данные позволяют установить прямую причинно-следственную связь между оксидативным стрессом и развитием синдрома эндогенной интоксикации. Выявленная сильная положительная корреляция между уровнем продуктов ПОЛ (ДК, КТ, МДА) и концентрацией среднемолекулярных пептидов (r = 0,63–0,73) указывает на общность их происхождения. Накопление СМП является интегральным показателем усиленного протеолиза и нарушения детоксикационной функции, усугубляющим системное повреждение.
Особого внимания заслуживает установленная роль фосфолипазы А2 в механизмах мембранной деструкции. Значительное увеличение ее активности, достигающее к 7-м суткам 500% от исходного уровня, является не только следствием, но и мощным фактором усугубления патологического процесса. Активация фосфолипазы А2, находящаяся в прямой корреляционной связи с интенсивностью ПОЛ (r = 0,71–0,78), запускает два разрушительных процесса: во-первых, прямое повреждение фосфолипидного слоя клеточных мембран, и во-вторых, генерацию провоспалительных медиаторов из освобождающихся жирных кислот.
Нарушение структурной организации мембран подтверждается глубоким ремоделированием их фосфолипидного состава. Выявленные изменения — значительное снижение фосфатидилхолина, увеличение доли лизофосфатидилхолина и фосфатидилсерина, рост коэффициента (ФС+ФЭА)/(СФМ+ФХ) — являются классическими признаками мембранной патологии. Снижение содержания ФХ отражает угнетение процессов его ресинтеза, вероятно, блокады трансметилирования ФЭА и подавления активности лизолецитин-ацилтрансферазы. Увеличение же доли легкопероксидируемых фосфолипидов (ФС, ФЭА) значительно повышает уязвимость мембран к дальнейшему окислительному повреждению.
Вывод
Полученные результаты позволяют сформулировать целостную патогенетическую концепцию развития деструктивного холецистита. Инициирующим звеном выступает массивная активация свободнорадикальных процессов, приводящая к истощению антиоксидантной системы. Продукты ПОЛ, с одной стороны, оказывают прямое цитотоксическое действие, а с другой — активируют фосфолипазу А2, что приводит к дестабилизации фосфолипидного матрикса мембран. Разрушение клеточных структур сопровождается выходом в системный кровоток продуктов деградации, формирующих синдром эндогенной интоксикации, который, в свою очередь, потенцирует исходный оксидативный стресс. Критическим моментом в развитии заболевания являются 7-е сутки, когда наблюдается одновременная максимальная активация ПОЛ, глубокая супрессия АОЗ, пик фосфолипазной активности и нарастание эндотоксикоза.


