Патоморфологические аспекты регенераторного процесса ран, обусловленные применением коллагеновых раневых покрытий, у больных синдромом диабетической стопы
Автор: Луценко Ю.Г., Сычва Д.Р.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.20, 2025 года.
Бесплатный доступ
Цель работы. Оценить морфологические особенности течения репаративных процессов у пациентов с синдромом диабетической стопы (СДС,) обусловленные применением коллагеновых раневых покрытий.Материал и методы. В работе представлен сравнительный ретроспективный анализ гистологического материала тканей ран 112 пациентов СДС. Морфологическое исследование материала проведено при помощи микроскопа «Micros MC 50», объектива «WF EWF 10х/18». Изученный материал разделён на две группы: основную - 62 микропрепарата ткани ран пациентов СДС, при комплексном лечении раневых дефектов использовали коллагеновые раневые покрытия («Зелёная Дубрава» ЗАО, РФ); контрольную - 60 микропрепаратов тканей ран пациентов СДС, местное лечение раневых дефектов состояло из ежедневных перевязок с антисептиками.Результаты и обсуждение. Анализ полученных результатов показал, что применение коллагеновых раневых покрытий влияет на каждую фазу репаративного процесса хронических ран пациентов СДС, способствует более быстрому переходу из альтеративно-экссудативной стадии воспалительной реакции в пролиферативную и в фазу эпителизации; коллаген всасывает раневой экссудат, выполняя дренажную функцию, способствуя ускорению процессов очищения раны, снижает воспалительную реакцию, нормализует работу сосудов микроциркуляторного русла, стабилизируя кровоснабжение в области раневого дефекта и уменьшая гипоксию, приводит к активации репаративных процессов; использование коллагеновых раневых покрытий активирует процесс миграции лейкоцитов, значительно увеличивает число макрофагов, способствуя повышению экспрессии провоспалительных цитокинов, ускоряет процесс ангиогенеза, миграции и пролиферации фибробластов - грануляционная ткань в ранах проходит процесс созревания гораздо быстрее по сравнению с группой пациентов, пролеченных с использованием ежедневных повязок с антисептиками и мазями.Заключение. Применение коллагеновых раневых покрытий в комплексном лечении пациентов с гнойно-некротическими формами СДС может значительно ускорять течение каждой фазы репаративного процесса в раневых дефектах- за счёт влияния данной методики грануляционная ткань способна проходить процесс созревания за более короткий временной промежуток, позволяя сократить сроки подготовки раны к пластическому закрытию с 20-22-х до 12-16 суток.
Сахарный диабет, диабетическая стопа, коллагеновые раневые покрытия, коллаген, макрофаги, фибробласты, регенерация
Короткий адрес: https://sciup.org/140309985
IDR: 140309985 | DOI: 10.25881/20728255_2025_20_1_88
Pathomorphological aspects of the regenerative process of wounds caused by the use of collagen wound coatings in patients with diabetic foot syndrome
The purpose: to evaluate the morphological features of the course of reparative processes in patients with diabetic foot syndrome (DFS) due to the use of collagen wound coatings.Material and methods. The paper presents a comparative retrospective analysis of the histological material of wound tissues of 112 DFS patients. Morphological examination of the material was carried out using a microscope “Micros MC 50”, a lens “WF EWF 10x/18”. The studied material is divided into two groups: the main one is 62 micro-preparations of the wound tissue of DFS patients, collagen wound coatings (“Green Oak”, RF) were used in the complex treatment of wound defects; The control group consisted of 60 micro-preparations of wound tissues of DFS patients, local treatment of wound defects consisted of daily dressings with antiseptics and ointments.Results and discussion. Analysis of the obtained results showed that the use of collagen wound coatings affects each phase of the reparative process of chronic wounds of DFS patients, contributes to a faster transition from the alternativeexudative stage of inflammatory reaction in proliferative and epithelial phase; collagen absorbs wound exudate, performing a drainage function, contributing to acceleration of wound cleansing processes, reduces inflammatory reaction, normalizes the functioning of microcirculatory vessels, stabilizing blood supply in the area of wound defect and reducing hypoxia, leads to the activation of reparative processes; the use of collagen wound coatings activates the process of leukocyte migration, significantly increases the number of macrophages, promoting increased expression of proinflammatory cytokines, speeds up the process of angiogenesis, migration and proliferation of fibroblasts - granulation tissue in the wounds undergoes a maturation process much faster than the group of patients, treated with daily bandages with antiseptics and ointments.Conclusion. The use of collagen wound coatings in the complex treatment of patients with purulent necrotic DFS forms can significantly accelerate the course of each phase of the reparative process in wound defects due to the influence of this technique granulation tissue is able to pass the process of maturation in a shorter period of time, allowing to reduce the time of preparation for plastic closure from 20-22 to 12-16 days.
Текст научной статьи Патоморфологические аспекты регенераторного процесса ран, обусловленные применением коллагеновых раневых покрытий, у больных синдромом диабетической стопы
Диабетическая стопа (синдром диабетической стопы, СДС)-тяжёлое осложнение сахарного диабета (СД), проявляющееся в виде язв с разрушением глубоких тканей стопы, которое возникает в связи с нарушением микроструктуры стопы и микроциркуляции крови, сопровождается разрушением нервных окончаний и нервных волокон [1]. По данным Международной Диабетической Федерации численность пациентов с СД в возрасте от 20 до 79 лет в мире на 1января 2018 г. превысила 425 млн. человек [2; 3]. Распространенность СД в РФ стабильно растёт: на 569 тыс. пациентов по сравнению с 3,779 млн. на декабрь
PATHOMORPHOLOGICAL ASPECTS OF THE REGENERATIVE PROCESS OF WOUNDS CAUSED BY THE USE OF COLLAGEN WOUND COATINGS IN PATIENTS WITH DIABETIC FOOT SYNDROME
Lutsenko Yu.G., Sycheva D.R.*
Donetsk State Medical University named after M. Gorky, Donetsk
Material and methods. The paper presents a comparative retrospective analysis of the histological material of wound tissues of 112 DFS patients. Morphological examination of the material was carried out using a microscope “Micros MC 50”, a lens “WF EWF 10x/18”. The studied material is divided into two groups: the main one is 62 micro-preparations of the wound tissue of DFS patients, collagen wound coatings (“Green Oak”, RF) were used in the complex treatment of wound defects; The control group consisted of 60 micro–preparations of wound tissues of DFS patients, local treatment of wound defects consisted of daily dressings with antiseptics and ointments.
Results and discussion. Analysis of the obtained results showed that the use of collagen wound coatings affects each phase of the reparative process of chronic wounds of DFS patients, contributes to a faster transition from the alternativeexudative stage of inflammatory reaction in proliferative and epithelial phase; collagen absorbs wound exudate, performing a drainage function, contributing to acceleration of wound cleansing processes, reduces inflammatory reaction, normalizes the functioning of microcirculatory vessels, stabilizing blood supply in the area of wound defect and reducing hypoxia, leads to the activation of reparative processes; the use of collagen wound coatings activates the process of leukocyte migration, significantly increases the number of macrophages, promoting increased expression of proinflammatory cytokines, speeds up the process of angiogenesis, migration and proliferation of fibroblasts – granulation tissue in the wounds undergoes a maturation process much faster than the group of patients, treated with daily bandages with antiseptics and ointments.
Conclusion. The use of collagen wound coatings in the complex treatment of patients with purulent necrotic DFS forms can significantly accelerate the course of each phase of the reparative process in wound defects due to the influence of this technique granulation tissue is able to pass the process of maturation in a shorter period of time, allowing to reduce the time of preparation for plastic closure from 20–22 to 12–16 days.
2012 г.; на 254 тыс. по сравнению с 4,094 млн. пациентов на январь 2015 г. [4]. В 79 регионах РФ в 2016 г. зарегистрировано 235 173 новых случаев СД: СД 1-го типа – у 8516 пациентов (3,6%), СД 2-го типа – у 214 668 пациентов (91,3%), другие типы СД – у 11 989 больных (5,1%) [4]. Раневые дефекты, возникающие у пациентов с СД, имеют хроническое течение, склонны к длительному «застреванию» в альтеративной фазе воспаления-в ранах данной этиологии преобладают дистрофические и некротические изменения, значительно замедлены процессы регенерации. Из-за длительно незаживающих раневых дефектов у пациентов СДС значительно возрастает риск

Луценко Ю.Г., Сычёва Д.Р.
ПАТОМОРФОЛОГИЧЕСКИЕ АСПЕКТЫ РЕГЕНЕРАТОРНОГО ПРОЦЕССА РАН, ОБУСЛОВЛЕННЫЕ ПРИМЕНЕНИЕМ КОЛЛАГЕНОВЫХ РАНЕВЫХ ПОКРЫТИЙ, У БОЛЬНЫХ СИНДРОМОМ ДИАБЕТИЧЕСКОЙ СТОПЫ присоединения вторичной бактериальной инфекции, с развитием различных грозных тяжёлых осложнений: гангрены стопы, остеомиелита, анаэробной флегмоны, остеоартропатической формы диабетической стопы с развитием гнойных артритов и артрозов мелких суставов, с дальнейшей деформацией стопы. Данные осложнения значительно снижают качество жизни пациентов, в случаях несвоевременного обращения или неправильно подобранного лечения приводят к ампутации стопы, дальнейшей инвалидизации. Понимание особенностей процессов репарации раневых дефектов и поиск методик, способных ускорить регенерацию ран пациентов СДС чрезвычайно важен в хирургической практике. Одна из проблем лечения раневых дефектов-стимуляция процесса эпителизации, с восстановлением субдермальных, дермальных и эпителиальных слоёв [5]. На сегодняшний день перспективным направлением в решении данной проблемы является использование коллагена. Коллагеновые материалы обладают биосовместимостью с тканями ран пациентов, не токсичны, не являются канцерогенами, сочетают в себе характеристики синтетических полимеров (эластичность, прочность, упругость и другие) [6]. Коллагеновые повязки способны защищать раневую поверхность от попадания вторичной инфекции и бактериальной микрофлоры, препятствуют избыточной потере жидкости, стимулируют ангиогенез, миграцию и пролиферацию фибробластов, обеспечивая созревание грануляционной ткани, стимулируют синтез собственного коллагена, способствуя более быстрому заживлению раневых дефектов [7]. Изученные в данной работе морфологические особенности течения репаративных процессов в тканях ран пациентов СДС, обусловленные применением коллагеновых раневых покрытий в комплексном лечении осложнённых форм диабетической стопы, позволяют понять, насколько эффективна данная методика, возможно ли после её применения сократить сроки подготовки раны к пластическому закрытию с 20–22 до 12–16 суток.
Цель работы: оценить морфологические особенности течения репаративных процессов в тканях нижних конечностей у пациентов СДС, обусловленные применением коллагеновых раневых покрытий в комплексном лечении осложнённых форм диабетической стопы.
Материалы и методы
Проведён сравнительный ретроспективный анализ гистологического материала тканей раневых дефектов 112 пациентов СДС, находившихся на стационарном лечении в специализированных хирургических отделениях ГБУ «ЦГКБ №9», «ГКБ №21» г. Донецка за 2023 г. Среди пациентов с СДС было 56 % мужчин и 44 % женщин в возрасте от 50 до 75 лет с медианным значением 62 (60–70) лет. У всех больных установлен диагноз СД II типа с длительностью заболевания 8,4±4,5 лет. Объем поражения тканей стопы варьировал от I до II степени по классификации Wagner (I степень диагностирована в 59,5 % случаев). Основную группу составили 62 пациента СДС, которым в комплексном лечении ран использовали коллагеновые раневые покрытия («Зелёная Дубрава», ЗАО, РФ).
Группу контроля составили 60 пациентов с гнойнонекротическими формами СДС, местное лечение раневых дефектов которых состояло из ежедневных перевязок с антисептиками и мазями. Морфологическое исследование проводились на базе централизованного патологоанатомического отделения Центральной городской клинической больницы №1 города Донецка. Материал для гистологического исследования – микропрепараты ткани раневых дефектов нижних конечностей пациентов СДС- образцы фиксировались в 5% растворе нейтрального формалина, заливались в парафиновые блоки. Методом последовательных биопсий исследовали кусочки ткани, изъятые со дна раневых дефектов в сроки от 1 до 12–16 суток после начала лечения. Для исследования полученных фрагментов ткани при световой микроскопии использовали окраску срезов гематоксилином и эозином, толуидиновым синим, по ван Гизону, ШИК реакцию. Скорость закрытия язвенного дефекта определялась по расчету его площади и глубины в миллиметрах 1 раз в 7 суток в течение 4 недель. В исследование включались раны площадью более 35 мм2. Площадь раны и ее изменения на фоне лечения оценивались количественно с помощью прозрачной пленки в начале, после 2-х недель лечения, в конце исследования. С помощью микроскопа «Micros MC 50», объектива «WF EWF 10х/18» изучались и сравнивались морфологические особенности течения репаративного процесса в тканях ран пациентов СДС, обусловленные применением коллагеновых раневых покрытий и перевязок с антисептиками и мазями: характер клеточного состава и степень его выраженности в острую фазу воспаления, наличие некротически изменённых тканей, количественные характеристики макрофагов и фибробластов, появление грануляционной ткани, степень её васкуляризации. Для статистической обработки полученных данных была использована программа Microsoft Excel.
Результаты и обсуждение
Процесс заживления раневого дефекта состоит из последовательных стадий: фазы воспалительных изменений, пролиферативной фазы, фазы эпителизации. При острых ранах в каждой из фаз все морфологические процессы протекают параллельно друг другу – для хронического течения процесса, при длительно существующем раневом дефекте, характерном для СДС, хронология этапов заживления нарушается. Хронические раны диабетической этиологии имею тенденцию к длительному «застреванию» в фазе воспалительных изменений, значительно замедляя процесс регенерации. Фаза воспаления начинается в течение 6-8 часов после воздействия травмирующего агента, достигает максимальной реакции на 2-4 суток, постепенно проходит в течение нескольких недель. Данная фаза реализуется за счёт вазоконстрикции, ретракции повреждённых кровеносных сосудов, отложения фибрина и свёртывания крови. Характерно увеличение притока крови к травмиро-

Луценко Ю.Г., Сычёва Д.Р.
ПАТОМОРФОЛОГИЧЕСКИЕ АСПЕКТЫ РЕГЕНЕРАТОРНОГО ПРОЦЕССА РАН, ОБУСЛОВЛЕННЫЕ ПРИМЕНЕНИЕМ КОЛЛАГЕНОВЫХ РАНЕВЫХ ПОКРЫТИЙ, У БОЛЬНЫХ СИНДРОМОМ ДИАБЕТИЧЕСКОЙ СТОПЫ ванному участку, что проявляется отёком, покраснением и припухлостью. Основная задача фазы воспалительных изменений – остановить кровотечение и элиминировать некротизированные участки (альтеративный компонент воспаления) ткани посредством фагоцитоза. В фазу альтерации, морфологическим субстратом которой являются ткани в состоянии дистрофии и/или некроза, происходит активация и выброс биологические активных веществ – медиаторов воспаления клеточного генеза (базофилов, тромбоцитов, лимфоцитов, моноцитов) и медиаторов плазменного генеза (калликреин-кининовая система, система комлемента, свертывающая и противосвертывающая системы) [8]. Данные медиаторы повышают проницаемость стенок сосудов микроциркуляторного русла, активируют хемотаксис лейкоцитов, внутрисосудистое свёртывание, вторичную альтерацию – происходит формирование экссудативной фазы воспаления. В данную фазу в очаге воспаления возникает венозная и артериальная гиперемия, прогрессирует процесс повышения проницаемости сосудистой стенки-в очаг повреждения начинает проникать жидкость, крупнодисперсные белки плазмы крови, гематогенные клетки. Основные типы клеток, находящиеся в участке воспаления в данную фазу – нейтрофилы (осуществляют фагоцитоз чужеродных агентов), макрофаги (принимают активное участие в процессе элиминации некротичесого детрита, очищают раневое ложе и подготавливают его к пролиферативной фазе, синтезируют факторы роста и монокины, активирующие фибробласты), лимфоциты (синтезируют лимфокины). У пациентов с СД повышенный уровень глюкозы замедляет процесс миграции лейкоцитов в очаг воспаления, снижает экспрессию макрофагов [9]. Макрофаги необходимы для осуществления фагоцитоза, поглощения некротизированных клеток, выделяют провоспалительные цитокины, стимулируют образование сосудов, активируют процесс миграции фибробластов в раневой дефект. В случае недостаточной экспресии макрофагов (что характерно для пациентов с СД) процесс регенерации значительно замедляется, нарушается последовательность стадий репаративного процесса, впоследствии могут формироваться грубые фиброзные рубцы. Для пролиферативной фазы характерно восстановление кровотока и заполнение раневого ложа новообразованной тканью – грануляционной, которая, проходя этапы созревания, в дальнейшем превратится в рубцовую ткань. Продолжительность данной фазы при неосложнённых условиях занимает от 10 до 28–30 суток. Для формирования грануляционной ткани и этапов дальнейшего её созревания необходимо наличие в раневом дефекте достаточного количества фибробластов и новообразованных тонкостенных сосудов. Фибробласты обладают высокой метаболической активностью, синтезируют коллаген, эластин, коллаген-ассоциированные белки и протеогликаны [9]. В зоне повреждения фибробласты, активированные факторами роста и монокинами, синтезируемыми макрофагами, появляются за 1–2 суток до формирования кровеносных капилляров в грануляционной ткани и за 3–5 суток до образования коллагеновых волокон.
Высокий уровень глюкозы в крови оказывает негативное влияние на способность фибробластов к миграции и пролиферации в области раневого ложа. Фаза эпителизации завершает процесс регенерации и является самой продолжительной – может занимать несколько месяцев, начинается с момента образования в раневом дефекте достаточного количества коллагена. Процесс рубцевания осуществляется путём прогрессивного уменьшения количества капилляров в грануляционной ткани, макрофагов, фибробластов, тучных клеток, и увеличения числа коллагеновых волокон. В результате грануляционная ткань уплотняется и огрубевает – формируется рубец, заполняющий рану. Параллельно процессу рубцевания идёт процесс эпителизаци – с одной стороны от грануляционной ткани исходят хемотаксические сигналы, регулирующие и направляющие миграцию краевого эпителия, с другой стороны, для миграции эпителиальным клеткам необходима гладкая, ровная, однородная поверхность (для перемещения клеточного состава из краёв в центр раны). У пациентов с СД часто наблюдается неполное заполнение раневого дефекта грануляционной тканью, что приводит к отсутствию условий для формирования ровной поверхности, замедляется процесс миграции клеточного состава – это приводит к отсутствию необходимых для дальнейшей эпителизации условий, значительной пролонгации длительности регенераторного процесса.
Процесс репарации раневых дефектов у пациентов с СД значительно замедлен. Для стимуляции процессов регенерации ран пациентов с СД целесообразно применять коллагеновые раневые покрытия (КРП). Влияние коллагена, содержащегося в данных покрытиях, выглядит следующим образом- после связывания коллагена с раной в его коллагеновую решётку из здоровой ткани мигрируют фибробласты. Клетки, заполнившие коллагеновую матрицу, начинают синтезировать собственный коллаген и другие компоненты межклеточного вещества [10]. Формируется переходный матрикс, стимулирующий иммунный ответ и активирующий гранулоциты, макрофаги и фибробласты. Коллаген способствует более быстрой активации факторов роста, высвобождающихся из клеток, также усиливает процесс пролиферации эпителиальных клеток [10]. Основываясь на гистологической картине, представленной в данной работе, можно определить особенности влияния КРП на течение раневого процесса у пациентов СДС, сравнить с морфологической картиной репаративных изменений у пациентов контрольной группы – биопсийным материалом больных, которые были пролечены при помощи ежедневных перевязок с антисептиками и мазями.
Морфологическое исследование показало, что у больных контрольной группы, местное лечение раневых дефектов которых состояло из ежедневных перевязок с антисептиками и мазями первые 3-ое суток в дне ран в 48 случаях определялась отёчность жировой ткани, с выраженной в 28 случаях и умеренной в 20 случаях лейкоцитарной инфильтрацией, с наличием единичных гистиоцитов, макрофагов, фрагментов раневого детрита в 42 случаях, масс фибрина в 30 случаях. В прилежащих

Луценко Ю.Г., Сычёва Д.Р.
ПАТОМОРФОЛОГИЧЕСКИЕ АСПЕКТЫ РЕГЕНЕРАТОРНОГО ПРОЦЕССА РАН, ОБУСЛОВЛЕННЫЕ ПРИМЕНЕНИЕМ КОЛЛАГЕНОВЫХ РАНЕВЫХ ПОКРЫТИЙ, У БОЛЬНЫХ СИНДРОМОМ ДИАБЕТИЧЕСКОЙ СТОПЫ
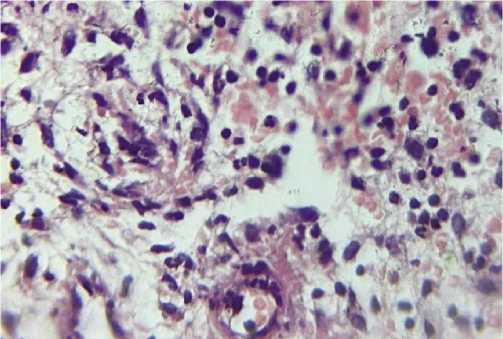
Рис. 1. Инфильтративно-продуктивный васкулит с инфильтрацией сосудистой стенки нейтрофилами, стаз эритроцитов в просвете сосуда. Сосочковый слой дермы пациента контрольной группы, 4-ые сутки. Окраска гематоксилином и эозином, х 400.
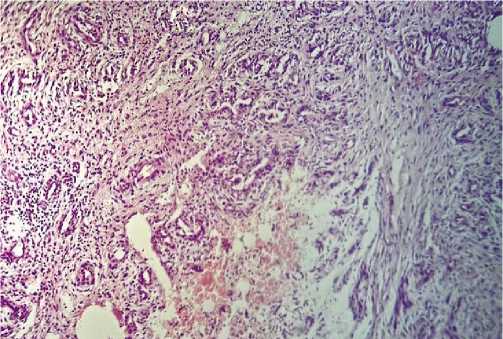
Рис. 2. Выраженная диффузная нейтрофильная инфильтрация сосочкового слоя дермы у пациента контрольной группы, конец 5-ых суток. Окраска гематоксилином и эозином, х 400.
к ране тканях пациентов контрольной группы определялись расстройства микроциркуляции к началу 2-х суток: набухание эндотелиальных клеток в 33 случаях, участки неоднородности и разрыхления базальных мембран в 29 случаях, стазы эритроцитов в сосудистом русле в 51 случае на 4–5 сутки, венозная гиперемия в 49 случаях к концу 3-х суток, плазматическое пропитывание сосудистой стенки с явлением десквамации эндотелиоцитов в 45 случаях на 5-е сутки. В сосочковом слое дермы 30 пациентов контрольной группы определялся инфильтративно-продуктивный васкулит (Рис. 1) к концу 4-х суток.
Лейкоцитарная инфильтрация, с наличием большого количества лейкоцитарно-некротического детрита, определялась в краях ран пациентов контрольной группы к концу 5-х суток – в 25 случаях выраженная, диффузная нейтрофильная инфильтрация сосочкового слоя дермы (Рис. 2), в 31 случае – слабовыраженная клеточная инфильтрация сетчатого слоя дермы.
В тканях ран материала контрольной группы в 50 случаях – лейкоцитарно-некротический детрит (ЛНД), с выраженной лейкоцитарной инфильтрацией, занимал всё поле зрения к 7–8-м суткам, в 14 случаях – ЛНД визуализировался к концу 6-х суток на 1/3 площади поверхности, с очаговой слабовыраженной лейкоцитарной инфильтрацией, стазами эритроцитов в просвете сосудов сосочкового слоя дермы и участками десквамации эндотелиальных клеток.
Очаговое разрастание грануляционной ткани, занимающей 1/3 поля зрения, с новообразованными, тонкостенными, вертикальными сосудами определялся у 30 пациентов контрольной группы к 8–9-м суткам после ежедневного применения перевязок с антисептиками и мазями. У пациентов контрольной группы в 33 случаях визуализировались единичные макрофаги в области краёв раны на 7-е сутки, в 19 случаях – умеренная макрофагальная инфильтрация, без тенденции к увеличению количества клеток от краёв к центру раневого дефекта к концу 7-х суток, в 2 случаях- выраженная инфильтрация макрофагами на 8-е сутки. В 22 случаях к концу 12-х суток в области дна раневого дефекта пациентов контрольной группы определялись адвентициальные клетки, малодифференцированные и юные фибробластоподобные клетки, с преимущественной локализацией по ходу капилляров, занимающие 1/3 поля зрения. В 18 случаях в ткани ран пациентов СДС контрольной группы визуализировались немногочисленные фибробласты, которые находились на значительном расстоянии друг от друга, с преимущественной локализацией в краях раневого дефекта – занимали 1/2 поля зрения к 14–15-м суткам, в 8 случаях отсутствовали как адвентициальные клетки, так и фибробласты на 14-е сутки. У 32 пациентов контрольной группы к 14–15-м суткам наблюдалась краевая эпителизация и постепенное фиброзирование грануляционной ткани. У 25 пациентов краевая эпителизация была минимально выражена к 14-м суткам, при этом отмечалась умеренная нейтрофильная инфильтрация стенок сосудов как сосочкового, так и сетчатого слоёв дермы с формированием гистологической картины продуктивноинфильтративного васкулита, со стазом эритроцитов в просветах части сосудов. В тканях ран 30 пациентов сохранялась умеренная эозинофильная инфильтрация, с наличием единичных лимфоцитов, нейтрофилов и макрофагов. В 29 случаях в части фибробластов, расположенных в краях ран, отмечались дистрофические изменения. Таким образом, у большей части пациентов контрольной группы, пролеченных при помощи ежедневных перевязок с антисептиками и мазями, даже на 12–15-ые сутки преобладали альтеративный и экссудативный компоненты воспаления, сам воспалительный процесс имел подострое течение, регенераторный процесс при этом был минимально выражен.
При гистологическом исследовании тканей ран пациентов основной группы, которым в комплексном лечении ран использовали коллагеновые раневые покрытия (КРП) «Зелёная Дубрава» на 2-е cутки в окружающих рану тканях только в 11 случаях определялся отёк, в 13 случаях лим-
Луценко Ю.Г., Сычёва Д.Р.
ПАТОМОРФОЛОГИЧЕСКИЕ АСПЕКТЫ РЕГЕНЕРАТОРНОГО ПРОЦЕССА РАН, ОБУСЛОВЛЕННЫЕ ПРИМЕНЕНИЕМ КОЛЛАГЕНОВЫХ РАНЕВЫХ ПОКРЫТИЙ, У БОЛЬНЫХ СИНДРОМОМ ДИАБЕТИЧЕСКОЙ СТОПЫ фостаз, в 12 венозное полнокровие, в 19 случаях эозинофильная инфильтрация. Явления гидратации в тканях 42 случаев были слабо выражены, в 13 случаях определялся стаз эритроцитов в просветах сосудов сетчатого слоя дермы, в 9 случаях инфильтративно-продуктивный васкулит в сосудах микроциркуляторного русла. В тканях раневых дефектов пациентов основной группы в 42-х случаях лейкоцитарно-некротический детрит (ЛНД) отсутствовал к началу 5-х суток, в 14 случаях – визуализировался в области краёв раны к началу 6-х суток, в 8 случаях занимал всё поле зрения к концу 5-х суток. В раневых дефектах тканей ран пациентов основной группы в 46 случаях определялась умеренная лейкоцитарная инфильтрация сетчатого слоя дермы к началу 4-х суток (Рис. 3), в 20 случаях визуализировался слабовыраженный нейтрофильный инфильтрат в сосочковом слое дермы к концу 5-х суток.
В сетчатом и сосочковом слоях дермы пациентов основной группы в 42 случаях определялась выраженная макрофагальная инфильтрация к началу 6-х суток, с тенденцией к увеличению их количества в направлении от краёв раны к центру, в 19 случаях- умеренная макрофагальная инфильтрация к концу 6-х суток.
У 45 пациентов основной группы к 8–9-м суткам после применения КРП формировались очаговые островки разрастания грануляционной ткани с вертикально расположенными сосудами, и активно пролиферирующими фибробластами. В поле зрения раневой области у 30 пациентов основной группы определялась грануляционная ткань, полностью восполняющая раневой дефект от сетчатого слоя дермы до рогового слоя эпидермиса к концу 8-х суток, у 15 пациентов -в сетчатом слое дермы к концу 9-х суток. В 37 случаях в тканях ран пациентов СДС основной группы визуализировались зрелые фибробласты, которые занимали 1/2 поля зрения к концу 10-х суток, в 12 случаях- всё поле зрения к началу 11-х суток. В 11 случаях к концу 10-х суток в области дна раневого дефекта пациентов контрольной группы определялись диффузно расположенные малодифференцированные фибробласты, располагающиеся по ходу капилляров. К концу 11-х суток в тканях ран 36 пациентов наряду с процессами созревания грануляционной ткани отмечалось появление горизонтального слоя зрелых фибробластов, занимающих 1/3 поля зрения в области дна раны (Рис. 4).
У 49 пациентов основной группы к 12–13-м суткам наблюдалась выраженная эпителизация как в области краёв, так и в области дна раны, с постепенным фиброзированием грануляционной ткани. У 10 пациентов краевая эпителизация была минимально выражена к концу 13-х суток, при этом нейтрофильная инфильтрация стенок сосудов как сосочкового, так и сетчатого слоёв дермы отсутствовала. В 22-х случаях отмечалось периваскулярное скопление тучных клеток на 13-е сутки, что свидетельствует о нормализации системы микроциркуляции в ткани раневых дефектов.
Таким образом, результаты проведенных гистологических исследований показали, что применение
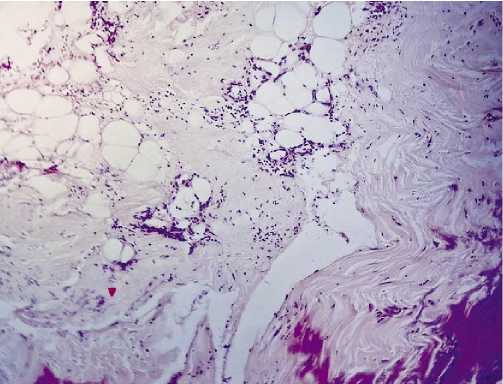
Рис. 3. Умеренная нейтрофильная инфильтрация сетчатого слоя дермы и части адипоцитов подкожно-жировой клетчатки у пациента основной группы, начало 4-х суток. Окраска гематоксилином и эозином, х 400.
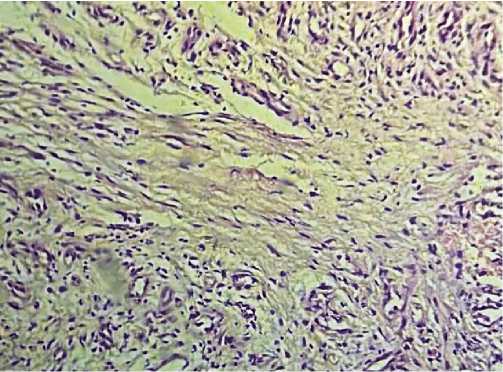
Рис. 4. Горизонтальный слой зрелых фибробластов, окружённых тонкими оксифильными коллагеновыми волокнами. Рана на 11-е сутки после применения коллагеновых раневых покрытий. Окраска гематоксилином и эозином, х 400.
коллагеновых раневых покрытий благотворно влияет на течение каждой фазы репаративного процесса в раневых дефектах пациентов СДС. Данная методика способствует своевременному и более быстрому переходу раны из фазы воспалительных изменений в пролиферативную, а затем в фазу эпителизации, предотвращая «застревание» раневого дефекта в альтеративно-экссудативной стадии воспалительной реакции по сравнению с группой пациентов, пролеченных при помощи ежедневных перевязок с антисептиками и мазями. Коллаген, содержащийся в КРП, способен всасывать раневой экссудат, в состав которого входят нейтрофилы, фибрин, фрагменты некротизированных тканей, способствуя, таким образом, очищению раны, ослаблению воспалительной реакции, уменьшению отёка, венозного полнокровия в окружающих тканях, нормализует работу сосудов микроциркуля-
Луценко Ю.Г., Сычёва Д.Р.
ПАТОМОРФОЛОГИЧЕСКИЕ АСПЕКТЫ РЕГЕНЕРАТОРНОГО ПРОЦЕССА РАН, ОБУСЛОВЛЕННЫЕ ПРИМЕНЕНИЕМ КОЛЛАГЕНОВЫХ РАНЕВЫХ ПОКРЫТИЙ, У БОЛЬНЫХ СИНДРОМОМ ДИАБЕТИЧЕСКОЙ СТОПЫ торного русла (предотвращает развитие пролиферативно-экссудативных форм васкулита, стаза). Нормализация кровоснабжения в области раневого дефекта, в свою очередь, уменьшает гипоксию и способствует активации репаративных процессов в ране. Коллаген благотворно влияет на количественные характеристики клеток острой фазы воспаления: активирует миграцию лейкоцитов, значительно увеличивает число макрофагов в области раневых дефектов. За счёт увеличенного КРП количества макрофагов, в свою очередь, вырабатывается большее количество провоспалительных цитокинов, стимулирующих ангиогенез и процесс миграции фибробластов в область раневого дефекта – на более ранних сроках, по сравнению с контрольной группой, формируется грануляционная ткань. За счёт большого количества зрелых фибробластов и новообразованных сосудов грануляционная ткань созревает и превращается в рубцовую за более короткий срок у пациентов, пролеченных КРП. Полученные результаты позволяют заключить, что применение коллагеновых раневых покрытий в комплексном лечении больных с гнойно-некротическими формами синдрома диабетической стопы способствует скорейшему переходу раневых дефектов из альтеративно-экссудативной фазы воспаления в пролиферативную, усилению макрофагальной реакции, устранению гипоксии и восстановлению работы сосудов микроциркуляторного русла, активации и дальнейшей пролиферации фибробластов, приводит к ускоренному созреванию грануляционной ткани и своевременной эпителизации с дальнейшим формированием рубца. Применение КРП за счёт выраженной стимуляции процесса регенераци позволяет сократить сроки подготовки раны к пластическому закрытию с 20–22-х до 12–16 суток, являясь одним из перспективных звеньев в комплексном лечении хронических ран пациентов СДС.
Выводы
-
1. Применение коллагеновых раневых покрытий благотворно влияет на каждую фазу репаративного процесса хронических ран пациентов СДС – способствует своевременному и более быстрому переходу из альтеративно-экссудативной стадии воспалительной реакции в пролиферативную и в фазу эпителизации по по сравнению с группой пациентов, пролеченных с использованием ежедневных повязок с антисептиками и мазями.
-
2. Коллаген, входящий в состав коллагеновых раневых покрытий, всасывает раневой экссудат, выполняя дренажную функцию, способствует процессам очищения раны за более короткий срок, снижает степень выраженности воспалительной реакции, уменьшает отёк окружающих тканей, восстанавливает работу сосудов микроцирку-лятоного русла, нормализует кровоснабжение в области раневого дефекта, уменьшает гипоксию, что приводит к активации репаративных процессов в ране.
-
3. Применение коллагеновых раневых покрытий в комплексном лечении гнойно-некротических ран нижних конечностей у больных сахарным диабетом благотворно
влияет на количественные характеристики клеток острой фазы воспаления: активирует процесс миграции лейкоцитов, значительно увеличивает число макрофагов, способствуя повышению экспрессии провоспалительных цитокинов, необходимых для ангиогенеза и стимуляции миграции фибробластов в рану; за счёт данных процессов грануляционная ткань созревает и превращается в рубцовую за более короткий временной промежуток, позволяя сократить сроки подготовки раны к пластическому закрытию с 20–22-х до 12–16 суток.
Список литературы Патоморфологические аспекты регенераторного процесса ран, обусловленные применением коллагеновых раневых покрытий, у больных синдромом диабетической стопы
- Российская ассоциация эндокринологов, Московская ассоциация хирургов. Синдром диабетической стопы: клинические рекомендации. - М., 2015. - 46 с.
- Галстян Г.Р., Токмакова А.Ю., Егорова Д.Н., Митиш В.А. и др. Клинические рекомендации по диагностике и лечению синдрома диабетической стопы. Раны и раневые инфекции // Журнал им. проф. Б.М. Костючёнка. - 2015. - №2. - С.61-83.
- Давиденко О.П. Синдром диабетической стопы. Его роль и место в современной диабетологии (обзор литературы) // Медицина и образование в Сибири: электронный журнал. - 2014. - №5. - C.16-23.
- Берченко Г.Н., Шехтер А.Б., Николаев А.В. и др. Особенности заживления гнойных ран у больных при лечении коллагеновыми препаратами (гистохимическое и электронно-микроскопическое исследование) // Архив патологии. - 1985. - №12. - С.37-44.
- Лисицын Ю.П. История медицины. М.: ГЭОТАР-Медиа, 2016. 400 с.
- Ваисов А.Ш., Дронов А.Ф., Истранов Л.П., Руденко Т.Г. Применение коллагеновых препаратов при лечении кожных ран // Медицинский журнал Узбекистана.
- Хилькин А.М., Шехтер А.Б., Леменев В.Л., Дронов А.Ф. Лечение скальпированных ран и ожогов кожи коллагеновыми пленками в эксперименте // Экспериментальная хирургия. - 1972. - №6. - С.37-41.
- Абдуллаев Р.Н. Комплексное лечение гнойно-некротических поражений нижней конечности у больных с синдромом диабетической стопы // Новый день в медицине. - 2021. - №2(34). - С.413-418. EDN: ITMTZE
- Белик Б.М. и др. Комплексное лечение больных с гнойно-некротическими осложнениями при нейропатической форме синдрома диабетической стопы // Хирургия. Журнал им. Н.И. Пирогова. - 2020. - №4. - С.81-87. EDN: VONCXW
- Мустаева А.С. Актуальные проблемы диагностики и лечения диабетической // Modern Science. - 2021. - №10. - С.230-233.


