Патоморфологические изменения правой ножки пучка Гиса проводящей системы сердца человека при инфекционных заболеваниях
Автор: Мозгалва Наталья Владимировна, Пархоменко Юрий Георгиевич, Чукбар Александр Владимирович, Колесников Лев Львович, Тишкевич Олег Александрович
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 2 т.23, 2015 года.
Бесплатный доступ
Проведено исследование патоморфологических изменений правой ножки пучка Гиса проводящей системы сердца у 100 лиц, умерших от различных инфекционных заболеваний: дифтерии, инфекционного эндокардита у наркоманов в сочетании с ВИЧ-инфекцией и без ВИЧ-инфекции, менингококковой инфекции, стафилококковой пневмонии и рожистого воспаления. Показано, что поражение правой ножки менее выражено, чем в рабочем миокарде и более характерно для длительного течения заболевания с большей частотой воспалительных изменений в дистальной части правой ножки.
Проводящая система сердца, правая ножка пучка гиса, инфекционные заболевания, инфекционный эндокардит, дифтерия
Короткий адрес: https://sciup.org/143177050
IDR: 143177050
Pathomorphological changes of the right His’ bundle branch of the human conductive system of the heart in cases of inflectional diseases
Pathomorphological changes of the right His’ bundle branch of the conductive system of the heart in 100 cases of the death of different infectional diseases was studied. It is shown that the right His’ bundle branch damage is rarer than in working myocardium and is more typical to a long course of the disease with higher frequency of inflammatory changes in the distal part of the right branch.
Текст научной статьи Патоморфологические изменения правой ножки пучка Гиса проводящей системы сердца человека при инфекционных заболеваниях
Введение. При некоторых инфекционных заболеваниях, таких как дифтерия, инфекционный эндокардит, сердце является «органом-мишенью», и его прямое поражение становится непосредственной причиной смерти больного [1,
3-4, 9, 11]. В то же время, сердечно-сосудистая недостаточность в составе синдрома полиорганной недостаточности может быть одним из ведущих компонентов танатогенеза практически при любом инфекционном заболевании. Наряду с общими закономерностями поражения сердца при различной инфекционной патологии представляет интерес анализ степени и частоты вовлечения в патологический процесс проводящей системы сердца, в частности, правой ножки пучка Гиса (ПН).
Цель исследования – изучить патоморфо-логические особенности ПН при инфекционных заболеваниях.
Материал и методы исследования. Объектом исследования послужили сердца пациентов, умерших от инфекционных заболеваний, всего 100 случаев. Исследованы сердца пациентов, умерших от дифтерии (60 случаев), инфекционного эндокардита (ИЭ) у наркоманов в сочетании с ВИЧ-инфекцией (22 случая) и без ВИЧ-инфекции (5 случаев), менингококковой инфекции (5 случаев), стафилококковой пневмонии (5 случаев) и рожистого воспаления (3 случая). Исследование ПН проводилось по модифицированной методике, предложенной Ю.Г. Пархоменко и соавт. [7]. Полученные на аутопсии кусочки сердца заливали в парафин с последующим изготовлением серийных срезов, которые окрашивали гематоксилином и эозином, по Ван Гизону, ШИФФ-реактивом. Для стандартизации оценки изменений в ПН выделены 2 части: проксимальная, начинающаяся от предсердно-желудочкового узла и проходящая в межжелудочковой перегородке, и дистальная, проходящая в перегородочно-краевой трабекуле к передней сосочковой мышце. Условной границей между проксимальной и дистальной частями ПН считали основание перегородочно-краевой трабекулы. При микроскопическом исследовании оценивали состояние не только ПН, но и окружающих ее структур сердца.
Результаты исследования и их обсуждение. Для случаев смерти от дифтерии, вызванной различными коринебактериями, было характер-
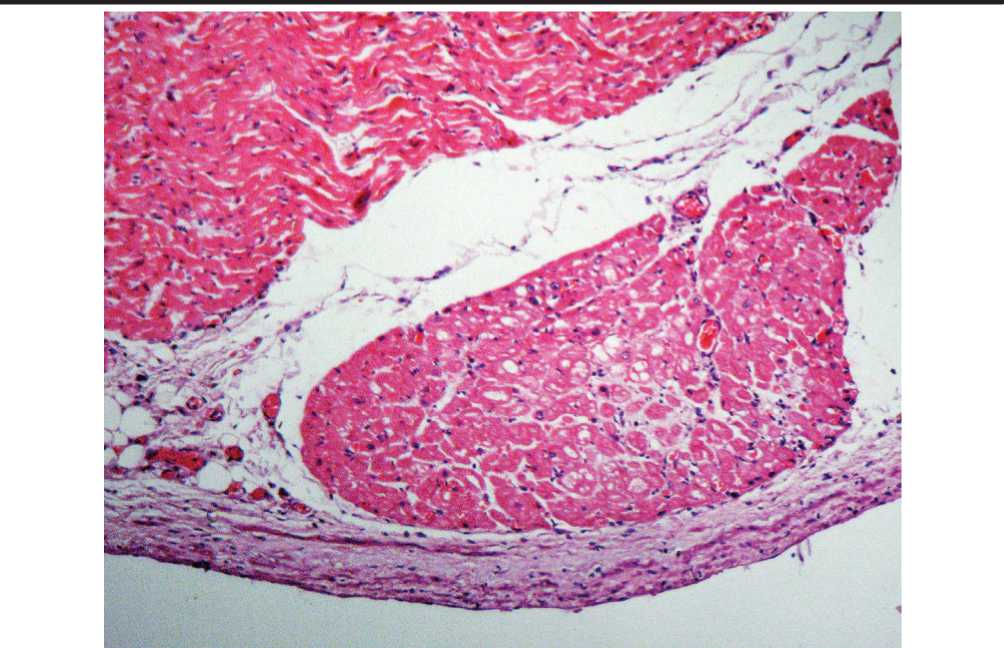
Рис. 1. Правая ножка пучка Гиса при инфекционном эндокардите у ВИЧ-инфицированного наркомана (дистальная часть). Правая ножка в виде округлого скопления вакуолизированных кардиомиоцитов располагается под утолщенным эндокардом, отделена от рабочего миокарда рыхлой соединительной тканью. Окраска гематоксилином и эозином, Х10.
ным выявление поражение миокарда во всех исследованных случаях (60 сердец), [4, 11]. При этом было выделено 3 группы по преобладающим патологическим признакам: с преимущественно циркуляторно-дистрофическими, воспалительными и склеротическими изменениями (25, 29 и 6 случаев соответственно), [4]. В первой группе, соответствующей острой фазе болезни (умершие на 2-10 день от начала заболевания), дистрофия проводящих миоцитов ПН была выявлена в 5 случаях (12%) и характеризовалась их вакуолизацией и нечеткостью контуров в сочетании с кровоизлияниями. Встречались мелкоочаговые лимфогисти-оцитарные инфильтраты. В рабочем миокарде в наблюдениях этой группы преобладали явления вакуолизации или миолиза кардиомиоцитов при отсутствии или незначительной выраженности воспалительной клеточной реакции, при этом в 13 случаях (45%) наблюдались массивные субэндокардиальные кровоизлияния в желудочках. Во второй группе (умершие с 6-го по 28 день от начала заболевания) в 6 случаях (7%) обнаружена лишь вакуольная дистрофия клеток ПН, в 7 случаях (24%) встречались некрозы, воспалительная инфильтрация и дистрофические изменения проводящих кардиомиоцитов. В окружающем миокарде при этом развивалась преимущественно воспалительная реакция, выраженная дистрофия, вплоть до миолиза кардиомиоцитов и диффузная и очаговая межуточная лимфогистиоцитарная инфильтрация с примесью полиморфноядерных лейкоцитов различной степени выраженности. В третьей группе (длительность течения заболевания более 30 дней) в рабочем миокарде преобладали склеротические изменения, при этом патологических процессов в ПН зафиксировано не было.
При ИЭ (27 случаев) смерть наступила на 3-64 сутки от возникновения клинических проявлений: в 24 случаях при развитии септикопиемии, в 3 случаях – от сочетания ИЭ и вторичных ВИЧ-ас-социированных инфекций, в том числе в 1 случае с развитием дилятационной кардиомиопатии после перенесенного ИЭ. В качестве возбудителя ИЭ в 89% (24 случая) выявлен Staphylococcus aureus, изолированно (10 случаев, 37%) или в сочетании с другими микробами (14 случаев, 52%). В поли-микробных ассоциациях помимо стафилококка
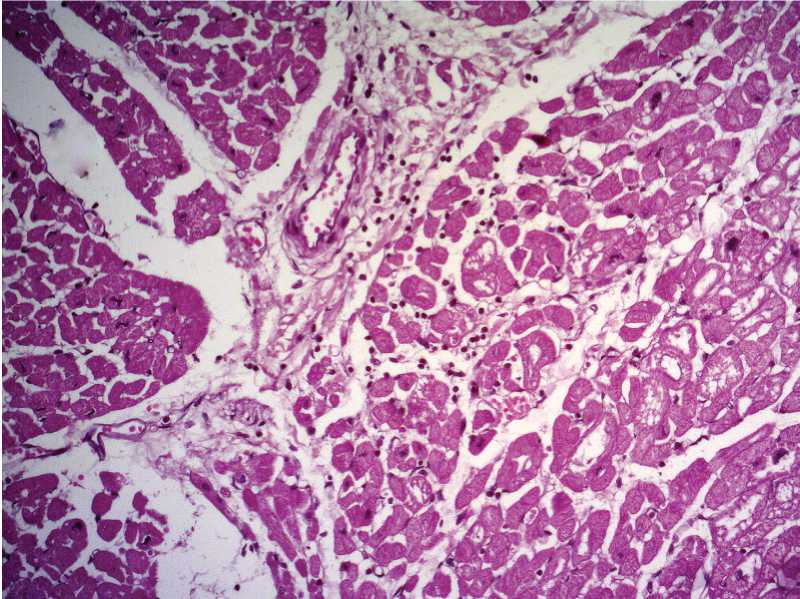
Рис. 2. Правая ножка пучка Гиса при инфекционном эндокардите у ВИЧ-инфицированного наркомана (дистальная часть). Очаговая лимфоидная инфильтрация окружающей клетчатки на границе с рабочим миокардом с распространением на проводящие кардиомиоциты. Окраска гематоксилином и эозином, Х20.
преобладали Klebsiella pneumoniae и грибы рода Candida (до 30%). Патологические изменения сократительного миокарда и других структур сердца были зарегистрированы во всех наблюдениях и проявлялись дистрофией и некрозом кардиомиоцитов, пристеночным эндокардитом, межуточной и паренхиматозной инфильтрацией миокарда вплоть до формирования абсцессов, эндокардиофиброзом и очаговым фиброзом миокарда, липоматозом.
ПН определялась в виде округлых или треугольной формы скоплений поперечно срезанных проводящих кардиомиоцитов, чаще окруженных рыхлой волокнистой соединительной тканью, причем в дистальной части располагалась субэн-докардиально в виде одного или двух (редко 3-х) стволов, а в проксимальной – преимущественно интрамиокардиально в виде одиночного ствола, реже (4 случая) в виде 2-х стволов (Рис. 1). Па-томорфологические изменения ПН проявлялись преимущественно нечеткостью контуров и некрозами проводящих кардиомиоцитов, отеком, воспалительной инфильтрацией внутри ПН и в окружающей ее клетчатке, очаговым фиброзом, некрозами кардиомиоцитов. Воспалительные изменения ПН встречались в 15 случаях (56%), причем в дистальной части в 2 раза чаще, чем в проксимальной (10 и 5 случаев соответственно, p<0,01), проявляясь очаговой воспалительной инфильтрацией преимущественно лимфогисти-оцитарного характера в окружающей ПН клетчатке, распространяющейся на межклеточное пространство ПН (рис. 2). При сопоставлении локализации эндокардита (правая или левая половина сердца) и развившихся воспалительных изменений отмечено, что для рабочего миокарда (РМ) и кардиомиоцитов ПН характерна сходная тенденция: максимальные воспалительные изменения зарегистрированы при двухстороннем ИЭ, минимальные - при правостороннем ИЭ, случаи ИЭ левой половины сердца занимают промежуточное положение. При этом общая частота обнаружения воспалительной инфильтрации в ПН была в среднем на 15 % меньше, чем в рабочем миокарде. Некрозы проводящих кардиомиоцитов наблюдались только при левостороннем и двухстороннем поражении сердца (8 случаев). Зарегистрированные явления фиброзирования ПН и РМ в большинстве случаев приходились на ИЭ левой половины сердца (7 из 9 для ПН, 8 из 12 для РМ). Фиброз РМ при двухстороннем ИЭ был отмечен лишь в 1 случае, а в ПН не наблюдался.
Достоверных различий в характере поражения ПН в случае наличия или отсутствия ВИЧ-инфекции обнаружено не было.
При стафилококковой пневмонии (5 случаев) и рожистом воспалении (3 случая) смерть наступала на 5-7 сутки. Характерным было выявление в рабочем миокарде субэндокардиальных кровоизлияний различной выраженности, дистрофии и некрозов кардиомиоцитов. При этом не наблюдалось вовлечения в патологический процесс элементов ПН, [6].
При генерализованной менингококковой инфекции , вызванной менингококками группы А и B, (5 случаев, смерть на 2-3 сутки) наблюдался выраженный геморрагический синдром, характеризующийся развитием в большинстве случаев (4) массивных, распространенных субэндокардиальных кровоизлияний. В ПН в 2 случаях определялись расстройства микроциркуляции в виде стаза эритроцитов, сладж-феномена, также выявлялась нечеткость контуров кардиомиоцитов и их миолиз. Аналогичные изменения наблюдались в рабочем миокарде.
По полученным нами данным, совпадающим с данными литературы, ПН на своем протяжении в основном представлена компактным одиночным пучком узких веретенообразных клеток, располагающимся интрамиокардиально. Однако ее дистальная часть сформирована другим типом клеток – крупными, вакуолизированными, Пуркинье-подобными клетками, которые в виде одного или нескольких пучков занимают, как правило, субэндокардиальное положение. Причем на всем протяжении ПН отграничена от окружающих структур лишь прослойкой рыхлой волокнистой соединительной ткани [5, 8]. Указанные структурно-топографические особенности ПН с одной стороны объясняют меньшую по сравнению с рабочим миокардом вовлеченность ПН в патологический процесс, с другой стороны – относительно более частое поражение дистальной части ПН по сравнению с проксимальной. Это соотносится с имеющимися в литературе данными об общих топографических закономерностях поражения сердца при миокардитах различной этиологии, согласно которым наиболее уязвимыми являются папиллярные мышцы и мясистые трабекулы, а также субэндокардиальные отделы сердца [10]. Это, в частности, связывают с выделением поврежденным эндотелием субстанций, оказывающих угнетающее действие на сократительную функцию подлежащих миоцитов [3-4, 6, 12].
Отмеченная взаимосвязь между выраженностью патологических изменений в ПН и локализацией ИЭ (наибольшее поражение при лево- и двухстороннем ИЭ) связана, по-видимому, с развивающимся метастазированием инфекцион- ного агента по большому кругу кровообращения и вторичным поражением сердца. При этом фиброзирование, как косвенный признак репарации, не характерно для двухстороннего эндокардита, который за счет более тяжелого течения, вероятно, приводит к летальному исходу ранее, чем успевают начаться репаративные процессы.
Выводы:
Патоморфологические изменения ПН при исследованных инфекционных заболеваниях были относительно менее выражены и встречались реже, чем в сократительном миокарде.
Максимально выраженное поражение ПН определялось в ее дистальной части, что объясняется структурно-топографическими особенностями ПН, и выражалось преимущественно дистрофическими изменениями в ранних фазах инфекционных заболеваний и воспалительными изменениями с развитием фиброза при их длительном течении.
В случае инфекционного эндокардита наибольшая выраженность патологических изменений ПН была характерна для левостороннего эндокардита и ИЭ с вовлечением обеих половин сердца.
Список литературы Патоморфологические изменения правой ножки пучка Гиса проводящей системы сердца человека при инфекционных заболеваниях
- Кадырова С.Н. Морфологические особенности дифтерии у взрослых в современных условиях/ С.Н. Кадырова, В.А. Цинзерлинг, Д.В. Комарова //Архив патологии. - 1996 г. - №6. - с. 28-32.
- Мозгалёва Н.В. Морфологические изменения правой ножки пучка Гиса при инфекционном эндокардите у ВИЧ-инфицированных наркоманов/ Н.В. Мозгалёва, Ю. Г. Пархоменко, А.В. Чукбар// Международная научная конференция «Актуальные вопросы морфогенеза в норме и патологии», г.Москва, 16-17.04.2014 г., Сборник тезисов, с.193-195
- Моисеева О.М. Спорные вопросы диагностики миокардитов/О.М. Моисеева, Л.Б. Митрофанова,А.В. Пахомов, Н.А. Митрофанов [и др.]//Сердце: журнал для практикующих врачей. - 2010. - Т. 9. -№4. - с.234-241.
- Пархоменко Ю.Г. Структурные закономерности морфологических изменений проводящей системы сердца и окружающего миокарда при заболевании дифтерией/ Ю. Г. Пархоменко, А. В. Чукбар, О. А. Тишкевич // Российские морфологические ведомости. - 2000. - № 3-4. - с. 121-125.
- Пархоменко Ю.Г. Закономерности строения и топографии образований проводящей системы сердца человека с позиций биомеханики/ Ю.Г. Пархоменко, Ю.М. Аникин, А.В. Чукбар [и др.]// Российские морфологические ведомости. - 2000. - № 1-2. - с. 69-74.
- Пархоменко Ю.Г. Структурные закономерности морфологических изменений проводящей системы и окружающего миокарда при менингококцемии, стафилококковой пневмонии и роже/ Ю. Г. Пархоменко, A. В. Чукбар, О. A. Тишкевич // Российские морфологические ведомости. - 2001. - № 3-4. - с. 56.
- Пархоменко Ю.Г. К методике морфологического исследования проводящей системы сердца человека/ Ю.Г. Пархоменко, A.В. Чукбар, О.A. Тишкевич //Aрхив патологии. - 2003. - Т. 65. - № 4. - с. 55-57.
- Пархоменко Ю.Г. Особенности гистоархитектоники правой ножки предсердно-желудочкового пучка проводящей системы сердца/Ю. Г. Пархоменко, A. В. Чукбар, О. A. Тишкевич//Российские морфологические ведомости. - 1999. - № 3-4. - с. 133-136.
- Пархоменко Ю.Г., Зайратьянц О.В., Макарова О.В. Сепсис. Инфекционный эндокардит. Этиология, патогенез, классификация, патологическая анатомия/ Руководство для врачей. - М.: Группа МДВ. - 2013. - 104 с., табл.
- Пауков В.С., Казанская T.A., Фролов В.A. // Aрхив патологии. - 1972. - №1. - с. 25-31.
- Ющук Н.Д. Клинические и структурные параллели изменений проводящей системы сердца и миокарда у больных дифтерией / Н. Д. Ющук, Ю. Г. Пархоменко, A. В. Чукбар [и др.]// Терапевтический архив. - 2002. - № 11. - с. 33-37.
- S. Price, P. B. Anning, J.A. Mitchell, T. W. Evans// European Heart Journal. - 1999. - 20. - p. 715-724


