Патоморфологические изменения в головном мозге при экспериментальном моделировании хронической ишемии
Автор: Смирнов А.В., Шмидт М.В., Березин Е.В., Замараев В.С., Пютая Е.Д.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Обзорные статьи
Статья в выпуске: 2 (62), 2019 года.
Бесплатный доступ
При сравнительном качественном и количественном структурном анализе выявлены патоморфологические изменения в церебральной коре, гиппокампе, стриопаллидарной системе, мозжечке и стволе головного мозга при экспериментальном моделировании ишемической энцефалопатии путем частичной двусторонней перевязки обеих общих сонных артерий. Наиболее выраженные признаки повреждения, подтвержденные значимыми изменениями морфометрических параметров, обнаружены в грушевидных нейронах мозжечка (клетки Пуркинье), а также нейронов отдельных крупноклеточных ядер ствола головного мозга.
Головной мозг, ишемия, мозжечок, ствол головного мозга
Короткий адрес: https://sciup.org/142224322
IDR: 142224322 | УДК: 616.61-091
Pathomorphological changes in the brain in experimental modeling of chronic ischemia
Comparative qualitative and quantitative structural analysis revealed pathological changes in the cerebral cortex, hippocampus, striopallidar system, cerebellum and brain stem in experimental modeling of ischemic encephalopathy by partial bilateral carotid artery stenosis. The most pronounced signs of damage, confirmed by significant changes in morphometric parameters, were found in the Purkinje neurons of cerebellum, as well as the neurons of some magnocellular nuclei of brain stem.
Текст научной статьи Патоморфологические изменения в головном мозге при экспериментальном моделировании хронической ишемии
Цереброваскулярные болезни (ЦВБ) – группа заболеваний головного мозга, обусловленных патологическими изменениями церебральных сосудов с нарушением мозгового кровообращения. Из хронических форм ЦВБ можно выделить церебральный атеросклероз, который характерен преимущественно для лиц пожилого возраста, однако встречается и у молодых людей с выраженными признаками метаболических нарушений. Наиболее частой локализацией атеросклеротических бляшек являются общая сонная артерия (ОСА), особенно в месте бифуркации. Выраженность клиникоморфологических изменений головного мозга определяется распространенностью патологического процесса, а также степенью стеноза [4].
Билатеральный стеноз общих сонных артерий (БССА, BCAS) – является одной из экспериментальных моделей нарушений мозгового кровотока, связанного с атеросклерозом коронарных артерий. Чаще всего данная модель используется для воспроизведения хронической ишемии головного мозга, сопровождающаяся развитием нейродегенеративных процессов, когнитивными расстройствами, что в клинической практике соответствует основным признакам сосудистой деменции [1, 5]. Анализ результатов научных исследований, базирующихся на данной модели, свидетельствует о развитии морфофункциональных изменений в наиболее чувствительных к гипоксии отделах головного мозга (церебральная кора, структуры гиппокампа), при этом практически отсутствует какая-либо информация о деталях патоморфо-логических изменений в стволовой части головного мозга и мозжечке [7].
ЦЕЛЬ РАБОТЫ
Выявить наличие и описать характер па-томорфологических изменений мозжечка, а также некоторых ядер продолговатого и заднего мозга крыс при частичном двустороннем стенозе общих сонных артерий.
МЕТОДИКА ИССЛЕДОВАНИЯ
Экспериментальные исследования проводили в условиях НИИ Фармакологии. В серии экспериментов (n = 10) хроническую недостаточность мозгового кровообращения вызывали частичным стенозированием общих сонных артерий, путем наложения трех лигатур. В результате кровоток по сонным артериям ограничивался в среднем на 50–60 %. Оценку уровня локального кровотока осуществляли до и после стенозирования ОСА – в месте сразу после наложения лигатур. Регистрацию проводили с помощью лазерного допплерографа Biopac Systems, Inc., США. Интактная группа животных аналогичных по весу, полу и возрасту состояла из 10 особей. Животные выводились из эксперимента на 30-й день после операции. Головной мозг фиксировали в 10%-м нейтральном формалине, с дальнейшим обезвоживанием в батарее спиртов и изготовлением парафиновых блоков. Срезы – толщиной 5–7 мкм. Производили окрашивание срезов гематоксилином и эозином, тионином по методу Ниссля. Фотодокументирование осуществляли цифровой фотокамерой Olympus (Япония). Оценку степени нейродегенеративных изменений головного мозга проводили путем подсчета относительной численной плотности поврежденных нейронов, которые делили на 2 группы: слабо-измененные нейроны (СН) с сохранением ядра, но со структурными или тинкториальными нарушениями компонентов цитоплазмы (набухание, гиперхроматоз, хроматолиз, центральная тинкториальная ацидофилия); грубо изме- ненные нейроны (ГН) с выраженным пикнозом, «тяжелыми изменениями», гомогенизирующими изменениями нейронов, появлением клеток-теней. Статистическую обработку данных проводили с использованием пакета программ Sta-tistica 6,0 (StatSoft, USA). Различия между группами оценивали по критерию Манна–Уитни (Mann-Whitney, U-test) и считали статистически значимыми при p < 0,05 [4].
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Комплексное морфологическое и морфометрическое исследование срезов мозжечка продемонстрировало наличие значимых патологических изменений клеток Пуркинье коры. Изменения носили мозаичный и нерегулярный характер, проявляющийся чередованием дисто-фически измененных клеток с грушевидными клетками, имеющими нормальную морфологию. Патоморфологические изменения выражались в уменьшении объема клеточных тел и усилении базофилии цитоплазмы (рис. 1).
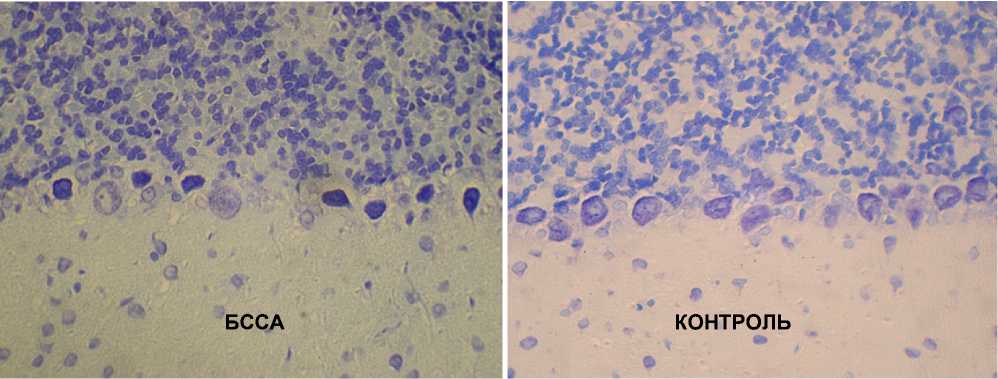
Рис.1. Уменьшение объема клеточных тел и усиление базофилии цитоплазмы клеток Пуркинье мозжечка. Головной мозг крысы. Окраска тионином по методу Ниссля. Ув. x 400
Пикнотические ядра таких клеток отличались более интенсивным окрашиванием, а также перераспределением гетерохроматина к периферии нуклеолеммы. Единичные клетки Пуркинье характеризовались выраженной гиперхромией и деформацией перикариона и ядра с признаками перицеллюлярного отека.
Статический анализ (табл. 1) продемонстрировал значительное увеличение относительной численной плотности слабо и грубо-поврежденных клеток [(17,60 ± 5,08 %) (39,04 ± 6,05 %) соответственно] по сравнению с контролем [(0,82 ± 0,52) % и (13,82 ± 4,94) % соответственно]. С другой стороны, не было выявлено достоверного уменьшения относительной площади перикарионов клеток Пуркинье (2,69 ± 0,25 % в опыте) по сравнению с интактными животными (2,75 ± 0,25 %).
В ядерных образованиях стволовой части головного мозга морфологические изменения носили нерегулярный характер. У части лабораторных животных (n = 3) значимые патоги-стологические изменения отсутствовали вовсе. В других наблюдениях (n = 5) изменения затрагивали отдельные ядерные образования и носили слабо выраженный характер. Так, в крупноклеточных двигательных ядрах тройничного и подъязычного нервов фиксировались единичные нейроны, характеризующиеся усилением базофилии ядра и цитоплазмы, без заметного уменьшения клеток в объеме. Только в единичных случаях (n = 2) выявлялись грубые изменения моторных нейронов подъязычного нерва со значительным пикнозом и гиперхромией перикарионов, при этом, нервные клетки приобретали вытянутую, палочкообразную форму (рис. 2). Дискриптивные данные подтверждались результатами статистического анализа, свидетельствующими о достоверном увеличении относительной численной плотности сла- боизмененных нейронов в двигательных ядрах тройничного нерва (V) и грубоизмененных нейронов в ядре подъязычного нерва (XII) (табл. 2). Тем не менее статистический показатель, отражающий относительную площадь нейронов, менялся незначительно. Для двигательного ядра тройничного нерва он составлял (6,47 ± 0, 38) %, при (7,23 ± 0,64) % в контроле, а для подъязычного нерва – (6,78 ± 0,54) % и (6,89 ± 0,77) % соответственно.
Таблица 1
Численная плотность дистрофически измененных клеток Пуркинье мозжечка M ± m, %
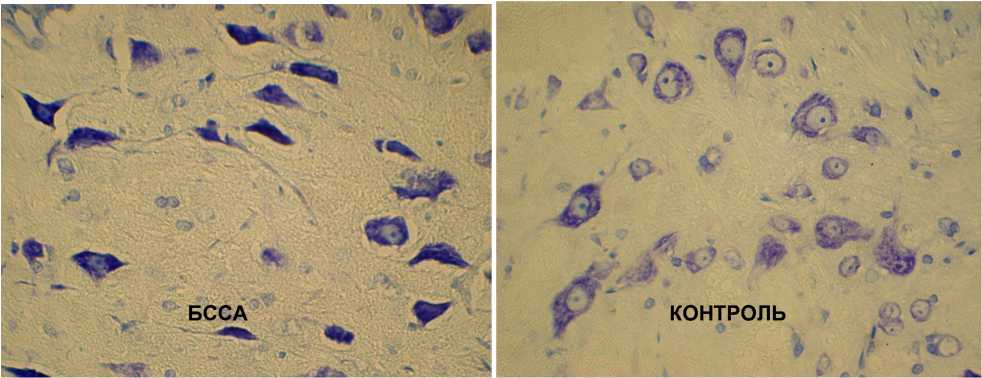
Рис. 2. Выраженный пикноз и гиперхромия крупноклеточных нейронов подъязычного нерва. Головной мозг крысы. Окраска тионином по методу Ниссля. Ув. x 400
|
Степень патоморфологических изменений |
Контроль |
Стеноз |
|
Неизмененные нейроны (НН) |
85,35 ± 4,90 |
43,35 ± 6,33* |
|
Слабоизмененные нейроны (СН) |
13,82 ± 4,94 |
39,04 ± 6,05* |
|
Грубо измененные нейроны (ГН) |
0,82 ± 0,52 |
17,60 ± 5,08* |
* Показатели статистически значимо отличаются от группы контроля при р < 0,05; Критерий Манна– Уитни.
Таблица 2
Численная плотность дистрофически измененных клеток отдельных ядерных образований ствола головного мозга M ± m, %
|
Ядерные образования ствола ГМ |
Степень патоморфологических изменений |
Контроль |
Стеноз |
|
V: моторное ядро тройничного нерва |
Неизмененные нейроны (НН) |
96,15 ± 2,77 |
71,58 ± 8,68* |
|
Слабоизмененные нейроны (СН) |
3,85 ± 2,77 |
28,42 ± 8,68* |
|
|
Грубо измененные нейроны (ГН) |
– |
– |
|
|
XII: ядро подъязычного нерва |
Неизмененные нейроны (НН) |
77,47 ± 7,49 |
53,47 ± 14,27 |
|
Слабоизмененные нейроны (СН) |
22,53 ± 7,49 |
30,03 ± 9,98 |
|
|
Грубо измененные нейроны (ГН) |
– |
16,49 ± 6,93* |
* Показатели статистически значимо отличаются от группы СД при р < 0,05; Критерий Манна–Уитни.
ЗАКЛЮЧЕНИЕ
Таким образом, морфологический и статистический анализ морфологических изменений, развивающихся в структурах головного мозга при месячном частичном билатеральном стенозе ОСА, свидетельствует о том, что данная модель приводит к развитию хронической гипоперфузии головного мозга и патоморфологиче- ским изменениям, развивающимся не только в церебральной коре, гиппокампе, стриопалли-дарной системе, но и в структурах мозжечка и стволе головного мозга. Полученные результаты, отражающие нейродегенеративные изменения клеток Пуркинье коры мозжечка, согласуются с литературными данными, свидетельствующими о высокой чувствительности данных клеток к ишемическому повреждению [1, 6]. В ядерных же образованиях ствола головного мозга патоморфологические изменения носили менее выраженный и нерегулярный характер, что, на наш взгляд, объясняется, во-первых, преимущественно вертебро-базилярным кровоснабжением данных отделов головного мозга, во-вторых, феноменом усиления растрокаудальной устойчивости нервных клеток головного мозга к повреждению, вызванному развитием острой или хронической ишемии [2, 3].
Список литературы Патоморфологические изменения в головном мозге при экспериментальном моделировании хронической ишемии
- A Novel Mouse Model of Ischemic Carotid Artery Disease / Y. Hattori [et al.] // PLoS ONE. - 2014. - № 9 (6). - Р. e100257. 10.1371/journal.pone. 0100257 DOI: 10.1371/journal.pone.0100257
- Brainstem Neurons Survive the Identical Ischemic Stress That Kills Higher Neurons: Insight to the Persistent Vegetative State / C. D. Brisson // PLoS ONE. - 2014. - № 9 (5). - Р. e96585. 10.1371/ journal.pone.0096585. DOI: 10.1371/journal.pone.0096585
- Brisson, C. D. A Distinct Boundary between the Higher Brain's Susceptibility to Ischemia and the Lower Brain's Resistance / C. D. Brisson, M. K. Lukewich, R. D. Andrew // PLoS ONE. -2013. - № 8 (11). - Р. e79589. 10.1371/journal. pone.0079589. DOI: 10.1371/journal.pone.0079589
- Carotid artery atherosclerosis, MRI indices of brain ischemia, aging, and cognitive impairment: The Framingham study / J. R. Romero [et al.] // Stroke. -2009. - № 40. - Р. 1590-1596. 10.1161/STR0-KEAHA. 108.535245. DOI: 10.1161/STR0-KEAHA.108.535245
- Dietmar, Rudolf Thal. Vascular dementia: different forms of vessel disorders contribute to the development of dementia in the elderly brain / Dietmar Rudolf Thal, Lea Tenenholz Grinberg, Johannes Attems // Exp Gerontol. - 2012. - № 47 (11). -Р. 816-824. DOI: 10.1016/j.exger.2012.05.023
- Inui, H. Matsunaga. Brainstem ischemic damage following occlusion of the blood vessels in the rat's posterior cerebral circulation / H. Inui, T. Murai -K. Yane, T. Matsunaga // Eur Arch Otorhinolaryngol. - 1996. - № 253. - Р. 176-181.
- Yorito Hattori, Junichiro Enmi, Satoshi Iguchi. Gradual Carotid Artery Stenosis in Mice Closely Replicates Hypoperfusive Vascular Dementia in Humans / Yorito Hattori, Junichiro Enmi, Satoshi Iguchi // J. Am Heart Assoc. - 2016. - № 5. -Р. e002757. DOI: 10.1161/JAHA.115.002757


