Патоморфология кардиальных изменений при синдроме внезапной детской смерти
Автор: Розумный Д.В.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Макро- и микроморфология
Статья в выпуске: 1 т.10, 2014 года.
Бесплатный доступ
С целью установления взаимосвязи между сроками облитерации фетальных коммуникаций и выраженностью ремоделирования камер сердца, как одного из возможных причинных факторов СВДС, на основе макро-морфометрического исследования был отобран материал, которым служили сердца 43 новорожденных и детей первого года жизни, умерших от СВДС. Контрольную группу составили сердца 48 детей, умерших внезапно от аспирации желудочным содержимым и от инфекционных заболеваний. Методами выбраны: макроскопическое исследование сердца по методике раздельного взвешивания с комплексом морфометрических исследований, гистологическое исследование (применялись следующие окраски: гематоксилин и эозин, пикрофуксин по Ван Гизону, окраска по Нисслю), иммуногистохимический метод с применением маркеров нейрофиламентов. В результате выявлено, что у детей, умерших от СВДС, облитерация фетальных коммуникаций наступает существенно в более поздние сроки — к 8-му месяцу жизни, а масса левого и правого желудочков сердца превышает возрастные границы нормы за счет преобладания мышечной массы желудочков и гипертрофии кар-диомиоцитов. Во всех отделах сердца отмечался субэндокардиальный фиброз, в желудочках — выраженный интерстициальный фиброз. В межпредсердной перегородке в месте локализации овального окна при морфо-метрическом исследовании наблюдалось выраженное преобладание процента площади соединительной ткани по отношению к мышечной ткани. На гистологических срезах выявлены элементы нервной ткани — неупорядоченно расположенные нервные ганглии с дистрофическими изменениями и нервные волокна. Заключение. Нарастание кардиосклероза во всех отделах сердца новорожденных и детей первого года жизни, умерших внезапно от СВДС, удлиняет сроки облитерации фетальных коммуникаций, а дистрофические изменения в нервных ганглиях приводят к нарушению подачи и распределения нервных импульсов, проходящих через них. Эти факторы способствуют развитию гемодинамических нарушений и могут иметь значение в развитии внезапной смерти детей.
Сердце, синдром внезапной детской смерти, фетальные коммуникации
Короткий адрес: https://sciup.org/14917924
IDR: 14917924
Текст научной статьи Патоморфология кардиальных изменений при синдроме внезапной детской смерти
-
1 В ведение. В патологоанатомической практике нередко приходится сталкиваться со случаями внезапной смерти ребенка. При этом подавляющее большинство случаев (70-80%) отмечается у детей первого года жизни на фоне относительного клинического благополучия и при отсутствии патоморфологи-ческих признаков, способных объяснить наступление летального исхода, что отражает понятие синдрома внезапной детской смерти (СВДС) [1]. На сегодняшний день в исследовании развития синдрома внезапной смерти детей доминирует сердечная гипотеза, отдающая предпочтение изменениям со стороны проводящей системы и кардиомиоцитов [2, 3].
Известно, что в течение первых часов жизни новорожденного физиологически происходит функциональное закрытие овального окна и артериального протока [4–6]. У новорожденных, в том числе недоношенных с экстремально низкой массой тела, перенесших преперинатальную гипоксию и имеющих тяжелую респираторную патологию, включающую в себя РДС и врожденную пневмонию, визуализируется открытое овальное окно [7, 8]. При исследовании
сердец детей 1-го года жизни, умерших на дому, обнаружена более поздняя облитерация и артериального протока, также выявлены изменения относительно нормальных величин в размерах сердечных отверстий легочного ствола и аорты [9].
Остается невыясненным значение нарушения сроков и механизмов облитерации фетальных коммуникаций при антенатальной и постнатальной гипоксии в развитии синдрома внезапной детской смерти.
Цель: установление взаимосвязи между сроками облитерации фетальных коммуникаций и выраженностью ремоделирования камер сердца, как одного из возможных причинных факторов СВДС, на основе макроморфометрического исследования.
Материал и методы. Исследован 91 случай смерти на дому младенцев в возрасте до 1 года за 2008–2013 гг., вскрытия проведены на базе патологоанатомического отделения ДГКБ № 1 г. Самары. Весь материал исследования разделен на 2 группы: 1) сердца новорожденных и грудных детей, умерших от СВДС (основная группа наблюдений), — 43 наблюдения; 2) сердца новорожденных детей, умерших от аспирации желудочным содержимым или инфекционных заболеваний без поражения сердца (группа сравнения), — 48 наблюдений. Данная группа слу- жила в качестве группы сравнения результатов, поскольку механизм смерти в этих случаях также носил острый характер.
При патологоанатомическом исследовании сердца детей в 5 возрастных группах (0–30 дн.; 1 мес. — 1 мес. 30 дн.; 2 мес. — 2 мес. 30 дн.; 3 мес. — 5 мес. 30дн.; 6 мес. — 1 год) применяли методику раздельного взвешивания сердца и комплекс макроморфо-метрических исследований с замерами общей массы сердца, диаметра открытых фетальных коммуникаций. Для гистологического исследования проводили забор фрагментов правого, левого желудочков, межпредсердной перегородки в месте локализации овального окна. Использовали следующие окраски гистологических препаратов: гематоксилин и эозин, пикрофуксин по Ван Гизону, окраска по Нисслю. Иммуногистохимически верифицировали нейрофиламенты с применением маркеров Moab anti Human Neurofilament (Clone 2F11, Cat. no. MON3004, “Monosan”); Rabbit Anti-Human S 100 Polyclonal Antibody (“Spring Bioscience”); Rabbit Anti-Human Synaptophy-sin Monoclonal Antibody (Clone SP11, “Spring Bioscience”). Проводили морфометрическое исследование относительной площади соединительнотканного и мышечного компонентов в гистологических препаратах, окрашенных пикрофуксином, с помощью программы «Видео Тест-Морфо 6.2». Математическая обработка результатов исследования проводилась с помощью статистического пакета программ Excel на персональном компьютере Intel (R) Core (TM) i7 CPU. Статистический анализ проводили с использованием пакета программ статистической обработки результатов SSPS 13.0 и 20.0 for Windows. В работе использованы методы вариационной статистики, оценку достоверности различий проводили по t-критерию Стьюдента.
Результаты. В группе сравнения антропометрические показатели сердца ребенка во всех подгруппах соответствовали возрастной норме (от 22±1,4 г у новорожденных до 35,5±3,4 г в подгруппе от 6 мес. до 1 года). В основной группе наблюдений макроскопически отмечалось увеличение сердца в объеме с некоторым преобладанием правых отделов сердца. При проведении макроморфометрии в подгруппах детей до 2 месяцев жизни общая масса сердца не отличалась от возрастной нормы, в старших возрастных подгруппах незначительно превышала ее (от 19,2±3,2 г у новорожденных до 41,5±3,5 г в подгруппе от 6 мес. до 1 года), однако различия ни в одной из подгрупп не были достоверными при р≤0,05. При раздельном взвешивании камер сердца в основной группе наблюдений получены достоверно (при р≤0,05) более высокие абсолютные значения массы правого желудочка сердца по сравнению с показателями группы сравнения (на 1,7±0,1 г у новорожденных и на 5,1±0,2 г в подгруппе от 6 мес. до 1 года), масса левого желудочка сердца достоверно превышала возрастную норму только в подгруппе от 6 мес. до 1 года (1,9±0,2 г). Таким образом, в первые 3 месяца жизни у детей с СВДС прирост массы сердца происходил преимущественно за счет правых отделов сердца.
Преобладание мышечной массы правого желудочка, по нашему мнению, может развиться вследствие гемодинамических нарушений, сопровождающих эктазию фетальных коммуникаций и более поздние сроки их облитерации. В группе наблюдений детей, умерших от СВДС, при патологоанатомическом исследовании нам часто встречались функционирующие фетальные коммуникации (рис. 1). Чтобы определить возрастной диапазон нарушения сроков облитерации фетальных коммуникаций все наши наблюдения основной группы (43 ребенка) были перегруппированы по возрастным периодам с равномерным шагом в два месяца. Функциональное закрытие овального окна в норме происходит в первые часы жизни, артериальный проток начинает функционально закрываться спустя 10–15 часов после родов, а через 96 часов жизни не определяется. У детей, умерших от СВДС, во всех возрастных подгруппах были выявлены открытые фетальные коммуникации, с большей частотой в первые 6 месяцев жизни (рис. 2). Предельным сроком наличия открытых коммуникаций в наших наблюдениях является срок в 8 месяцев. Таким образом, у детей с СВДС можно констатировать более поздние сроки облитерации овального окна. В основной группе детей, умерших от СВДС, отмечались следующие размеры открытого артериального протока: 0,4±0,1 см; овального окна: 0,9±0,4 см в диаметре. Встречались как случаи изолированного открытого овального окна различного диаметра, так и сочетание открытого овального окна с открытым артериальным протоком.
При микроскопическом исследовании гистологических препаратов во всех отделах сердца отмечался субэндокардиальный фиброз (рис. 3), в желудочках — выраженный интерстициальный фиброз. В межпредсердной перегородке в месте локализации
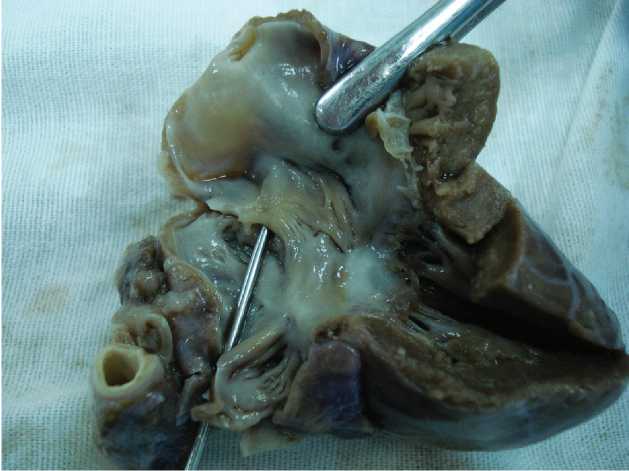
Рис. 1. Межпредсердная перегородка. Открытое овальное окно
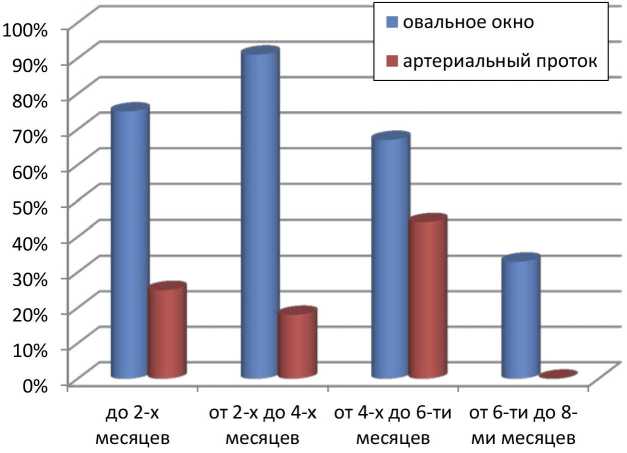
Рис. 2. Распределение по возрастным группам частоты встречаемости открытых фетальных коммуникаций
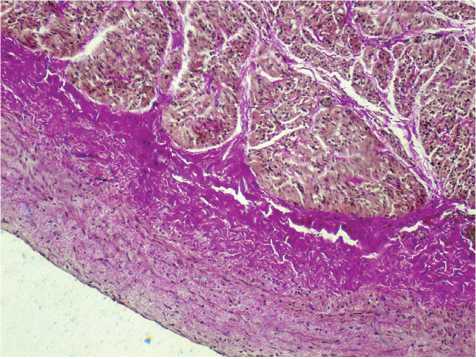
Рис. 3. Межпредсердная перегородка. Субэндокардиальный фиброз. Окраска пикрофуксином по Ван Гизону, х 150
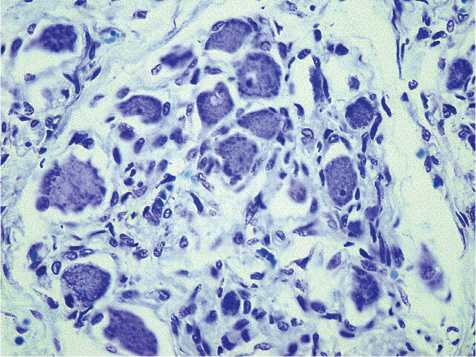
Рис. 4. Межпредсердная перегородка в области локализации овального окна. Нервный ганглий, часть клеток лишены ядер. Окраска по Нисслю, x 600.
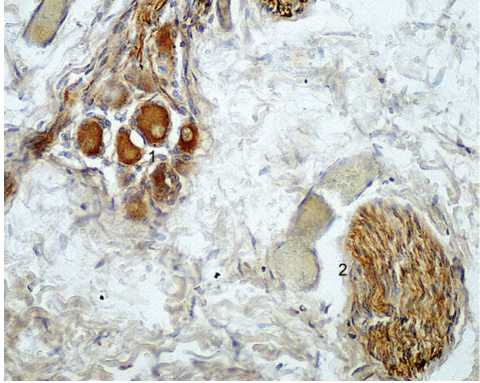
Рис. 5. Межпредсердная перегородка в области локализации овального окна. Отмечается экспрессия маркера нейрофиламента Moab anti Human Neurofilament (Clone 2F11, Cat. no. MON3004, “Monosan”) в цитоплазме клеток нервных ганглиев (1) и в нервных волокнах (2). Иммуногистохимическая реакция, x 600
овального окна выявлено выраженное преобладание площади соединительной ткани (в основной группе 75,48±0,001, в группе сравнения 47,87±0,003, р≤0,05) по отношению к мышечной ткани. В гистологических срезах межпредсердной перегородки выявлены элементы нервной ткани: нервные ганглии и нервные волокна. Нервные ганглии располагались неупорядоченно, обращало на себя внимание различие в размерах ганглиев в пределах межпредсердной перегородки (рис. 4). Некоторые клетки ганглиев были с дистрофическими изменениями, некробиозом. Рядом с ганглиями располагались, как правило, нервные волокна с отеком стромы (рис. 5).
Макропрепарат сердца мальчика 2 мес.14 дн., основная группа наблюдений
Обсуждение. Полученные при макроморфометрии данные в виде гипертрофии правых отделов сердца и более поздней облитерации овального окна свидетельствуют о дискоординации кардиоморфогенеза, характерной для детей первого года жизни, умерших от СВДС. Нарастающее преобладание мышечной массы и склеротических изменений стромы правого желудочка и сохранение функционирующих фетальных коммуникаций, в частности эктазии овального окна, взаимно отягощают друг друга. Кроме того, усиленная работа кардиомиоцитов желудочков сердца на фоне развивающегося в них склеротического компонента может оказаться важной при возникновении дисритмических осложнений как непосредственной причины смерти ребенка от СВДС. Учитывая наличие дистрофических изменений клеток нервных ганглиев и нервных волокон, можно предположить их патологическое влияние на кардиомиоциты и роль в нарушениях ритма сердечной деятельности.
Заключение. Нарастание кардиосклероза в правом и левом желудочках сердца, межпредсердной перегородке новорожденных и детей первого года жизни, умерших внезапно от СВДС, удлиняет сроки облитерации фетальных коммуникаций, что, в свою очередь, приводит к изменениям гемодинамики и гипертрофии желудочков сердца. Развитию соединительнотканного компонента способствует гипоксическое состояние тканей, что можно предположить и для сердца ребенка, перенесшего внутриутробную гипоксию и умершего внезапно от СВДС. Дистрофические изменения в нервных ганглиях приводят к нарушению подачи и распределения нервных импульсов, проходящих через них, и могут служить непосредственной причиной остановки сердца детей.
Список литературы Патоморфология кардиальных изменений при синдроме внезапной детской смерти
- Зубов Л. А., Богданов Ю.М., Вальков А. Ю. Синдром внезапной детской смерти. Экология человека 2004;(1): 22-29
- Willinger М, Sheers NJ. Changing concepts of Sudden Infant Death Syndrome implications for infant sleeping environment and sleep position (re9946). Pediat 2000; 105 (3): 650-656
- Глуховец Б. И., Глуховец Н. Г. Патоморфологические основы внутриутробной недостаточности сердечной деятельности плодов и новорожденных. Материалы 3-го съезда Рос. общ. детск. патологоанат. СПб., 2008: 25-28
- Белозеров Ю.М. Физиология сердечнососудистой системы плода в переходный период и у новорожденных. В кн.: Актуальные вопросы кардиологии детского возраста: Неонатальная кардиология. М., 1997: 5-16
- Булатов В. П., Алиева М.Н. Функциональное состояние миокарда у новорожденных и детей грудного возраста. Казанский медицинский журнал 2008; 89 (4): 507-510
- Афанасьев Ю.И., Горячкина В.Л. Сердечно-сосудистая система: Сердце. В кн.: Руководство по гистологии. Т. 2. СПб.: Спец. лит., 2001: 259-271
- Виноградова И. В., Краснов М.В., Иванова Н.Н. Особенности состояния сердечно-сосудистой системы у новорожденных с экстремально низкой массой тела. Медицинский альманах 2009;(4): 103-106
- Симонова Л. В., Котлукова Н.П., Гаудукова Н.В. Постгипоксическая дезадаптация сердечно-сосудистой системы у новорожденных детей. Российский вестник перинатологии и педиатрии 2001;(2): 8-12
- Котлукова Н.П. Современные представления о механизмах развития кардиоваскулярной патологии у детей раннего возраста. Российский вестник перинатологии и педиатрии 2003;(3): 28-33.


