Патоморфоз экспериментальной диабетической кардиомиопатии при фармакологической коррекции сукцикардом
Автор: Тюренков Иван Николаевич, Смирнов Алексей Владимирович, Бакулин Дмитрий Александрович, Великородная Юлия Ивановна, Быхалов Леонид Сергеевич
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 1 т.20, 2023 года.
Бесплатный доступ
Экспериментальное моделирование стрептозотоцин-индуцированного сахарного диабета длительностью 6 месяцев проводили на 30 белых беспородных лабораторных крысах-самках в возрасте 12 месяцев. Обнаружено развитие диабетической кардиомиопатии, которая проявлялась фиброзом миокарда левого желудочка сердца, контрактурными повреждениями и гипертрофией кардиомиоцитов. Лечение проводили сукцикардом в течение месяца. Индуцированный патоморфоз диабетической кардиомиопатии проявлялся снижением степени выраженности патологических изменений в миокарде левого желудочка и сопровождался уменьшением выраженности фиброза, значимым снижением диаметра кардиомиоцитов, что, по-видимому, обеспечивается за счет протективного влияния препарата на метаболические процессы в кардиомиоцитах и эндотелиоцитах кровеносных сосудов миокарда.
Сахарный диабет, кардиомипатия, сукцикард
Короткий адрес: https://sciup.org/142238042
IDR: 142238042 | УДК: 616-005.4:611.813.14:616-092.9
Pathomorphosis of experimental diabetic cardiomyopathy during pharmacological correction with succicard
Experimental modeling of streptozotocin-induced diabetes mellitus lasting 6 months was carried out on 30 white outbred laboratory female rats, aged 12 months. The development of diabetic cardiomyopathy, which was manifested by myocardial fibrosis of the left ventricle of the heart, contracture injuries and hypertrophy of cardiomyocytes, was detected. The treatment was carried out with succicard for a month. The induced pathomorphosis of diabetic cardiomyopathy was manifested by a decrease in the severity of pathological changes in the left ventricular myocardium and was accompanied by a decrease in severity of fibrosis, a significant decrease in the diameter of cardiomyocytes, which, apparently, is provided due to protective effect of the drug on metabolic processes in cardiomy-ocytes and endotheliocytes of myocardial blood vessels.
Текст научной статьи Патоморфоз экспериментальной диабетической кардиомиопатии при фармакологической коррекции сукцикардом
Funding : the work was carried out with the financial support of the RSF grant No. 21-15-00192.
Диабетическая кардиомиопатия (ДКМП) рассматривается как сердечная патология, которая не объясняется другими сердечно-сосудистыми или несердечно-сосудистыми заболеваниями, которые могут быть отнесены к сахарному диабету (СД) [1, 2]. Существование кардиомиопатии, связанной исключительно с диабетом при наличии значительного числа пациентов с коморбидной патологией, включающейся в общий патогенез [2], было и остается предметом споров, поскольку ДКМП предполагает уникальный патогенез, отличный от других заболеваний, что можно использовать для разработки новых методов лечения данного заболевании [3].
Частота сердечной недостаточности (СН) у мужчин и женщин с сахарным диабетом 2-го типа (СД2) как минимум в 2,4 и 5,1 раза выше соответственно, чем у лиц того же пола без СД [4].
Инсулинорезистентность, гиперинсулинемия и гипергликемия являются независимыми факторами риска развития ДКМП. К патофизиологическим факторам СД, которые способствуют развитию кардиомиопатии, относятся системные метаболические нарушения, неадекватная активация ренин-ангиотензин-альдосте-роновой системы, аномалии субклеточного компонента, окислительный стресс, воспаление и дисфункциональная иммуномодуляция.
Вышеуказанные факторы способствуют интерстициальному фиброзу сердечной ткани, гипертрофии кардиомиоцитов [5].
Диабетическая кардиомиопатия характеризуется нарушениями различных метаболических, паракринных и нейрогуморальных механизмов регуляции [6] кардиомиоцитов и эндотелия, опосредуя концентрическое ремоделирование и гипертрофию миокарда левого желудочка (ЛЖ), что способствуют диастолической дисфункции [7].
Новые данные о выявляемых при кластерном анализе у пациентов с СД2 различных фенотипах, регистрируемых с использованием комбинации клинических, биохимических, визуализационных и генетических переменных, отображающих спектр уникальных профилей сердечно-сосудистого риска [8], и данные о повышении риска сердечной недостаточности при использовании некоторых сахароснижающих препаратов по сравнению со стандартной терапией способствуют поиску новых путей коррекции ДКМП [9].
Так, поскольку гамма-аминомасляная кислота (ГАМК) значительно увеличивает уровни АТФ и активность НАДН-дегидрогеназы дозозависимым образом, даже демонстрирует новую физиологическую роль в продукции эритропоэтина [10] и может способствовать снижению метаболических нарушений и ишемических повреждений миокарда, разработанные производные ГАМК, например сукцикард (4-фенилпирацетам и этан-1,2-дикарбоновая кислота, 2:1), проявляющий выраженный мембранопротекторный эффект [11], представляют собой новый потенциальный класс протективных средств, которые могут быть использованы при комплексном лечении СД. Более того, показано, что под влиянием производного ГАМК мефаргина отмечено снижение выраженности патологических изменений в миокарде левого желудочка предположительно за счет протективного влияния препарата на эндотелий сосудов микроциркуляторного миокарда левого желудочка [5].
ЦЕЛЬ РАБОТЫ
Охарактеризовать морфологические изменения миокарда левого желудочка при экспериментальном сахарном диабете и его фармакологической коррекции сукцикардом.
МЕТОДИКА ИССЛЕДОВАНИЯ
Экспериментальное исследование проведено на 30 белых беспородных лабораторных крысах-самках в возрасте 12 месяцев. Моделирование стреп-тозотоцин-индуцированного СД длительностью 6 месяцев и его проявлений в виде диабетической кардиомиопатии проводили по ранее описанной методике [5]. Лечение начинали через 6 месяцев после моделирования СД.
Исследуемое производное ГАМК, сукцикард, вводили перорально в течение 30 дней в дозе
50 мг/кг. Группе негативного контроля вводили физиологический раствор (крысы с СД без лечения). В качестве позитивного контроля использовали крыс без СД (интактных) той же партии животных.
После курсового лечения у наркотизированных (хлоралгидрат, 400 мг/кг, внутрибрюшинно) животных проводили забор образцов тканей левого желудочка сердца. Образцы тканей левого желудочка сердца проводили у наркотизированных (хлоралгидрат, 400 мг/кг, внутрибрюшинно) животных. Материал фиксировали в течение 24 часов в 10%-м растворе нейтрального забуференного формалина (pH 7,4), обезвоживали и заливали в парафин по общепринятой гистологической методике. На роторном микротоме изготавливали срезы толщиной 4–5 мкм. Окрашивали парафиновые срезы гематоксилином и эозином, трихромом по Массону.
Оценивали структурные изменения миокарда, степень фиброза, наличие воспалительной инфильтрации, выраженность изменений кардиомиоцитов при стандартном освещении и в поляризованном свете.
Гистологические срезы фотографировали цифровой камерой AxioCam 305 color (Carl Zeiss Microscopy GmbH, Германия) на базе микроскопа AxioImager A2 (Carl Zeiss Microscopy GmbH, Германия) с использованием объективов ×10, ×20, ×40. Средний диаметр кардиомиоцитов (мкм) определяли с помощью морфометрического метода исследования в произвольно выбранных областях левого желудочка с использованием программного обеспечения Zeiss Zen Pro 2.3 2021 (Carl Zeiss Microscopy GmbH, Германия).
Статистическую обработку данных проводили с использованием пакета программы «Statistica 10.0» (USA). Проверку выборки на нормальность проводили с помощью теста Колмогорова – Смирнова. Сравнение двух независимых выборок проводили непараметрическим методом (парный тест Манна – Уитни). Сравнение трех и более независимых выборок проводили непараметрическим методом (критерий Краскела – Уоллиса с посттестом Данна). Гипотезу о существовании различий между выборками принимали при уровне р < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
При экспериментальном моделировании СД в миокарде левого желудочка помимо дистрофических изменений в кардиомицитах отмечалось увеличение очаговых контрактурных изменений в миокарде левого желудочка по сравнению с интактным контролем, определяем при поляризационной микроскопии (рис. 1, 2).
Выявлена гипертрофия в значительной части кардиомиоцитов в стенке левого желудочка. Отмечено фиброзирование миокарда, в большей степени в левом желудочке, за счет разрастания волокнистой соединительной ткани, преимущественно в субэндо- кардиальных отделах миокарда и переваскулярно субэпикардиальных отделах.
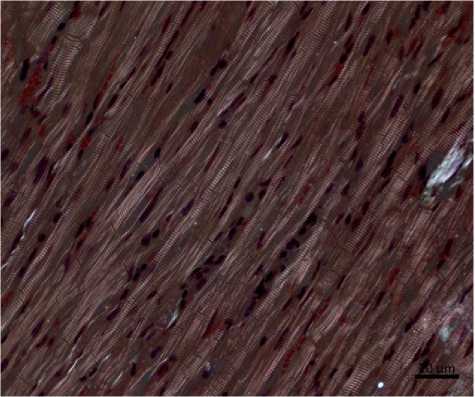
Рис. 1. Строение миокарда левого желудочка интактной крысы.
Окраска гематоксилином и эозином, поляризационная микроскопия

Рис. 2. Строение миокарда левого желудочка крысы с экспериментальным сахарным диабетом.
Окраска гематоксилином и эозином, поляризационная микроскопия
У животных с сахарным диабетом, получавших сукцикард, было отмечено менее выраженное фиброзирование миокарда за счет меньшего разрастания периваскулярной соединительной ткани, по сравнению с группой сахарного диабета. В кардиомиоцитах определялась поперечная исчерченность, наряду с наличием дистрофических изменений. Преобладали участки миокарда левого желудочка с умеренной гипертрофией, которые сочетались с наличием участков с атрофическими изменениями. Фиброзирование миокарда наблюдалось преимущественно в периваскулярных отделах, обнаруживались единичные прослойки фиброзной соединительной ткани в интерстиции миокарда при окраске по Массону. В целом степень фиброза в миокарде была оценена как слабо выраженная.
При поляризационной микроскопии гистологических препаратов, окрашенных гематоксилином и эозином, у животных с сахарным диабетом, получавших сукцикард, было выявлено наличие хорошо выявляемой поперечной исчерченности в кардиомиоцитах, отсутствие контрактурных изменений в миокарде левого желудочка (рис. 3).
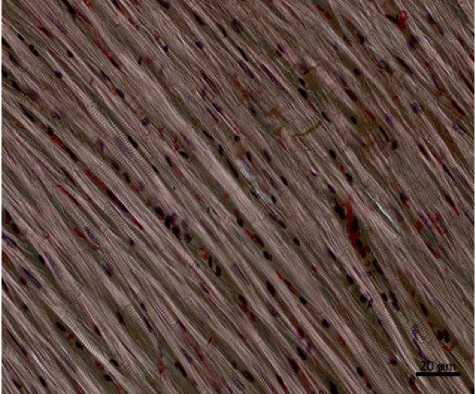
Рис. 3. Строение миокарда левого желудочка крысы с экспериментальным сахарным диабетом, получавших сукцикард. Окраска гематоксилином и эозином, поляризационная микроскопия
Морфометрическое исследование выявило увеличение размеров кардиомиоцитов левого желудочка у животных с сахарным диабетом: диаметр кардиомиоцитов левого желудочка у животных с сахарным диабетом составил 16,40 мкм (ДИ 14,11783; 18,42735), у интактных крыс – Ме 9,41 мкм (ДИ 8,32797; 10,74161), увеличение размеров кардиомиоцитов составило 74,3 % (при p < 0,01).
У животных с сахарным диабетом, получавших сукцикард, диаметр кардиомиоцитов по сравнению с группой интактных крыс вырос на 24,8 % (при p < 0,01) и составил Ме 11,74 мкм (ДИ 10,44734; 12,53243), что на 28,4 % (при p < 0,01) меньше по сравнению с группой животных с сахарным диабетом без лечения.
Результаты проведенного исследования уточняют количественные данные о морфогенезе ДКМП у экспериментальных животных, которая сопровождается диффузно-очаговым фиброзированием миокарда левого желудочка и значительной гипертрофией кардиомиоцитов.
При рассмотрении лекарственного патоморфоза ДКМП у экспериментальных животных выявлено про-тективное влияние сукцикарда на миокард левого желудочка, что проявлялось в снижении выраженности гипертрофии миокарда, контрактурных повреждений кардиомиоцитов, что может быть обусловлено мем-брано- и кардиопротективным действием производных ГАМК, механизм которого связан с симпатоинги-бирующими эффектами посредством активации рецепторов ГАМК, тормозных влияний на центральные симпатические структуры, ведущих к нормализации гемодинамики и нормализации метаболизма кардиомиоцитов [12].
Наблюдаемое в эксперименте снижение выраженности фиброза при исследовании индуцированного сукцикардом патоморфоза ДКМП может быть связано с уменьшением метаболических изменений в миокарде вследствие антиоксидантной защиты эндотелия производным ГАМК, сукцикардом, и снижением эндотелиальной дисфункции [13].
ЗАКЛЮЧЕНИЕ
Таким образом, обнаруженное при индуцированном патоморфозе диабетической кардиомиопатии при фармакологической коррекции сукцикардом снижение выраженности фиброзирования и гипертрофии миокарда левого желудочка сердца рассматривается как морфологическое проявление ДКМП.
Наблюдаемое под влиянием сукцикарда снижение выраженности патологических изменений в миокарде левого желудочка, по нашему мнению, реализуется посредством протективного влияния препарата на метаболические процессы в кардиомиоцитах и эн-дотелиоцитах кровеносных сосудов миокарда. Изучение роли эндотелиальной дисфункции в патогенезе ДКМП требует дальнейшего углубленного анализа молекулярных механизмов.
Список литературы Патоморфоз экспериментальной диабетической кардиомиопатии при фармакологической коррекции сукцикардом
- Смирнов А. В., Бисинбекова А. И., Файбисович Т. И. Морфофункциональные изменения головного мозга при сахарном диабете // Вестник Волгоградского государственного медицинского университета. 2022. Т. 19, № 3. С. 3–8.
- Mechanisms of diabetic cardiomyopathy and potential therapeutic strategies: preclinical and clinical evidence / Y. Tan, Z. Zhang, C. Zheng [et al.] // Nat Rev Cardiol. 2020. No. 17(9). Р. 585–607.
- Lorenzo-Almorós A., Cepeda-Rodrigo J. M., Lorenzo Ó. Diabetic cardiomyopathy // Rev Clin Esp (Barc). 2022. No. 222(2). Р. 100–111.
- Prognostic impact of diabetes and prediabetes on survival outcomes in patients with chronic heart failure: A Post-Hoc Analysis of the GISSI-HF (Gruppo Italiano per lo Studio della Sopravvivenza nella Insufficienza Cardiaca-Heart Failure) / M. Dauriz, G. Targher, P. L. Temporelli [et al.] // Trial. J Am Heart Assoc. 2017. No. 6(7). e005156.
- Тюренков И. Н., Смирнов А. В., Бакулин Д. А., Великородная Ю. И. Морфологические особенности миокарда при экспериментальном сахарном диабете и его фармако-логической коррекции мефаргином // Волгоградский научно-медицинский журнал. 2022. № 4. С. 25–29.
- Phenotype-specific treatment of heart failure with pre-served ejection fraction: a multiorgan roadmap / S. J. Shah, D. W. Kitzman, B. A. Borlaug [et al.] // Circulation. 2016. No. 134(1). Р. 73–90.
- Wan A., Rodrigues B. Endothelial cell-cardiomyocyte crosstalk in diabetic cardiomyopathy // Cardiovasc Res. 2016. No. 111(3). Р. 172–183.
- Clinical phenotypes in patients with type 2 diabetes mellitus: characteristics, cardiovascular outcomes and treat-ment strategies / P. Gouda, S. Zheng, T. Peters [et al.] // Curr Heart Fail Rep. 2021. No. 18(5). Р. 253–263.
- Udell J. A., Cavender M. A., Bhatt D. L. Glucose-lowering drugs or strategies and cardiovascular outcomes in patients with or at risk for type 2 diabetes: a meta-analysis of randomised controlled trials // Lancet Diabetes Endocrinol. 2015. No. 3. Р. 356–366.
- Park K. T., Han J. K., Kim S. J., Lim Y. H. Gamma-aminobutyric acid increases erythropoietin by activation of cit-rate cycle and stimulation of hypoxia-inducible factors expres-sion in rats // Biomolecules. 2020. No. 10(4). Р. 595.
- Изменение деформабельности и резистентности мембран эритроцитов у потомства крыс с экспериментальной преэклампсией под действием производных гамма-аминомасляной кислоты / Е. А. Музыко, Л. В. Науменко, В. Н. Перфилова [и др.] // Российский медико-биологический вестник им. академика И. П. Павлова. 2022. Т. 30, № 1. C. 13–20.
- Перфилова В. Н. Кардиопротекторные свойства структурных аналогов ГАМК: автореф. дис. … докт. биол. наук: 14.00.25 / Перфилова Валентина Николаевна. Волгоград, 2009. 49 с.
- Антиоксидантная терапия эндотелиальной дис-функци / И. Н. Тюренков, А. В. Воронков, А. А. Слиецанс [и др.] // Обзоры по клинической фармакологии и лекарственной терапии. 2013. Т. 11, № 1. С. 14–25.


