Переработка руды месторождения Нюд II методом низкотемпературного обжига с сульфатом аммония
Автор: Горячев А. А., Макаров Д. В., Потапов С. С., Беляевский А. Т., Семушин В. В., Компанченко А. А.
Журнал: Вестник Мурманского государственного технического университета @vestnik-mstu
Рубрика: Науки о земле
Статья в выпуске: 2 т.26, 2023 года.
Бесплатный доступ
Мурманская область располагает значительным объемом сульфидного медно-никелевого сырья. Перспективными для переработки являются месторождения массива Нюд, связанные с Мончеплутоном (Нюд II и Терраса). В качестве объекта исследования выбрана забалансовая руда месторождения Нюд II с исходным содержанием никеля 0,45 % и меди 0,39 %. В процессе исследования руду смешивали с сульфатом аммония, измельчали и обжигали полученную смесь в муфельной печи в статической атмосфере воздуха. Обожженную смесь выщелачивали в подогретой дистиллированной воде при постоянном перемешивании. Максимальное извлечение металлов достигается при измельчении до класса –40 мкм, соотношении руды и сульфата аммония 1 : 7, температуре обжига 400 °С, продолжительности обжига 300 мин. В обожженной при данных параметрах смеси в ходе рентгенофазового анализа фиксируются рефлексы сульфатов меди и никеля. На стадии водного выщелачивания максимальное извлечение никеля составило 79,1 %, меди – 75,8 %.
Медно-никелевые руды, низкотемпературный обжиг, сульфат аммония, месторождение Нюд II, выщелачивание, цветные металлы, copper-nickel ores, low-temperature roasting, ammonium sulfate, Nud II deposit, leaching, non-ferrous metals
Короткий адрес: https://sciup.org/142237547
IDR: 142237547 | УДК: 622.78(470.21) | DOI: 10.21443/1560-9278-2023-26-2-137-149
Текст статьи Переработка руды месторождения Нюд II методом низкотемпературного обжига с сульфатом аммония
e-mail: , ORCID:
e-mail: , ORCID:
Рост потребления цветных металлов обусловлен их востребованностью в базовых отраслях промышленности. Медь в чистом виде широко используется в электротехнике при производстве силовых кабелей; она является важным компонентом генераторов, трансформаторов, двигателей и систем возобновляемой энергетики. Этот металл применяется для изготовления систем связи, мобильных телефонов и персональных компьютеров, а также в строительной отрасли в ходе создания санитарно-технических систем ( Кондратьев и др., 2019 ). Основная часть вырабатываемого никеля расходуется на производство жаропрочных, конструкционных, инструментальных и нержавеющих сталей, где никель применяется в качестве легирующего элемента; до 20 % никеля используется в производстве сплавов и суперсплавов совместно с железом, хромом, медью, цинком и другими металлами ( Игревская, 2005 ). Значительную роль медь и никель играют в транспортной промышленности. Вследствие увеличения производства электротранспорта спрос на эти металлы существенно возрос. В 2022 г. отмечен значительный рост цен на медь и никель, так как их рыночные запасы находятся на многолетних минимумах. Кроме того, влияние на рост цен оказала геополитическая обстановка.
Авторы работы ( Henckens et al., 2020 ) отмечают тенденцию роста производства меди и никеля и прогнозируют рост объема их производства более чем в 12 раз к 2100 г. В Российской Федерации активно разрабатываются сульфидные медно-никелевые месторождения, на долю которых приходится около 37 % мировых запасов никеля. Характерной особенностью сульфидных месторождений является относительно выдержанный минеральный состав руд. Главными рудными минералами являются пирротин, пентландит, халькопирит и магнетит. Среди второстепенных минералов характерны пирит, кубанит, миллерит, валлериит, минералы группы платины. Руды содержат никель, медь, кобальт, платиноиды, а также селен и теллур, золото, серебро и серу. Месторождения сульфидных руд являются ведущими в запасах и добыче никеля в России.
С Мурманской областью связаны значительные запасы медно-никелевого сырья природного и техногенного происхождения. В проведенных ранее исследованиях по обогащению руд большое внимание уделяется залежам массива Нюд, а именно месторождениям Нюд II и Терраса. Содержание никеля и меди в образцах руды ниже бортового, составляющего для никеля 0,55 % ( Терновой и др., 2009 ). В этом случае эффективность традиционных способов обогащения существенно снижается. Для руд данных месторождений предложены схемы обогащения на основе кучного выщелачивания с применением растворов серной кислоты, а также бактериальных культур ( Фокина и др., 2018; Masloboev et al., 2018 ).
Проведенные исследования указали на перспективность вовлечения забалансовых руд данных месторождений в переработку при создании альтернативных технологий обогащения. По этой причине для переработки руды выбран химический метод обогащения с использованием сульфата аммония, что обусловлено его высокой реакционной способностью и наличием в исходной руде сульфидов цветных металлов, механизм взаимодействия которых с сульфатом аммония был описан нами в предыдущих работах ( Горячев и др., 2022 ). Технология низкотемпературного обжига сульфидного сырья с сульфатом аммония успешно применялась в мировой практике для различных видов сырья ( Ju et al., 2023 ), например латеритных и сульфидных никелевых руд ( Li et al., 2018 ; Cui et al., 2020 ), бокситовых ( Xu et al., 2022 ), окисленных цинковых ( Sun et al., 2015 ), марганцевых руд ( Deng et al., 2018 ) и др. Технология апробирована ранее для руды отвала Аллареченского месторождения ( Горячев и др., 2020 ) и чернового медно-никелевого концентрата, полученного из руды месторождения Заполярное Печенгского рудного поля ( Goryachev et al., 2021 ).
Материалы и методы
Отбор проб руды месторождения Нюд II выполнен в летний период 2021 г. (рис. 1); руда взята с бортов карьера; среднее содержание Ni составляет 0,45 %, Cu – 0,39 %. Основными рудными минералами являются пирротин, пентландит, халькопирит, магнетит.
В ходе лабораторных исследований сульфидное сырье перемешивали с сульфатом аммония квалификации "химически чистый" (ГОСТ 3769-78) и измельчали полученную смесь в шаровой мельнице BMU-100 (HT Machinery Co. Ltd., КНР). После этого смесь обжигали в муфельной печи СНОЛ 3/11 (ООО "НПФ Термикс", Россия), варьируя температуру (300–500 °С) и продолжительность обжига (60–340 мин) в статической атмосфере воздуха. После обжига смесь охлаждали на открытом воздухе при температуре ≈ 20 °С в течение 60 мин. Затем обожженную смесь выщелачивали в подогретой до ≈ 80 °С дистиллированной воде в течение 40 мин при постоянном перемешивании интенсивностью 230 мин–1, используя верхнеприводную мешалку MV-6 (ООО "НВ-ЛАБ", Россия).
Для диагностики минерального состава экспериментальных проб был применен метод порошковой рентгеновской дифракции (CuK α -излучение, длина волны 0,154184 Å) на приборе ДРОН-2.0 (АО "ИЦ Буревестник", Россия). Расшифровка дифрактограмм выполнена c использованием эталонов сравнения картотеки рентгеновских данных JCPDS или ASTM. Определение морфологии и состава частиц руды произведено с помощью сканирующего цифрового электронного микроскопа с программным обеспечением
SEM Leo-420 (Carl Zeiss Ltd., Германия) и микрозондовой приставки INKA ENERGY-400 (Oxford Instruments plc., Великобритания).



Рис. 1. Отработанный карьер месторождения Нюд II Fig. 1. Excavated quarry of the Nud II deposit
Концентрации ионов никеля, меди и железа в продуктивных растворах определены методом атомноабсорбционной спектроскопии (Shimadzu-AA7000G, Shimadzu Corp., Япония) с электротермической атомизацией (ПНД Ф 14.1:2:4.140-98). Обработка результатов экспериментов произведена в программном продукте Microsoft Excel.
Результаты и обсуждение
В исходном образце руды месторождения Нюд II с помощью метода РФА1 обнаружено значительное количество рефлексов нерудных минералов: полевые шпаты, амфиболы, серпентины, тальк Mg3Si4O10(OH)2, кварц SiO 2 . Помимо нерудных минералов выявлены сульфиды: пентландит (Fe, Ni) 9 S 8 , пирротин Fe 1-x S n и халькопирит CuFeS 2 (рис. 2, а ); зафиксированы рефлексы магнетита FeFe 2 O 3 . После перемешивания руды с сульфатом аммония на дифрактограмме отмечены рефлексы масканьита (NH4)2SO4, являющегося природным аналогом данного соединения (рис. 2, б ). После добавления сульфата аммония не зафиксированы рефлексы халькопирита и магнетита из-за снижения их относительного содержания в смеси. Остальные минералы, входящие в состав исходной руды, главным образом нерудные, диагностируются.
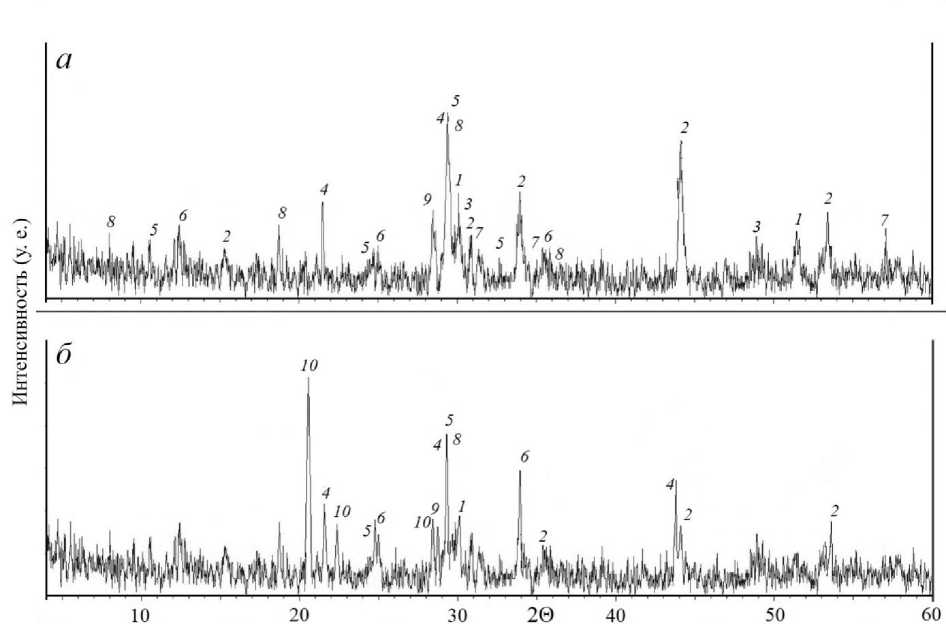
Рис. 2. Дифрактограммы руды месторождения Нюд II ( а ) и смеси руды с сульфатом аммония ( б ). Рефлексы: 1 – пентландит; 2 – пирротин; 3 – халькопирит; 4 – полевой шпат; 5 – амфибол;
6 – серпентин; 7 – магнетит; 8 – тальк; 9 – кварц; 10 – масканьит
Fig. 2. X-ray diffraction patterns of the Nud II deposit ore ( a ) and a mixture of ore with ammonium sulfate ( б ). Reflexes: 1 – pentlandite; 2 – pyrrhotite; 3 – chalcopyrite; 4 – feldspar; 5 – amphibole;
6 – serpentine; 7 – magnetite; 8 – talc; 9 – quartz; 10 – mascagnite
Электронный снимок образца исходной вкрапленной руды месторождения Нюд II представлен на рис. 3, где отмечены зерна, представляющие собой сростки практически всех минералов, определенных методом рентгенофазового анализа исходного образца руды. Вкрапленники представляют собой сростки сульфидов, содержащих в небольшом количестве примеси магнетита, который развивается по трещинам. Доминирующим минералом вкрапленников является пирротин, внутри которого развивается пентландит, образуя крупные зерна неправильной или округлой формы. Самостоятельные вкрапления пентландита встречаются редко, в противоположность халькопириту, вкрапленность которого обычно мономинеральная. В сульфидных сростках халькопирит встречается редко в виде линзовидных и прожилковых зерен. Размер вкрапленников варьирует от 0,15 до 1,5 мм, но могут встречаться и более мелкие эмульсионные вкрапления в виде каплевидных и мелкоточечных зерен.

Рис. 3. СЭМ-изображение исходного образца руды месторождения Нюд II: Mgt – магнетит; Pyr – пирротин; Sil – силикаты
Fig. 3. SEM-image of the original ore sample from the Nud II deposit: Mgt – magnetite; Pyr – pyrrhotite; Sil – silicates
Для эффективного извлечения металлов из руды с высоким содержанием сростков требуется измельчение до тонких классов, что позволит обеспечить контакт сульфидных минералов с реагентом. Сульфиды вступают в реакцию как с расплавом сульфата аммония, так и c соединениями, образующимися при его разложении в процессе плавления [уравнения (1)–(3)]. В процессе нагрева сульфат аммония постепенно разлагается на смесь газов: SO2, SO3, NH3, N2 и H2O. Стадии термического разложения выглядят следующим образом:
(NH 4 ) 2 SO 4 = NH 4 HSO 4 + NH 3 (1) 2NH 4 HSO 4 = (NH 4 ) 2 S 2 O 7 + H 2 O (2)
3(NH 4 ) 2 S 2 O 7 = 2NH 3 + 2N 2 + 6SO 2 + 9H 2 O (3)
После обжига смеси руды с сульфатом аммония при соотношении 1 : 7 и температуре 300 °С на дифрактограмме фиксируются рефлексы масканьита, что указывает на его неполное разложение при данной температуре (рис. 4, а ). В обожженной смеси также отмечены рефлексы всех исходных сульфидов. После обжига появляются фазы сульфата железа – сабиита (NH 4 )Fe(SO 4 ) 2 , зафиксированы гидроксид-железистые фазы – гетит α-FeO(OH) и аммониоярозит (NH 4 )(Fe) 3 (SO 4 ) 2 (OH) 6 . В остатке после выщелачивания из исходных сульфидов остаются рефлексы пирротина (рис. 4, б ). Остаток характеризуется преобладанием рефлексов талька.
После обжига при температуре 350 ºС в смеси отмечены рефлексы сульфата никеля NiSO 4 (рис. 5, а ). Масканьит при данной температуре полностью расходуется. Из исходных сульфидов были зафиксированы рефлексы пирротина. Остаток после выщелачивания характеризуется значительным количеством рефлексов гетита (рис. 5, б ). Пирротин также остается в остатке.
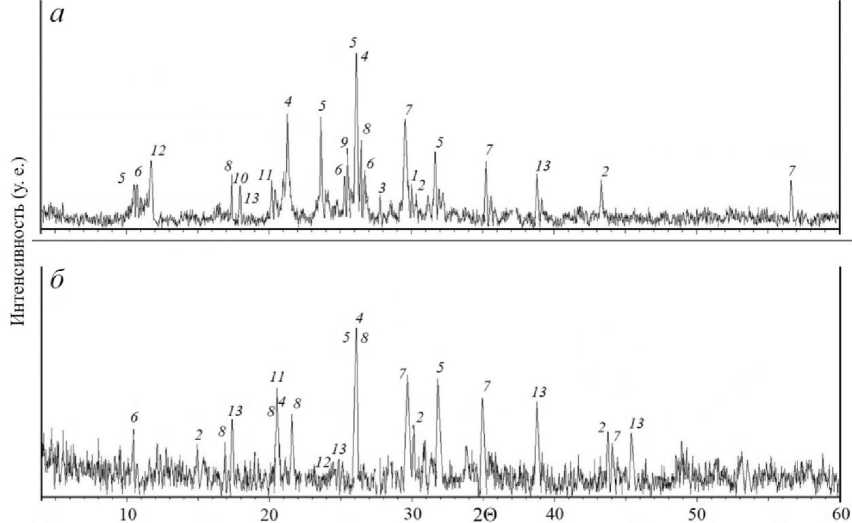
Рис. 4. Дифрактограммы смеси руды и сульфата аммония (1 : 7) после обжига при температуре 300 °С ( а ) и остатка после выщелачивания ( б ). Рефлексы: 1 – пентландит; 2 – пирротин; 3 – халькопирит; 4 – полевой шпат; 5 – амфибол; 6 – серпентин; 7 – магнетит;
8 – тальк; 9 – кварц; 10 – масканьит; 11 – гетит; 12 – сабиит; 13 – аммониоярозит
Fig. 4. X-ray diffraction patterns of ore and ammonium sulfate mixture (1 : 7) after roasting at the temperature of 300 °C ( a ) and of the leaching residue ( б ). Reflexes: 1 – pentlandite; 2 – pyrrhotite;
3 – chalcopyrite; 4 – feldspar; 5 – amphibole; 6 – serpentine; 7 – magnetite; 8 – talc;
9 – quartz; 10 – mascaignite; 11 – goethite; 12 – sabiite; 13 – ammoniojarosite
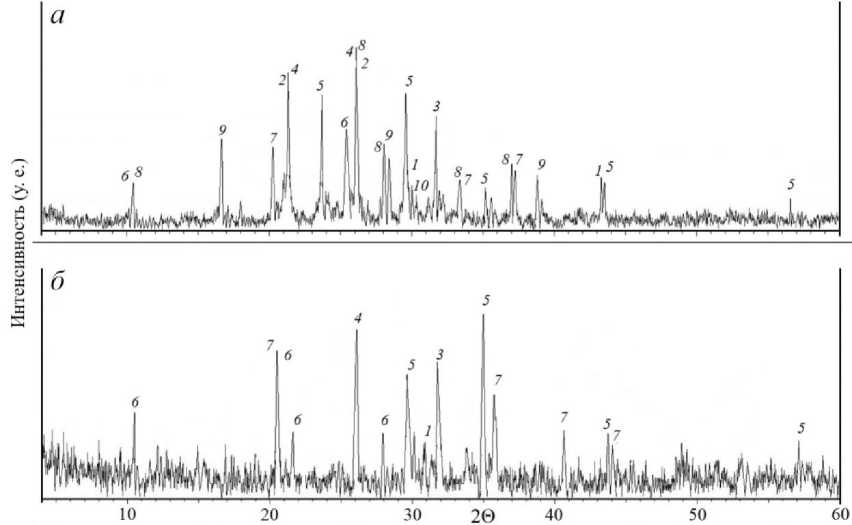
Рис. 5. Дифрактограммы смеси руды и сульфата аммония (1 : 7) после обжига при температуре 350 °С ( а ) и остатка после выщелачивания ( б ). Рефлексы: 1 – пирротин; 2 – полевой шпат; 3 – амфибол;
4 – серпентин; 5 – магнетит; 6 – тальк; 7 – гетит; 8 – сабиит; 9 – аммониоярозит; 10 – сульфат никеля Fig. 5. X-ray diffraction patterns of ore and ammonium sulfate mixture (1 : 7) after roasting at the temperature of 350 °C ( a ) and of the leaching residue ( б ). Reflexes: 1 – pyrrhotite; 2 – feldspar;
3 – amphibole; 4 – serpentine; 5 – magnetite; 6 – talc; 7 – goethite; 8 – sabiite;
9 – ammoniojarosite; 10 – nickel sulfate
После обжига смеси руды с сульфатом аммония при 400 °С в обожженной смеси фиксируются рефлексы сульфатов никеля и меди CuSO4 (рис. 6, а ). Повышение температуры обжига до 400 °С приводит к увеличению интенсивности пиков сульфатных минералов. Остаток после выщелачивания характеризуется наличием силикатных минералов и магнетита, отмечена некоторая часть непрореагировавших сульфидов (рис. 6, б ). Сульфаты, образованные в процессе обжига, полностью растворяются на стадии водного выщелачивания.
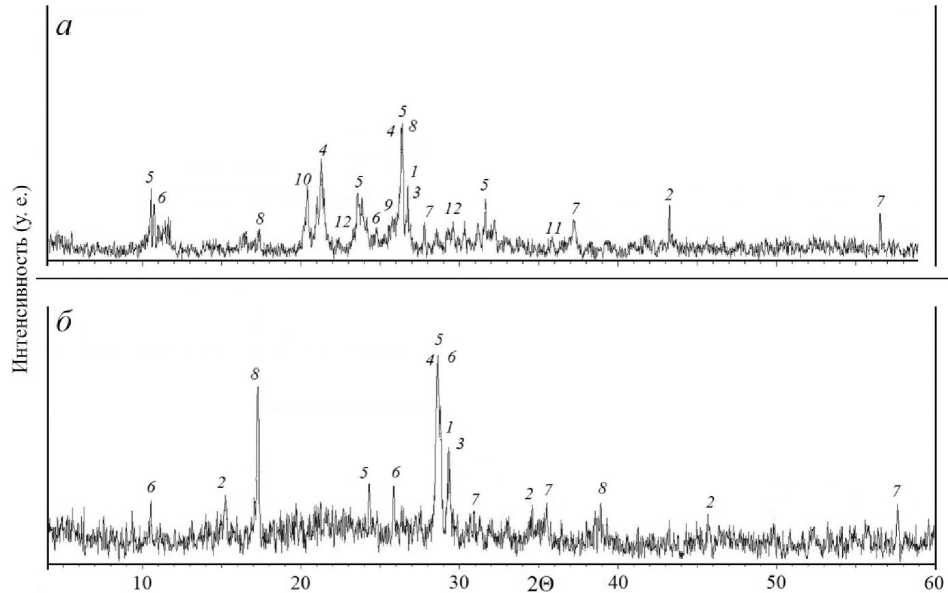
Рис. 6. Дифрактограммы смеси руды и сульфата аммония (1 : 7) после обжига при температуре 400 °С ( а ) и остатка после выщелачивания ( б ). Рефлексы: 1 – пентландит;
2 – пирротин; 3 – халькопирит; 4 – полевой шпат; 5 – амфибол; 6 – серпентин;
7 – магнетит; 8 – тальк; 9 – кварц; 10 – гетит; 11 – халькоцианит; 12 – сульфат никеля Fig. 6. X-ray diffraction patterns of ore and ammonium sulfate mixture (1 : 7) after roasting at the temperature of 400 °C ( a ) and of the leaching residue ( б ). Reflexes: 1 – pentlandite;
2 – pyrrhotite; 3 – chalcopyrite; 4 – feldspar; 5 – amphibole; 6 – serpentine; 7 – magnetite;
8 – talc; 9 – quartz; 10 – goethite; 11 – chalcocyanite; 12 – sulfate nickel
Исследования, направленные на определение механизма взаимодействия сульфидов с сульфатом аммония с применением метода синхронного термического анализа, были выполнены ранее ( Горячев и др., 2022 ). В ходе изучения установлено, что взаимодействие сопровождается образованием аммонийсодержащих сульфатов железа, таких как пиракмонит (NH4)3Fe(SO4)3 и сабиит NH4Fe(SO4)2, а также вторичных обогащенных цветными металлами сульфидов никеля и меди: краунингшилдит (Ni0.9Fe0.10)S, полимидит Ni3S4, борнит Cu5FeS4, фукучилит Cu3FeS8, ковеллин CuS. Конечным продуктом взаимодействия являются сульфаты никеля и меди. Упрощенные схемы реакций можно представить следующими уравнениями:
4Fe7S8 + 54(NH4)2SO4 + 69O2 = 28(NH4)3Fe(SO4)3 + 24NH3 + 14H2O + 2SO2
4CuFeS2 + 22(NH4)2SO4 + 17O2 = 4(NH4)3Fe(SO4)3 + 4CuSO4 + 4NH3 + 2H2O(5)
8(Ni,Fe)9S8 + 112(NH4)2SO4 + 93O2 = 36NiSO4 + 36(NH4)3Fe(SO4)3 + 58NH3 + 29H2O(6)
После обжига при температуре 450 °С не отмечено рефлексов исходных сульфидных минералов. Обожженная смесь характеризуется преобладанием рефлексов серпентина, полевого шпата и амфибола; зафиксировано интенсивное формирование сульфатов цветных металлов (рис. 7, а ). Образованные в процессе обжига сульфаты железа и цветных металлов полностью растворяются, и остаток характеризуется увеличением относительного содержания магнетита (рис. 7, б ).
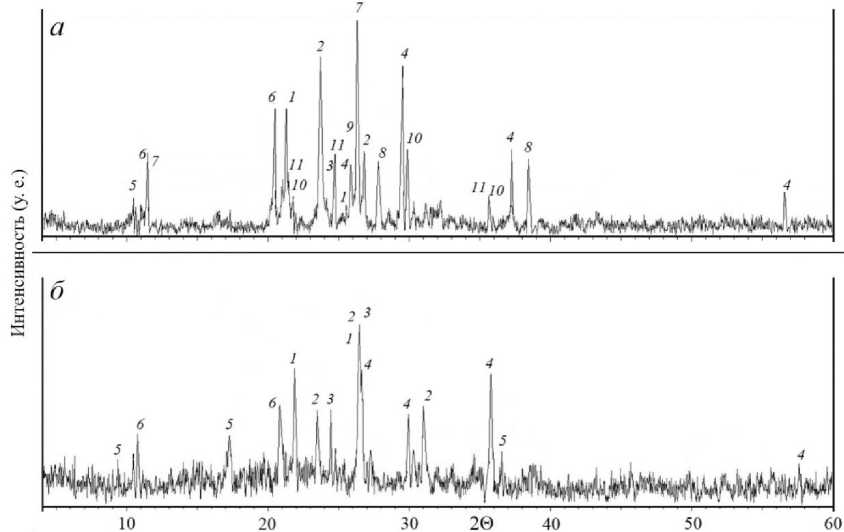
После обжига при температуре 500 °С отмечено более интенсивное формирование сульфата меди – халькоцианита (рис. 8, а ); зафиксированы пики железосодержащих фаз: гетита, сабиита, аммониоярозита и магнетита. В остатке после выщелачивания в значительном количестве остаются инертные минералы (полевой шпат, амфибол, серпентин), увеличивается доля магнетита (рис. 8, б ).
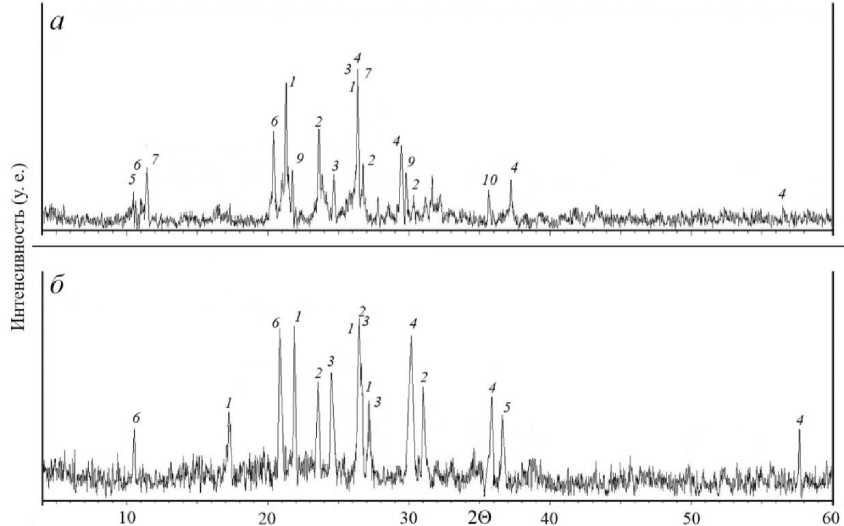
Рис. 7. Дифрактограммы смеси руды и сульфата аммония (1 : 7) после обжига при температуре 450 °С ( а ) и остатка после выщелачивания ( б ). Рефлексы: 1 – полевой шпат; 2 – амфибол; 3 – серпентин;
4 – магнетит; 5 – тальк; 6 – гетит; 7 – сабиит; 8 – аммониоярозит; 9 – сульфат никеля; 10 – халькоцианит Fig. 7. X-ray diffraction patterns of ore and ammonium sulfate mixture (1 : 7) after roasting at the temperature of 450 °C ( a ) and of the leaching residue ( б ). Reflexes: 1 – feldspar;
2 – amphibole; 3 – serpentine; 4 – magnetite; 5 – talc; 6 – goethite; 7 – sabiite;
8 – ammoniojarosite; 9 – nickel sulfate; 10 – chalcocyanite
6 1
Рис. 8. Дифрактограммы смеси руды месторождения Нюд II и сульфата аммония (1 : 7) после обжига при температуре 500 °С ( а ) и остатка после выщелачивания ( б ). Рефлексы: 1 – полевой шпат; 2 – амфибол; 3 – серпентин; 4 – магнетит; 5 – тальк; 6 – гетит; 7 – сабиит;
8 – аммониоярозит; 9 – кварц; 10 – сульфат никеля; 11 – халькоцианит
Fig. 8. X-ray diffraction patterns of ore and ammonium sulfate mixture (1 : 7) after roasting at the temperature of 500 °C ( a ) and of the leaching residue ( б ). Reflexes: 1 – feldspar; 2 – amphibole;
3 – serpentine; 4 – magnetite; 5 – talc; 6 – goethite; 7 – sabiite; 8 – ammoniojarosite;
9 – quartz; 10 – nickel sulfate; 11 – chalcocyanite
Дальнейшее повышение температуры будет приводить к снижению количества реагента, участвующего в реакции, а также к образованию оксидов металлов. Это, вероятно, помимо увеличения энергозатрат, приведет к снижению извлечения при последующем водном выщелачивании.
Морфология частиц исходной руды месторождения Нюд II, смеси руды с сульфатом аммония, обожженной смеси и остатка после выщелачивания показана на рис. 9. Частицы руды после измельчения характеризуются оскольчатой формой (рис. 9, а ), что обеспечивает наилучший контакт с реагентом в процессе смешивания и последующего обжига. На рис. 9, б показаны изображения поверхности минеральных зерен в смеси с сульфатом аммония. Измельчение в шаровой мельнице позволяет раскрыть зерна и сростки минералов и, как следствие, обеспечить их контакт с реагентом. На рис. 9, в представлена поверхность частиц после обжига руды с сульфатом аммония при соотношении 1 : 7. Анализ микроснимков обожженной смеси позволяет говорить о высокой интенсивности взаимодействия частиц руды с сульфатом аммония, так как практически все исходные частицы покрыты сульфатной коркой после обжига. На частицах остатка после выщелачивания сульфатная корка отсутствует. Для поверхности частиц остатка после выщелачивания характерно появление трещиноватости (рис. 9, г ).

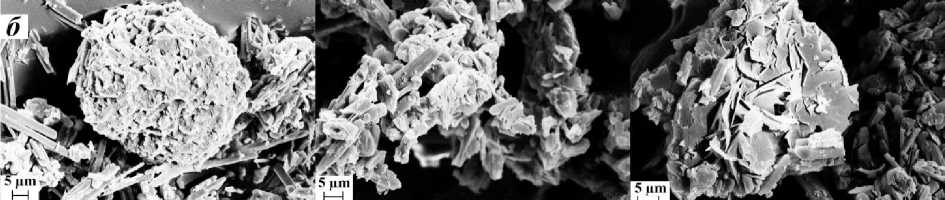


Рис. 9. СЭМ-изображения габитуса частиц руды Нюд II ( а ), смеси руды с сульфатом аммония ( б ), обожженной при 400 °С смеси ( в ), остатка после выщелачивания обожженной смеси ( г )
Fig. 9. SEM images of the particle surface of ( a ) Nud II ore, ( б ) mixture of ore with ammonium sulfate, ( в ) mixture roasted at 400 °C, ( г ) residue after roasted mixture leaching
В процессе обжига смеси руды (частицы крупностью –100 мм) с сульфатом аммония при соотношении 1 : 2 установлено, что с увеличением температуры и продолжительности обжига извлечение металлов при последующем выщелачивании возрастало (рис. 10, а и б). Наименьшее извлечение металлов отмечено при температуре обжига 300 °С и продолжительности 60 мин, никеля извлечено 3,6 %, меди – 3,5 %. Существенное увеличение извлечения никеля отмечено при температуре 400 °С и продолжительности 240 мин – 33,6 %. Максимальный уровень извлечения металлов отмечен при температуре 500 °С, однако отличия от извлечений при температуре 400 °С незначительны.
Учитывая резкий рост извлечений после обжига смеси при 400 °С, целесообразно рассмотреть способы интенсификации перехода металлов в водорастворимую форму при данной температуре и продолжительности 240 мин. Увеличение расхода сульфата аммония привело к более интенсивному извлечению металлов в раствор (рис. 10, в и г). При соотношении 1 : 7 к концу эксперимента извлечено 52,1 % меди и 56,7 % никеля. Для более значительного повышения извлечения металлов смесь перед обжигом измельчали до более тонких классов. Извлечения обоих металлов возрастали по мере увеличения степени измельчения сырья, подаваемого на обжиг. Из класса –40 мкм извлечено 73,5 % никеля и 72,1 % меди. Для повышения извлечения металлов увеличили продолжительность обжига. После обжига при температуре 400 °С в течение 300 мин в раствор удалось извлечь 79,1 % никеля и 75,8 % меди; дальнейшее увеличение времени обжига не приводило к увеличению извлечения металлов при данной крупности частиц и расходе реагента.
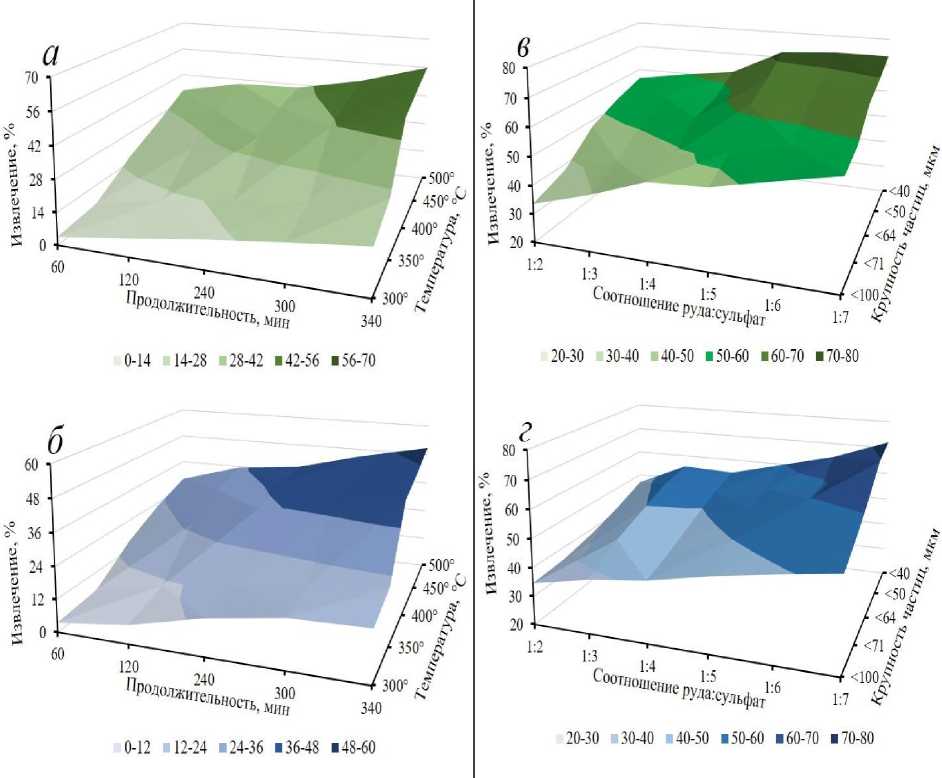
Рис. 10. Извлечение никеля ( а ) и меди ( б ) в раствор при различных продолжительности и температуре обжига; извлечение никеля ( в ) и меди ( г ) при различных расходе сульфата аммония и крупности частиц смеси
Fig. 10. Recovery of nickel ( a ) and copper ( б ) into the solution at different duration and roasting temperature, recovery of nickel ( в ) and copper ( г ) at different consumption of ammonium sulfate and particle size of the mixture
Заключение
Проведенные лабораторные исследования позволили определить оптимальные параметры процесса низкотемпературного обжига руды месторождения Нюд II в смеси с сульфатом аммония: соотношение руды и сульфата аммония равно 1 : 7; крупность частиц обжигаемого сырья составляет –40 мкм; температура обжига 400 °С, время 300 мин. При данных параметрах извлечение цветных металлов в раствор в ходе последующего водного выщелачивания обожженной смеси в подогретой до ≈80 °С дистиллированной воде в течение 40 мин при постоянном перемешивании с интенсивностью 230 мин–1 составляет 79,1 % никеля и 75,8 % меди. Для переработки продуктивных растворов предлагается схема последовательного выделения металлов, при которой на первой стадии методом цементации осаждается медь, на второй стадии производится повышение рН до значения, способствующего выпадению железа в осадок, на третьей стадии дальнейшим повышением значения рН из раствора извлекаются товарные гидроксиды никеля и кобальта.
Извлечения металлов, полученные при переработке руды месторождения Нюд II, ниже по сравнению с извлечениями из чернового медно-никелевого концентрата и руды Аллареченского техногенного месторождения, исследования по которым проводились ранее. Это связано как со значительным преобладанием инертных минералов в исходной руде, что затрудняет контакт сульфата аммония с сульфидными зернами в процессе обжига, так и с низким исходным содержанием цветных металлов. Таким образом, возникает необходимость продолжить исследования процесса низкотемпературного обжига руды месторождения Нюд II, направленные на поиск путей повышения извлечения из нее цветных металлов.
Работа выполнена в рамках тем НИР № 122022400093-9 и 1021051803684-1. Авторы благодарны Е. Д. Зенович и Н. В. Паршиной (Институт минералогии Южно-Уральского федерального научного центра минералогии и геоэкологии УрО РАН, г. Миасс) за выполнение рентгенофазового анализа.


