Пермангант-окисляемый углерод как маркер качества почв агроландшафтов
Автор: Прохоров А.А., Борисов Б.А., Ефимов О.Е.
Журнал: Бюллетень Почвенного института им. В.В. Докучаева @byulleten-esoil
Рубрика: Статьи
Статья в выпуске: 121, 2024 года.
Бесплатный доступ
На примере почв Северо-Предкавказской провинции рассмотрены различные лабораторные методы оценки качества почв. В работе приведен подробный протокол проведения количественного определения фракции Permanganate oxidizable carbon (POXC) при использовании 0.2 н. раствора перманганата калия. Данные представлены для почв черноземного типа Ростовской области, принадлежащих к различным агроэкологическим группам. Были использованы образцы черноземов обыкновенных (Haplic Chernozems) и луговато-черноземных (Gleyic Chernozems) почв агроландшафтов. Для оценки фоновых параметров использовались данные необрабатываемых участков. Оценивались корреляционные зависимости POXC с фракцией бихромат-окисляемого углерода, легкой (
Почвенное органическое вещество, агроэкологические группы почв, активный углерод
Короткий адрес: https://sciup.org/143184043
IDR: 143184043 | УДК: 631.417.1 | DOI: 10.19047/0136-1694-2024-121-47-69
Permangant-oxidizable carbon as a marker of soil quality in agrolandscapes
Different laboratory methods of soil quality assessment are considered by the example of soils of the North-Pre-Caucasian province. The article presents a detailed protocol for quantitative determination of Permanganate oxidizable carbon (POXC) fraction using 0.2 M potassium permanganate solution. The data are presented for chernozem type soils of Rostov region belonging to different agroecological groups. Samples of ordinary chernozems (Haplic Chernozems) and meadow-chernozems (Gleyic Chernozems) soils of agrolandscapes were used. Data from non-tilled plots were used to estimate background parameters. Correlation POXC with fraction of bichromate-oxidizable carbon, light fraction (LF
Текст научной статьи Пермангант-окисляемый углерод как маркер качества почв агроландшафтов
49 Timiryazevskaya Str., Moscow 127434, Russian Federation, *, e-mail: , **e-mail: , ***e-mail:
Почва – один из наиболее значимых резервуаров углерода в биосфере (Lal, 2004). Процессы стабилизации углерода преимущественно реализуются через фиксацию органического вещества в виде органоминеральных комплексов, устойчивых к биологическому разложению (Тулина, Семенов, 2015). С точки зрения устойчивости концептуально выделяют пулы по: химической структуре биополимеров (Холодов, 2011), связи с минеральной частью почвы (Борисов, 2022; John, 2005), способности к микробному разложению (Тулина, Семенов, 2015) и времени пребывания углерода в почве (Артемьева и др., 2021). Среди методов, характеризующих свойства органических веществ в почве, выделяют три основных кластера: химический, физический, биологический. В нашей стране традиционно наиболее широко используется химический анализ. Оксидиметрический метод Тюрина в различных его модификациях, в основе которого лежит использование хромовой смеси в качестве окислителя, остается единственным используемым показателем при проведении агрохимического обследования почв (Прохоров, 2022). Помимо валового определения окисляемого углерода, широко распространены методы оценки фракционно-группового состава (Фоминых и др., 2009). Соотно- шения групп и фракций гумусовых веществ используют для характеристики качественного состава органического вещества и оценки плодородия почв (Заварзина и др., 2021). Следует отметить, что в отечественных работах достаточно мало внимания уделяется рассмотрению процессов окисления углерода при использовании различных окислителей, таких как: перманганат калия, перекись водорода, хлористая кислота и т. д. В работе (Weil, 2003) авторы отмечают высокую информативность количества POXC при использовании в качестве окислителя KMnO4 в концентрации 0.02 н. В дальнейшем в работе (Culman, 2012) было установлено, что фракция перманганат окисляемого углерода наиболее тесно связана с фракцией углерода микробной биомассы. В работе (Fine, 2017) POXC была охарактеризована как лучший предиктор в модели комплексной оценки состояния почв “Soil health”. При этом фракция POXC в рамках предложенного метода (Culman, 2012) выступает как часть наиболее активного почвенного углерода, а сама методика определения, с точки зрения оптимизации лабораторной работы, является интересным методом оценки гумусового состояния почв.
Цель данной работы состояла в изучении свойств почв разных агроэкологических групп, приуроченных к территории Севе-ро-Предкавказской провинции с использованием различных групп лабораторных методов, а также поиск наиболее чувствительных маркеров качества почв.
ОБЪЕКТЫ И МЕТОДЫ
Для апробации методики были использованы образцы черноземов обыкновенных и луговато-черноземных почв агроландшафтов Зерноградского района Ростовской области. Структура почвенного покрова исследуемого района, представлена неконтрастными вариациями черноземов, разной степени смытости, с луговато-черноземными почвами. В рамках данной работы почвы объединяли в агроэкологические группы (Кирюшин, 2005).
Образцы обыкновенных черноземов – (Haplic Chernozems) и луговато-черноземных почв (Gleyic Chernozems) (IUSS, 2014) были отобраны в рамках проведения почвенно-ландшафтного обследования территории Зерноградского района Ростовской области
(п. Путь правды). Агроэкологические группы почв представлены плакорной группой – черноземы обыкновенные предкавказские, слабоэрозионной группой – черноземы обыкновенные предкавказ-ские слабосмытые, слабополугидроморфной группой – луговаточерноземные почвы (Кирюшин, 2005). Помимо почв агроландшафтов анализы были проведены с пробами, отобранными на смежной территории, не входящей в состав пашни. Точки отбора проб представлены на рисунке 1. Отбор образцов производился из почвенных разрезов – средний образец для слоя горизонта А пах , средний образец для горизонта АВ. Общее количество рассмотренных почвенных разрезов – 33 шт.
Образцы высушивали в течение двух недель на воздухе, после чего хранили при комнатной температуре в темном месте.
В пробах почв определяли: содержание бихромат-окисляемой фракции путем мокрого озоления пробы в присутствии K 2 Cr 2 O 7 : H 2 SO 4 (1 : 1) в соответствии с методом Тюрина, выход легкой фракции LF < 1.6 г/см3 (Прохоров, 2023), содержание водоэкстрагируемого углерода (HWC) в соответствии с методом экстракции, предложенным в работе (Ghani, 2007) и последующим определением фотометрическим способом концентрации мг углерода в аликвоте вытяжки – 25 мл после выпаривания, при использовании 0.4 н. раствора хромовой смеси в качестве окислителя. Плотность почвы определяли методом режущего кольца, содержание общего азота (TN) на автоматическом анализаторе.
На основании известного протокола (Weil, 2003) анализа для определения фракции “активного углерода” или Permanganat ox-idyzale carbon (POXC) Испытательным центром почвенноэкологических исследований РГАУ–МСХА имени К.А. Тимирязева был апробирован протокол, приведенный ниже.
Оптическую плотность измеряли на фотоэлектрокалориметре СФ-2000 при длине волны 550 нм в кварцевой кювете с длиной оптического пути 1 см. При реализации схемы анализа возникали не прописанные в используемом протоколе проблемы, в том числе связанные с необходимостью корректировки рН раствора. Поэтому считаем полезным привести подробный протокол проведения анализа, принятый в нашей лаборатории, с рядом комментариев.
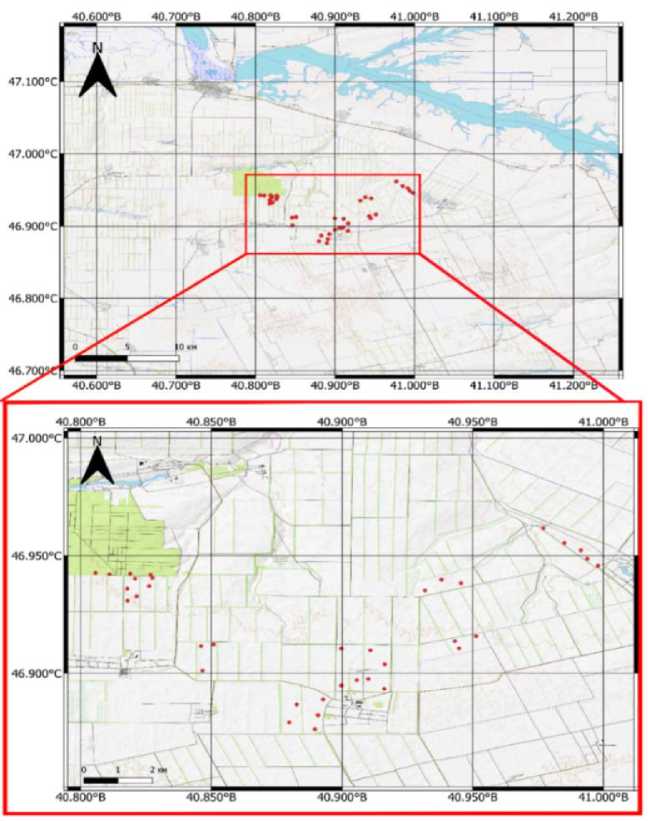
Рис. 1. Точки пробоотбора.
Fig. 1. Sampling points.
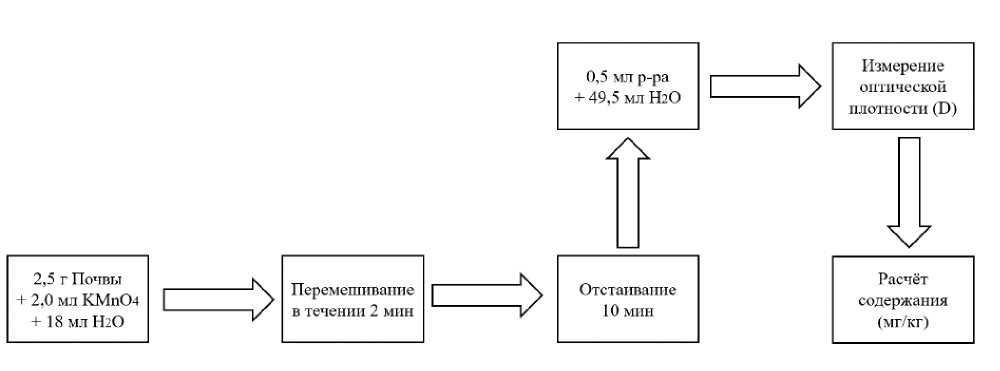
Рис. 2. Схема проведения анализа.
Fig. 2. Scheme of analysis.
Протокол оценки оксидиметрических фракций в Испытательном центре почвенно-экологических исследований РГАУ-МСХА им. К.А. Тимирязева.
Суть метода заключается в использовании MnO 4 - как мощного окислителя в нейтральной, слабокислой и слабощелочной среде за счет большой разницы потенциалов между ионами Mn2+ и MnO 4 -. Реагируя с почвенным органическим веществом (наиболее активной его частью), раствор, содержащий KMnO 4 , постепенно обесцвечивается: темно-фиолетовая окраска переходит в слаборозовую, а затем раствор становится практически бесцветным.
Приготовление раствора окислителя производят согласно методике, предложенной в работе (Culman, 2012), 147 г хлористого кальция необходимо полностью растворить в 800 мл дистиллированной воды при использовании ультразвука, либо при слабом нагревании и использовании магнитной мешалки. По истечении 10–15 минут проверить раствор на наличие кристаллов нераство-ренного KMnO 4 , при необходимости декантировать. Далее, в соответствии с методикой, pH раствора довести до величины 7.2 ед. с помощью 0.1 н растворов NaOH и HCl. После этого объем окислителя довести до 1 л, перенести в емкость из темного стекла и хранить в темном месте.
Градуировочный график строят по четырем калибровочным растворам при следующих концентрациях KMnO 4 : 0.005; 0.01; 0.015; и 0.02 н. Объем исходного 0.2 н раствора, необходимый для приготовления калибровочных растворов, указан в таблице 1.
Таблица 1. Приготовление калибровочных растворов
Table 1. Preparation of calibration solutions
|
Концентрация |
Объем 0.2 н KMnO 4 , мл |
Объем H 2 O, мл |
|
0.005 М |
0.25 |
9.75 |
|
0.01 М |
0.5 |
9.5 |
|
0.015М |
0.75 |
9.25 |
|
0.02 М |
1.0 |
9.0 |
Калибровочные растворы разбавляют аналогично исследуемым образцам: 0.5 мл раствора вносят в пробирки или колбы и добавляют 49.5 мл бидистиллированной воды.
Для повышения качества определения и исключения аналитических ошибок, связанных с приготовлением стандартных растворов, для лаборатории следует подготовить один–два стандартных образца почвы, которые будут храниться для проверки воспроизводимости результатов и оценки годности раствора окислителя.
Для анализа исследуемых образцов в центрифужные пробирки объемом 50 мл необходимо взять навеску 2.50 г воздушносухой почвы, добавить 18 мл дистиллированной воды, затем 2.0 мл исходного 0.2 н. раствора KMnO 4. Далее, плотно закрыв крышку, в течение 2 мин. интенсивно перемешивать полученную суспензию вручную или на ротаторе. По истечении 2 мин. пробирки необходимо встряхнуть для исключения оседания почвы на крышке и в верхней части и поставить на 10 мин. в темное место для отстаивания. В рамках данного метода время экспозиции является одним из важнейших факторов, определяющих качество аналитических данных, поэтому следует его четко выдерживать, ограничивая количество образцов в одной партии до 7 шт., так как реакция окисления будет протекать в течение всего времени контакта почвы с KMnO 4 . По истечении 10 мин. отобрать 0.5 мл надосадочного раствора в колбу на 50 мл и добавить 49.5 мл дистиллированной воды. Затем измерить оптическую плотность (D) полученных растворов при длине волны 550 нм.
Количество окисленного углерода соответствует количеству восстановленного перманганата и, следовательно, чем меньше интенсивность окраски раствора, тем большее количество фракции POXC содержится в пробе.
Для расчета содержания фракции РОХС необходимо использовать уравнение (1) (Weil, 2003):
POXC (мг/кг) = [0.02 – (a + b*D)] *(9 000)*(0.02L/Wt), (1)
где: 0.02 – концентрация р-ра перманганата калия, контактирующего с пробой почвы, моль/л;
a – пересечение градуировочной кривой с осью ординат;
b – наклон (угловой коэффициент) градуировочной кривой;
D – оптическая плотность при 550 нм;
9 000 – количество миллиграммов углерода, окисляемого 1 моль КMnO 4 при переходе Mn+7 в Mn+4;
0.02L – объем раствора перманганата, контактировавшего с почвой;
Wt – навеска почвы в кг.
Нами при проведении анализа на 5-ый день после приготовления исходного раствора было установлено, что его рН снизился до 6.89 ед. При определении содержания POXC в образцах, которые были проанализированы ранее (в первый день после приготовления раствора), существенных отличий при измерениях зафиксировано не было. рН исходного раствора окислителя продолжал снижаться в течение 20 дней, после чего на уровне 6.62 ед. стабилизировался. При повторном измерении содержания POXC, в образцах, анализ которых был произведен в первый день после приготовления раствора, установлено, что уровень рН не оказывал существенного влияния на итоговые числовые значений POXC. Каждое измерение произведено в трехкратной повторности для каждого уровня рН для исключения и минимизации случайных ошибок. Для значений POXC, полученных при каждом уровне рН исходного раствора, построены доверительные интервалы при уровне p = 0.05. Расчет доверительных интервалов производили в соответствии с формулой:
(ДИ) = X ± Z (S ÷ √n), (2)
где: X – среднее значение POXC для выборки; Z – значение коэффициента Стьюдента (1.96);
S – величина среднеквадратического отклонения; n – число наблюдений.
В таблице 2 представлены результаты измерения содержания POXC при различном значении рН исходного раствора окислителя, показатели СКО, а также рассчитанные доверительные интервалы для измеренных значений POXC:
Только для 2 значений из 45 показатель POXC выходит за рамки рассчитанного доверительного интервала (выделены в таб- лице). В соответствии с этим корректировка рН раствора до величины 7.2 ед. рН, согласно протоколу (Weil, 2003), с высокой долей вероятности не оказывает существенного влияния на результаты измерений.
Таблица 2. Содержание POCX в зависимости от рН исходного раствора
Table 2. POCX content as a function of pH of the initial solution
|
№ пробы |
POXC средн. рН р-ра 7.20 ед. |
POXC средн. рН р-ра 6.90 ед. |
POXC средн. рН р-ра 6.68 ед. |
Показатель СКО |
Доверительный интервал при p = 0.05 |
|
1 |
848 |
835 |
868 |
27 |
831–868 |
|
2 |
716 |
701 |
731 |
27 |
698–734 |
|
3 |
848 |
859 |
842 |
16 |
839–860 |
|
4 |
423 |
396 |
409 |
21 |
396–423 |
|
5 |
783 |
765 |
749 |
29 |
747–785 |
|
6 |
408 |
365 |
389 |
30 |
367–407 |
|
7 |
753 |
720 |
742 |
29 |
719–757 |
|
8 |
681 |
692 |
671 |
31 |
661–702 |
|
9 |
433 |
400 |
412 |
25 |
399–431 |
|
10 |
753 |
735 |
746 |
16 |
734–755 |
|
11 |
459 |
482 |
472 |
29 |
457–495 |
|
12 |
349 |
342 |
347 |
24 |
330–362 |
|
13 |
402 |
421 |
392 |
32 |
384–426 |
|
14 |
450 |
465 |
447 |
29 |
435–473 |
|
15 |
798 |
779 |
756 |
25 |
761–794 |
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Оксидиметрические фракции. С использованием методов перманганатного и бихроматного окисления оценивались пулы ок-сидиметрических фракций почвенного органического вещества (ПОВ). К фракции POXC в данном случае следует отнести наиболее “активную” часть ПОВ, легкоокисляемую и потенциальноминерализуемую (Culman, 2012). Бихромат-окисляемая фракция показывает долю почвенного органического углерода входящую в состав как активных, так и медленных и стабильных пулов (Тулина, Семенов, 2015). Результаты определений представлены в виде коробчатых диаграмм на рисунке 3. Содержание фракции POXC на исследуемых участках варьировало в диапазоне 126–1 006 мг/кг, при этом максимальные значения содержания углерода данной фракции, в среднем 925 мг/кг, отмечались в пробах гумусовых горизонтов необрабатываемых черноземов. Минимальным же содержанием углерода фракции POXC характеризовались пробы горизонтов АВ (в среднем глубина отбора от 35 см и ниже) почв пахотных плакорных и пахотных слабо и среднеэрозионных агроэкологических групп (Кирюшин, 2005), в среднем 218 и 137 мг/кг соответственно. Стоит отметить, что для агроландшафтов максимальное содержание углерода фракции POXC детектировалось на слабогидроморфных участках в пахотных горизонтах лу-говато-черноземных почв – в среднем 724 мг/кг. Оценивая пла-корную и слабоэрозионную агроэкологические группы стоит отметить, что содержание фракции POXC в пахотном горизонте черноземов обыкновенных, подверженных процессам водной эрозии, было выше фактически на 14–20% по всем наблюдаемым значениям. Напротив, содержание фракции бихромат-окисляемого углерода было в среднем на 17% ниже на участках, почвенный покров которых был представлен слабо- и среднесмытыми аналогами обыкновенных черноземов. Среднее содержание фракции для горизонтов А и Апах снижалось в ряду: чернозем обыкновенный – естественный луг (в среднем 3.2%), луговато-черноземная – пашня (в среднем 2.6%), чернозем обыкновенный пашня (в среднем 2.6%), чернозем обыкновенный смытый – пашня (в среднем 2.2%). Для горизонтов АВ и АВСа было характерно идентичное распределение с учетом меньшего количественного содержания углерода данной фракции. Содержание углерода POXC и бихро-мат-окисляемой фракции представлено на рисунке 3 в виде коробчатых диаграмм.
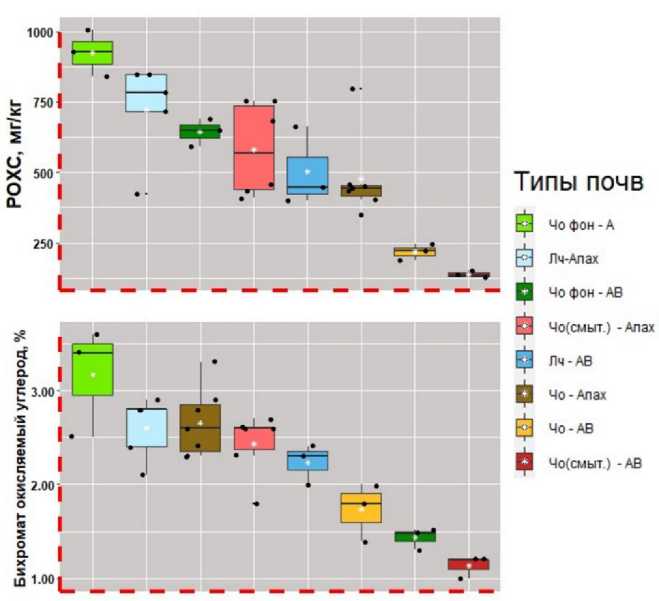
Рис. 3. Содержание фракции POXC и бихромат-окисляемой фракции, определяемой методом Тюрина в разных типах почв.
Fig. 3. Content of POXC fraction and bichromate-oxidizable fraction determined by the Tyurin method in different soil types.
Гранулоденситометрические и водоэкстрагируемые фракции. В результате проведения гранулоденситометрического фракционирования были выделены фракции LF < 1.6 г/см3, при этом участки, входящие в состав пашни, и необрабатываемые участки существенно различались по массовому содержанию данной фракции. На рисунке 4 представлен ранжированный ряд коробчатых диаграмм. Анализируя полученные данные, следует отметить, что по массовому отношению данной фракции к объему почв следует выделить три кластера:
-
1. черноземы под естественной степной растительностью;
-
2. черноземы плакорной и луговато-черноземные слабополу-гидроморфной агроэкологических групп;
-
3. Черноземы эрозионной агроэкологической группы.
При этом идентичная тенденция характерна как для горизонтов А и А пах , так и для горизонтов АВ и АВ Са .
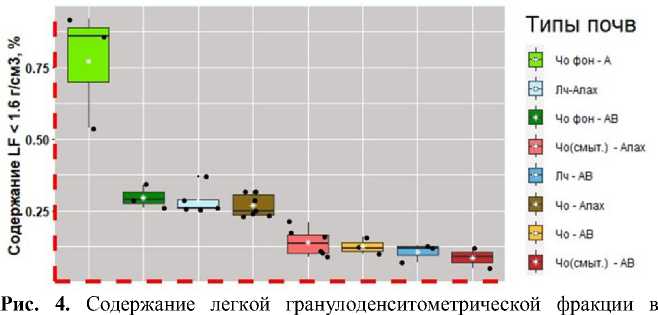
разных типах почв.
Fig. 4. Content of light fraction in different soil types.
При оценке фракции водоэкстрагируемого углерода (HWC) все почвы, функционирующие в условиях агроландшафтов, попадали в единый кластер по количественному содержанию, существенно отличаясь лишь от группы черноземов обыкновенных под естественной степной растительностью. При проведении анализа в трехкратной повторности содержание углерода данной фракции так же характеризовалось высоким коэффициентом вариации даже в рамках одного и того же образца (выше 30%). С нашей точки зрения, пул растворимого органического углерода, определяемый при термической экстракции дистиллированной водой при t = 90 °С (Ghani, 2007), возможно с высокой точностью детектировать только при наличии в лаборатории анализатора общего углерода с возможность определения C-total в жидкой фазе, а метод определения, используемый в данной работе, по окислению выпаренной аликвоты водной вытяжки не является точным.
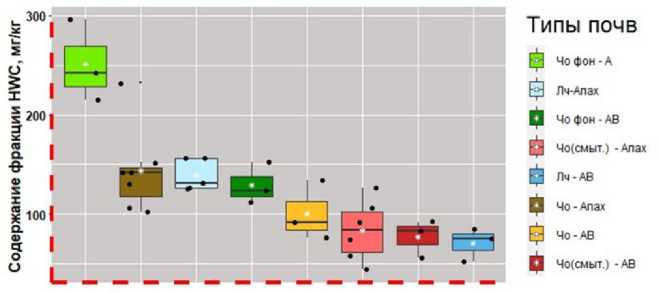
Рис. 5. Содержание фракции HWC в разных типах почв.
Fig. 5. HWC fraction content in different type soils.
Оценка линейных зависимостей между различными фракциями показала, что фракция POXC имеет существенные взаимосвязи с такими показателями, как: содержание фракции LF < 1.6 г/см3, содержание бихромат-окисляемой фракции, содержанием общего азота и плотностью почвы при n = 33 и величинами r2 = 0.45; 0.47; 0.42 и 0.50 и уровне значимости p = 0.05 соответственно. В свою очередь бихромат-окисляемый углерод в линейной модели сильнее связан с показателем плотности почвы при n = 33, величина r2 составила 0.88, что согласуется с работами ряда авторов (Fine, 2017; Kuzyakov, 2020). Также следует отметить, что фракция POXC, в отличие от бихроматной фракции, характеризуется большей изменчивостью между агроэкологическими группами при среднем содержании: на слабогидроморфной группе –
724 мг/кг, слабоэрозионной – 580 мг/кг, плакорной – 476 мг/кг, для пахотного горизонта, и 925 мг/кг – для плакорной группы горизонта А участка, не входящего в состав пашни. Содержание POXC является более чувствительным к изменению экзогенных факторов, таких как гидроморфизм, проявление процессов эрозии, тип землепользования. Идентичная тенденция накопления на необрабатываемых участках характерна и для гранулоденситомет-рической фракции LF < 1.6 г/см3. При этом фракцию LF < 1.6 г/см3 в ряде работ было предложено использовать как маркер качества почв в агроландшафтах для оценки степени выпаханности (Борисов, 2022; Шпедт, 2015).
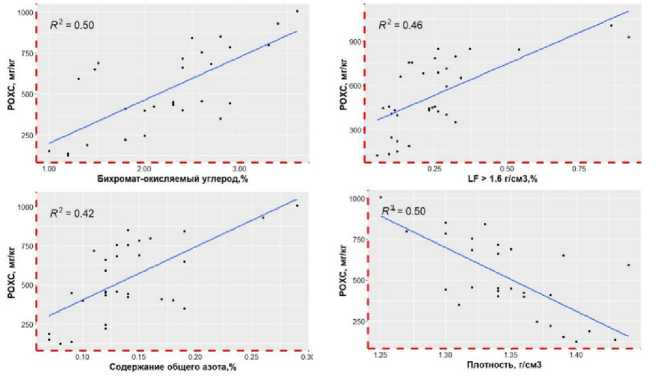
Рис. 6. Линейные зависимости между POXC и другими маркерами качества почв агроландшафтов.
Fig. 6. Linear relationships between POXC and other agrolandscape soil quality markers.
Данные, представленные на рисунке 6, согласуются с выводами ряда авторов, среди которых стоит отметить работу (Culman, 2012), в которой при обработке агрегированных данных нескольких групп исследований установлено, что фракция POXC значимо связана со многими пулами ПОВ, а также является индикатором качества при оценке различных систем обработки почвы и систем минерального питания. В работе (Fine, 2017) при проведении многомерного анализа и построения оценочных функций, также было отмечено, что фракция POXC является одним из лучших предикторов в модели оценки свойств почв “Comprehensive Assessment of Soil Health” (CASH).
ЗАКЛЮЧЕНИЕ
В результате исследования было установлено, что POXC чувствителен к сокращению фракции бихромат-окисляемого углерода, определяемого методом Тюрина, а также к содержанию легкой фракции (LF < 1.6 г/см3). В условиях Северо-Предкавказской провинции на почвах черноземного типа данная фракция также может являться маркером агроэкологических условий. На почвах плакорной, слабоэрозионной и слабогидроморфной групп были отмечены закономерные тенденции к повышению или снижению содержания POXC в горизонтах А пах и АВ, выраженные в большей степени, чем различия по содержанию бихроматного углерода. Фракция чувствительна к типу землепользования: содержание POXC на землях, вовлеченных в пашню, в среднем на 20–50% ниже, чем на участках, не входящих в состав агроландшафтов. Содержание POXC было связано с долей легкой фракции. В линейной модели при n = 33 величина r2 соответствовала 0.46. Исходя из этого, можно утверждать, что использование такого простого в исполнении и относительно недорогого метода, как определение POXC, в качестве альтернативы выделения фракции LF < 1.6 г/см3 при проведении агрохимической оценки состояния почв может позволить уточнить оценки и снизить трудоемкость выполнения работ.
Также в рамках данной работы было установлено, что выделение одоэкстрагируемого углерода (HWC) с последующим его определением по методике, предложенной в работе (Ghani, 2007), невозможно производить с фотометрическим окончанием при окислении выпаренной аликвоты водной вытяжки, т. к. воспроизводимость в таком подходе достаточно низкая.
При проведении анализа и определения POXC в соответ- ствии с протоколом (Weil, 2003) было установлено, что показатель рН исходного раствора снижался в период первых 14 дней после его приготовления. Было установлено, что при проведении измерений с использованием раствора с рН в диапазоне 6.6–7.2 существенных изменений концентрации POXC не происходит.
Список литературы Пермангант-окисляемый углерод как маркер качества почв агроландшафтов
- Артемьева З.С., Данченко Н.Н., Зазовская Э.П. и др. Изотопный состав углерода и химическая структура органического вещества типичного чернозема в условиях контрастного землепользования // Почвоведение. 2021. № 6. С. 686-700. https://doi.org/10.31857/S0032180X21060034.
- Борисов Б.А., Ефимов О.Е., Наумов В.Д., Прохоров А.А. Органическое вещество и агрегатное состояние чернозема выщелоченного и его полугидроморфного аналога // АгроЭкоИнфо: Электронный научнопроизводственный журнал. 2022. № 2. URL: http://agroecoinfo.ru/STATYI/2022/2/st_236.pdf. https://doi.org/10.51419/202122236.
- Заварзина А.Г., Данченко Н.Н., Демин В.В., Артемьева З.С., Когут Б.М. Гуминовые вещества - гипотезы и реальность (обзор) // Почвоведение. 2021. № 12. С. 1449-1480. https://doi.org/10.31857/S0032180X21120169.
- Классификация и диагностика почв СССР. М.: Колос, 1977. С. 86-98.
- Кирюшин В.И., Иванов А.Л. и др. Агроэкологическая оценка земель, проектирование адаптивно-ландшафтных систем земледелия и агротехнологий / Методическое руководство МСХ РФ, РАСХН. М.: ФГНУ “Росинформагротех”, 2005. 784 с.
- Лебедева Т.Н., Соколов Д.А., Семенов М.В., Зинякова Н.Б., Удальцов С.Н., Семенов В.М. Распределение органического углерода между структурными и процессными пулами в серой лесной почве разного землепользования // Бюллетень Почвенного института имени В.В. Докучаева. 2024. Вып. 118. С. 79-127. https://doi.org/10.19047/0136-1694-2024-118-79-127.
- Прохоров А.А. Характеристика методов выделения фракций почвенного органического вещества и их использование для оценки гумусового состояния почв // АгроЭкоИнфо: Электронный научно-производственный журнал. 2022. № 6. URL: http://agroecoinfo.ru/STATYI/2022/6/st_604.pdf. https://doi.org/10.51419/202126604.
- Прохоров А.А., Борисов Б.А., Ефимов О.Е. Индексная оценки степени выпаханности черноземов предкавказской провинции // Агрохимический вестник. 2023. № 5. С. 50-55. https://doi.org/10.24412/1029-2551-2023-5-009.
- Смагин А.В. Структурно-функциональная организация почв как динамических биокосных систем: Автореф. дис. … д. б. н. 03.02.13. М., 2004. 44 с.
- Тулина А.С., Семенов В.М. Оценка чувствительности минерализуемого пула почвенного органического вещества к изменению температуры и влажности // Почвоведение. 2015. № 8. С. 952-962. https://doi.org/10.7868/S0032180X15080109.
- Фоминых Л.А., Золотарева Б.Н., Холодов А.Л., Ширшова Л.Т. Фракционно-групповой состав гумуса почв тундровой зоны Евразии // Криосфера Земли. 2009. Т. 13. № 2. С. 44-54.
- Холодов В.А., Константинов А.И., Кудрявцев А.В., Перминова И.В. Строение гуминовых кислот почв зонального ряда по данным спектроскопии ЯМР 13 // Почвоведение. 2011. № 9. С. 1064-1073.
- Холодов В.А., Фарходов Ю.Р., Ярославцева Н.В., Данченко Н.Н., Ильин Б.С. Лазарев В.И. Водоэкстрагируемый и микробный углерод черноземов разного вида использования // Бюллетень Почвенного института имени В.В. Докучаева. 2022. 112. С. 122-133. https://doi.org/10.19047/0136-1694-2022-112-122-133.
- Шпедт А.А., Вергейчик П.В., Картавых В.В. Оценка легкоразлагаемого органического вещества почв сельскохозяйственных угодий Красноярского края // Агрохимия. 2015. № 12. С. 36-43.
- Borisov B.A., Efimov O.E., Eliseeva O.V. et al. Organic matter of sodpodzolic soil after transition to a fallow state // IOP Conference Series: Earth and Environmental Science. 2021. P. 022022. https://doi.org/10.1088/1755-1315/1010/1/012108.
- Culman S., Freeman M., Snapp S. Procedure for determination of permanganate oxidizable carbon. Kellogg Biological Station, Michigan State University, Hickory Corners, 2012. MI 49060. URL: http://lter.kbs.msu.edu/protocols/133.
- Culman S. et al. Permanganate Oxidizable Carbon Reflects a Processed Soil Fraction that is Sensitive to Management // Soil Science Society of America Journal. 2012. Vol. 76. P. 494-504. https://doi.org/10.2136/sssaj2011.0286.
- den Boef G., Polak H.L. Oxidimetric determination of organic compounds by means of strong oxidising agents // Talanta. 1962. Vol. 9. Iss. 3. P. 271- 284. https://doi.org/10.1016/0039-9140(62)80061-7.
- Fine A.K., van Es H., Schindelbeck R. Statistics, Scoring Functions, and Regional Analysis of a Comprehensive Soil Health Database // Soil Science Society of America Journal. 2017. Vol. 81. https://doi.org/10.2136/sssaj2016.09.0286.
- Ghani A., Dexter M., Perrott K.W. Hot-water extractable carbon in soils: a sensitive measurement for determining impacts of fertilisation, grazing and cultivation // Soil Biology & Biochemistry. 2003. Vol. 35. P. 1231-1243. https://doi.org/10.1016/S0038-0717(03)00186-X.
- Hartemink A.E., Gerzabek M.H., Lal R., Mc. Sweeney K. “Soil Carbon Research Priorities”. New York, Dordrecht London: Springer Cham Heidelberg, 2014. https://doi.org/10.1007/978-3-319-04084-4_48.
- IUSS Working Group WRB. World Reference Base for Soil Resources 2014, update 2015. International soil classification system for naming soils and creating legends for soil maps. World Soil Resources Reports No. 106. FAO, Rome.
- John B., Yamashita T., Ludwig B., Flessa, H. Storage of organic carbon in aggregate and density fractions of silty soils under different types of land use // Geoderma. 2005. Vol. 128. P. 63-79. https://doi.org/10.1016/j.geoderma.2004.12.013.
- Kuzyakov Y., Gunina A., Zamanian K., Tian J., Luo Y., Xu X., Yudina A., Aponte H., Alharbi H., Ovsepyan L., Kurganova L., Ge T., Guillaume T. New approaches for evaluation of soil health, sensitivity and resistance to degradation // Frontiers of Agricultural Science and Engineering. 2020. Vol. 7(3). P. 282-288. https://doi.org/10.15302/J-FASE-2020338.
- Lal R. Soil Carbon Sequestration Impacts on Global Climate Change and Food Security // Science. 2004. Vol. 304. P. 1623-7. https://doi.org/10.1126/science.1097396.
- Weil R., Kandikar R., Melissa A., Gruver J.B., Susan E. Estimating active carbon for soil quality assessment: A simplified method for laboratory and field use // American Journal of Alternative Agriculture. 2003. Vol. 18. P. 3- 17. https://doi.org/10.1079/AJAA200228.


