Пероксидаза печеночницы благородной ( Hepatica nobilis)
Автор: Лапина Галина Петровна, Гаевская Виктория Викторовна, Лихуша Павел Сергеевич
Журнал: Вестник Тверского государственного университета. Серия: Биология и экология @bio-tversu
Рубрика: Биохимия
Статья в выпуске: 2, 2015 года.
Бесплатный доступ
Проведено выделение и очистка пероксидазы из биотканей печеночницы, подтверждена гомогенность выделенного биокатализатора. Рассчитано содержание фермента (5,32 мг/мл г/г сырой ткани). Исследованы важнейшие ферментативные параметры биокатализатора в рамках разработанного многоэтапного научно-методического подхода по изучению каталитических свойств пероксидазы в модельных системах в присутствии регуляторов каталитической активности: определены значения важнейших ферментативных параметров каталитической активности пероксидазы из биотканей печеночницы благородной: K M = 2.23·10 -3 М, V max = 9,52·10 -3. Полученные характеристики согласуются с данными литературы, что указывает на достоверность полученных параметров.
Пероксидаза, печеночница благородная, кинетические параметры, зависимости d-τ, спрямление в координатах лайнуивера-берка, константа михаэлиса (k m), максимальная скорость (v max)
Короткий адрес: https://sciup.org/146116579
IDR: 146116579 | УДК: 541.647.577.1
Peroxidase of the common hepatica ( Hepatica nobilis)
An extracition and purification of the peroxicdase from the tissuies of the common hepatica have been carried out. The homogeneity of the extracted catalizator has been proved. The enzyme content was calculated (5,32 mg/ml g/g of the raw tissue). The most important enzymatic parameters of the biocatalizator have been investigated on the course of the multispep methodic and scientific approach for the studying of the catalytic properties of the peroxidase in model systems under the presence of the regulators of the catalytic activity. Values of the most important enzymatic parameters of the catalytic activity of the hepatica peroxidase have been determined: K M = 2.23·10 -3 М, V max = 9,52·10 -3. The results are plausible and correspond to the data from the literature sources.
Текст научной статьи Пероксидаза печеночницы благородной ( Hepatica nobilis)
Введение. Пероксидазы - ферменты класса оксидоредуктаз, катализирующие окисление с помощью Н2О2 в присутствии бензидина. Наиболее изучена пероксидаза из корней хрена, молекула которой состоит из одной полипептидной цепи (308 аминокислотных остатков), связанной ковалентно с 8-ю олигосахаридными цепями. Пероксидазы существует в виде нескольких форм (изоферментов), состав и соотношение между которыми зависит от состояния и вида растения (Андреева, 1988).
Пероксидаза - гликопротеид, для которого носителем соответствующей изменчивости могут быть и углеводные компоненты. Такой компонент, даже небольшой по массе, может сообщать молекуле качественно новое состояние и регулировать отношение фермента к различным изменениям среды (pH, температуре, посторонние примеси и др.). Показано и доказано, что углеводная часть придает белку гораздо большую специфичность. Это своего рода векторные группы протеидов, которые «узнают» участки других структур, иные макромолекулы и поверхность клеток (Строев, 1986). В связи с этим представляют интерес данные Несселя и Мэдера (Nessel, Mader, 1977) о том, что кислые пероксидазы, как биохимические соединения, занимают особые положения, а содержание углеводов у них достигает примерно 20%.
Реакции, катализируемые пероксидазой, характеризуются переносом водорода от молекулы субстрата к перекисям, в результате чего возникают радикалы субстратов, являющиеся сильнореакционными соединениями. Большинство субстратов этого фермента - соединения фенольной природы (бензидин). Окисляясь до хинонов, они обладают сильным окислительно-восстановительным действием. Фенолы могут также ковалентно связываться с молекулой пероксидазы, изменяя ее каталитическое действие (Srivastava, Huystee, 1977). Особенности строения молекулы и возможности ее изменения играют немаловажную роль при активации индивидуальных изопероксидаз.
Пероксидаза - двухкомпонентный фермент, представляющий собой сочетание активной группы в активном центре, вступающей в химическое взаимодействие с субстратами, и белкового «носителя», усиливающего каталитическое действие этой группы. Это глобулярный белок диаметром 50 A (Clementi, Palade, 1969), который содержит около 43% а-спиральных участков в составе белковой части молекулы (Strickland, 1968). По номенклатуре ферментов, принятой на Международном биохимическом съезде в 1979 году, пероксидаза -фермент, действующий на перекись водорода в качестве акцептора. Единственный подподкласс (1.11.1) составляют пероксидазы, где под кодовым номером семь стоит истинная пероксидаза-донор: Нг СЬ -оксидоредуктаза (КФ 1.11.1.7), что относится к растительным и животным пероксидазам.
Методика. В экспериментальной программе по исследованию пероксидазы печеночницы благородной (Hepatica nobilis} был применён многоступенчатый подход, а именно:
-
1) выделение пероксидазы из тканей растения;
-
2) очистка полученного экстракта;
-
3) определение содержания активного фермента;
-
4) расчёт ферментативных параметров;
-
5) анализ и обсуждение полученных параметров.
Поиск оптимальных условий для проведения каталитической реакции требовал исследования модельной ферментативной системы: пероксидаза печеночницы, бензидин (5-10"3 М), при варьировании концентраций Н2О2 (2-8)-(10"4М) с шагом в единицу, t=25°C, pH 5,3.
Первый этап. Выделение фермента пероксидаза печеночницы благородной (Hepatica nobilis} из биотканей (листья и стебли растений). 4 г ткани растений печеночницы гомогенизировали в 10 мл 0,1 М фосфатного буфера (1 = 0,35 М), содержащего 1,5-10 М бензойной кислоты и 1-10 М аскорбиновой кислоты (pH 5,3). Гомогенат отжимали, оставляли на 15 мин при периодическом перемешивании, центрифугировали при 10000 об/мин в течение 15 минут. Осадок отбрасывали. К надосадочной жидкости добавляли сухой (NH4)2SO4 до 20% насыщения. Через 3 часа осадок собирали центрифугированием при 5000 об/мин, его отбрасывали, в над осадочной жидкости -пероксидаза.
Метод биуретовой реакции. Готовят биуретовый реактив, растворяя последовательно в мерной колбе на 250 мл 0,375 г CuSO4-5H2O и 1,5 г сегнетовой соли (KOOC-CHOH-COONa-4 Н2О) в 150 мл воды. Приливают медленно при постоянном перемешивании 75 мг 10%-ного раствора гидроксида натрия и доводят содержимое до 250 мл водой. Биуретовый реактив не подлежит длительному хранению в стеклянной посуде.
Фосфатный буфер

3 часа
Надосадочная жидкость, содержащая пероксидазу

Рис. 1. Схема выделения и очистки пероксидазы из биоматериала печеночницы благородной (Hepatica nobiUs)
по методу В.Д. Анисимова и Т.Б. Кастальевой (1978)
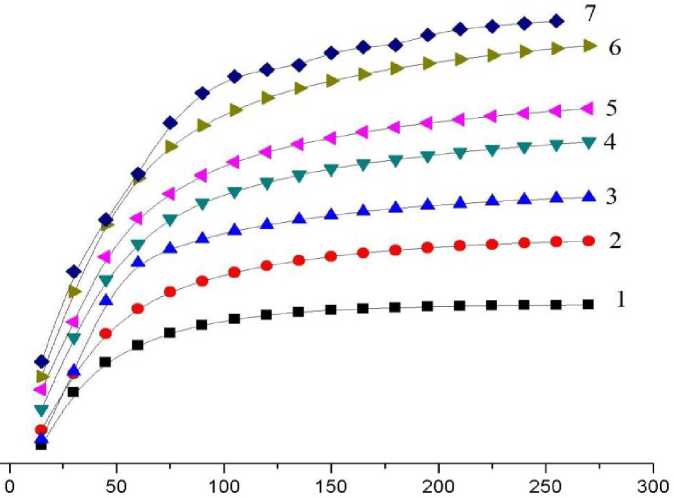
Далее определяли важнейшие ферментативные параметры - Км и Vmax. Для этого изучали кинетику хода биокаталитической реакции по изменению величины оптической плотности (D) во времени (т) для изучаемой системы. В качестве примера представлены зависимости D~t для водного раствора пероксидазы, входящего в состав изучаемой системы (рис. 2).
D
1,05 ^ 1,00 -0,95 2 0,90 -0,85 -0,80 -0,75 -0,70 -0,650,60 2 0,55 -0,50 -0,45 -0,40 -0,35 -0,30 -0,25 2 0,20 -0,15 -0,1 о -
т, с
Рис. 2. Зависимости «D-т» для изучаемой системы при варьировании концентрации пероксида водорода (2-8)-(10"4М) с шагом в единицу:
1: 2-10'4М; 2; 310"4М; 3: 4-10 4М; 4; 5-10"4М; 5: 6-10"4М; 6: 7-10"4М; 7: 8-10 4М
На втором этапе работы определены кинетические параметры каталитической активности пероксидазы в изучаемой системе: бензидин (510'3 М), при варьировании концентраций Н2О2 (2-8)-(10~4М).
Результаты и обсуждение. На основе кинетических зависимостей D-т для изучаемой системы (рис. 2) рассчитаны начальные скорости (Vo) пероксидазозависимых ферментативных реакций (Vo), далее проведено спрямление в координатах двойных братных величин: 1/V и 1/[S] (координатах Лайнуивера-Берка) (рис. 3).
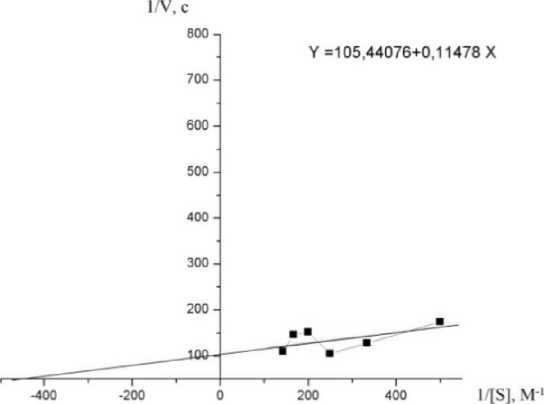
Рис. 3 . Спрямление кинетических зависимостей в координатах двойных обратных величин - координатах Лайнуивера-Берка (1/V - 1/[S]) для изучаемой системы
-33-
По отработанной схеме построены спрямленные кинетические зависимости в координатах Лайнуивера-Берка (рис. 3) и рассчитаны параметры Км и Vmax; Км = 2,23*10"3M;Vmax = 9, 52*10"3с"1.
Заключение. Экспериментально определенные значения ферментативных параметров - Км и Vmax - для исчезающего вида печеночницы благородной находятся в полном соответствии с данными литературы (Лапина, Лихуша, 2010). Это позволяет считать пероксидазу печеночницы благородной тестовым ферментом при изучении разного рода (благоприятных и неблагоприятных) воздействий на экологическое состояние лесопарковых зон.
Список литературы Пероксидаза печеночницы благородной ( Hepatica nobilis)
- Андреева В.А. 1988. Фермент пероксидаза: участие в защитном механизме растений. М.: Наука, 1988. С. 7-24.
- Лапина Г.П., Лихуша П.С. 2010. Закономерности хода ферментативной реакции, катализируемой о-дифенолоксидазой льна при варьировании ионной силы раствора//Вестн. ТвГУ. Сер.: Биология и экология. Вып. 20. № 32. С. 23-26.
- Строев Е.А. 1986. Биологическая химия. М.: Высшая школа. 479 с.
- Clementi, F., Palade, G.E. 1969. Intestinal capillaries. Permiability to peroxidase and ferritin//J. Cell. Biol. V. 41. P. 33-38.
- Nessel A., Mader M. 1977. Über die physiologische Bedeutung der Peroxidase-Isoenzymgruppen des Tabaks anhand einiger biochemischer-Eigenschaften, I. Prennung, Reinigung, chemische und physikalische//Daten. L. Pflanzenphysiol. Bd. 82. S. 235-246.
- Strickland E.H. 1968 Circular dichroism of horseradish peroxidase and its enzyme-substrate compounds//Biochim. Biophys. Acta. V. 151. P. 70-75.
- Srivastava O.P., van Huystee R.B. 1977. Evidence for close association of peroxidase, polypenol oxidase, and IAA oxidase isozyme of peanut suspension culture medium//Can. J. Bot. V. 55. P. 2630-2635.


