Перспектива применения клеточных технологий в лечении пациентов с энтезопатиями
Автор: Крайнюков П.Е., Кокорин В.В., Чеснаков А.Н., Евтушенко А.А., Епифанов С.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.16, 2021 года.
Бесплатный доступ
В настоящее время выбор оптимального подхода в лечении пациентов, страдающих энтезопатиями различной локализации, а так же сокращение сроков их реабилитации остаются актуальной и значимой медико-социальной проблемой современного общества. Она затрагивает большую часть населения в течение жизни и охватывает все сферы трудовой деятельности. Отсутствие общепринятых стандартов лечения, запоздалая диагностика, длительный и упорный характер болезни обуславливают неоднозначные исходы и высокий процент рецидивов, приводят к запущенности процесса, ухудшению качество жизни пациентов и потере трудоспособности работающего населения. Рассмотрены методы регенеративной терапии, применяемые при лечении больных энтезопатиями. Проведен анализ результатов использования современных методик и отражены возможные сроки реабилитации пациентов.
Энтез, энтезопатия, регенерация, аутоткани, реабилитация
Короткий адрес: https://sciup.org/140290426
IDR: 140290426 | DOI: 10.25881/20728255_2021_16_3_12
Prospects for cell technologies in the treatment of patients with enthesopathies
At present, the choice of the optimal approach in the treatment of patients suffering from enthesopathies of various localization, as well as the reduction of the terms of their rehabilitation, remains an urgent and significant medical and social problem of modern society. The problem affects most of the population during life and covers all areas of work. Lack of generally accepted standards of treatment, delayed diagnosis, long-term and persistent nature of the disease, cause ambiguous outcomes and a high percentage of relapses, leads to neglect of the process, deterioration of the quality of life of patients and disability of the working population. The article discusses the methods of regenerative therapy used in the treatment of patients with enthesopathies. The analysis of the characteristics of the use of modern techniques is carried out and the possible terms of rehabilitation of patients are reflected.
Текст научной статьи Перспектива применения клеточных технологий в лечении пациентов с энтезопатиями
В настоящее время выбор оптимального подхода в лечении пациентов страдающих энтезопатиями различной локализации, а так же сокращение сроков их реабилитации остается актуальной и значимой медикосоциальной проблемой современного общества. Она затрагивает большую часть населения в течение жизни и охватывает все сферы трудовой деятельности. Отсутствие общепринятых стандартов лечения, запоздалая диагностика, длительный и упорный характер болезни, обуславливают неоднозначные исходы и высокий процент рецидивов, приводят к запущенности процесса, ухудшению качество жизни пациентов и потере трудоспособности работающего населения [1–3].
Фоном развития энтезопатий у одной группы лиц является профессиональная деятельность, включающая повторяющиеся, стереотипные движения, у спортсменов или военнослужащих, этому способствуют физические перегрузки и характер выполняемых специальных задач. В других случаях причиной становится инфекционный, аутоиммунный агент, стрессовый фактор или беспричинное появление признаков на фоне полного благополучия. Все это свидетельствует об актуальности данной проблемы у населения во всех сферах деятельности современного общества [4–8].
Проведенное исследование позволяет сформулировать концепцию мультиструктурного воздействия имплантированного клеточного концентрата на ткани человека (цитокинов, микроэлементов, тромбоцитов, стволовых клеток и продуктов их экзоцитоза). По мнению авторов имплантация клеточного концентрата стимулирует развитие естественных патофизиологиче-

ских реакций, характерных для процесса репарации. В результате регенераторно-восстановительных реакций организма развиваются основные терапевтические эффекты, наблюдаемые после их введения.
Цель:
– изучить и дать оценку эффективности применения современных методик клеточной инженерии в лечении энтезопатий;
– совершенствовать подход в выборе предпочтительной тактики лечения данной группы пациентов:
– уменьшить сроки лечения и реабилитации пациентов с энтезопатией верхних конечностей.
Материалы и методы
В период с 2016 по 2021 гг. проведено обследование 93 больных, проходивших лечение в ФКУ ЦВКГ им. П.В. Мандрыка, с признаками энтезопатии верхней конечности — плечевого, локтевого и лучезапястного суставов, в возрасте от 25 до 75 лет, из них 41 женщина и 52 мужчины. Период появления первых признаков функциональных расстройств, варьировал в диапазоне — от нескольких суток до 6 месяцев, в среднем 24,5 суток. Все больные проходили лечение амбулаторно, за исключением 15 случаев, когда потребовалась госпитализация в стационар в связи с неврологической симптоматикой. Из исследования исключены пациенты, имеющие: острые респираторные, онкологические, гематологические, ау-тоимунные заболевания, сахарный диабет, анорексию и дефицит жировой ткани, а так же период беременности и лактации.
Больные разделены на 3 группы, в зависимости от применяемого метода лечения, первая и вторая группа составили 30 человек, третья (контрольная) 33, соответственно. Первой группе проводилось комплексное лечение, включающее применение обогащенной тромбоцитарной плазмы (ОТП), второй — стромально-васкулярной фракции (СВФ), третью составили больные с общепринятой тактикой консервативного лечения, включающего нестероидные противовоспалительные средства местного и системного действия. Все группы были сопоставимы по ключевым статистическим параметрам.
Обследование больных проводилось по стандартному протоколу: сбор анамнестических данных (давность, повторяемость, предрасполагающие, сопутствующие факторы); клинические локальные признаки (боль, отек, цвет кожных покровов, напряжение тканей, температура, локализация, трофические расстройства, неврологическая симптоматика, дисфункция); параклинические исследования (оценивали воспалительную реакцию крови, уровень лейкоцитарного индекса интоксикации, биохимические изменения, рентгенографические, УЗ, КТ, МРТ признаки). В обязательном проядке выполняли ультразвуковое исследование (УЗИ) сосудов верхних конечностей и области повреждения тканей. При необходимости выполняли компьютерную (КТ), магнито-резонансную томографию (МРТ).
Полученные данные оформляли протоколом исследования, вносили объективные отличительные признаки, проводили сравнительный анализ.
У большинства больных имел место схожий анамнестический фактор связанный с механическими перегрузками — часто повторяющиеся, монотонные, циклические движения, на протяжении продолжительного периода времени. В 17 случаях причина возникновения жалоб не имела четкой связи с известными факторами и осталась нераспознанной.
Данные, полученные при физикальном осмотре, находили подтверждение при инструментальных методах исследования (R-графия, УЗИ, КТ, МРТ), и определяли субклинические изменения позволяющие выявить объективные критерии анатомо-функциональных нарушений характеризующие энтезопатию (Рис. 1–3).
При допплерографическом исследовании выявлены объективные признаками энтезита, — снижение эхогенности энтеза (неупорядоченность фибриллярной структуры), утолщение энтеза (повреждения коллагеновых волокон), разнонаправленные структурные изменения сухожильной, хрящевой, костной ткани (энтезофиты, эрозии костного компонента, рубцы), а также усиление сосудистого рисунка (Рис. 3).
В настоящее время, современные методы лечения энтезопатий включают применение клеточных технологий, из которых наиболее распространенные это аутологичная плазма крови обогащенная тромбоцитарными факторами роста (ОТП — PRP, platelet-rich plasma in eng.) и клеточный концентрат жировой ткани, в котором присутствуют стромальные клетки и клетки крови — стромально-васкулярная фракция (СВФ — SVF, stromal-vascularfraction in eng.).
В первой группе исследования (N = 30) пациентам, страдающим энтезопатией, применяли концентрат тромбоцитов, обогащенный лейкоцитами и тромбоцитами (Л-ОТП). Эксфузию крови проводили путем венепункции, в стерильные контейнеры, содержащие антикоагулянт. Далее их помещали в центрифугу и проводили короткое центрифугирование с мягким вращением. При этом цельная кровь сепарировалась на три слоя: супернатант (бесклеточная плазма), промежуточный «лейкоцитная пленка» (концентрированные тромбоциты) и нижний (богатый эритроцитами). После первого центрифугирования проводили второе более быстрое и более продолжительное, чтобы изолировать «лейкоцитную пленку». Производили забор Л-ОТП. Для стимулирования дегрануляции тромбоцитов, и активации экзоцитоза накопленных в их цитоплазматических гранулах биостимулирующих факторов, к конечному концентрату добавляли тромбин. Количественные показатели плазмы определяли волюметрическим методом на автоматическом гематологическом анализаторе CELL-DYN Ruby, Abbott (США). В асептических условиях, под УЗИ-контролем, перкутантно, произ-

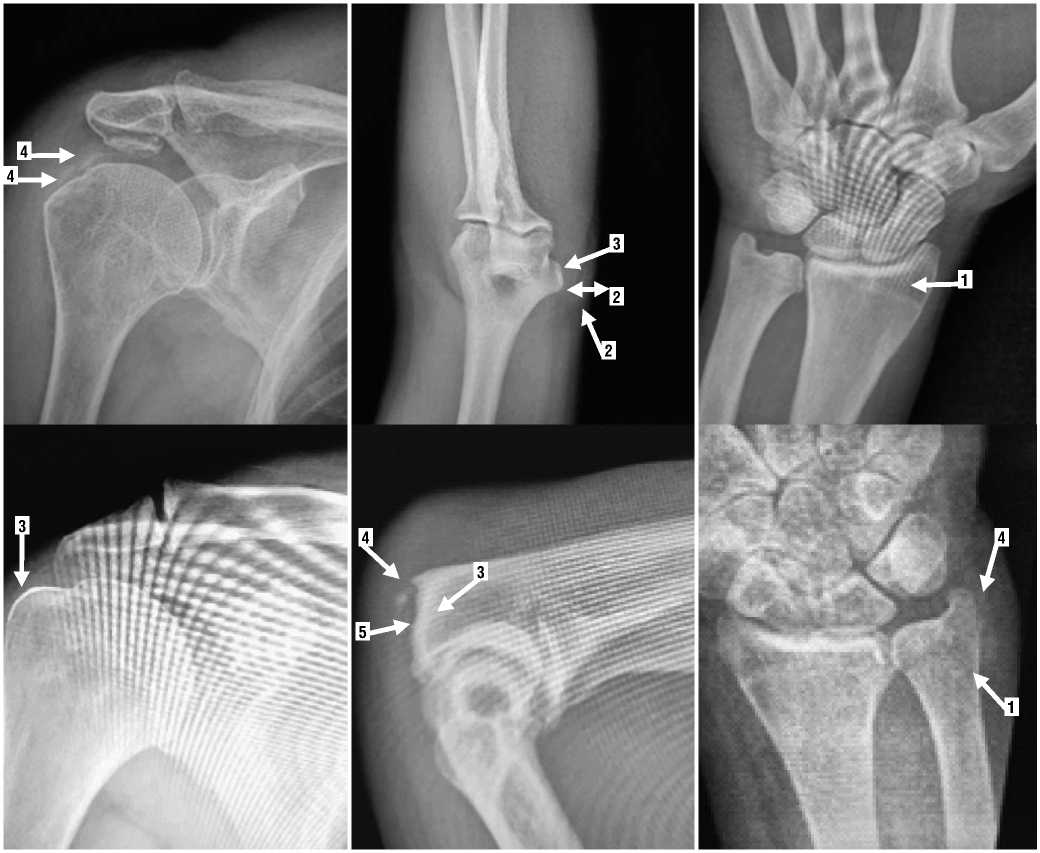
ПЛЕЧЕВОЙ СУСТАВ
ЛОКТЕВОЙ СУСТАВ
ЛУЧЕЗАПЯСТНЫЙ СУСТАВ
Рис. 1. Рентгенография суставов верхней конечности. В начальной фазе энтезопатий рентгенограммы показывают остеопороз энтезеального костного компонента (1) и утолщение мягких тканей (2). На более поздних стадиях мы наблюдали субхондральный склероз (3), энтезофиты (4) и эрозии (5).
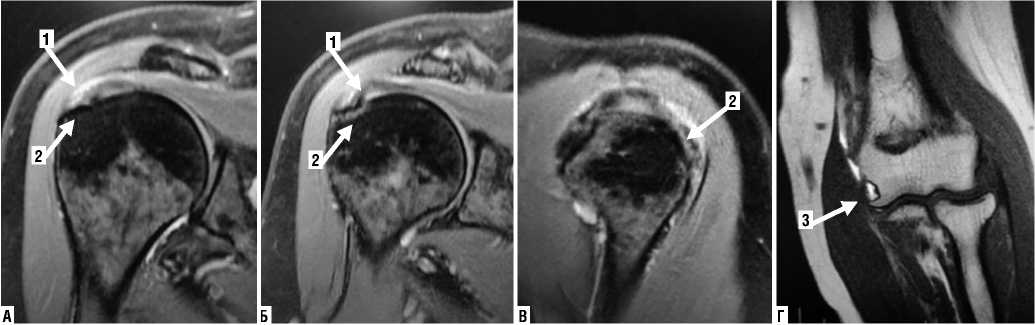
Рис. 2. МРТ плечевого (А–В) и локтевого суставов (Г). При МРТ исследовании волокнистая часть энтезиса плохо видна из-за низкого содержания воды. Стрелками выделены изменения в энтезисе надостной мышцы (1) и прилегающих тканях (отек костного мозга в субхондральной ткани — 2). При МР исследовании локтевого сустава (Г) по поводу медиального эпикондилита, выявлена кистообразная перестройка прилежащих тканей (указана стрелкой — 3).

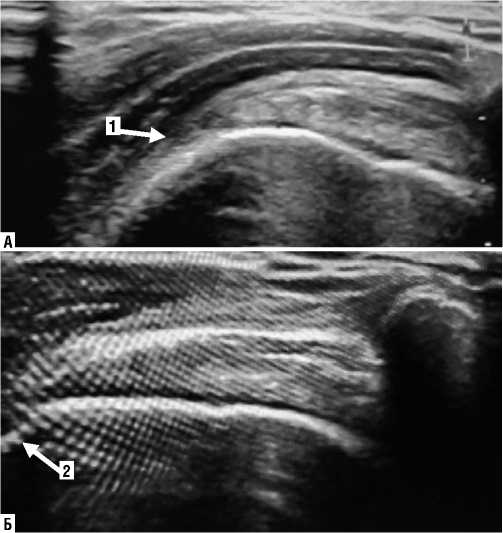
Рис. 3. Допплерографическое исследовании. Энтезопатические поражения: А. пациент С., 45 лет, энтезопатия надостной мышцы плечевого сустава. утолщенный, гипоэхогенный энтез с незначительный эрозией в костной части (1); Б. пациент К., 40 лет, энтезопатия надостной мышцы плечевого сустава, гипоэхогенный энтез, минерализованные (энтезофиты) рубцово-измененные, расслоенные сухожилия в фиброзной и фиброхрящевой частях (2).
водили имплантацию концентрата к месту повреждения. Место инъекции закрывали асептической повязкой. Процедуру проводили от 3 до 7 раз, с интервалом 5–7 суток, в зависимости от выраженности клинических проявлений заболевания и полученных объективных данных исследования (УЗИ, КТ, МРТ).
Во второй группе (N = 30), использовали стромально-васкулярную фракцию (СВФ) — гетерогенную клеточную популяцию, выделяемую из жировой ткани (ЖТ) и обладающую существенным регенеративным потенциалом. Клетки, входящие в ее состав, обеспечивают иммуномодулирующее, антиапоптотическое, противовоспалительное действие, стимулируют рост и дифференцировку клеток, а также ангиогенез в месте повреждения. Принцип выделения СВФ-ЖТ основан на бережной ферментативной диссоциации жировой ткани до состояния отдельных жизнеспособных клеток с последующим фракционированием клеточной суспензии на центрифуге (Zuk P.A. et al., 2001; Yu G. et al., 2011). Преимущества способа — быстрота приготовления и наименьший контакт с реагентами, является относительно безопасным и регулируется меньшим числом законодательных актов (Bora P., Majumdar A.S., 2017).
В условиях операционной, с соблюдением правил асептики и антисептики, под местной инфильтрационной анестезией, путем липосакции из параумбиликальной области передней брюшной стенки живота, получали до 100 мл липоаспирата. Стандартным протоколом изоляции СВФ-ЖТ, в лабораторных условиях, получали осадок, состоящий из сосудистой стромы и стволовых клеток (СК), в количестве от 2x108 до 4x108. Данного количества СК достаточно для клинического применения. Полученный концентрат СВФ ЖТ, под УЗ-контролем, имплантировали в область повреждённого энтеза.
В послеоперационном периоде все пациенты находились под наблюдением в течение 60–120 мин. Осложнений в группах исследования не возникло.
В группе контроля (N = 33), пациенты получали консервативное лечение включающее, противовоспалительную терапию местного и системного действия, антигистаминную и витаминотерапию, физиолечение (УВТ, электрофорез, электромиостимуляция, вакуум-аспирация, иглорефлексотерапия, массаж) проводили при отсутствии или стихании острых воспалительных явлений.
Всем пациентам тщательно указывали на соблюдение послеоперационного ортопедического режима и проводили курс восстановительного лечения.
Результаты и обсуждение
На основании анализа полученных данных выделен общий ряд жалоб характерных для данной патологии: устойчивый болевой синдром в области сустава при движениях и в ночное время; постоянное ощущение дискомфорта в области повреждения; боль при пальпации; локальная отечность и гипертермия тканей; уменьшение амплитуды движений в суставах.
Наличие сосудов при исследовании энтезиса считается характерным признаком энтезопатии. Обследовано 93 пациента с болью в суставах верхних конечностей. Для сравнения обследовали группу из 30 пациентов, не имеющих указанных жалоб и анамнестических данных. Группа наблюдения была представлена 35 больными с механической болью в плечевом суставе (МБП), 35 — в локтевом суставе (ЛС), 15 — лучезапястном суставе (ЛЗС) и 8-тендинитом разгибателя I пальца (ТР). Васкуляризированные энтезы выявлены лишь в 64% случаев, что свидетельствует о неоднозначности признака. При исследовании выявлены признаки воспаления подкожно-жировой ткани, бурсита, синовиита, а также повреждения тканей прилегающей зоне энтеза (эрозии, кисты, рубцовые и дистрофические изменения сухожилий).
Проведение хирургической имплантации клеточного концентрата в первой и второй группах позволило сократить сроки восстановления функции конечности. Так, в первой группе (n = 30) пациентам, в лечении которых применялась ОТП, срок купирования острых воспалительных явлений составил в среднем 7 суток, период начальных УЗ-признаков репарации энтеза составил от 10 до 14 суток, восстановление структуры энтеза, в
среднем, — 8 нед., купирование клинических проявлений заболевания с момента имплантации Л-ОТП — 3 недели. В период динамического наблюдения за пациентами, который составил до 24 мес., рецидив заболевания отмечен только у 10% больных группы исследования. Однако выраженность и клинические проявление в отличие от первоначальных, имели более сглаженных характер. Факторами, способствующими рецидиву, явились: острые респираторные заболевания в 2 случаях, и погрешность в диете (злоупотребление спиртсодержащими продуктами) в одном. Этим пациентам проведена консервативная терапия и физиолечение с положительным результатом.
Во второй группе (n = 30) пациентам, в лечении которых применялась СВФ-ЖТ, срок купирования острых воспалительных явлений составил в среднем 5 суток, период начальных УЗ-признаков репарации — энтеза от 7 до 10 суток, восстановление структуры энтеза, в среднем, — 6 нед., купирование клинических проявлений заболевания с момента имплантации СВФ-ЖТ — 2,5 недели. В период динамического наблюдения за пациентами (24 мес.), рецидив заболевания отмечен всего в одном случае, после перенесенной новой острой коронавирусной инфекции (COVD-19). Однако у данного пациента признаки энтезопатии имели место наряду с, пока еще малоизученным, посткоронавирусным костно-мышечным синдромом. Период реабилитации этого пациента составил до 6 мес.
Третья исследуемая группа (n = 33) пациентов, которым проводилась консервативная терапия, срок купирования острых воспалительных явлений составил в среднем 10 суток, период начальных УЗ-признаков репарации энтеза — до 3–4 недель, восстановление структуры энтеза в среднем — 12 нед., купирование клинических проявлений заболевания с момента имплантации Л-ОТП — 6 недель (таблица 1).
Выводы
Диагностика энтезопатий является не простой задачей. Как правило, основными диагностическими этапами являются — анамнестический, физикальный и инструментальный. Для постановки точного диагноза требуется применение высокотехнологичных методов — КТ, МРТ, УЗИ, и специфических лабораторных показателей крови [9; 10].
Неинвазивная ультразвуковая диагностика дает оценку состоянию патологически измененных мягких и периартикулярных тканей, как до и так и во время лечения, что служит дополнительной и важной информацией для клиницистов позволяя подобрать адекватную схему терапии [11; 12]. Как правило, все пациенты, имеют ультразвуковые признаки дегенеративно-дистрофических изменений фиброзно-костно-сухожильно-связочного комплекса — эксудация, разволокнение, истончение, замещение фиброзными тканями [13; 14].
Жировая ткань пациента является богатым источником аутогенного клеточного материала, что предотвращает риск имуннологического отторжения и позволяет получить большое количество клеток. Клетки СВФ, полученные из жировой ткани, подвергнутой ферментной обработке, содержат ММСК, эндотелиальные прогениторные клетки, М2 поляризированные макрофаги и Т-лимфоциты, которые служат источником регенерации энтеза.
Имплантацию клеточного концентрата возможно выполнить в амбулаторных условиях, при отработанном хирургическом менеджменте и наличии необходимого оборудования в течение 3-4 часов.
В основе современных методик, лежит способность человеческого организма к ауторепарации, инициации генетически обусловленных механизмов, способных купировать болевой синдром, вернуть физиологическую локомоторную функцию и снизить при этом фармакологическую нагрузку [15–18].
По нашему мнению наличие лейкоцитов в составе ОТП позволяет оказывать более продолжительное воздействие концентрата за счет увеличения продолжительности жизни тромбоцитов [19–21].
Благодаря тому, что применяемые методы инъекционной регенеративной терапии основаны на технологиях клеточной инженерии, составными компонентами которой является аутоткань, осложнений и побочных реакций практически не встречается, что положительно сказывается на сроках реабилитации. Учитывая универсальный механизм действия, который направлен на естественное стимулирование репаративных функций организма, их потенциал довольно велик [22–26].
В данном исследовании проведен анализ характеристик используемых современных методов лечения и
Табл. 1. Сравнение групп исследования
|
Группа исследования |
Применяемый метод |
Кол-во процедур |
Интервал процедур (сут.) |
ДП* васкуляризации энтеза (%) |
ДП* начала репарации энтеза (нед.) |
ДП* восстановления структур энтеза (нед.) |
Купирование острых воспалительных проявлений (сут.) |
Купирование клинических проявлений заболевания (нед.) |
|
|
Группа 1 (n = 30) |
Л-ОТП |
5–7 |
5–10 |
13 |
43% |
3 |
8 |
7 |
3 |
|
Группа 2 (n = 30) |
СВФ-ЖТ |
2–3 |
5–7 |
12 |
40% |
2,5 |
6 |
5 |
2,5 |
|
Группа 3 (n = 33) |
Консервативное лечение +ФТЛ |
10–14 |
3–10 |
17 |
52% |
4 |
12 |
10 |
4 |
Примечание : ДП* — допплерографические признаки.
отражены возможные сроки реабилитации пациентов. Однако, с учетом определенных требований по оснащению и квалификации персонала, выбор предпочтительных методик остается за врачом специалистом.
Таким образом, способ стимуляции регенерации клетками, полученными из собственной ткани пациента, представляется перспективным для лечения энтезопатий любой локализации и подтверждает безопасность их применения в хирургии.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Перспектива применения клеточных технологий в лечении пациентов с энтезопатиями
- Балабанова Р.М. Энтезиты: диагностика и лечение // Русский медицинский журнал. — 2012. — №11. — С.538. [Balabanova RM. Enthe-sitis: diagnosis and treatment. Russian Medical Journal. 2012; 11: 538. (In Russ).]
- Dennis MG, Kay-Geert AH, Ai LT. Differentiation between osteoarthritis and psoriatic arthritis: implications for pathogenesis and treatment in the biologic therapy era. Rheumatology. 2015; 54(1): 29-38.
- Juneja SC, Veillette C. Defects in Tendon, Ligament, and Enthesis in Response to Genetic Alterations in Key Proteoglycans and Glycoproteins: A Review. Arthritis. 2013; 154812. doi. 10.1155/2013/154812.
- Wang X, Xie L, Crane J, et al. Aberrant TGF-|3 activation in bone tendon insertion induces enthesopathy — like disease. Journal of Clinical Investigation. 2018; 128(2): 846-860.
- Хитров Н.А. Параартикулярные ткани: варианты поражения и их лечение // Русский медицинский журнал. — 2017. — №3. — С.177-184. [Khitrov NA. Paraartikulyarnyye tkani: varianty porazheniya i ikh lecheniye. Russian Medical Journal. 2017; 3: 177-187. (In Russ).]
- Загородный Г.М., Карпенков К.М., Тихоненков А.А., Ясюкевич А.С. Особенности применения препаратов гиалуронана внутрисуставно в спортивной практике // Медицинские новости. — 2014. — №11-(242). — С. 69-73. [Zagorodnyj GM, Karpenkov KM, Tihonenkov AA, Yasyukevich AS. Osobennosti primeneniya preparatov gialuronana vnu-trisustavno v sportivnoj praktike. Medical news. 2014; 11(242): 69-73. (In Russ).]
- Ясюкевич А.С., Гулевич Н.П., Муха П.Г. Анализ уровня и структуры случаев спортивного травматизма в отдельных видах спорта // Прикладная спортивная наука. — 2016. — № 1(3). — С. 89-99. [Yasyukevich AS, Gulevich NP, Muha PG. Analiz urovnya i struktury sluchaev sportivnogo travmatizma v otdel'nyh vidah sporta. Applied sports science. 2016; 1(3): 89-99. (In Russ).]
- Кокорин В.В., Кузьмин Д.Б., Крайнюков П.Е., Епифанов С.А. Роль инфекции в этиопатогенезеэнтезопатий // Вестник национального медико-хирургического Центра им. Н.И. Пирогова. — 2020. — Т.15. — №3. — C.141 -149. [Kokorin VV, Kuz'min DB, Kraynyukov PYe, Ye-pifanov SA. Rol' infektsii v etiopatogenezeentezopatiy. Bulletin of the National Medical and Surgical Center N.I. Pirogov. 2020; 15(3): 141-149. (In Russ).]
- Arend CF. Role of sonography and magnetic resonance imaging in detecting deltoideal acromialenthesopathy: an early finding in the diagnosis of spondyloarthritis and an under-recognized cause of posterior shoulder pain. Journal of ultrasound in medicine. 2014; 33(4): 557-61.
- Каратеев А.Е., Каратеев Д.Е., Орлова Е.С. и др. «Малая» ревматология: несистемная ревматическая патология околосуставных мягких тканей верхней конечности. Часть 1 // Современная ревматология. — 2015. — №9(2). — С.4-15. [Karateev AE, Karateev DE, Orlova ES, et al. «Malaya» revmatologiya: nesistemnaya revmaticheskaya patologiya okolosusta-vnyh myagkih tkanej verhnej konechnosti. CHast' 1. Modern rheumatology. 2015; 9(2): 4-15. (In Russ).]
- Годзенко А.А. Лечение периартикулярных болевых синдромов // Русский медицинский журнал. — 2012. — №7. — С.382-384. [Godzenko AA. Lechenie periartikulyarnyh bolevyh sindromov. Russian Medical Journal. 2012; 7: 382-384. (In Russ).]
- Малахов Н.Б., Пыков М.И., Чочиев Г.М. Нормальная эхоанатомия параартикулярных тканей коленного сустава у детей и методика их ультразвукового обследования // Ультразвуковая и функциональная диагностика. — 2002. — №2. — С.101-111. [Malahov NB, Pykov MI, CHochiev GM. Normal'naya ekhoanatomiya paraartikulyarnyh tkanej kolen-nogo sustava u detej i metodika ih ul'trazvukovogo obsledovaniya. Ultrasonic and functional diagnostics. 2002; 2: 101-111. (In Russ).]
- Иванова О.Н., Соболев Ю.А., Пядова Е.А. и др. Сравнительный анализ артросонографических и рентгенографических изменений суставов при ревматических заболеваниях // Научно-практическая ревматология. — 2004. — №4 (приложение). — С.11. [Ivanova ON, Sobolev YUA, Pyadova EA, et al. Sravnitel'nyj analiz artrosonograficheskih i rentgenogr-aficheskih izmenenij sustavov pri revmaticheskih zabolevaniyah. Scientific practical rheumatology. 2004; 4 (prilozhenie): 11 (In Russ).]
- Аджигайтканова С.К. Диагностика и лечение отдельных форм ревматических заболеваний с позиции доказательной медицины / Учебно-методическое пособие. — 2013. — С.6-23. [Adzhigajtkanova SK. Diagnostika i lechenie otdel'nyh form revmaticheskih zabolevanij s pozicii dokazatel'noj mediciny. Teaching manual. 2013. Р.6-23. (In Russ).]
- Ахмеров Р.Р., Зарудий Р.Ф., Хайруллин Ф.Р. Применение технологии Pasmolifting в травматологии и восстановительной медицине // Сборник методических рекомендаций по применению тромбоцитарной аутоло-гичной плазмы. Технология Плазмолифтинг Plasmolifting TM. — Москва, 2016. — С.24-33. [Ahmerov RR, Zarudij RF, Hajrullin FR. Primenenie tekhnologii Pasmolifting v travmatologii i vosstanovitel'noj medicine. A collection of methodical recommend ations on the use of platelet autologous plasma. Plazmolifting TM technology. Moskva, 2016. Р.24-33. (In Russ).]
- Теплов О.В., Теплова Ю.С., Плаксейчук Ю.А. и др. Методика применения аутологичной богатой тромбоцитами плазмы в лечении пациентов c остеоартрозом коленных суставов. Методические рекомендации. — Казань, 2017. [Teplov OV, Teplova YUS, Plaksejchuk YUA, et al. Metodika primeneniya autologichnoj bogatoj trombocitami plazmy v lechenii pa-cientov c osteoartrozom kolennyh sustavov. Metodicheskie rekomendacii. Kazan', 2017 (In Russ).]
- Wu PI, Diaz R, Borg-Stein J. Platelet-rich plasma. Physical Medicine and Rehabilitation Clinics of North America. 2016; 27(4): 825-853.
- Papalia R, Diaz Balzani L, Torre G, Tirindelli MC, et al. Intraoperative application platelet rich fibrin, postoperative injections of PRP or microfracture only for osteochondral lesions of the knee: a five-year retrospective evaluation. Journal of biological regulators & homeostatic agents. 2016; 30(4): 41-49.
- Cole BJ, Karas V, Hussey K, Pilz K. Hyaluronic acid versus platelet-rich plasma: a prospective, double-blind randomized controlled trial comparing clinical outcomes and effects on intraarticular biology for the treatment of knee osteoarthritis. American Journal of Sports Medicine. 2017; 45(2): 339-346.
- Laver L, Marom N, Dnyanesh L, Mei-Dan O, et al. PRP for degenerative cartilage disease. Cartilage. 2016; 1.
- Joshi Jubert N, Rodriguez L, Reverte-Vinaixa MM, Navarro A. Platelet-rich plasma injections for advanced knee osteoarthritis: a prospective, randomized, double-blinded clinical trial. Orthopaedic journal of sports medicine. 2017; 5(2).
- D'souza N, Rossignoli F, Golinelli G, Grisendi G, Spano C, Candini O, Domi-nici M. Mesenchymal stem/ stromal cells as a delivery platform in cell and gene therapies. BMC Medicine. 2015; 13(1): 186.
- Ennis WJ, Sui A, Bartholomew A. Stem cells and healing: impact on inflammation. Advances in Wound Care. 2013; 2(7): 369-378.
- Fodor PB, Paulseth SG. Adipose derived stromal cell (ADSC) injections for pain management of osteoarthritis in the human knee joint. Aesthetic Surgery Journal. 2015; 36(2): 229-236.
- Ude CC, Sulaiman SB, Min-Hwei N, Hui-Cheng C, Ahmad J, Yahaya NM, Saim AB, Idrus RBH. Cartilage regeneration by chondrogenic induced adult stem cells in osteoarthritic sheep model. PLoS One. 2014; 9(6): e98770. doi: 10.1371/journal.pone.0098770.
- Bourin P, Bunnell BA, Casteilla L, Dominici M, Katz AJ, March KL, Redl H, Rubin JP, Yoshimura K, Gimble JM. Stromal cells from the adipose tissue-derived stromal vascular fraction and culture expanded adipose tissue-derived stromal/stem cells: a joint statement of the International Federation for Adipose Therapeutics and Science (IFATS) and the International Society for Cellular Therapy (ISCT). Cytotherapy. 2013; 15(6): 641-648.


