Перспективные технологии молекулярно-генетической диагностики у пациентов с протоковой аденокарциномой поджелудочной железы
Автор: Шабунин А.В., Тавобилов М.М., Багателия З.А., Лебедев С.С., Кобзев Ю.Н., Ланцынова А.В., Абрамов К.А., Кудряш Е.Б., Аладин М.Н.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 1 т.25, 2026 года.
Бесплатный доступ
Цель исследования – оценка диагностических и прогностических возможностей технологии QClamp™ real-time ПЦР для выявления цоДНК с мутациями гена KRAS у пациентов с протоковой аденокарциномой поджелудочной железы. Материал и методы. В исследование включено 119 пациентов с различной распространенностью рака поджелудочной железы (РПЖ). Из плазмы крови выделяли внеклеточную ДНК и проводили детекцию наиболее распространенных соматических мутаций KRAS с использованием XNA-опосредованного подавления амплификации дикого типа. Результаты. Мутации KRAS в плазме крови выявлены у 23,5 % пациентов, при этом частота обнаружения цоДНК возрастала с прогрессированием заболевания и достигала при местнораспространенном РПЖ – 66,7 % и при метастатическом – 25,0 %. У больных с резектабельными стадиями (I–II) рака поджелудочной железы цоДНК выявлялась в 15,6 % случаев, однако ее наличие было ассоциировано с достоверно худшей общей и безрецидивной выживаемостью. Концентрация общей внеклеточной ДНК существенно варьировала и не коррелировала напрямую со стадией заболевания, что подтверждает ограниченную информативность этого показателя без молекулярного анализа. Заключение. Полученные данные свидетельствуют, что QClamp™ ПЦР является быстрым и технически выполнимым методом детекции цоДНК, обладающим высокой специфичностью. Наибольшее клиническое применение технология может иметь в прогнозировании течения заболевания и мониторинге минимальной остаточной болезни после хирургического лечения, дополняя существующие клинико-инструментальные подходы.
Рак поджелудочной железы, жидкостная биопсия, цоДНК, молекулярногенетическая диагностика, минимальная резидуальная болезнь, NGS, real-time PCR
Короткий адрес: https://sciup.org/140314344
IDR: 140314344 | УДК: 616.37-006.66:577.21 | DOI: 10.21294/1814-4861-2026-25-1-18-27
Promising molecular genetic diagnostic technologies in patients with pancreatic ductal adenocarcinoma
The aim of this study was to evaluate the diagnostic and prognostic potential of QClamp™ real-time PCR technology for the detection of ctDNA carrying KRAS gene mutations in patients with pancreatic ductal adenocarcinoma. Material and Methods. The study included 119 patients with different stages of pancreatic cancer. Cell-free DNA was isolated from blood plasma, and the most common somatic KRAS mutations were detected using XNA-mediated suppression of wild-type DNA amplifcation. Results. KRAS mutations in plasma were identifed in 23.5 % of patients, with the detection rate of ctDNA increasing with disease progression, reaching 66.7 % in locally advanced disease and 25.0 % in metastatic pancreatic cancer. In patients with resectable stages (I–II), ctDNA was detected in only 15.6 % of cases; however, its presence was associated with signifcantly worse overall survival and recurrence-free survival. The concentration of total cell-free DNA varied substantially and did not directly correlate with disease stage, indicating the limited informative value of this parameter in the absence of molecular analysis. Conclusion. The results obtained demonstrate that QClamp™ PCR is a rapid and technically feasible method for ctDNA detection with high specifcity. The greatest clinical applicability of this technology may lie in prognostication and monitoring of minimal residual disease after surgical treatment, complementing existing clinical and instrumental approaches.
Текст научной статьи Перспективные технологии молекулярно-генетической диагностики у пациентов с протоковой аденокарциномой поджелудочной железы
Рак поджелудочной железы (РПЖ) относится к наиболее агрессивным злокачественным опухолям и занимает одно из ведущих мест по смертности от рака во всем мире. На момент постановки диагноза большинство пациентов имеют местнораспространенную или метастатическую стадию РПЖ, при которой радикальное хирургическое лечение невозможно. Даже у оперированных больных прогноз остается неблагоприятным, в зависимости от стадии медиана общей выживаемости при РПЖ составляет 7–18 мес. Таким образом, актуальной задачей является поиск новых методов ранней диагностики и мониторинга течения рака поджелудочной железы.
В последние годы появилось много сообщений о возможностях определения опухоль-специфических биомаркеров в жидких средах организма, к этим диагностическим технологиям, в частности, относится анализ циркулирующей опухолевой ДНК (circulating tumor DNA, ctDNA, цоДНК). В ряде исследований показано, что наличие цоДНК у больных РПЖ ассоциируется с более высокой опухолевой нагрузкой и неблагоприятным прогнозом. Кроме того, динамика уровня цоДНК может отражать ответ на лечение и служить маркером рецидива задолго до радиологических признаков. Такие свойства делают цоДНК многообещающим биомаркером для диагностики, прогноза и мониторинга терапии при РПЖ [1].
Детекция цоДНК может быть сопряжена с определенными методическими трудностями. Доля цоДНК от всей циркулирующей внеклеточной ДНК может составлять от 0,01 % до нескольких процентов в зависимости от размера опухоли, ее васкуляризации и биологических свойств. Секвенирование по Сангеру обнаруживает мутации с максимальной чувствительностью ~10 %, и для преодоления этого ограничения разработаны более чувствительные методы: аллель-специфическая ПЦР (ARMS, TaqMan и др.), цифровая капельная ПЦР (ddPCR), высокопроизводительное секвенирование (NGS).
Метод QClampТМ ПЦР представляет собой относительно новый подход к высокочувствительному выявлению соматических мутаций, основанный на принципе аллель-специфического молекулярного подавления амплификации нормальной ДНК-последовательности за счет связывания участка неизмененной ДНК-последовательности комплементарным ксено-олигонуклеотидом. Если мутация присутствует, ксено-олигонуклеоид не препятствует эффективной амплификации тар-гетного участка ДНК «клэмпинга». По данным производителя DiaCarta, Inc (США), технология QClampТМспособна обнаруживать мутантную ДНК при ее содержании менее 0,1 % и сопоставима с более дорогостоящими технологиями. Благодаря этим преимуществам QClampТМ ПЦР представляется перспективным инструментом «жидкостной биопсии» для быстрого выявления известных драйверных мутаций в образцах крови.
Цель исследования – оценка возможности применения технологии QClampТМ ПЦР для выявления цоДНК с мутацией в гене KRAS у пациентов с протоковой аденокарциномой поджелудочной железы (ПЖ).
Материал и методы
В исследование включено 119 пациентов с морфологически верифицированной протоковой аденокарциномой ПЖ, проходивших лечение в отделении гепатопанкреатобилиарной хирургии ММНКЦ им. С.П. Боткина. У всех пациентов была взята венозная кровь в объеме 20 мл в пробирки с ЭДТА. Плазма была выделена центрифугированием крови при 1 600 g в течение 10 мин с последующим осадком при 6 000 g (10 мин). Из плазмы каждого образца выделяли внеклеточную ДНК с использованием наборов QClamp® Circulating Nucleic Acid Kit согласно инструкции производителя.
Клиническая характеристика пациентов по стадиям: резектабельный рак ПЖ (стадии I–II) – 45, местнораспространенный нерезектабельный рак (стадия III) – 6, метастатический рак (стадия IV) – 69 больных. Средний возраст пациентов составил 63 года (диапазон 38–79 лет); соотношение мужчин и женщин – 1,1:1). Все пациенты с резек-табельными формами прооперированы в объеме панкреатодуоденальной резекции.
Концентрацию выделенной ДНК измеряли флюорометрическим методом (QuBit dsDNA HS Assay Kit, Thermo Fisher Scientific). Для выявления цоДНК с KRAS мутациями использовали набор QClamp® KRAS Mutation Detection Test (DiaCarta Inc., США), предназначенный для качественного определения наиболее частых соматических мутаций гена KRAS . Набор выявляет точковые (single nucleotide variants – SNV) мутации в кодонах 12, 13, 59, 61, 117 и 146 гена KRAS (экзоны 2–4), которые охватывают >95 % известных мутаций KRAS при ПАПЖ. Реакции ПЦР проводили в 96-луночном формате на приборе LightCycler®96 (Roche Diagnostics). В каждую пробирку вносили 2,5–10 нг ДНК и реагенты согласно протоколу производителя. Выполняли мультиплексную ПЦР в реальном времени: параллельно с амплификацией целевого гена KRAS осуществлялась амплификация внутреннего контроля. Для каждой реакции регистрировали пороговый цикл (Cq), а мутационный статус определяли подсчетом разницы между Cq в исследуемом образце и внутреннем контроле (ВК): ΔCq) = Cq образец – Cq ВК. Положительными считались образцы, соответствовавшие таблицам ΔCq производителя.
Статистическая обработка данных проводилась с использованием пакета статистических программ (SPSS v.27, IBM). Для описания количественных переменных использовались медианы и межквартильный размах (IQR), поскольку распределение концентрации цоДНК существенно отличалось от нормального (по критерию Шапиро–Уилка). Сравнение распределений концентрации между двумя группами осуществляли с помощью непараметрического критерия Манна–Уитни, а между тремя группами (стадии заболевания) – теста Крускала–Уоллиса. Доля пациентов с обнаруженной цоДНК сравнивалась между подгруппами по стадиям при помощи точного критерия Фишера или χ2 Пирсона (при достаточности величины выборки). Для оценки взаимосвязи бинарных и количественных показателей дополнительно вычисляли коэффициент ранговой корреляции Спирмена. Статистически значимыми считались различия при уровне двустороннего p<0,05. Для множественных сравнений использовали поправку Бонферрони.
Результаты
Проанализировано 119 образцов плазмы у пациентов с верифицированным раком поджелудочной железы. Медиана концентрации общей циркулирующей ДНК (cell-free DNA, cfDNA) в плазме составила 5,0 нг/мл (IQR 3,1–9,5 нг/мл). При анализе взаимосвязи концентрации общей цоДНК со стадией заболевания не выявлено зависимости увеличения уровня свободно циркулирующей ДНК от прогрессирования заболевания. Напротив, медианная концентрация свободно-клеточной ДНК при резектабельном РПЖ (стадии I–II) оказалась несколько выше (7,0 нг/мл, IQR 3,7–11,4), чем при метастатическом (4,1 нг/мл, IQR 3,0–8,2), различия статистически значимы (p=0,027 по критерию Манна–Уитни). У больных с местнораспространенным РПЖ медиана была промежуточной (6,3 нг/мл, IQR 2,4–8,6). Однако вследствие малого размера этой подгруппы различия уровней свободно-клеточной ДНК между тремя категориями стадий не достигли статистической значимости (p=0,088, тест Крускала–Уоллиса).
Эти данные суммированы в таблице и на рис. 1, они показывают существенную вариабельность содержания ДНК в плазме. Повышенная концентрация наблюдалась у отдельных пациентов даже на ранней стадии, что может быть связано с сопутствующим воспалительным процессом или индивидуальными особенностями опухоли (некроз, опухолевая нагрузка). В то же время у некоторых больных с отдаленными метастазами общий уровень свободно-клеточной ДНК был относительно невысок. Таким образом, сама по себе концентрация внеклеточной ДНК не является надежным маркером наличия и стадии опухоли в данной выборке.
Выявляемость мутантногоKRAS (цоДНК) методом QClamp
В 28 (23,5 %) из 119 проанализированных образцов с помощью real-time ПЦР с применением XNA обнаружены мутации KRAS , что свидетельствует о присутствии циркулирующей опухолевой ДНК. При этом частота положительных результатов существенно различалась в зависимости от стадии заболевания (таблица, рис. 2). В группе пациентов с резектабельным раком поджелудочной железы (стадия I–II, n=45) цоДНК выявлена лишь у 7 (15,6 %) больных. Напротив, при местнораспространенном РПЖ (стадия III, n=6) мутации KRAS в плазме обнаружены в 4 (66,7 %) случаях. В когорте больных с метастатическим РПЖ (стадия IV, n=68) доля положительных результатов составила 25,0 % (17 из 68 пациентов). Таким образом, наблюдается тенденция к более частому высвобождению цоДНК при распространенных формах заболевания по сравнению с локализованными.
Тем не менее статистический анализ показал, что различие долей выявляемости цоДНК
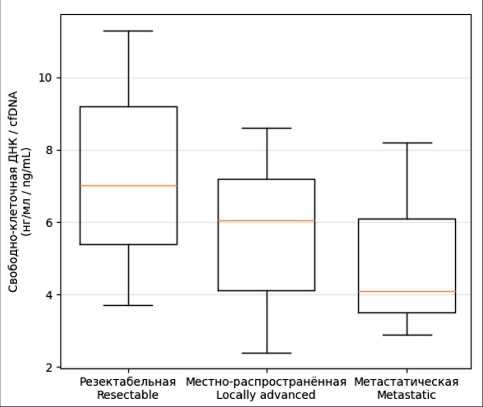
Рис. 1. Распределение концентрации внеклеточной ДНК в плазме у больных раком поджелудочной железы разных стадий. Примечание: рисунок выполнен авторами
Fig. 1. Distribution of cell-free DNA concentration in plasma among patients with different stages of pancreatic cancer. Note: created by the authors
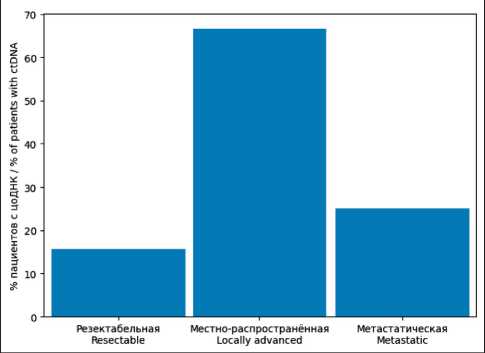
Рис. 2. Частота обнаружения циркулирующей опухолевой ДНК (KRAS) в плазме крови у пациентов с РПЖ разных стадий. Примечание: рисунок выполнен авторами Fig. 2. Frequency of detection of circulating tumor DNA (KRAS) in blood plasma of patients with pancreatic cancer at different stages of the disease. Note: created by the authors
Таблица/table
Частота выявления цоДНК и концентрация внеклеточной ДНК в зависимости от стадии заболевания (протоковая аденокарцинома ПЖ)
Frequency of ctdna detection and concentration of cell-free dna depending on disease stage (pancreatic ductal adenocarcinoma)
|
Распространенность процесса/ Cancer staging |
Число образцов/ Number of samples |
Обнаружена цоДНК/ ctDNA detected |
Медиана свободноклеточной ДНК, нг/мл/ Median cell-free DNA, ng/mL (IQR) |
p-value |
|
Резектабельный РПЖ (I–II стадия)/ Resectable pancreatic cancer (I–II stage) |
45 |
7 (15,6 %) |
7,0 (3,7–11,4) |
– |
|
Местнораспространенный РПЖ (III стадия)/ Locally advanced pancreatic cancer (III stage) |
6 |
4 (66,7 %) |
6,3 (2,4–8,6) |
0,015 (по сравнению с I–II)/ 0.015 ( vs I–II) |
|
Метастатический РПЖ (IV стадия)/ Metastatic pancreatic cancer (IV stage) |
68 |
17 (25,0 %) |
4,1 (3,0–8,2) |
0,25 (цоДНК и I–II); 0,027 (свободноклеточной ДНК и I–II)/ 0.25 (ctDNA vs I–II); 0.027 (cfDNA vs I–II) |
Примечание: таблица составлена авторами.
Note: created by the authors между группами больных с метастатическим и резектабельным РПЖ не достигает значимости (p=0,25). В то же время у пациентов с местнораспространенным РПЖ значимо чаще определялась циркулирующая ДНК опухоли, чем у больных с резектабельными опухолями (p=0,015). Следует подчеркнуть, что группа с РПЖ III стадии была малочисленной, и полученное высокое значение (2/3 пациентов с цоДНК) может быть случайным артефактом выборки.
В целом, отсутствие цоДНК в плазме не означает отсутствия опухоли, особенно на ранней стадии: подавляющее большинство пациентов с локализованным РПЖ в нашем исследовании имели отрицательный результат QClamp, несмотря на то, что их опухоли почти наверняка несли мутацию KRAS. Если принять во внимание, что мутации KRAS присутствуют примерно у 95 % пациентов с РПЖ, то чувствительность метода QClamp в данной когорте для выявления опухолевой ДНК можно оценить как ~16 % при раннем (I–II) и ~25 % при метастатическом раке (рис. 2). В таблице столбцы показывают долю процента пациентов с положительным результатом QClamp real-time ПЦР (обнаружена цоДНК). Различия между группами: резектабельные (I–II) и местнораспространенные
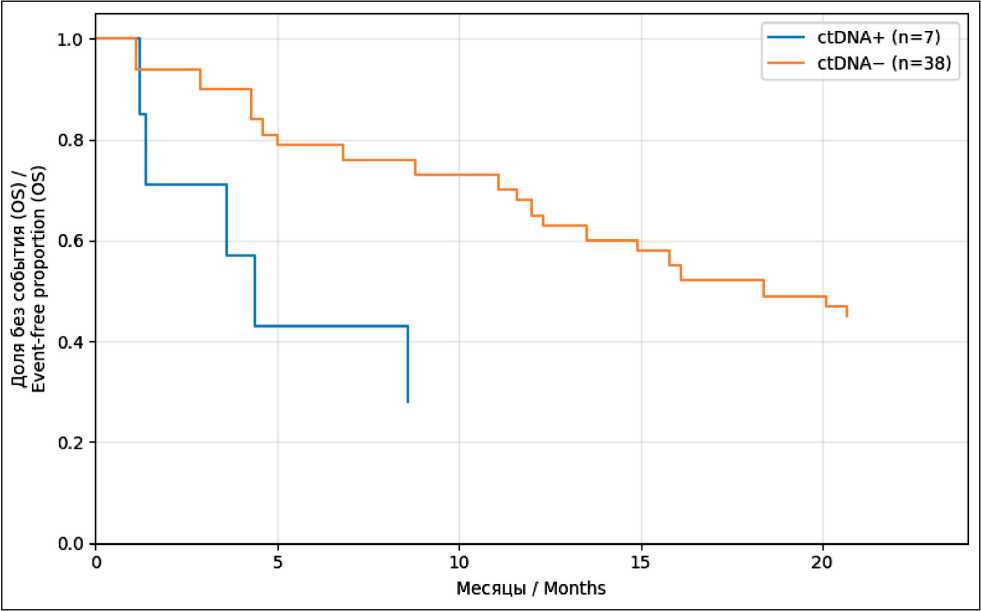
Рис. 3. Кривые Каплана–Мейера общей выживаемости (OS) у пациентов с резектабельным РПЖ. Примечание: рисунок выполнен авторами
Fig. 3. Kaplan–Meier curves of overall survival (OS) in patients with resectable pancreatic cancer.
Note: created by the authors
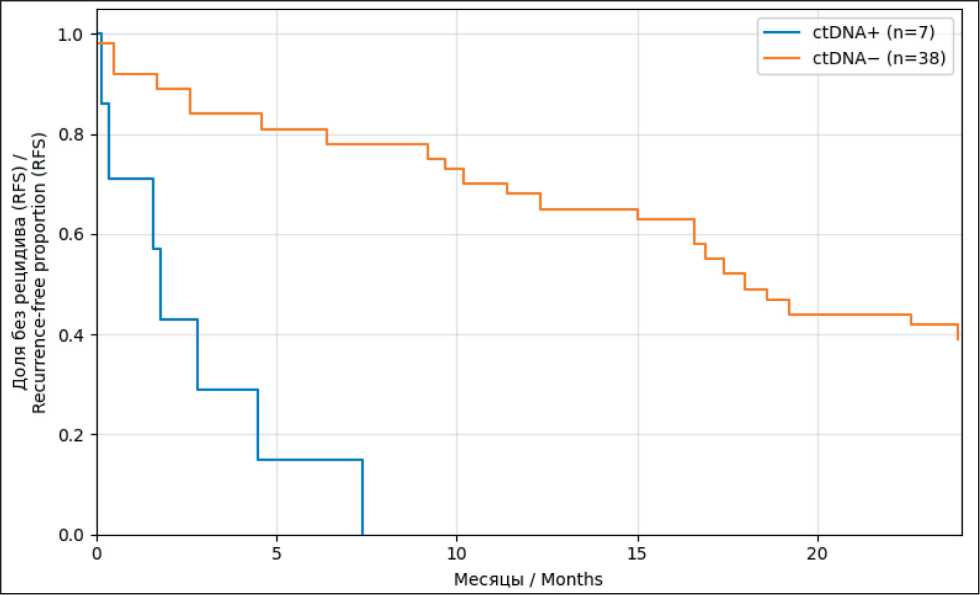
Рис. 4. Кривые Каплана–Мейера безрецидивной выживаемости (RFS) у пациентов с резектабель-ным РПЖ. Примечание: рисунок выполнен авторами
Fig. 4. Kaplan–Meier curves of recurrence-free survival (RFS) in patients with resectable pancreatic cancer.
Note: created by the authors
-
(III) опухоли (p=0,016); резектабельные и метастатические (IV) опухоли (p=0,25).
В группе пациентов с резектабельным раком поджелудочной железы (стадии I-II , п= 45) циркулирующая опухолевая ДНК была выявлена лишь у 7 (15,6 %) больных, в то время как у 38 пациентов результаты анализа оказались отрицательными. Проведенный анализ выживаемости выявил различия между подгруппами. У пациентов с положительным статусом цоДНК медиана общей выживаемости составила 7,2 мес, тогда как у пациентов без выявленной опухолевой ДНК этот показатель достигал 21 мес. Эти данные свидетельствуют о том, что наличие цоДНК в предоперационный период ассоциировано с достоверно худшим прогнозом даже при резектабельных стадиях заболевания.
Аналогичные закономерности выявлены и при оценке безрецидивной выживаемости. У пациентов с цоДНК-положительными результатами медиана безрецидивной выживаемости составила 5,5 мес, в то время как в подгруппе с отрицательными значени- ями цоДНК она достигала почти 18,8 мес (рис. 3, 4). Таким образом, обнаружение циркулирующей опухолевой ДНК у пациентов с резектабельным РПЖ свидетельствует о крайне высоком риске раннего рецидива заболевания после хирургического лечения. Наличие циркулирующей опухолевой ДНК является неблагоприятным прогностическим маркером, способным идентифицировать пациентов с повышенным риском рецидива и меньшей продолжительностью жизни.
Обсуждение
Анализ взаимосвязи между концентрацией свободно-клеточной ДНК и наличием цоДНК показал следующую тенденцию: в образцах, где была обнаружена мутантная ДНК опухоли, наблюдались более высокие уровни общей ДНК. Медиана концентрации свободно-клеточной ДНК у цоДНК-положительных пациентов составила 6,6 нг/мл (IQR 4,1–14,8), тогда как у цоДНК-отрицательных – 4,35 нг/мл (IQR 3,0–8,2). Несмотря на почти 1,5-кратную разницу медиан, с учетом большой вариа- ции показателей она не достигла статистической значимости (p=0,104, критерий Манна–Уитни). На рис. 5 представлены распределения концентраций свободно-клеточной ДНК в группах с обнаруженной и необнаруженной цоДНК.
Полученные результаты подтверждают, что обнаружение цоДНК при раке поджелудочной железы является сложной задачей, особенно на ранних стадиях. Частота выявления мутантного KRAS в плазме (≈16 % для РПЖ I–II стадии и 25 % для РПЖ IV стадии) в нашем исследовании ниже, чем сообщалось в некоторых работах с использованием ПЦР-методик. Так, в исследовании C. Bettegowda et al. [2] с применением цифровой ПЦР сообщалось об обнаружении цоДНК примерно у 48 % пациентов с локализованным и у >75 % с метастатическим раком поджелудочной железы. Причиной более низкой чувствительности в нашей работе может быть как объективно меньший уровень цоДНК у некоторых пациентов (например, небольшие опухоли), так и технические аспекты и то, что тест QClamp охватывал только ген KRAS . Около 5–10 % аденокарцином поджелудочной железы не содержат мутаций KRAS , а имеют драйверные мутации в других генах ( TP53 , SMAD4 , BRCA2 и др.). Добавление параллельного анализа мутаций TP53 и других характерных мишеней могло бы повысить совокупную чувствительность. Например, в недавнем исследовании T. Theparee et al. [3] с применением таргетного NGS панели генов KRAS / TP53 суммарно обнаружены мутации в плазме у ~30,9 % пациентов, при этом у части больных отмечались исключительно мутации TP53 при отсутствии KRAS . Тем не менее даже с расширением панели до двух генов более чем у 60–70 % пациентов с резектабельным РПЖ циркулирующие опухолевые ДНК не определяются. Интересно, что в ряде работ предложено комбинировать несколько методик, чтобы повысить чувствительность: так, одновременное использование анализа цоДНК и четырех белковых биомаркеров (в т.ч. CA 19–9) позволило выявлять до ~64 % случаев рака поджелудочной железы [4–6].
Важным преимуществом метода является скорость выполнения исследования: полный анализ занимает около 2 ч, тогда как даже ускоренное NGS требует несколько дней, а цифровая ПЦР – не менее 4–5 ч. QClamp не требует сложного оборудования помимо стандартного амплификатора; кроме того, производитель разработал протокол прямого лизиса крови (Qzol), позволяющий обходиться без этапа выделения ДНК. В нашем исследовании мы проводили стандартную экстракцию свободноклеточной ДНК для лучшей аналитической чувствительности, однако теоретически QClamp можно выполнять практически «у постели больного», получив результат в день забора крови, – такой оперативности не обеспечивает ни одна другая технология выявления мутаций.
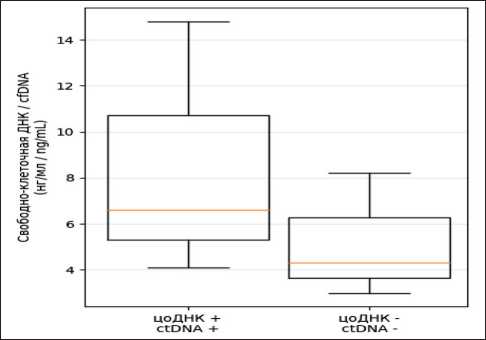
Рис. 5. Распределение концентрации внеклеточной ДНК в плазме у пациентов с обнаруженной («цоДНК +») и необнаруженной («цоДНК –») мутантной ДНК KRAS. Примечание: рисунок выполнен авторами
Fig. 5. Distribution of cell-free DNA concentration in plasma in patients with detected (“ctDNA+”) and undetected (“ctDNA–”) mutant KRAS DNA. Note: created by the authors
Анализ корреляций показал, что обнаружение цоДНК чаще происходит при большей общей концентрации ДНК в образце, хотя само по себе повышение уровня свободно-клеточной ДНК не гарантирует наличия опухолевых мутаций. Это подтверждает, что циркулирующая ДНК является мозаичной смесью фрагментов разного происхождения. Известно, что у больных РПЖ помимо цоДНК в кровотоке могут присутствовать фрагменты ДНК из разрушенных клеток нормальной поджелудочной железы (при сопутствующем панкреатите), из печени (при холестазе, метастазах) и др. С другой стороны, сочетание двух параметров – повышение суммарной ДНК и наличие цоДНК – может указывать на значительный объем опухолевой массы и активное прогрессирование заболевания. Часть авторов указывают, что количество цоДНК (например, в копиях/мл плазмы, подсчитанное по цифровой ПЦР) хорошо коррелирует с объемом опухоли по данным визуализации и числом метастатических очагов [7]. M. Strijker et al. [8] показали, что при метастатическом РПЖ концентрация цоДНК коррелирует с опухолевой нагрузкой и может служить важным прогностическим фактором [8]. В нашем исследовании мы не измеряли количественно аллельную фракцию мутантного KRAS, однако косвенным образом (через частоту детекции) также видна связь с распространенностью опухоли. Так, цоДНК выявлялась у 2/3 пациентов с местнораспространенным РПЖ (III стадия) и лишь у 1/6 больных с ранним РПЖ (I–II), что указывает на резкое увеличение опухолевой ДНК при переходе от небольшой локализованной опухоли к крупной или инфильтративной форме. Отсутствие значимых различий разницы между группами больных с метастатическим и резектабельным РПЖ в нашей выборке можно объяснить неоднородностью подгруппы больных с РПЖ IV стадии. Некоторые пациенты с отдаленными метастазами имели относительно небольшую первичную опухоль (особенно при отдаленной лимфогенной диссеминации), что сопровождалось невысоким уровнем цоДНК.
Сравнение QClamp с NGS и цифровой ПЦР
Ранее другие авторы проводили прямое сопоставление чувствительности различных подходов для обнаружения мутаций KRAS в плазме. Так, O.A. Zill et al. [6] применили NGS-секвенирование для пациентов с опухолями панкреатобилиарной зоны и обнаружили цоДНК приблизительно у 43 % больных РПЖ [6]. В то же время в параллельных образцах, протестированных методами BEAMing и ARMS, результаты были сходными, что свидетельствует о сопоставимой чувствительности продвинутых ПЦР-подходов и NGS. Описана также методика COLD-PCR/HRM, позволяющая выявлять мутантный KRAS ~у 40 % пациентов с местнораспространенным/метастатическим РПЖ, тогда как обычное секвенирование выявляло его только у 12,5 % больных [8–9]. Эти данные вписываются в общий диапазон (12–88 %) доли выявления цоДНК при PDAC. Наши результаты (16–25 %) находятся в нижней части этого диапазона, что ожидаемо для популяции, где лишь четверть пациентов имели отдаленные метастазы. Учитывая небольшие объемы плазмы и фокусировку на одном гене, полученную чувствительность QClamp можно считать приемлемой. Преимущества QClamp – простота и быстрота – могут оправдать несколько менее высокую чувствительность по сравнению с секвенированием, особенно в условиях рутинной клиники. Таким образом, первые результаты свидетельствуют об эффективности метода в качестве скрининга у пациентов с ранними стадиями протоковой аденокарциномы. Необходимо дальнейшее изучение возможностей способа, сделав акцент на особенностях преаналитического этапа для повышения чувствительности.
В отношении прогноза и мониторинга имеются убедительные доказательства, что цоДНК является маркером минимальной остаточной болезни. В ряде работ показано, что наличие мутантной ДНК KRAS в плазме до или сразу после хирургического вмешательства связано с более высоким риском рецидива и худшей выживаемостью. D. Pietrasz et al. [7] продемонстрировали, что у радикально оперированных пациентов с положительным KRAS цоДНК медиана безрецидивной выживаемости составила 4,6 мес, тогда как у пациентов без обнаруженной цоДНК – 17,6 мес; наличие цоДНК было независимым фактором неблагоприятного прогноза. В исследовании Y. Kitahata et al. [10] показано, что после неоадъювантной терапии с последующей резекцией положительный статус цоДНК коррелировал с наличием микрометастазов и ранним прогрессированием. Более того, серийное мониторирование цоДНК позволяет предсказывать рецидив за несколько месяцев до его клинического проявления. Эти данные подчеркивают, что такой высокочувствительный метод, как QClamp, может найти применение для послеоперационного наблюдения, поскольку регулярный неинвазивный тест крови на цоДНК способен обнаружить рецидив заболевания намного раньше рентгенологических признаков.
Наше исследование продемонстрировало принципиальную возможность применения технологии QClamp XNA-mediated ПЦР для детекции циркулирующей опухолевой ДНК при раке поджелудочной железы. Показано, что с помощью данного метода возможно выявлять мутантные копии KRAS в плазме крови пациентов с РПЖ, включая некоторые случаи ранних стадий. Доля положительных результатов (∼24 % в общей группе) соответствует данным литературы для сопоставимых когорт и методов средней чувствительности.
С практической точки зрения применение жидкостной биопсии на основе QClamp ПЦР может иметь наибольшее клиническое применение в мониторинге пациентов после радикального лечения. Как показали другие исследования, обнаружение цоДНК после радикальной операции служит маркером минимальной остаточной болезни и предсказывает скорый рецидив. В условиях, когда стандартный маркер CA 19–9 не всегда информативен (например, при Lewis-негативном фенотипе у ~5 % пациентов), высокочувствительный молекулярный тест может стать незаменимым средством мониторинга [11, 12]. Кроме того, в последние годы разрабатываются терапевтические стратегии, нацеленные на мутации KRAS (например, ингибиторы специфичных G12C-мутаций).
Для широкого внедрения технологии в практическую деятельность необходимы дальнейшие исследования, однако на данный момент показано, что детекция цоДНК коррелирует с исходом заболевания и может дополнять прогностические модели. Возможно повышение чувствительности теста для ранних стадий – например, за счет сочетания нескольких панелей мутаций (добавить TP53 , SMAD4 и др.) или за счет преаналитических улучшений (больший объем плазмы, оптимизация хранения).
Заключение
Первый опыт использования QClamp real-time ПЦР показал явные преимущества метода: высокую специфичность, чувствительность и оперативность получения результата. Метод позволил выявить циркулирующую мутантную ДНК KRAS у значимой части пациентов с распространенным раком поджелудочной железы, а также в отдельных случаях при локализованной форме, что подтверждает его потенциал для ранней диагностики. С точ- ки зрения клинической значимости использование данной технологии может значительно расширить возможности персонализированной онкологии. В сочетании с традиционными методами (лучевая диагностика, биохимические маркеры) жидкост- ная биопсия позволит более точно стадировать заболевание, на дооперационном этапе выявлять группу с неблагоприятным прогнозом, определять минимальную резидуальную болезнь после радикального оперативного вмешательства.


