Перспективы эпигенетических исследований нейрофиброматоза 1-го типа
Автор: Мустафин Р.Н.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Обзоры
Статья в выпуске: 5 т.24, 2025 года.
Бесплатный доступ
Актуальность. Нейрофиброматоз 1-го типа (НФ1) является моногенной болезнью с выраженным клиническим полиморфизмом. При НФ1 определяется повышенный риск развития злокачественных опухолей из оболочек периферических нервов, лейкоза, стромальных опухолей желудочно-кишечного тракта, рака молочной железы, рабдомиосаркомы, карционоидов и феохромацитомы. Мутации в гене NF1 служат драйверами различных спорадических злокачественных опухолей. Цель исследования – оценить механизмы влияния эпигенетических факторов на развитие НФ1 и возможность их использования в диагностике и лечении болезни. Материал и методы. Поиск соответствующих источников проводился в системах Scopus, Web of Science, PubMed, Elibrary, включая публикации с февраля 1995 по февраль 2025 г. Из 1 432 найденных научных статей 56 были использованы для написания систематического обзора. Результаты. Анализ литературы показал, что мРНК гена NF1 является мишенью 13 микроРНК, участвующих также в канцерогенезе спорадических опухолей нервной системы (miR-9, miR-10b, miR-16, miR-21, miR-27a, miR-27b-3p, miR-34a, miR-125a-3p, miR-128-3p, miR-137-3p, miR-147a, miR-193b, miR204-5p). Кроме того, имеются свидетельства эволюционной и функциональной взаимосвязи гена NF1 с ретроэлементами: образование 12 псевдогенов NF1 на 7 разных хромосомах с помощью ферментов ретроэлементов, в интронах гена содержатся Alu и LINE, являющиеся источниками альтернативного сплайсинга и рекомбинаций, наличие горячих точек инсерционного мутагенеза. Заключение. Генетические исследования не подтвердили роль генов-модификаторов в качестве провоцирующих факторов развития и прогрессирования опухолевого синдрома при НФ1. Однако определена роль изменений экспрессии специфических микроРНК при формировании кожных, подкожных и плексиформных нейрофибром, злокачественных опухолей из оболочек периферических нервов. Данный факт позволяет предположить перспективность исследования роли эпигенетических факторов в патогенезе болезни с целью таргетной терапии развивающихся опухолей. Сделано предположение, что дальнейшее исследование взаимосвязей гена NF1 с ретроэлементами позволит определить новые пути лечения НФ1 и спорадических опухолей с воздействием на «порочный круг», описанный в отношении взаимосвязи других генов-супрессоров опухолей с ретроэлементами. В частности, предполагается использование произошедших от ретроэлементов микроРНК, мишенями которых является мРНК гена NF1.
Ген NF1, злокачественные опухоли, микроРНК, нейрофибромы, нейрофибромин, псевдогены, эпигенетические факторы
Короткий адрес: https://sciup.org/140312770
IDR: 140312770 | УДК: 616.833-006-056.7 | DOI: 10.21294/1814-4861-2025-24-5-128-139
Prospects for epigenetic research in neurofibromatosis type 1
Background. Neurofibromatosis type 1 (NF1) is a monogenic disease with a wide range of clinical manifestations. NF1 is associated with increased risk of malignant peripheral nerve sheath tumors (MPNST), leukemia, gastrointestinal and breast cancer, rhabdomyosarcoma, carcinoid tumors, and pheochromocytoma. NF1 gene mutations serve as drivers of various sporadic malignancies. the purpose of the study was to evaluate the mechanisms by which epigenetic factors influence the development of NF1 and the potential for their use in diagnosis and treatment. Material and Methods. The search for relevant sources was carried out in Scopus, Web of Science, PubMed, Elibrary, including publications from February 1995 to February 2025. Of the 1432 scientific articles found, 56 were used to write the review. Results. An analysis of scientific literature showed that NF1 mRNA is a target of 13 microRNAs that are also involved in carcinogenesis of sporadic nervous system tumors (miR-9, miR-10b, miR-16, miR-21, miR-27a, miR-27b-3p, miR-34a, miR125a-3p, miR-128-3p, miR-137-3p, miR-147a, miR-193b, miR-204-5p). There is evidence of an evolutionary and functional relationship between NF1 gene and retroelements: the formation of 12 NF1 pseudogenes on 7 different chromosomes with the help of retroelement enzymes, NF1 introns contain Alu and LINE, which are sources of alternative splicing and recombination, and the presence of insertional mutagenesis hot spots in NF1. Conclusion. Genetic studies have not confirmed the role of modifier genes as triggers for the development and progression of tumor syndrome in NF1. However, changes in the expression of specific microRNAs have been identified in the development of cutaneous, subcutaneous, and plexiform neurofibromas, MPNST. This suggests the potential of studying of epigenetic factors in NF1 pathogenesis for targeted therapy. Further studies of the relationship between the NF1 gene and retroelements will identify new treatment options for NF1 and sporadic tumors by addressing the “vicious cycle” described in the relationship between other tumor suppressor genes and retroelements.
Текст научной статьи Перспективы эпигенетических исследований нейрофиброматоза 1-го типа
Нейрофиброматоз 1-го типа (НФ1) является одним из самых распространенных моногенных заболеваний с аутосомно-доминантным типом наследования и встречается с частотой 1:2 500 новорожденных [1]. Нейрофиброматоз 1-го типа характеризуется развитием доброкачественных неоплазм (нейрофибром) и повышенным по сравнению с общей популяцией на несколько порядков (рис. 1) риском развития различных злокачественных новообразований (ЗНО): опухолей оболочек периферических нервов (MPNST), лейкоза [2], стромальных опухолей желудочно-кишечного тракта, рака молочной железы, рабдомиосаркомы, карционоидов и феохромацитомы [3]. Кроме того, анализ научной литературы показал, что мутации в гене NF1 являются частым событием в канцерогенезе спорадических ЗНО (рис. 2), способствующим химиорезистентности [4].
Ген NF1 является супрессором опухолей, локализован на 17q11.2 и состоит из 57 экзонов. Белковый продукт гена NF1, нейрофибромин [5], экспрессируется преимущественно в нейронах, олигодендроцитах, клетках Шванна и лейкоцитах. Нейрофибромин является крупным белком, регулирующим различные внутриклеточные процессы, главным образом RAS-циклической АМФ, ERK/MAP киназный каскад [6]. Поэтому для лечения плексиформных нейрофибром разработан и введен в клиническую практику ин-
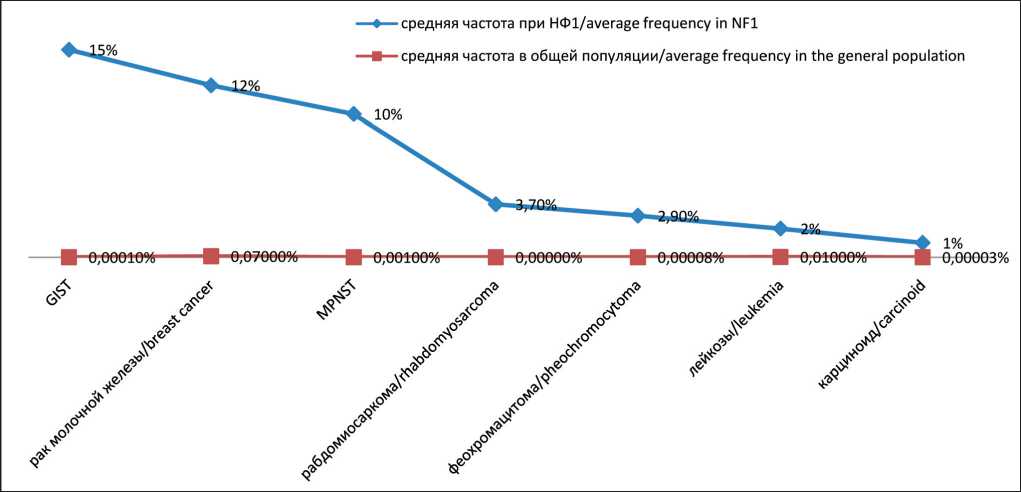
Рис. 1. Сравнительная характеристика частоты злокачественных новообразований при НФ1 и в общей популяции (по данным Z. Lim et al., 2024 [1], P. Saharafi et al., 2024 [2], S. Patil et al., 2012 [3]). Примечания: GIST – стромальные опухоли желудочнокишечного тракта, MPNST – злокачественные опухоли из оболочек периферических нервов; рисунок выполнен автором
Fig. 1. Comparative characteristics of the incidence of malignant neoplasms in NF1 and in the general population (according to Z. Lim et al., 2024 [1], P. Saharafi et al., 2024 [2], S. Patil et al., 2012 [3])). Notes: GIST – gastrointestinal stromal tumors, MPNST –malignant peripheral nerve sheath tumors; created by the author
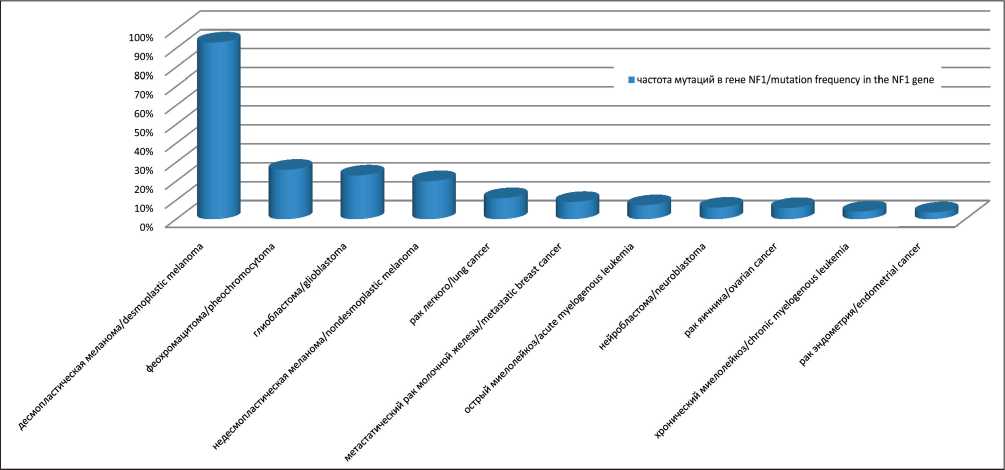
Рис. 2. Роль мутаций в гене NF1 в развитии спорадических злокачественных опухолей. Примечание: рисунок выполнен автором
Fig. 2. The role of mutations in the NF1 gene in the development of sporadic malignant tumors. Note: created by the author
гибитор митоген-активируемой протеинкиназы селуметиниб. Однако он назначается строго по показаниям детям до 18 лет при наличии у них неоперабельных плексиформных нейрофибром [7]. Актуальным остается вопрос по разработке новых способов лечения НФ1, не только плексиформных нейрофибром, но также когнитивного дефицита и множественных опухолей на теле. Нейрофиброматоз 1-го типа характеризуется также выраженным клиническим полиморфизмом и наличием атипичных форм [8]. Более чем у 70 % больных НФ1 развивается поражение ЦНС, включая различные доброкачественные и злокачественные опухоли, а также аномалии без неопластических процессов [9]. Согласно проведенному систематическому обзору, в литературе нет достоверных данных о роли генов-модификаторов в патогенезе болезни [8]. Однако описаны эпигенетические особенности механизмов развития опухолевого синдрома, исследование которых перспективно как для прогнозирования течения болезни, так и для таргетной терапии НФ1.
Клиническая значимостьэпигенетических факторов при НФ1
В ряде клинических исследований определено изменение эпигенетических факторов при развитии опухолей у больных НФ1. Кожные и плексиформ-ные нейрофибромы при НФ1 характеризуются идентичной гистологией, но разной скоростью роста и риском злокачественной трансформации. Однако исследование профилей метилирования показало, что данные типы опухолей являются эпигенетически различными. Также определена корреляция между метилированием CpG и размером опухоли [10]. По характеру метилирования
ДНК глиомы подразделены на 2 подгруппы. Для 1-й подгруппы «пилоцитарной астроцитомы, возникающей на фоне НФ1» с вялотекущим клиническим течением определена уникальная эпигенетическая сигнатура с биаллельной инактивацией гена NF1. Для 2-й подгруппы с агрессивным течением высокозлокачественной астроцитомы выявлены дополнительные онкогенные изменения, такие как гомозиготная делеция супрессора опухоли CDKN2A и мутации гена ATRX [11]. Показана роль гиперметилирования энхансера NF1 в образцах высокозлокачественной астроцитомы с пилоидными признаками как при спорадическом типе опухоли, так и у больных НФ1 с данным типом астроцитомы [12].
Исследование образцов MPNST у больных НФ1 позволило идентифицировать эпигенетическую инактивацию второго аллеля NF1, а также биал-лельную инактивацию генов-супрессоров опухолей CDKN2A, ТР53, PRC2 и уникальный статус триметилирования H3K27. MPNST с потерей H3K27me3 развивались путем значительных хромосомных перестроек с низким уровнем инфильтрации иммунными клетками [13]. Описано изменение ландшафта метилирования ДНК, характерное для MPNST у больных НФ1. При полногеномном профилировании метилирования ДНК у больных с MPNST и клеточных линий MPNST выявлено 73 кандидатных CpG, метилирование которых специфично для данного ЗНО и значимо отличалось от обычных нейрофибром при НФ1. Чувствительность данных оказалась >88 %, специфичность >91 %. Более того, в ДНК образцов плазмы больных НФ1 с MPNST определено 15 дифференциально метилированных CpG-островков, отличающих от больных НФ1 без MPNST. Это свидетельствует о возможности применения полученных данных для раннего выявления MPNST при НФ1 [14]. В то же время исследование атипичных нейрофибром, которые характеризуются высокой частотой малигнизации, показало, что, несмотря на гистологические отличия, они обладают особенностями метилирования ДНК, сходными с доброкачественными нейрофибромами. Поэтому эпигенетические особенности могут служить более специфическими диагностическими маркерами, чем результаты гистологического анализа [15].
Эпигенетические нарушения у больных НФ1 могут служить также причинами патологии ЦНС без неопластических изменений. Например, развивающиеся не менее чем у 4 % пациентов кисты головного мозга [16] могут представлять собой беловатые желеобразные массы из веретенообразных клеток (напоминающих трабекулярные клетки паутинной оболочки) и не отличаться по данным электронной микроскопии от нормальных клеток паутинной оболочки. Однако анализ метилирования ДНК показал, что данные поражения отличаются от здоровых мозговых оболочек, что свидетельствует о роли нарушений метилирования в таких процессах [9]. Можно предположить, что эпигенетические нарушения могут также лежать в основе когнитивных нарушений и психических расстройств у больных НФ1. Исследование процессов, лежащих в основе данных нарушений, перспективно в связи с обратимостью изменений и возможностью таргетного воздействия с использованием микроРНК в качестве инструментов и мишеней. Это связано с тем, что микроРНК оказывают ингибирующий эффект на экспрессию генов не только путем связывания со специфическими последовательностями мРНК и блокируя трансляцию, но также служат гидами для ДНК-метилтрансфераз, вызывая таким образом эффект на метилирование ДНК в специфических участках генома. Данный механизм, называемый РНК-зависимое метилирование ДНК (RdDM – RNA-de-pendent DNA methylation), ранее описанный только у растений, открыт также в клетках человека [17, 18]. МикроРНК относятся к некодирующим РНК (нкРНК), которые принадлежат к эпигенетическим факторам, регулирующим экспрессию генов на транскрипционном и посттранскрипционном уровнях, ремоделирующим хроматин и изменяющим сигнальную трансдукцию. К нкРНК относятся также длинные нкРНК и кольцевые РНК.
Систематические обзоры научной литературы свидетельствуют о вовлеченности ряда микроРНК и длинных нкРНК в развитие опухолей при НФ1 [19]. Дисрегуляция микроРНК играет решающую роль в инициировании и развитии MPNST у больных НФ1 [20]. Данные изменения могут служить причинами описанных специфических изменений метилирования ДНК при MPNST [13, 14], поскольку микроРНК являются гидами для
ДНК-метилтрансфераз в механизмах RdDM [17, 18]. Определено влияние повышенной экспрессии специфических микроРНК, регулирующих онкогены и онкосупрессоры, на развитие плекси-формных нейрофибром и MPNST. В клинических исследованиях в плексиформных нейрофибромах больных НФ1 был определен повышенный уровень miR-486-3p, а также нарушение экспрессии miR-143, miR-145, miR-181a, miR-370, регулирующих RAS-MAK. В образцах MPNST, взятых от больных НФ1, в клинических исследованиях определено значительное нарушение экспрессии miR-19a, miR-106b, miR-301a (регулируют PTEN ), miR-10b, miR-195, let-7b (вовлечены в управление RAS-MAPK), miR-9, miR-135a, miR-135b, miR-200c, let-7b (регулируют мезенхимальный переход), miR-9, miR-10b, miR-210, miR-196b (ингибируют гены HOX ), miR-20a, miR-106b, miR-129-3p, miR-195, miR-449a, let-7b (регулируют клеточный цикл) [21].
В образцах MPNST, взятых у больных НФ1, выявлена сниженная экспрессия miR-143-3p, miR-145-5p, let-7b-5p, а также повышенная – miR-135b-5p, miR-889-3p [22]. Повышенные уровни в образцах плексиформных нейрофибром определены для miR-143 (влияет на KRAS ), miR-145 (влияет на RREB1 ), miR-181, miR-181a (влияет на KRAS и ATM ), miR-193a-5p, miR-362-5p, miR-370 (влияет на M AP3K8 ), miR-483-5p, miR-486-3p (влияет на PTEN ). В дальнейшем в исследованиях in vivo и in vitro выявлено, что развитию MPNST способствуют miR-9 (мишени – CDH1, CDX2 ), miR-10a (мишень – HOXD10 ), miR-10b (мишени – HOXA3, HOXD10, NF1 ), miR-18a, miR-19a (мишени – PTEN, CCND1 ), miR-19b, miR-20a (мишени – CCND1, E2F1 ), miR-31, miR-93, miR-106b (мишени – PTEN, CCND1, E2F1 ), miR-129-3p (мишень – CDK6 ), miR-130b, miR-135a, miR-135b (мишень – APC ), miR-137, miR-148a, miR-192, miR-196b (мишень – HOXB8 ), miR-210 (мишени – HOXA1, HOXA3, HOXA9, E2F3 ), miR-224, miR-301a, miR-301b (мишень – PTEN), miR-425, miR-452, miR-454, miR-484, miR-449a (мишени – CCND1, HDAC1 ) [23]. Таким образом, в развитии плексиформных нейрофибром и MPNST в клинических и экспериментальных исследованиях обнаружено эпигенетическое влияние микроРНК на различные гены-супрессоры опухолей (табл. 1). Определена роль повышенной экспрессии miR-155, регулирующей RAS/MAPK, в развитии плексиформных нейрофибром. Фармакологическое и генетическое ингибирование miR-155 уменьшало количество сфер в данных опухолях, а делеция miR-155 in vivo снижала количество и объем плекси-формных нейрофибром [24]. Достоверно сниженный уровень miR-612 определен в MPNST больных НФ1. Данная микроРНК подавляет пролиферацию и миграцию клеток и вызывает апоптоз клеток. Мишенью miR-612 является мРНК гена FAIM2 [20].
Помимо микроРНК перспективно исследование влияния различных препаратов на эпигенетиче-
Роль специфических микроРНК в развитии опухолей у больных НФ1
the role of specific microRnas in tumor development in patients with nF1
Таблица 1/table 1
|
Опухоль/Tumor |
микроРНК/miRNA |
Эффект воздействия/Impact effect |
|
Плексиформные |
miR-143, miR-145, miR-181a, miR-370 |
Регулируют RAS-MAK/Regulate RAS-MAK [21, 23] |
|
нейрофибромы/ |
miR-193a-5p, miR-362-5p, miR-370 |
Регулируют MAP3K8/Regulate MAP3K8 [23] |
|
Plexiform neurofibromas |
miR-483-5p, miR-486-3p |
Регулируют PTEN/Regulate PTEN [23] |
|
miR-19a, miR-106b, miR-301a |
Регулируют PTEN/Regulate PTEN [21] |
|
|
miR-10b, miR-195, let-7b, miR-155 |
Регулируют RAS-MAPK/Regulate RAS-MAPK [21, 24] |
|
|
miR-9, miR-135a, miR-135b, miR-200c, |
Регулируют мезенхимальный переход/ |
|
|
let-7b |
Regulate mesenchymal transition [21–23] |
|
|
miR-9, miR-10a, miR-10b, miR-210, miR-196b |
Ингибируют гены HOX /inhibit HOX genes [21–23] |
|
|
miR-20a, miR-106b, miR-129-3p, miR-195, miR-449a, let-7b |
Регулируют клеточный цикл/Regulate the cell cycle [21–23] |
|
|
Ингибирование генов LZTS1, SYT2, SMIM13, NR3C2, |
||
|
miR-135b-5p |
TMEM168, FOXN3, CPLX2, RUNX2, B3GLCT, CPLX1/ Inhibits LZTS1, SYT2, SMIM13, NR3C2, TMEM168, FOXN3, |
|
|
CPLX2, RUNX2, B3GLCT, CPLX1 genes [22] |
||
|
miR-889-3p |
Ингибируют гены TMC1, RPS6KA6, FLII, PHF6, DDX3X, ABI1/ inhibits RPS6KA6, FLII, PHF6, DDX3X, ABI1 genes [22] |
|
|
MPNST |
miR-9 |
Ингибирует гены CDH1, CDX2 / Inhibits CDH1 and CDX2 genes [23] |
|
miR-18a, 19a, miR-224, miR-301a, miR- |
Ингибируют гены PTEN, CCND1/ |
|
|
301b |
Inhibit PTEN and CCND1 genes [23] |
|
|
miR-19b, miR-20a |
Ингибируют гены CCND1, E2F1/ Inhibit CCND1 and E2F1 genes [23] |
|
|
miR-31, miR-93, miR-106b |
Ингибируют гены PTEN, CCND1, E2F1/ Inhibit PTEN, CCND1 and E2F1 genes [23] |
|
|
miR-130b, miR-135a, miR-135b |
Ингибируют ген APC /Inhibit APC gene [23] |
|
|
miR-137, miR-148a, miR-192, miR-196b |
Ингибируют ген HOXB8/ Inhibit HOXB8 gene [23] |
|
|
miR-210 |
Ингибирует гены HOXA1, HOXA3, HOXA9, E2F3/ Inhibits HOXA1, HOXA3, HOXA9, E2F3 genes [23] |
|
|
miR-425, miR-452, miR-454, miR-484, |
Ингибируют гены CCND1, HDAC1/ |
|
|
miR-449a |
Inhibit CCND1 and HDAC1 genes [23] |
|
|
miR-612 |
Ингибирует ген FAIM2/ Inhibits FAIM2 gene [20] |
Примечание: таблица составлена автором.
Note: created by the author.
Взаимосвязь гена NF1 с микроРНК
Изменение экспрессии NF1 оказывает свое влияние на канцерогенез не только непосредственным снятием контроля активации онкогенов RAS, но также эпигенетическими путями за счет изменения взаимодействия белка нейрофибромина с различными субстратами (в связи с наличием множества функциональных доменов (рис. 3)) [6]. Кроме того, мРНК гена NF1 взаимодействует со специфическими микроРНК. В тканях глиомы определена повышенная экспрессия miR-9, мишенями которой являются гены NF1 и CREB [28]. NF1 является мишенью miR-16, которая комплементарно связывается с кольцевой РНК circNF1 (образуется путем обратного сплайсинга экзонов
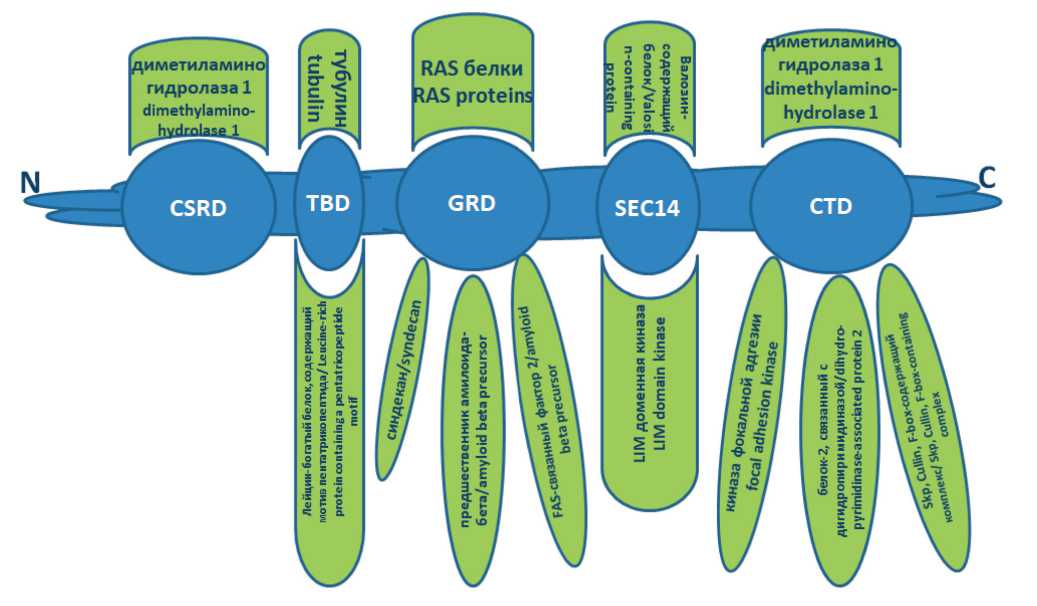
Рис. 3. Схема строения белка нейрофибромина и взаимодействия его доменов с различными белками. Примечание: CSRD – цистеин-серин-богатый домен, TBD – тубулин-связывающий домен, GRD – GAP-связанный домен, SEC14 – Sec14 домен, CTD – С-концевой домен; рисунок выполнен автором
Fig. 3. Schematic diagram of the structure of the neurofibromin protein and the interaction of its domains with various proteins. Notes: CSRD – cysteine-serine-rich domain, TBD – tubulin-binding domain, GRD – GAP-associated domain, SEC14 – Sec14 domain, CTD – C-terminal domain; created by the author
2‒8 гена NF1). Мишенями miR-16 являются также гены AKT3, MAP7 [29]. Также в тканях глиомы по сравнению с контрольными образцами определен повышенный уровень miR-27a-3p, которая подавляла мРНК гена NF1. В то же время усиление экспрессии NF1 отменяло регуляторные эффекты miR-27a-3p резистентных клеток глиомы [30]. miR-27a-3p и miR-27b-3p способствуют развитию НФ1 путем воздействия на мРНК гена NF1 . В клетках Шванна кожных и плексиформных нейрофибром, а также в линиях клеток MPNST определены повышенные уровни miR-27a-3p и miR-27b-3p. В экспериментах миметики этих микроРНК способствуют пролиферации, миграции и инвазии опухолевых клеток. Ингибиторы miR-27a-3p и miR-27b-3p оказывали противоположный эффект [31]. Ген NF1 является также мишенью miR-147a, повышенная экспрессия которой определена при прогрессирующем надъядерном параличе [32].
Транскрипт гена NF1 является также мишенью различных специфических микроРНК (рис. 4), таких как miR-10b [33], miR-21, miR-34a, miR-204-5p [34], miR-103 miR-128-3p, miR-137-3p [35], miR-193b [36], повышенные уровни которых подавляют экспрессию нейрофибромина и способствуют избыточной пролиферации клеток. Согласно анализу репортера люциферазы, ген NF1 является мишенью miR-125a-3p [37]. Помимо участия в канцерогенезе при НФ1, вышеперечисленные микроРНК, мишенью которых является ген NF1, участвуют в развитии спорадических злокачественных новообразований нервной системы. miR-16 характеризуется низкой экспрессией в астроцитомах головного мозга, подавляя пролиферацию клеток и стимулируя апоптоз [38]. Онкосупрессорная miR-21 ингибирует развитие глиомы путем нацеливания на S100A10 [39]. miR-27b-3p подавляет прогрессирование глиомы за счет регуляторного воздействия на YAP1 [40]. Определены низкие уровни miR-34a при мультиформной глиобластоме. Данная микроРНК связывается с 3’UTR гена SV2B (кодирует гликопротеин синаптических везикул) [41]. В тканях глиомы miR-125a-3p проявляла функцию супрессора опухоли за счет ингибирования пути p38/MAPK [42].
В экспериментах in vivo и in vitro показано, что miR-128-3p в клетках глиобластомы ингибирует экспрессию мРНК NUSAP1 (nucleolar and spindle-associated protein 1), участвующего в развитии глиобластомы. Соответственно, данная микроРНК проявляет онкосупрессорные свойства [43]. miR-137-3p, ингибирующая мРНК гена MITF (microphthalmia-associated transcription factor) и Wnt сигнальные пути, подавляет развитие пролактиномы [44]. В тканях глиобластомы снижены уровни miR-147a. Эксперименты на клеточных линиях глиобластомы показали, что miR-147a ингибирует SLC40A1, нарушая опосредованный белком SLC40A1 экспорт железа и индуцируя таким образом ферроптоз [45]. В сыворотке крови больных глиомами, а также в тканях и клеточных линиях глиомы определена повышенная экспрессия miR-193b [46]. Анализ экспрессии miR-204-5p в тканях глиомы показал значительное снижение уровней данной микроРНК, которая является мишенью длинной нкРНК XIST, проявляющей онкогенные свойства [47]. Повы-
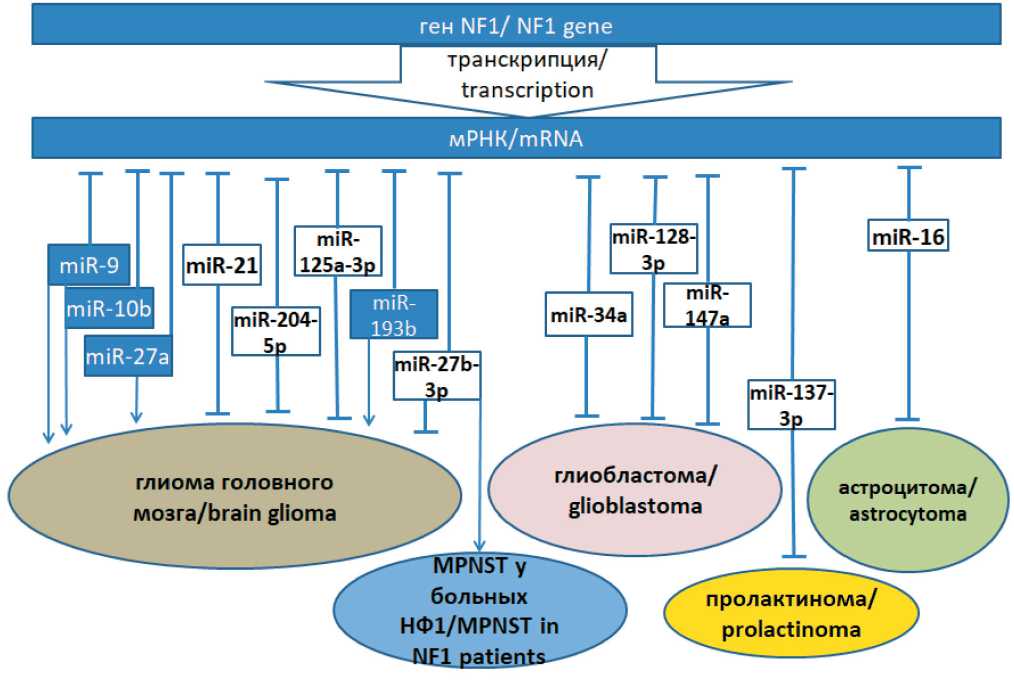
Рис. 4. Схема участия взаимодействующих с мРНК гена NF1 в канцерогенезе спорадических злокачественных новообразований головного мозга (знаком ┬ обозначено ингибирование экспрессии и подавление развития опухоли, знаком ↓ – стимулирование развитие опухоли). Синим цветом обозначены микроРНК, онкогенные в отношении спорадических новообразований, белым цветом – онкосупрессорные микроРНК. Примечание: рисунок выполнен автором
Fig. 4. Scheme of participation of NF1 gene mRNA interacting with carcinogenesis of sporadic malignant neoplasms of the brain (the ┬ sign indicates inhibition of expression and suppression of tumor development, the ↓ sign indicates stimulation of tumor development). MicroRNAs that are oncogenic in relation to sporadic neoplasms are shown in blue, and tumor suppressor microRNAs are shown in white. Note: created by the author
шенная экспрессия miR-10b-5p оказалась наиболее повышенной в глиоме головного мозга высокой степени злокачественности. В экспериментах снижение уровня miR-10b-5p приводило к снижению инвазии в линиях клеток данного типа глиомы [48]. На рис. 4 представлены данные об участии в канцерогенезе спорадических ЗНО микроРНК, взаимодействующих с мРНК гена NF1.
Интересно отметить, что из 13 микроРНК, взаимодействующих с мРНК гена NF1, 9 микроРНК проявляют свойства супрессоров опухолей, хотя в путях ингибирования NF1 они являются онкогенными (поскольку подавляют экспрессию нейрофибромина). Таким образом, при использовании специфических микроРНК в качестве мишеней для воздействия в таргетной терапии опухолевого синдрома при НФ1 нужно учитывать многостороннее влияние данных молекул. Одни и те же микроРНК могут проявлять как онкогенные свойства при НФ1 (miR-21, miR-27b-3p, miR-125a-3p, miR-204-5p, miR-34a, miR-128-3p, miR-147a, miR-137-3p, miR-16) за счет подавления экспрессии нейрфромина, так и онкосу-прессорные свойства при спорадических опухолях головного мозга за счет связывания с мРНК онкогенов. Данный факт свидетельствует о необходимости глубоких биоинформационных исследований для проектирования таргетной терапии опухолевого синдрома при НФ1 с использованием микроРНК в качестве инструментов или мишеней.
Взаимосвязь гена NF1 с ретроэлементами
Вышеописанная роль микроРНК в патогенезе опухолей при НФ1, а также участие взаимодействующих с мРНК гена NF1 микроРНК в канцерогенезе спорадических опухолей позволяют предположить значение ретроэлементов в данных процессах. Поскольку гены-супрессоры опухолей, такие как ATM, BRCA1, р53, RB1, VHL, характеризуются свойством ингибировать РЭ, тем самым предотвращая геномную нестабильность, а также формированием «порочного круга» вследствие наличия в них горячих точек инсерционного мутагенеза [49], можно предположить наличие подобных свойств в отношении гена NF1. Действительно, интроны NF1 обогащены полиморфными инсерциями LINE и SINE. Для гена NF1 выявлена повышенная частота мутабельности вследствие инсерций. Определено, что инсерции ретроэлементов в ген NF1 являются причинами НФ1 более чем в 0,4 % случаев (выявлено 14 инсерций Alu и 3 инсерции LINE1), что свидетельствует о наличии горячих точек инсерционного мутагенеза гена NF1 . Кроме того, обогащение локуса NF1 ретротранспозициями способствует повышенной частоте делеций вследствие рекомбинаций с РЭ на других хромосомах [50].
РЭ представляют собой участки генома, способные к перемещениям в новые локусы с помощью кодируемых собственными (автономные РЭ) генами ферментов или с помощью ферментов других РЭ
(неавтономные РЭ). К автономным РЭ относятся содержащие длинные концевые повторы (LTR) РЭ, главным образом, представленные эндогенными ретровирусами человека (HERV), которые занимают 8 % генома человека [49]. LINE1 представляют собой автономные ретроэлементы, не содержащие длинные концевые повторы (LTR). В геноме человека они занимают около 17 % всех нуклеотидных последовательностей, составляя около 500 000 копий, из которых полностью сохранили свою активность около 100. Среди неавтономных не содержащих LTR элементов SINE наиболее распространены в геноме человека Alu. Они занимают около 10 % всех последовательностей ДНК. Alu используют ферменты LINE1 для своих транспозиций, представлены более 1 млн копий, из которых 100 000 способны к перемещениям [51]. Известны также составные РЭ, такие как SVA (SINE-VNTR-Alu), которые представляют 0,2 % генома человека [52].
Большинство LINE1 утратили способность к транспозициям благодаря накоплению точковых мутаций, 5’-укорочения, делеций и других перестроек [50]. Такие LINE1 состоят из 6 000 пар нуклеотидов, содержат 3’-поли-А хвост и две открытые рамки считывания, которые кодируют белки pORF1 и pORF2. Из них pORF2 состоит из обратной транскриптазы и интегразы – ферментов, необходимых для образования кДНК из РНК и ее встраивания в новый локус генома. При этом данные ферменты не отличаются высокой специфичностью, поэтому, помимо собственных мРНК LINE1, они могут образовывать копии кДНК неавтономных РЭ и даже мРНК белок-кодирующих генов (в том числе NF1 ) с их инсерцией [50]. Этим можно объяснить формирование 12 псевдогенов NF1 в геноме человека, распределенных по 7 хромосомам: 2, 12, 14, 15, 18, 21 и 22. Большинство из них локализуются в перицентромерных областях, а на хромосоме 2 в локусе остатка предковой центромеры (2q21). Вследствие отсутствия селективного давления псевдогены могут аккумулировать мутации и рекомбинировать с функциональным NF1 путем межхромосомной генной конверсии (нереципрокного обмена нуклеотидами) [5].
В некоторых случаях причиной НФ1 могут быть мутации в областях интронов гена NF1 (создающие альтернативные сплайсинговые варианты) и структурные перестройки повторяющихся последовательностей. Поскольку Alu-элементы являются важными источниками сайтов альтернативного сплайсинга [53], инсерции РЭ являются источниками глубоких интронных вариантов мутаций, приводящих к аберрантному сплайсингу, являющихся причинами НФ1 [53]. Опубликованы результаты исследования семьи с НФ1, который обусловлен вставкой LINE1 в интрон 15 гена NF1, что привело к пропуску экзона 15. Данный вариант обнаружен с помощью комбинированного подхода оптического картирования генома, WGS (whole- genome sequencing) и исследования кДНК [50]. Последовательности Alu являются источниками полиморфных сайтов сплайсинга [54]. О роли РЭ в регуляции функционирования гена NF1 свидетельствует существование нескольких сплайсинговых вариантов продуктов экспрессии гена. Это связано со способностью РЭ образовывать альтернативные сайты сплайсинга с включением 4 нормальных внутрирамочных изоформ альтернативного сплайсинга продукта гена NF1 [53].
РЭ также играют роль в формировании протяженных делеций в локусе 17q11.2 с охватом гена NF1, которые определяются у 5–10 % больных НФ1 и происходят в повторяющихся (рекуррентных) точках разрыва вследствие неаллельной гомологичной рекомбинации (NAHR) между высокогомологичными дуплицированными последовательностями в области гена NF1. Около 70–80 % случаев делеций (1-го типа) имеют размеры 1,4 мегабаз с точками разрывов в низкоко-пийных повторах NF1-REPa и NF1-REPc. Делеции 2-го типа, размером 1,2 мегабаз, представлены точками разрывов в гене SUZ12 и его псевдогене SUZ12P, определяются в 10–20 % случев. Делеции 3-го типа происходят в точках разыва в пределах NF1-REPb и NF1-REPc и наблюдаются в 1,4–4 % случаев. Описанные три типа делеций являются рекуррентными у множества больных НФ1. Рекомбинирующие в точках разрывов низкокопийные повторы, такие как NF1-REPa и NF1-REPc, характеризуются высокой гомологией последовательностей в пределах 50 килобаз [19]. РЭ являются важными источниками NAHR в канцерогенезе [55] и поэтому могут быть важными причинами делеций NF1 с инактивацией гена как при НФ1, так и в спорадическом канцерогенезе. Хотя подобно другим генам-супрессорам опухолей (ATM, BRCA1, р53, RB1, VHL), напрямую ингибирующим ретроэлементы [49], для гена NF1 пока не описано таких свойств, имеются опосредованные данные такого влияния. Это связано с взаимодействием транскрипта NF1 со специфическими микроРНК, образующимися из последовательностей РЭ. Анализ баз данных mRDB и MDTE о происхождении микроРНК от ретроэлементов [56] позволил выявить 24 таких микроРНК, среди которых 12 микроРНК произошли от LINE, 12 – от SINE (табл. 2).
Заключение
НФ1 обусловлен мутациями в гене NF1 и характеризуется выраженным повышением риска развития специфических ЗНО. В то же время во многих спорадических ЗНО обнаруживаются мутации в гене NF1 , играющие роль драйверов канцерогенеза и участвующие в формировании фармакорезистентности. У больных НФ1 определяется выраженная клиническая вариабельность с разной степенью проявлений опухолевого синдрома и
Таблица 2/table 2
Произошедшие от line и sine микроРНК, мишенями которых является NF1 line and sine derived microRnas targeting NF1 gene
|
No № |
Название микроРНК/ |
Ретроэлемент-источник микроРНК/ |
Характеристика ретроэлемента/ |
|
miRNA name |
Retroelement source of miRNA |
Characteristics of a retroelement |
1. miR-374c-5p LINE2
|
2. |
miR-552-3p |
LINE1 |
Автономный ретроэлемент, не содержащий LTR/ Autonomous non-LTR retroelement |
|
3. |
miR-576-5p |
LINE1 |
|
|
4. |
miR-582-5p |
LINE-CR1 |
|
|
5. |
miR-625-5p |
LINE1 |
|
|
6. |
miR-1271-5p |
LINE2 |
|
|
7. |
miR-1285-3p |
SINE-Alu |
|
|
8. |
miR-3163 |
SINE-MIR |
|
|
9. |
miR-3168 |
SINE-MIR |
Неавтономный ретроэлемент, не содержащий LTR/ Nonautonomous non-LTR retroelement |
|
10. |
miR-3617-5p |
SINE-MIR |
|
|
11. |
miR-4452 |
SINE-Alu |
|
|
12. |
miR-4457 |
LINE1 |
Автономный ретроэлемент, не содержащий LTR/ |
|
13. |
miR-4676-3p |
LINE2 |
Autonomous non-LTR retroelement |
|
14. |
miR-4797-3p |
SINE-5S-Du-L2 |
|
|
15. |
miR-4801 |
SINE-MIR |
|
|
16. |
miR-5003-3p |
SINE-MIR |
Неавтономный ретроэлемент, не содержащий LTR/ Nonautonomous non-LTR retroelement |
|
17. |
miR-5584-5p |
SINE-MIR |
|
|
18. |
miR-5684 |
SINE-Alu |
|
|
19. |
miR-6887-5p |
LINE2 |
Автономный ретроэлемент, не содержащий LTR/ |
|
20. |
miR-7151-3p |
LINE1 |
Autonomous on-LTR retroelement |
|
21. |
miR-7851-3p |
SINE-Alu |
Неавтономный ретроэлемент, не содержащий LTR/ Nonautonomous non-LTR retroelement |
|
22. |
miR-8084 |
LINE1 |
Автономный ретроэлемент, не содержащий LTR/ |
|
23. |
miR-9985 |
LINE1 |
Autonomous non-LTR retroelement |
|
24. |
miR-10523-5p |
SINE-MIR |
Неавтономный ретроэлемент, не содержащий LTR/ Nonautonomous non-LTR retroelement |
Примечание: таблица составлена автором.
Note: created by the author.
развития ЗНО. Поэтому выяснение причин, провоцирующих развитие нейрофибром, может стать основой для их прогнозирования, профилактики и таргетной терапии. Значение генов-модификаторов в данных процессах не доказано. Однако определена роль специфических микроРНК. В обзоре описано участие специфических микроРНК в развитии плексиформных нейрофибром и MPNST, которые могли бы быть использованы в качестве прогностических маркеров и мишеней в таргетной терапии. Анализ литературы позволил найти 13 специфических микроРНК, нацеленных на мРНК гена NF1 и участвующих в канцерогенезе других спорадических опухолей нервной системы, что свидетельствует о возможности модулирования экспрессией гена при НФ1 и спорадических ЗНО с использованием этих микроРНК. Поскольку для генов-супрессоров опухолей характерна взаимо-регуляция с ретроэлементами, приводящая к про- грессированию канцерогенеза, проведен поиск данных о влиянии ретроэлементов на ген NF1. Обнаружено, что в гене NF1 находятся горячие точки инсерционного мутагенеза, сам ген содержит полиморфные интеграции LINE и SINE. С помощью ферментов LINE в эволюции сформировано 12 псевдогенов, распределенных по 7 различным хромосомам. Расположенные в интронах гена NF1 ретроэлементы также являются причиной мутаций вследствие рекомбинаций с гомологичными последовательностями. Кроме того, определено 24 произошедших от LINE и SINE микроРНК, мишенью которых является мРНК гена NF1. Описанные взаимосвязи гена NF1 с ретроэлементами свидетельствуют о возможности воздействия на развитие опухолевого синдрома при НФ1 с помощью модулирования активности ретроэлементов, в том числе с использованием в качестве объектов вышеописанных 24 микроРНК.


