Первичный и вторичный (индуцированный) иммобилизирующий интерстициальный фиброз сердца
Автор: Шевченко Ю.Л., Плотницкий А.В., Ульбашев Д.С.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 4-2 т.17, 2022 года.
Бесплатный доступ
Фиброз сердца может отражать активацию репаративных или дезадаптивных процессов. При нарушении регуляции синтеза коллагеновых волокон происходит увеличение объема интерстициального пространства, качественно изменяется межуточная соединительная ткань (увеличивается ее плотность, структура «оплетения», меняется расположение волокон и др.) – это часто становится причиной дисфункции сердца: происходит механическое сдавление здоровых кардиомиоцитов извне, ограничение их нормального движения и функционирования. В статье приведены два клинических наблюдения, которые демонстрируют пример первичного и вторичного (индуцированного) иммобилизирующего интерстициального фиброза сердца. В основе первичного иммобилизирующего интерстициального фиброза сердца лежат изменения соединительной ткани, без изначального повреждения кардиомиоцитов. Развитие заболевания происходит постепенно, начиная с незначительного увеличения объема интерстиция, вплоть до формирования грубого фиброза со сдавлением артериол. В основе вторичного (индуцированного) иммобилизирующего интерстициального фиброза сердца лежит процесс диффузных изменений межуточной соединительной ткани в результате стимуляции его сформировавшимися постинфарктными рубцами.
Интерстициальный фиброз, сердечная недостаточность, ИБС
Короткий адрес: https://sciup.org/140300778
IDR: 140300778 | DOI: 10.25881/20728255_2022_17_4_2_136
Primary and secondary (induced) immobilizing interstitial cardiac fibrosis
Fibrosis of the heart may reflect the activation of reparative or maladaptive processes. When the regulation of collagen fiber synthesis is disrupted, the volume of the interstitial space increases, the interstitial connective tissue changes qualitatively (its density increases, the structure of the “braiding” changes, the location of the fibers changes, etc.) – this often causes cardiac dysfunction: there is mechanical compression of healthy cardiomyocytes from the outside, restriction of their normal movement and functioning. The article presents two clinical observations that demonstrate an example of primary and secondary (induced) immobilizing interstitial cardiac fibrosis. Primary immobilizing interstitial cardiac fibrosis is based on changes in connective tissue, without initial damage to cardiomyocytes. The development of the disease occurs gradually, starting with a slight increase in the volume of the interstitium, up to the formation of gross fibrosis with compression of arterioles. Secondary (induced) immobilizing interstitial cardiac fibrosis is based on the process of diffuse changes in the interstitial connective tissue as a result of stimulation by its formed postinfarction scars.
Текст научной статьи Первичный и вторичный (индуцированный) иммобилизирующий интерстициальный фиброз сердца
Фиброз сердца — это закономерное следствие различных заболеваний как самой сердечно-сосудистой системы (включая ИБС, кардиомиопатии, артериальную гипертензию, пороки сердца и прочее), так и других органов и систем (вирусные и бактериальные инфекции легких и желудочно-кишечного тракта, эндокринные заболевания, почечные патологии и др.) [1–5]. Специфические изменения структуры межуточной соединительной ткани миокарда могут привести к механическому ограничению сократимости и расслабления кардиомиоцитов, препятствовать электропроводимости, региональной трофики и, таким образом, быть причиной развития про- грессирующей хронической сердечной недостаточности [6–8].
Фибробласты являются одними из самых распространенных типов клеток в сердце [9]. Их основная роль заключается в создании поддерживающего каркаса сердца, преобразовании сокращения отдельных кардиомиоцитов и их ассоциаций в один целостный энергетически эффективный мышечный насос [10]. Это обеспечивается продуцированием ими множества структурных белков, наиболее важными из которых являются коллагены, особенно I и III типов [11–12]. Регуляция их количества и соотношения, структуры всего внеклеточного матрикса представляет собой динамический процесс, включающий как выработку, так и деградацию соединительнотканных элементов. Сердечный фиброз возникает при дисбалансе между этими процессами, в результате чего увеличивается объем, качественно изменяется межуточная соединительная ткань (увеличивается плотность, структура «оплетения», меняется расположение волокон, соотношение неколлагеновых компонентов к элементам коллагеновой матрицы) [9].
Фиброз разделяют на два основных типа: репаративный (отложение коллагена в зонах поврежденного миокарда) и реактивный (диффузное увеличение количества соединительнотканных волокон без повреждения миокарда) [13].
Репаративный фиброз развивается в ответ на повреждение кардиомиоцитов

и является важной защитной реакцией при инфаркте миокарда. Своевременное формирование замещающего рубца в зоне некроза уменьшает риск фатального осложнения — постинфарктного разрыва стенок сердца [14–15].
Реактивный фиброз проявляется диффузным отложением коллагена в ин-терстиции. Это происходит в отсутствие гибели кардиомиоцитов и может стимулироваться длительным стрессом, воздействием профибротических медиаторов, чрезмерными перегрузками работы сердца (пороки сердца, артериальная гипертензия и прочее) [16]. Активация нейрогормональных реакций, как внутрисердечных, так и системных (ангиотензин II, альдостерон, катехоламины) приводит к повышению уровня медиаторов, стимулирующих фибробласты [17]. Системная или локальная воспалительная реакция, ожирение, сахарный диабет, метаболический синдром, сердечные, легочные или кишечные инфекции, лекарственные препараты и радиация тоже стимулируют развитие реактивного фиброза [18–20]. Он может формироваться по всему миокарду (интерстициальная фиброз), либо ограничиваться вокруг периферических кровеносных сосудов (периваскулярный фиброз) [9].
Учитывая тесную связь между соединительной тканью сердца и кардиомиоцитами, изменения физических свойств фиброзной сетки неблагоприятно влияют на сократительную функцию миокарда, сдавливая нормальные клетки. Результаты специальных исследований позволили определить отдельный тип фиброза сердца — «иммобилизирующий интерстициальный фиброз сердца» (ИИФС) , в составе которого выделено еще две взаимосвязанные его формы: первичный и вторичный ИИФС [21–23].
Первичный ИИФС представляет собой, по сути, реакцию соединительной ткани на различные локальные или системные факторы. Изменения эндомизия и перимизия становятся первопричиной дисфункции миокарда: происходит механическое сдавление здоровых кардиомиоцитов извне, ограничение их нормального движения и нарушение функционирования сердца в целом.
Условно выделяются следующие клинико-морфологические стадии развития ИИФС:
-
I — латентная стадия, период бессимптомного течения (ранние изменения соединительной ткани);
-
II — стадия первичных минимальных проявлений (умеренная степень фиброза с увеличением коллагена I и III типа);
-
III — стадия диастолической дисфункции (выраженная степень фиброза со значимым преобладанием коллагена I типа);
-
IV — стадия систолической и диастолической дисфункции (тяжелая степень фиброза);
-
V — стадия коронарной ангиопатии (крайне тяжелая степень фиброза с вовлечением периферического коронарного русла) [23].
Вторичный ИИФС — фиброз, как правило, индуцированный ранее перенесенным инфарктом миокарда в результате ИБС.
Значимым отличием первичного и вторичного ИИФС от других форм фиброза является иммобилизация кардиомиоцитов, высокая степень их сдавления, что объясняет появление и прогрессирование сердечной недостаточности у таких больных вплоть до тяжелых состояний с выраженной коронарной ангиопатией (при экстраваскулярной констрикции артериол измененной соединительной тканью).
Для демонстрации вышеописанного приводим два клинических наблюдения.
В первом клиническом наблюдении представляем пример первичного ИИФС в стадии коронарной ангиопатии, когда пусковым механизмом фиброза явился целый комплекс причин.
Пациентка К., 53 лет поступила в отделение кардиологии НМХЦ им Н.И. Пирогова в тяжелом состоянии с жалобами на дискомфорт за грудиной и одышку при минимальной физической нагрузке (ходьба менее 150 м) и в покое, общую слабость, выраженные отеки нижних конечностей.
Из анамнеза известно, что длительное время страдает артериальной гипертензией, с максимальным подъемом АД до 200 и 100 мм рт.ст., адаптирована к 120–130 и 80 мм рт.ст. На фоне постоянной гипотензивной терапии АД стабилизировано. ИМ, ОНМК, СД 2 типа отрицает. После перенесенной вирусной пневмонии (SARS-CoV-2), в 2021 г., стала беспокоить одышка. Ухудшение состояния в начале 2022 г., когда жалобы появились при незначительной физической нагрузке. В июне 2022 г. была госпитализирована в отделение кардиологии по поводу декомпенсации ХСН. Выявлена нефропатия смешанного характера (гиперурикемический хронический тубулоинтерстициальный нефрит, ишемическая в рамках кардиоренального синдрома) с усугублением выраженности на фоне декомпенсации ХСН. На фоне проведенного лечения отмечена незначительная положительная динамика, в виде уменьшения отеков и одышки.
С 1986 г. диагностирован узловой зоб , после вирусной пневмонии (в 2021 г.) отмечено увеличение щитовидной железы (консультирована хирургом–эндокринологом, определены показания к оперативному лечению). В анамнезе остеохондроз грудного и поясничного отделов позвоночника; посттромботическая болезнь глубоких вен нижних конечностей; перенесенная тромбоэмболия легочной артерии от 2020 г.; нарушения ритма и проводимости сердца : AV-узловой ритм, пароксизмальная форма фибрилляции предсердий.
При поступлении установлен диагноз:
Основное заболевание : ИБС: Стабильная стенокардия IV ФК.
Фоновое заболевание : гипертоническая болезнь III стадии, контролируемая артериальная гипертензия (целевой уровень АД менее 130/80 мм рт.ст), риск ССО4. Дислипидемия. Нефропатия смешанного генеза.
Осложнения основного заболевания : хроническая сердечная недостаточность IIБ ФК III (NYNA). Умеренная легочная гипертензия (СДЛА 57 мм рт. ст.). Правосторонний малый гидроторакс. Нарушение ритма и проводимости сердца: AV-узловой ритм, пароксизмальная форма фибрилляции предсердий (риск тромбоэмболических осложнений по CHA2DS2VASc — 3 балла, риск кровотечений по HAS-BLED — 1 балл).
Сопутствующие заболевания : нетоксический одноузловой коллоидный загрудинный зоб 2 ст. по ВОЗ. Остеохондроз грудного и поясничного отделов позвоночника. Посттромботические изменения глубоких вен нижних конечностей. Нестенозирующий атеросклероз артерий нижних конечностей. Тромбоэмболия легочной артерии от 2020 г.
Эхокардиография : клапаны уплотнены, митральная регургитация — 1 степени, трикуспидальная регургитация — 1–2 степени. Дилатация предсердий (ЛП — 103 мл (норма до 65 мл); ПП — 87 мл (норма до 30 мл)). Умеренная гипертрофия стенок левого желудочка (ЛЖ) (МЖП — 1,6 см, З ст 1,4). Систолическая функция ЛЖ диффузно снижена, ФВ ЛЖ 48%. Признаки умеренной легочной гипертензии (СДЛА — 57 мм рт.ст.). Правосторонний малый гидроторакс.

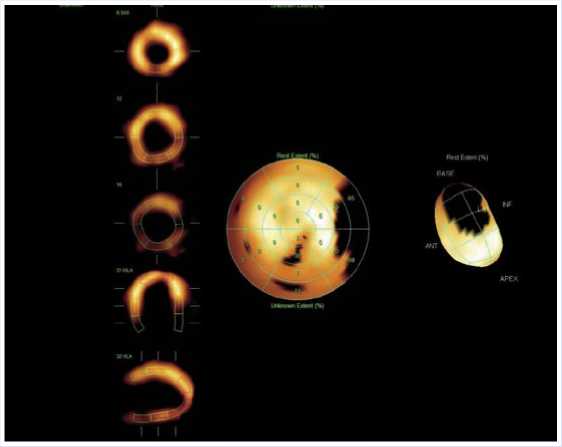
Рис. 1. Сцинтиграфия миокарда с 99тТс-Технетрилом в покое пациентки К., 53 лет.
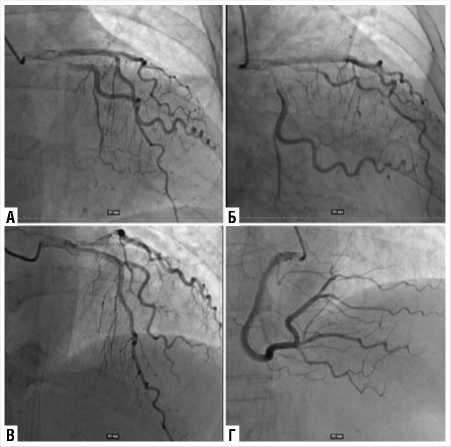
Рис. 3. Коронароангиография пациентки К.,53 лет. А, Б, В — бас-
сейн левой коронарной артерии, Г — бассейн правой коронарной артерии.
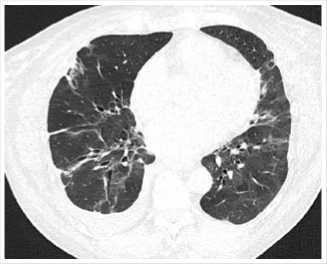
Рис. 2. Компьютерная томография органов грудной клетки пациентки К., 53 лет.
Сцинтиграфия миокарда с 99тТс-Технетрилом в покое : сцинтиграфические признаки снижения перфузии в области боковой стенки ЛЖ (частично базальные и средние сегменты), соответствующие гибернированному миокарду указанной локализации. Зона поражения 10–12%, диффузное снижение регионального систолического утолщения (Рис. 1).
Компьтерная томография органов грудной клетки: пневматизации паренхимы обоих легких снижена, преимущественно в периферических отделах определяются множественные полиморфные участки уплотнения (фиброзное изменения, ателектазы на уровне субсегментарных бронхов). В нижних долях обоих легких утолщение междолькового интерстиция, участки снижения воздушности. Изменения в легких соответствуют поствоспалительным участкам пневмофиброза. Правосторонний малый гидроторакс. Узловое образование правой доли щитовидной железы. Лимфо-аденопатия средостения. Грыжа пищеводного отверстия диафрагмы (Рис. 2).
Учитывая жалобы, клиническое проявление сердечной недостаточности, данные обследования, проведена коро-нароангиография, однако атеросклеротического поражения венечного русла выявлено не было (Рис. 3).
В вечерние часы того же дня у пациентки появились жалобы на общую слабость, тошноту, эпизод рвоты. Отмечалась тенденция к гипотонии. В связи с последующим усугублением тяжести состояния (гипотония, брадикардия) пациентка переведена в реанимационное отделение. Верифицированы сложные нарушения ритма и проводимости сердца, дыхательная недостаточность, водноэлектролитные нарушения, нарушения метаболизма (лактат-ацидоз, гипергликемия). Проводилась инотропная терапия, и в связи с выраженной дыхательной недостаточностью переведена на искусственную вентиляцию легких.
Эхокардиография : в положении лежа на спине сепарации листков перикарда не лоцируется. Насосная функция сердца диффузно значительно снижена, убедительных зон нарушения локальной сократимости не выявлено. Правые камеры сердца не расширены, по размерам меньше левых. Оценка внутрисердечной гемодинамика не представляется возможной (прогрессирующая брадикардия, вплоть до асистолии).
В 22:40 отметилось развитие фибрилляции желудочков. Кардиоверсия
200 кДЖ (безуспешно), комплекс реанимационных мероприятий неэффективен, в 23:50 констатирована биологическая смерть.
По данным гистоморфологиче-ского исследования выявлен тотальный миокардиальный склероз — иммобилизирующий интерстициальный фиброз сердца (Рис. 4, 5).
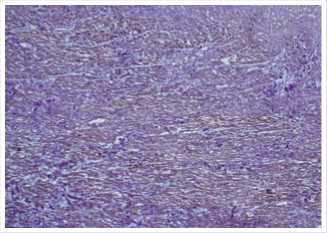
Рис. 4. Диффузный склероз с иммобилизацией кардиомиоцитов (окраска по Массону, увеличение х80).
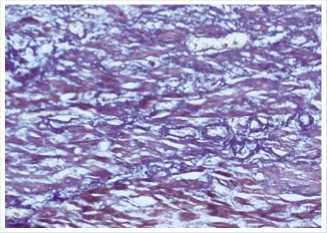
Рис. 5. Иммобилизирующий интерстициальный фиброз сердца (окраска по Массону, увеличение х 200).

Рис. 7. Иммобилизирующий интерстициальный фиброз сердца, диффузная экспрессия металлопротеиназ-9 (иммуногистохимическое исследование, увеличение х40).

Рис. 8. Иммобилизирующий интерстициальный фиброз сердца, диффузная экспрессия металлопротеиназ-9 (иммуногистохимическое исследование, увеличение х200).

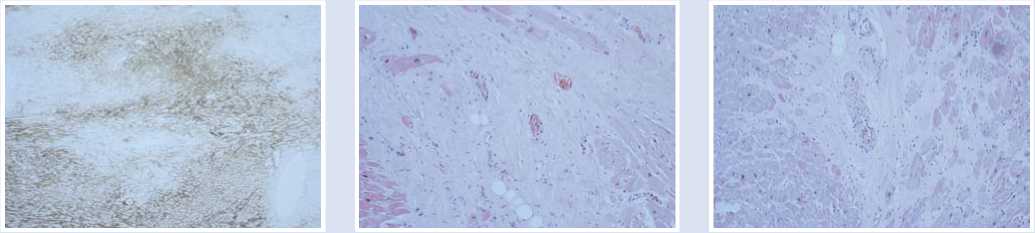
Рис. 6. Иммобилизирующий интерстициальный фиброз сердца, диффузное определение экспрессии тенасцина-С (иммуногистохимическое исследование, увеличение х40).
Рис. 9. Крайне тяжелая степень фиброза со значительным сдавлением коронарных артериол (окраска гематоксилином и эозином, увеличение х200).
Рис. 10. Стадия коронарной ангиопатии первичного ИИФС (окраска гематоксилином и эозином, увеличение х400).
Иммуногистохимическим методом была определена экспрессия фиброгенных маркеров (тенасцин-С, металлопротеиназы и др.) на разных участках миокарда, что свидетельствовало о диффузном распространении фиброза (Рис. 6–8).
В представленном клиническом наблюдении выявлена стадия крайне тяжелой степени изменения соединительной ткани при первичном ИИФС с вовле- чением периферического коронарного русла (стадия коронарной ангиопатии) (Рис. 9, 10). У пациентки отмечались признаки коронарной недостаточности, при этом положительного ответа на инотропную медикаментозную терапию не происходило.
Вирусная пневмония, эндокринные заболевания, нефропатия — все это послужило пусковым механизмом к развитию первичного ИИФС , который клинически проявлялся сердечной недостаточностью с нарушением ритма и проводимости сердца. Отмечалось диффузное снижение сократительной функции сердца по эхокардиографии, появление зон гибернированного миокарда по данным сцинтиграфии. При этом видимых изменений венечного русла при коронарографии обнаружено не было. А экстраваскулярная иммобилизация коронарных артериол верифицированна только при гистоморфологическом исследовании.
В следующем клиническом наблюдении приводим пример вторичного (индуцированного) ИИФС , когда причиной и пусковым механизмом его развития послужил инфаркт миокарда.
Пациент М., 68 лет поступил в клинику грудной и сердечно-сосудистой хирургии им. Святого Георгия НМХЦ им. Н.И. Пирогова с жалобами на периодически возникающее ощущение дискомфорта в прекардиальной области, одышку при ходьбе и периодически даже в покое.
Из анамнеза известно, что в течение нескольких лет страдает гипертонической болезнью с максимальным повышением АД до 150 и 90 мм рт.ст. Адаптирован к АД 130 и 80 мм рт.ст. Медикаментозную терапию постоянно не принимал, только при повышении АД. ОНМК, сахарный диабет отрицает. С марта 2022 г. беспоко- или загрудинные боли, возникавшие при физической нагрузке и проходившие в покое. В апреле 2022 г. был госпитализирован в областную больницу с приступом интенсивных давящих болей в области груди. Диагностирован первичный инфаркт миокарда. В ходе обследования проведена коронарография, выявившая многососудистое стенозирующее атеросклеротическое поражение коронарных артерий.
Коронарография : левый тип кровоснабжения, ствол левой коронарной артерии (ЛКА) — стеноз в проксимальной 1/3 60%, стеноз дистальной 1/3 90%; передняя межжелудочковая артерия (ПМЖА) — стеноз проксимальной 1/3 60%; интемедиальная артерия (ИМА) — стеноз 60%; задняя базальная ветвь от огибающей артерии (ЗБВ ОА) — стеноз 60%, задняя межжелудочковая ветвь от огибающей артерии (ЗМЖВ ОА) — стеноз 50-60%; правая коронарная артерия (ПКА) — окклюзирована в проксимальном и среднем сегменте, дистальные сегменты контрастируются через внутрисистемные коллатерали (Рис. 11).
Эхокардиография: камеры сердца расширены. Расширение левого предсердия. Глобальная систолическая функция ЛЖ — 50%. Локальная систолическая функция ЛЖ нарушена: выраженный гипокинез базального и среднего сегментов задне-боковой стенки ЛЖ, нормокинез верхушечного; выраженный гипокинез базального сегмента нижней стенки ЛЖ. Недостаточность митрального клапана с регургитацией 0–1 степени. Недостаточность аортального клапана с регургитацией 1 степени. Диастолическая функция ЛЖ изменена по I типу. Признаков повышения расчетного давления в ЛА не выявлено.
Сцинтиграфия миокарда с 99тТс-Технетрилом в покое : сцинтигра-
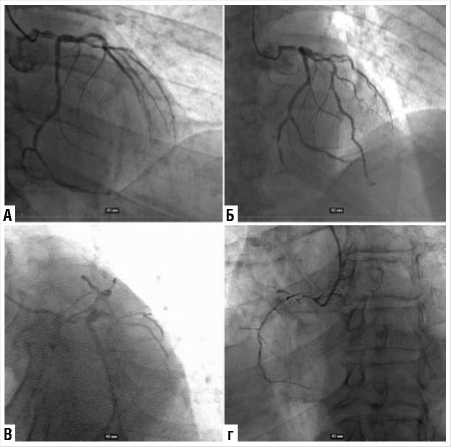
Рис. 11. Коронароангиография пациента М.,68 лет. А, Б, В — бассейн левой коронарной артерии, Г — бассейн правой коронарной артерии.
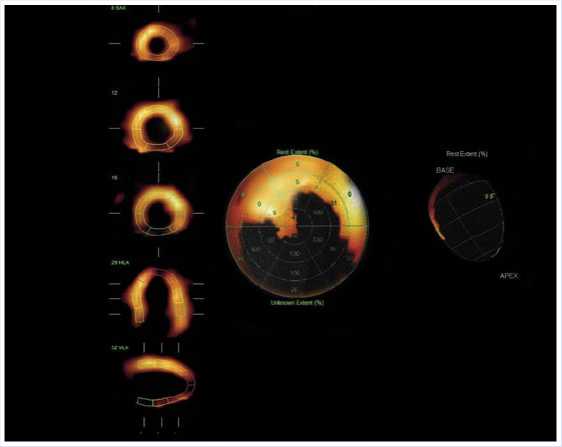
Рис. 12. Сцинтиграфия миокарда с 99тТс-Технетрилом в покое пациента М., 68 лет.
фические признаки снижения перфузии в области задне-боковой, задней стенок, задней МЖП, верхушки, передней, переднебоковой стенок, соответствующие рубцовым изменениям с гибернированным миокардом, указанной локализации. Зона поражения 50%. Сократительная способность миокарда ЛЖ умеренно снижена: ОФВ 49%. Признаки снижения регионального систолического утолщения в зоне локальной гипоперфузии. Жизнеспособный миокард 48%. Необратимые рубцовые изменения 12% (Рис. 12).
Установлен диагноз:
Основное заболевание: ИБС: стенокардия напряжения IV ФК. Постинфарктный кардиосклероз (инфаркт миокарда от апреля 2022 г.) Стенозирующий атеросклероз коронарных артерий.
Фоновое заболевание: артериальная гипертензия III стадии, риск ССО 4.
Осложнения основного заболевания: хроническая сердечная недостаточность IIБ ФК III (NYNA).
Сопутствующие заболевания: хронические гастрит и холецистит вне обострения; атеросклероз брахиоцефальных артерий и артерий нижних конечностей без гемодинамически значимых стенозов.
Учитывая IV ФК стенокардии напряжения, многососудистое поражение коронарных артерий, высокий риск развития жизнеугрожающих осложнений и бесперспективность консервативной терапии, пациенту предложено аортокоронарное шунтирование в бассейне пораженных артерий.
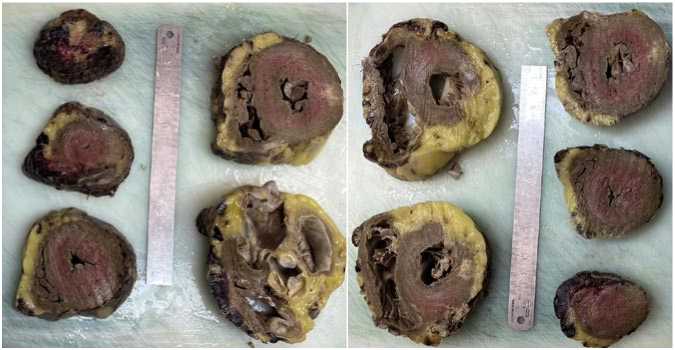
Рис. 13. Макропрепарат сердца пациента М., 68 лет. Визуализируется сформированный рубец по задней стенке миокарда левого желудочка в результате инфаркта от апреля 2022 г.
Выполнена операция: аорто-коронарное аутовенозное шунтирование ПМЖА, ВТК, ИМА в условиях искусственного кровообращения.
При интраоперационном флоуме-трическом контроле потока крови по шунтам, установлены адекватные показатели (объемная скорость кровотока (Q) — более 20 мл/мин., индекс сопротивления (PI) — менее 5 ед., диастолическое наполнение (DF) — более 50%).
По завершению операции и остановки аппарата искусственного кровообращения проявилась тяжелая сердечная недостаточность с последующей стойкой гипотензией и асистолией, рефрактерной к электрокардиостимуляции, что потребовало длительного вспомогательного искусственного кровообращения. Весь комплекс мероприятий восстановления полноценной сердечной деятельности был безуспешным. При времени пережатия аорты на основном этапе 30 мин., общее время искусственного кровообращения составило 270 мин. Констатирована биологическая смерть пациента.
Результаты аутопсии свидетельствуют о том, что помимо репаративного фиброза, который развился с образованием замещающего рубца на месте инфаркта миокарда от апреля 2022 г., выявлен диффузный ИИФС на разных стадиях формирования (Рис. 13–17).
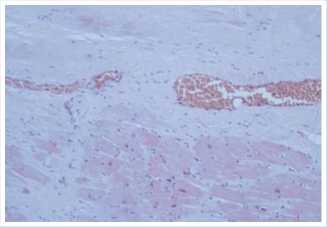
Рис. 14. Микропрепарат сердца пациента М., 68 лет, индуцированный ИИФС, экс-траваскулярное сдавление коронарных артериол, зоны сформированного рубца (окраска гематоксилином и эозином, увеличение х400).
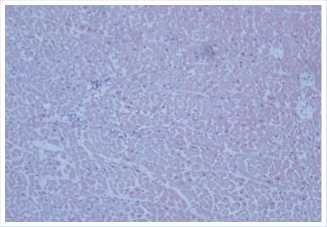
Рис. 15. Диффузное распространение индуцированного ИИФС, ранние стадии фиброгенеза (примерно 3–4 недели), видимая инфильтрация полинуклеарами (окраска гематоксилином и эозином, увеличение х100).
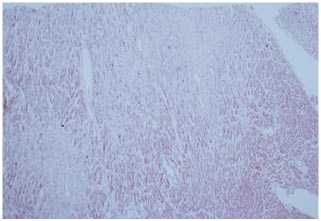
Рис. 16. Диффузное распространение индуцированного ИИФС, ранние стадии формирования (приблизительно 1 месяц) (окраска гематоксилином и эозином, увеличение х80).
В данном случае рубцовый очаг после инфаркта миокарда индуцировал формирование иммобилизирующего интерстициального фиброза . В перифокальной соединительнотканной зоне под действие специфических медиаторов, подобно цепной реакции, активизировался процесс «ползучего» развития повреждения интерстиция с выделением матрикс-
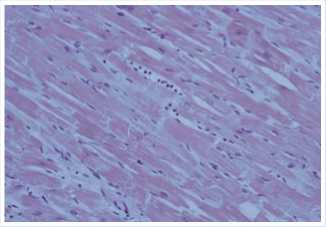
Рис. 17. Индуцированный ИИФС (окраска гематоксилином и эозином, увеличение х400).
ных металлопротеиназ, перестройкой межуточной ткани в отдаленных зонах. Диффузный фиброз утяжелил состояние пациента, а сердечную недостаточность в этом случае следует расценивать как совокупность двух ее причин: с одной стороны — ишемической болезни сердца, а с другой — индуцированного ИИФС неишемизированных зон сердца. Реваскуляризация миокарда не привела к восстановлению сократимости, повышенная жесткость миокарда в результате диффузных изменений соединительной ткани обусловила невосприимчивость к инотропной поддержке.
Заключение
Иммобилизирующий интерстициальный фиброз сердца — самостоятельное заболевание и одна из главных причин развития хронической сердечной недостаточности.
В основе первичного ИИФС лежат изменения соединительной ткани, которые часто бывают первопричиной дисфункции миокарда: происходит механическое сдавление здоровых кардиомиоцитов извне, ограничение их нормального движения и функционирования. Развитие заболевания происходит постепенно, начиная с незначительного увеличения объема интерстиция, вплоть до формирования грубого фиброза со сдавлением артериол.
В основе вторичного (индуцированного) ИИФС лежит процесс диффузных изменений интерстициальной ткани здоровой части миокарда в результате стимуляции его сформировавшимися постинфарктными рубцами.
Патофизиологическая гетерогенность фиброзных состояний сердца усложняют выбор тактики лечения больных сердечно-сосудистыми заболеваниями. Особо стоит отметить, что у пациентов, перенесших острый инфаркт миокарда, с одной стороны, необходимо как можно раньше в программу лечения включить меры предупреждения развития индуцированного ИИФС здоровой части миокарда, с другой стороны, такой терапией можно замедлить формирование полноценного рубца в зоне инфаркта и таким образом повысить риск разрыва стенки сердца. Поэтому следует учитывать сроки формирования надежного рубца и проявлять разумную сдержанность в расширении физической активности после острого инфаркта миокарда. Исследования в этой области сердечной патологии продолжаются.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Первичный и вторичный (индуцированный) иммобилизирующий интерстициальный фиброз сердца
- Frangogiannis NG. Cardiac fibrosis. Cardiovasc. Res. 2020; 117: 1450-1488. doi: 10.1093/cvr/cvaa324.
- Eijgenraam TR, Silljé HHW, de Boer RA. Current understanding of fibrosis in genetic cardiomyopathies. Trends Cardiovasc. Med. 2019; 30: 353-361. doi: 10.1016/j.tcm.2019.09.003.
- Treibel TA, López B, González A, et al. Reappraising myocardial fibrosis in severe aortic stenosis: An invasive and non-invasive study in 133 patients. Eur. Heart J. 2017; 39: 699-709. doi: 10.1093/eurheartj/ehx353.
- Hinderer S, Schenke-Layland K. Cardiac fibrosis–A short review of causes and therapeutic strategies. Adv. Drug Deliv. Rev. 2019; 146: 77-82. doi: 10.1016/j.addr.2019.05.011.
- Li L, Zhao Q, Kong W. Extracellular matrix remodeling and cardiac fibrosis. Matrix Biol. 2018; 68: 490-506. doi: 10.1016/j.matbio. 2018.01.013.
- Krejci J, Mlejnek D, Sochorova D, Nemec P. Inflammatory Cardiomyopathy: A Current View on the Pathophysiology, Diagnosis, and Treatment. Biomed. Res. Int. 2016; 2016: 4087632. doi: 10.1155/2016/4087632.
- Imanaka-Yoshida K, Tawara I, Yoshida T. Tenascin-C in cardiac disease: A sophisticated controller of inflammation, repair, and fibrosis. Am. J. Physiol.-Cell Physiol. 2020; 319: 781-796. doi: 10.1152/ajpcell.00353.2020.
- Sygitowicz G, Maciejak-Jastrzębska A, Sitkiewicz D. A Review of the Molecular Mechanisms Underlying Cardiac Fibrosis and Atrial Fibrillation. J. Clin. Med. 2021; 10: 4430. doi: 10.3390/jcm10194430.
- Cowling RT, Kupsky D, Kahn AM, et al. Mechanisms of cardiac collagen deposition in experimental models and human disease. Transl Res. 2019; 209: 138-155. doi:10.1016/j.trsl. 2019.03.004.
- Souders CA, Bowers SL, Baudino TA. Cardiac fibroblast: the renaissance cell. Circ Res. 2009; 105: 1164-76.
- González A, López B, Ravassa S, et al. The complex dynamics of myocardial interstitial fibrosis in heart failure. Focus on collagen cross-linking. Biochim. Et Biophys. Acta Mol. Cell Res. 2019; 1866: 1421-1432. doi: 10.1016/j.bbamcr.2019.06.001.
- Caulfield JB, Norton P, Weaver RD. Cardiac dilatation associated with collagen alterations. Mol. Cell Biochem. 1992; 116: 171-179. doi: 10.1007/BF00299396.
- Frangogiannis NG. Cardiac fibrosis: cell biological mechanisms, molecular pathways and therapeutic opportunities. Mol Aspects Med. 2019; 65: 70-99.
- Prabhu SD Frangogiannis NG. The Biological Basis for Cardiac Repair After Myocardial Infarction: From Inflammation to Fibrosis. Circ Res 2016; 119: 91-112.
- Frangogiannis NG. The Extracellular Matrix in Ischemic and Nonischemic Heart Failure. Circ. Res. 2019; 125: 117-146. doi: 10.1161/ CIRCRESAHA.119.311148.
- Dusenbery SM, Jerosch-Herold M, Rickers C, et al. Myocardial extracellular remodeling is associated with ventricular diastolic dysfunction in children and young adults with congenital aortic stenosis. J Am Coll Cardiol. 2014; 63: 1778-85.
- Schnee JM, Hsueh WA. Angiotensin II, adhesion, and cardiac fibrosis. Cardiovasc Res. 2000; 46: 264-8.
- Leask A. Getting to the heart of the matter: new insights into cardiac fibrosis. Circ Res. 2015; 116: 1269-76.
- Wenzl FA, Ambrosini S, Mohammed SA, et al. Inflammation in Metabolic Cardiomyopathy. Front. Cardiovasc. Med. 2021; 8: 742178. doi: 10.3389/fcvm.2021.742178.
- Imanaka-Yoshida K. Inflammation in myocardial disease: From myocarditis to dilated cardiomyopathy. Pathol. Int. 2020; 70: 1-11. doi: 10.1111/pin.12868.
- Bovelli D, Plataniotis G, Roila F. Cardiotoxicity of chemotherapeutic agents and radiotherapy-related heart disease: ESMO clinical practice guidelines. Ann Oncol. 2010; 21(5): v277-82.
- Шевченко Ю.Л. Иммобилизирующий интерстициальный фиброз сердца. Часть I // Вестник НМХЦ им. Н.И. Пирогова. — 2022. — Т.17. — №2. — С.4-10. doi:10.25881/20728255_2022_17_2_4.
- Шевченко Ю.Л., Плотницкий А.В., Судиловская В.В. и др. Морфология и маркеры иммобилизирующего интерстициального фиброза сердца // Вестник НМХЦ им. Н.И. Пирогова. — 2022. — Т.17. — №3. — С.84-93. doi: 10.25881/20728255_2022_17_3_84.
- Шевченко Ю.Л., Ульбашев Д.С. Иммобилизирующий интерстициальный фиброз сердца. Часть II // Вестник НМХЦ им. Н.И. Пирогова. — 2022. — Т.17. — №3. — С.4-10. doi: 10.25881/20728255_2022_17_3_4.


