Первый опыт выполнения трансаксиллярных эндоскопических операций на эндокринных органах шеи
Автор: Глушков П.С., Азимов Р.Х., Шемятовский К.А., Горский В.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Хирургия головы и шеи
Статья в выпуске: 1 (79), 2022 года.
Бесплатный доступ
Введение. Разрез по Кохеру оставался единственным адекватным доступом для операций на щитовидной и паращитовидных железах на протяжении более 100 лет. Развитие технологий позволило разработать и внедрить в клиническую практику минимально инвазивные доступы к эндокринным органам шеи, одним из которых является эндоскопический трансаксиллярный.Цель исследования. Оценить результаты первого опыта выполнения эндоскопических операций на щитовидной и паращитовидных железах.Материалы и методы. С сентября 2018 г. по июнь 2021 года в отделении хирургии ЦКБ РАН было выполнено 52 трансаксиллярных эндоскопических операций на щитовидной железе и 6 эндоскопических паратиреоидэктомий. Среди эндоскопических операций на щитовидной железе было выполнено 26 тиреоидэктомий, 17 гемитериоидэктомий, 9 экстирпаций доли щитовидной железы с перешейком.Результаты. Среднее время выполнения эндоскопических операций на щитовидной железе составило от 82,5±12,1минут для гемитиреоидэкмий до 117,5±21,6 минут до тиреоидэктомий при раке щитовидной железы. Средний койко-день составил 4,5±1,2 суток. Основным преимуществом операции, по мнению пациентов, было отсутствие разреза на шее. На этапе освоения техники было отмечено 2 интраоперационных и одно послеоперационное осложнение.Заключение. Первый опыт выполнения эндоскопических трансаксиллярных операций показал перспективность и безопасность доступа при соблюдении стандартной техники операции.
Рак щитовидной железы, эндоскопическая тиреоидэктомия, хирургия щитовидной железы
Короткий адрес: https://sciup.org/142234541
IDR: 142234541 | УДК: 617-089
First experience of performing transaxillary endoscopic surgery on the endocrine organs of the neck
Introduction. Te Kocher incision remained the only adequate access for operations on the thyroid and parathyroid glands for over 100 years. Te development of technologies made it possible to develop and introduce into clinical practice minimally invasive approaches to the endocrine organs of the neck, one of which is the endoscopic transaxillary.Purpose of the study. To evaluate the results of the frst experience of performing endoscopic operations on the thyroid and parathyroid glands.Materials and methods. From September 2018 to June 2021, 52 transaxillary endoscopic operations on the thyroid gland and 6 endoscopic parathyroidectomies were performed at the Department of Surgery of the Central Clinical Hospital of the Russian Academy of Sciences. Among endoscopic operations on the thyroid gland, 26 thyroidectomies, 17 hemiterioidectomies, and 9 extirpations of the thyroid lobe with an isthmus were performed.Results. Te average time to perform endoscopic operations on the thyroid gland ranged from 82,5-12,1 minutes for hemithyroidectomy to 117.5-21.6 minutes for thyroidectomy about thyroid cancer. Te average bed-day was 4.5 ± 1.2 days. During the frst two days, all patients noted a slight pain syndrome, which was stopped by NSAIDs. Te main advantage of the operation, according to patients, was the absence of an incision in the neck. At the stage of mastering the technique, 2 intraoperative and one postoperative complications were noted.Conclusion. Te frst experience in performing endoscopic transaxillary operations has shown the promising and safe access provided that the standard surgical technique is followed.
Текст научной статьи Первый опыт выполнения трансаксиллярных эндоскопических операций на эндокринных органах шеи
Созданная в начале XX в. хирургическая техника операций на щитовидной железе (ЩЖ) не претерпевала никаких существенных изменений до начала -90х годов. Появление новых электрохирургических инструментов, прежде всего ультразвуковых ножниц, избавило хирургов от необходимости накладывать множество зажимов и переводить километры лигатур. Затем внедрение новых эндоскопических методов постепенно дошло и до хирургии ЩЖ, что привело к появлению более десятка различных миниинвазивных доступов. Одним из таких методов является трансаксиллярная эндоскопическая тиреоидэктомия (ТАТЭ) и паратиреоидэктомия [1]. Первым опытом выполнения подобных операций хотим поделиться в данной статье.
Цель: оценить результаты первого опыта выполнения эндоскопических операций на щитовидной и паращитовидных железах.
Материалы и методы
Характеристика пациентов
В период с сентября 2018 по июнь 2021 года нами проведено 52 трансакциллярных эндоскопических операций на щитовидной железе и 6 трансаксиллярных эндоскопических паратиреоидэктомий. Среди пациентов было 10 мужчин (средний возраст 54,710,1± лет) и 49 женщин (средний возраст 44,9±10,5 лет) (табл. 1).
Как видно из представленной таблицы, большинство прооперированных мужчин относилось к группе пожилых, тогда как для женщин был характерен преимущественно молодой и средний возраст. Среди мужчин молодого возраста операции выполнялись по поводу узлового зоба, у пожилых по поводу узлового и диффузного токсического зоба. Все возрастные группы женщин преимущественно оперировались по поводу узлового зоба и в одном случае – по поводу хронического аутоиммунного тиреоидита.
В таблице 2 представлено распределение больных по индексу массы тела, что немаловажно для выполнения эндоскопических операций на шее, т. к. оперировать худых больных намного сложнее.
Средний индекс массы тела у оперированных пациентов составлял 29,9±6,6 кг. Среди мужчин преобладали пациенты с индексом массы тела в пределах от 30 до 40 кг., а среди женщин – от 25 до 35 кг.
Сопутствующая патология у пациентов была в основном представлена гипертонической болезнью (18 больных), ишемической болезнью сердца (4), постменопаузальным остеопорозом (2), подагрой (1).
Методы обследования
Перед операцией пациентам проводили необходимый объем обследования, включающий физикальные, лабораторные (стандартные клинические и биохимические анализы), инструментальные методы и обязательную консультацию специалиста- эндокринолога. При необходимости в дополнении к стандартной ЭКГ выполнялись эхокардиография и консультация кардиолога.
Таблица 1
Распределение пациентов по полу , возрасту и нозологическим формам
Table 1
Distribution of patients by sex, age, and nosological forms
|
Пол/нозология Sex / nosology |
Возраст (лет) Age (years) |
Количество Amount |
||
|
18–44 |
45–59 |
60–74 |
58 |
|
|
Мужчины (n) Men (n) |
2 |
4 |
4 |
10 |
|
Узловой зоб Nodular goitre |
2 |
4 |
3 |
9 |
|
Диффузный токсический зоб Diffuse toxic goiter |
– |
– |
1 |
1 |
|
Женщины (n) Women (n) |
11 |
21 |
17 |
48 |
|
Узловой зоб Nodular goitre |
5 |
22 |
10 |
36 |
|
Диффузный токсический зоб Diffuse toxic goiter |
2 |
2 |
– |
4 |
|
Хронический тиреоидит Chronic thyroiditis |
– |
– |
2 |
2 |
|
Первичный гиперпаратиреоз, аденома околощитовидной железы Primary hyperparathyroidism, parathyroid adenoma |
– |
3 |
3 |
6 |
Таблица 2
Распределение пациентов по индексу массы тела
Table 2
Distribution of patients by body mass index
|
Пол Sex |
Индекс массы тела Body mass index |
Всего Amount |
||||
|
<24 |
25–30 |
30–35 |
35–40 |
>40 |
||
|
Мужчины (n) Men (n) |
– |
2 |
4 |
3 |
1 |
10 |
|
Женщины (n) Women (n) |
1 |
22 |
15 |
8 |
2 |
48 |
Ультразвуковое исследование (УЗИ) ЩЖ выполняли на аппарате Logic V2 (General Electric, США). Определяли объем ЩЖ, характер структурных изменений, состояние регионарных лимфатических узлов со стратификацией рисков по шкале TI-RADS. Тонкоигольная аспирационная биопсия узловых образований под контролем УЗИ с дальнейшим цитологическим исследованием выполнена 46 больным c оценкой полученных результатов по классификации Bethesda.
Большинство пациентов имело избыточную массу тела (ИМТ >25) и 1–2 степень увеличения ЩЖ, что не создавало технических трудностей при планировании и выполнении эндоскопического оперативного вмешательства. При цитологическом исследовании узловых образований у 20 пациентов выявлены доброкачественные изменения, у 10 – подозрение на фолликулярную опухоль, у 7 – подозрение на малигнизацию (Bethesda 5), а у 8 пациентов при цитологии была поставлена категория 6 по Bethesda. Показания к операции и их объем определяли согласно национальным клиническим рекомендациям Российской ассоциации эндокринологов [2, 3].
Подготовка больных к операции
Подготовка пациентов к операции была стандартной: голод за 12 часов до операции, очистительные клизмы утром и вечером. В качестве антибактериальной профилактики использовали введение цефазолина 2,0 в/в за 30 мин до операции согласно национальным клиническим рекомендациям по профилактики хирургической инфекции [4]. Специальной медикаментозной коррекции не проводили. Пациенты с диффузным токсическим зобом на момент операции имели медикаментозно компенсированное эутиреоидное состояние. У всех пациентов с аденомой околощитовидной железы проводили сцинтиграфическое исследование околощитовидных желез с 99mTc-технетрилом.
Принципиально важным аспектом подготовки пациентов мы считаем разметку точек доступа и патологического образования ЩЖ под УЗ наведением. Эта необходимая процедура облегчает ориентировку во время вмешательства и сокращает его сроки (рис. 1). При этом неоднократно убеждались, что проекции на кожу ключиц, границ подмышечных впадин в горизонтальном и вертикальном положении не совпадают и могут отличаться у разных пациентов на 5–7 см.
Техническое обеспечение операции
Операции выполняли под комбинированным эндотрахеаль-ным наркозом на аппаратуре фирмы «Karl Storz» (Германия) со стандартным оборудованием для выполнения эндоскопических операций. На этапе доступа использовали один 10 мм и два 5 мм троакара с винтовой резьбой без стилета и жесткий эндоскоп с углом обзора 30°, на этапе оперативного приема - ультразвуковой скальпель Harmonic (Ethicon, США), диссектор, граспер. У 2 больных потребовалось применение аппарата Ligasure для обработки щитовидных артерий большого диаметра во время операций по поводу хронического аутоиммунного тиреоидита и диффузного токсического зоба.
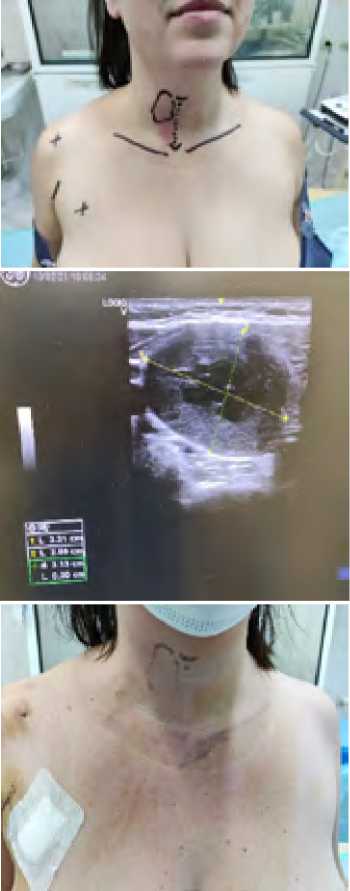
Рис.1. Разметка ориентиров до операции (а), данные
УЗИ (б), вид на 1 сутки после операции (c)
Fig. 1. Marking of landmarks before surgery (a), ultrasound data (b), view at 1 day after surgery (c)
Технические особенности выполнения операции и полученные результаты
По передней подмышечной линии со стороны измененной доли щитовидной железы выполнялся разрез кожи длинной около 30 мм. Используя палец, проводилась тупая препаровка подкожной клетчатки максимально возможного размера до уровня ключицы. Латеральным ориентиром создаваемой полости служил наружный край большой грудной мышцы. Далее в полость устанавливался 10 мм троакар с 300 оптикой. Вокруг первого 10 мм троакара накладывался кисетный шов для придания дополнительной герметичности полости в подкожной клетчатке. Первый рабочий 5 мм троакар устанавливался ниже 10 мм троакара по передней подмышечной линии. С использованием ультразвуковых ножниц ранее созданная полость в подкожной клетчатке расширялась, после чего устанавливался еще один 5 мм троакар выше камеры. Инсуффляция СО2 проводилась под давлением 6 мм рт. ст., при необходимости скорость потока увеличивали до 10 л/мин. Особое внимание уделялось разделению тканей в области ключицы, поскольку в этом месте слой подкожной жировой клетчатки наименее выражен, что может привести к термическому повреждению кожи изнутри.
Дальнейшую диссекцию тканей производили сразу за медиальным краем грудинно-ключично-сосцевидной мышцы. Волокна грудинно-подъязычной мышцы отводили кверху, а грудинно-щитовидную мышцу рассекали ультразвуковыми ножницами. Используя тракцию ЩЖ вниз с помощью ультразвуковых ножниц, пересекали верхние щитовидные сосуды как можно ближе к ткани самой железы во избежание повреждения верхнего гортанного нерва. Затем осуществляли тракцию ЩЖ кверху для идентификации трахеи. Нижние щитовидные сосуды пересекались ультразвуковым скальпелем. В одном случае у пациентки с хроническим аутоиммунным тиреоидитом и увеличением ЩЖ до 120 см3 пришлось использовать биполяр LigaSure 5 мм для проведения окончательного гемостаза. Для профилактики повреждения возвратного гортанного нерва в непосредственной близости от него пассивную браншу ультразвуковых ножниц всегда поворачивали в его сторону. Наш протокол проведения тиреоиэктомии подразумевал обязательное использование интраоперационного нейромониторинга с регистрацией нейро-мышечного ответа до и после резекции каждой доли ЩЖ. Выделение ткани заканчивали пересечением связки Берри. Удаленный орган извлекали в контейнере через центральный троакарный доступ. Ревизию области операции и окончательный гемостаз в ложе ЩЖ проводили при нулевом давлении углекислого газа, используя для лифтинга один из инструментов. В сочетании с увеличением давления на выдохе, это позволяло проверить гемостаз мелких венозных сосудов. Операцию заканчивали установкой активного дренажа через нижний троакарный доступ и наложением давящей повязки типа Дезо.
В таблице 3 представлено среднее время оперативных вмешательств на эндокринных органах шеи в зависимости от нозологической формы заболевания и выполненного оперативного приема.
Как видно из таблицы 3, время операции было закономерно больше при тиреоидэктомии, чем при гемитиреоидэктомии. Длительность операций, выполненных по поводу рака ЩЖ составляла в среднем около 2-х часов.
В таблице 4 приведены данные морфологической верификации у оперированных больных в сравнении предоперационными цитологическими результатами.
Таблица 3
Виды проведенных эндоскопических вмешательств на ЩЖ и среднее время их выполнения
Table 3
Types of operations on the thyroid gland and the average time to complete them
|
Нозология, по поводу которой были оперированы пациенты Nosology |
Вид операции Type of operation |
Кол - во пациентов Number of patients |
Время операции ( мин ) Operation time (minutes) |
|
Узловой зоб Nodular goiter |
Гемитиреоидэктомия Hemithyroidectomy |
17 |
82,5 ± 12,1 |
|
Многоузловой зоб Multinodular goiter |
Тиреоидэктомия Thyroidectomy |
13 |
121 ± 23,3 |
|
Хронический аутоиммунный тиреоидит Chronic autoimmune thyroiditis |
2 |
175 ± 22,1 |
|
|
Диффузный токсический зоб Diffuse toxic goiter |
5 |
110 ± 14,2 |
|
|
Рак щитовидной железы (Категория 5, 6 по Bethesda) Thyroid cancer (Bethesda 5,6) |
6 |
117,5 ± 21,6 |
|
|
Рак щитовидной железы (Категория 5, 6 по Bethesda) Thyroid cancer (Bethesda 5,6) |
Экстирпация доли ЩЖ с перешейком Extirpation of the thyroid lobe with isthmus |
9 |
68,5 ± 10,7 |
|
Первичный гиперпаратиреоз, аденома околощитовидной железы Primary hyperparathyroidism, parathyroid adenoma |
Паратиреоидэктомия Parathyroidectomy |
6 |
48,5 ± 12,7 |
На этапе освоения техники авторы статьи столкнулись с двумя интраоперационными и одним послеоперационным осложнениями. В одном случае возникло кровотечение из-за пересечения ультразвуковым скальпелем верхней щитовидной артерии, которое было остановлено аппаратом Ligasure. У другой пациентки кровотечение возникло из срединной щитовидной вены. Потребовалась конверсия для перевязки вены и остановки кровотечения. Еще в одном случае возник термический ожог кожи в области ключицы. У астеничных женщин кожа и подкожная мышца в этой области особенно тонки, и использование ультразвуковых ножниц может привести к появлению кожного ожога в этой области, выявляющегося в раннем послеоперационном периоде, что наблюдалась нами в одном случае (рис. 2).
Средний койко-день составил 4,5±1,2 суток. Все пациенты отмечали незначительный болевой синдром после операции, который купировался внутримышечным введением НПВС в первые сутки после вмешательства. Безусловным преимуществом операции, отмеченным пациентами, был хороший косметический эффект, заключавшийся в отсутствии разреза на шее.
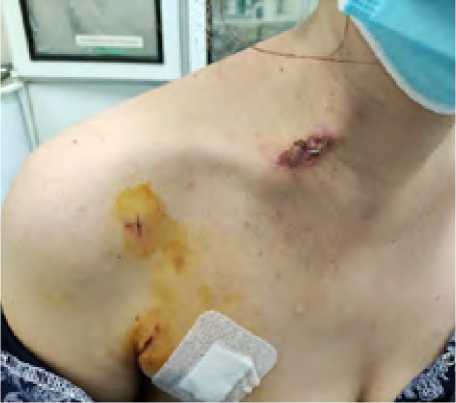
Рис . 2. Пациентка с ожогом кожи ультразвуковыми ножницами
Fig. 2. A patient with skin burns by ultrasonic scissors
Таблица 4
Характеристика результатов морфологического исследования
Characteristics of the results of the morphological study
Table 4
|
Первичная нозология Primary nosology |
Категория цитологии по Bethesda Cytology by Bethesda |
Количество пациентов Number of patients |
Результаты гистологического исследования Histological examination results |
|
Узловой и многоузловой зоб Nodular and multinodular goiter |
В2 |
20 |
Коллоидный зоб – 15 Colloidal goiter - 15 Фолликулярная аденома – 5 Follicular adenoma - 5 |
|
В2 |
4 |
Коллоидный зоб – 2 Colloidal goiter - 2 Фолликулярная аденома – 2 Follicular adenoma - 2 |
|
|
В4 |
6 |
Хронический тиреоидит – 1 Chronic thyroiditis Фолликулярная аденома – 3 Follicular adenoma - 3 Папиллярный рак – 2 Papillary cancer - 2 |
|
|
В5 |
7 |
Фолликулярная аденома – 3 Папиллярный рак – 4 Follicular adenoma - 3 Papillary cancer - 4 |
|
|
В6 |
8 |
Папиллярный рак – 8 Papillary cancer - 8 |
|
|
Диффузный токсический зоб Diffuse toxic goiter |
- |
5 |
Диффузный токсический зоб – 5 Diffuse toxic goiter - 5 |
|
Хронический аутоиммунный тиреоидит Chronic autoimmune thyroiditis |
B2 |
1 |
Хронический аутоиммунный тиреоидит – 2 Chronic autoimmune thyroiditis -2 |
|
B4 |
1 |
||
|
Первичный гиперпаратиреоз, аденома околощитовидной железы Primary hyperparathyroidism, parathyroid adenoma |
- |
6 |
Светлоклеточная аденома околощитовидной железы – 6 Clear cell adenoma of the parathyroid gland - 6 |
Обсуждение
Первая трансаксиллярная эндоскопическая тиреоидэктомия была выполнена в 1999 году Ikeda и Ohgami [1, 5]. В англоязычной литературе она известна под названием TATE (transaxillary totally endoscopic thyroid lobectomy). Развитие отечественной мини-инвазивной хирургии ЩЖ подробно описано у ряда авторов [6, 7]. Если вспомнить историю развития эндоскопической хирургии, то следует отметить, что некоторые методики быстро нашли широкое распространение и остались с нами навсегда, а другие, сверкнув в течение двух-трех лет, не прижились. К последним следует отнести операции SILS и NOTES, не получившие отклик у хирургов. Будем надеяться, что операции ТАТЕ войдут в арсенал хирурги- ческих вмешательств не только из-за косметического эффекта. Преимуществами метода являются хороший обзор ключевых структур (околощитовидные железы, возвратный гортанный нерв, сосудистый пучок) в сочетании с минимальными разрезами кожи, расположенными в подмышечной впадине.
Показаниями для ТАТЕ у пациентов с узловыми образованиями ЩЖ являются их размеры не более 6 см в наибольшем измерении, а у пациентов диффузным токсическим зобом объем органа не более 100 см3. В последние годы показания к данной операции были дополнены дифференцированным раком ЩЖ без признаков регионального и отдаленного метастазирования и прорастания опухоли в окружающие ткани [8].
Одним из основных противопоказаний к данному вмешательству считаются проведенные ранее оперативные вмешательства на ЩЖ [9]. Однако наш скромный опыт проведения подобной операции после ранее выполненной субтотальной резекции контрлатеральной доли ЩЖ позволил усомниться в наличии технических ограничений. Можно предположить, что по мере накопления опыта появится возможность в ряде случаев расширять показания. Еще одним противопоказанием к операции является загрудинное расположение узлов. По нашему мнению, вопрос проведения эндоскопической операции в подобных ситуациях зависит от личного опыта хирурга. Если это загрудинный, а не истинно грудной зоб, он может быть выведен из-под грудины с помощью эндоскопических инструментов.
Безусловно, успешному выполнению ТАТЕ должно предшествовать тщательное дооперационное обследование пациента. Стандартными методами обследования, предшествующими любой операции на ЩЖ, являются: исследование гормонального статуса, УЗИ ЩЖ, проведение пункционной тонкоигольной биопсии, при необходимости проведение МСКТ шеи [10, 11]. Как и при любом оперативном вмешательстве, необходима оценка общего статуса пациента, его коморбидности и ИМТ. Все рекомендации выполнялись неукоснительно, что позволило избежать ненужных осложнений у наших больных как в ближайшем, так и в отдаленном послеоперационном периоде.
Следует учитывать специфические параметры, которые необходимо оценивать при выборе методики операции – тип телосложения, объем и длину шеи, проекцию на шею гортани и ЩЖ, подвижность верхнего плечевого пояса, возможность поднятия пациентом руки в виде «салюта». По нашему мнению, женщина с высоким ИМТ, но длинной шеей и высоко расположенной щитовидной железой, является более подходящим кандидатом для операции, чем худой мужчина с короткой шеей, ограниченной подвижностью плечевого пояса и загрудинным расположением узла.
В ходе обследования следует акцентировать внимание на локальные данные образования ЩЖ: размер, смещаемость, плотность, возможное загрудинное положение. Важным для дальнейшей интраоперационной навигации является разметка ЩЖ на поверхности шеи с помощью УЗ датчика.
Существуют различные технические нюансы при выполнении вмешательства. Для создания необходимой визуализации оно может выполняться как с использованием газовой инсуффляции (эндоскопическая тиреоидэктомия), так и с применением специальных ретракторов (эндоскопически ассистированная тиреоидэктомия). Считается, что использование газа позволяет минимизировать длину кожных разрезов в подмышечной впадине и травму тканей по ходу установленных троакаров [12, 13]. Мы выполняли операции с использованием газовой инсуффляции под давлением 6–10 мм рт. ст., которая обеспечивала хорошее рабочее пространство во всех случаях.
По литературным данным использование ТАТЕ не приводит к увеличению частоты послеоперационных осложнений по сравнению с открытыми операциями [14, 15]. Более того, хороший обзор под восьмикратным оптическим увеличением уменьшает частоту повреждения возвратных нервов. Мы получили 2 осложнения: одно в виде интраоперационного кровотечения (справились эндоскопически), второе – некроз кожи у субтильной женщины, который потребовал лишь непродолжительного амбулаторного лечения. Повреждения возвратных нервов не было. Мы не ставили себе задачи сравнительной оценки осложнений ТАТЕ и открытой тиреоидэктомии в данной статье ввиду незначительного, на наш взгляд, количества эндоскопических операций.
Заключение
Наш первый опыт выполнения ТАТЕ показал не только перспективность, но и необходимость внедрения данного вмешательства в клинику. Залогом успеха проведения такой операции является как тщательный подбор пациентов с правильным дооперационным обследованием, так и обладание хирургом достаточного опыта в эндоскопической и традиционной хирургии. Мы надеемся, что методика найдет свою нишу в хирургии эндокринных органов шеи.
Список литературы Первый опыт выполнения трансаксиллярных эндоскопических операций на эндокринных органах шеи
- Ikeda Y., Takami H., Sasaki Y., Kan S., Niimi M. (2000) Endoscopic neck surgery by the axillary approach. J Am Coll Surg, 2000, 191(3), pp, 336–340. https://doi.org/10.1016/S1072-7515(00)00342-2
- Бельцевич Д. Г., Ванушко В. Э., Мельниченко Г. А. и др. Клинические рекомендации Российской ассоциации эндокринологов по диагностике и лечению узлового зоба: (новая редакция 2015 года). Эндокринная хирургия. 2016. № 10 (1). С. 5–12. https://doi.org/10.14341/serg2015115-21
- Бельцевич Д. Г., Ванушко В. Э., Мельниченко Г. А. Российские клинические рекомендации по диагностике и лечению дифференцированного рака щитовидной железы у взрослых. 2020. URL: https://mosgorzdrav.ru/ru RU/science/default/download/629.html
- Клинические рекомендации «Профилактика инфекций области хирургического вмешательства» МЗ РФ 2018. URL: http://nasciru/?id=2260
- Ohgami M., Ishii S., Arisawa Y., Ohmori T., Noga K., Furukawa T., Kitajima M. Scarless endoscopic thyroidectomy: breast approach for better cosmesis. Surg Laparosc Endosc Percutan Tech, 2000, № 10(1), pp. 1–4. https://doi.org/10.1097/00129689-200002000-00001
- Решетов И. В., Севрюков Е. Ф., Голубцов А. К., Крехно О. П. Видеоассистированная резекция щитовидной железы из одностороннего подмышечного доступа. Голова и шея, 2014. № 3. С.15–19.
- Лядов В. К., Неклюдова М. В., Пашаева Д. Р. Опыт эндоскопических трансаксиллярных вмешательств на щитовидной железе. Хирургия. Журнал им. Н.И. Пирогова. 2016. № 11. С. 4–7. https://doi.org/10.17116/hirurgia2016114–7
- Miccoli P., Bellantone R., Mourad M., Walz M., Raffaelli M., Berti P. Minimally invasive video-assisted thyroidectomy: multiinstitutional experience. World J Surg, 2002, № 26(8), рр. 972–975. https://doi.org/10.1007/s00268-002-6627-7
- Rao R.S., Duncan T.D. Endoscopic total thyroidectomy. JSLS, 2009, № 13(4), рр. 522–527. https://doi.org/10.4293/108680810X12924466009249
- Gagner M., Inabnet W.B. Endoscopic thyroidectomy for solitary thyroid nodules. Thyroid, 2001, № 11(2), рр. 161–163. https://doi.org/10.1089/105072501300042848
- Miccoli P., Berti P., Bendinelli C., Conte M., Fasolini F., Martino E. (2000) Minimally invasive video-assisted surgery of the thyroid: a preliminary report. Langenbecks Arch Surg, 2000, № 385(4), рр. 261–264. https://doi.org/10.1007/s004230000141
- Bellantone R., Lombardi C.P., Rubino F., Perilli V., Sollazzi L., Mastroianni G., Gagner M. Arterial PCO 2 and cardiovascular function during endoscopic neck surgery with carbon dioxide insufflation. Arch Surg, 2001, № 136(7), рр. 822–827. https://doi.org/10.1001/archsurg.136.7.822
- Ochiai R., Takeda J., Noguchi J., Ohgami M., Ishii S. Subcutaneous carbon dioxide insufflation does not cause hypercarbia during endoscopic thyroidectomy. Anesth Analg, 2000, № 90(3), рр. 760–762. https://doi.org/10.1097/00000539-200003000-00046
- Udomsawaengsup S., Navicharern P., Tharavej C., Pungpapong S.U. Endoscopic transaxillary thyroid lobectomy: flexible vs rigid laparoscope. J Med Assoc Thai, 2004, № 87(2), рр. 10–14.
- Miyano G., Lobe T.E., Wright S.K. Bilateral transaxillary endoscopic total thyroidectomy. J Pediatr Surg, 2008, № 43(2), рр. 299–303. https://doi.org/10.1016/j.jpedsurg.2007.10.018


