Первый в России опыт применения пептид-рецепторной радионуклидной терапии 177Lu-DOTA-TATE при метастатических нейроэндокринных опухолях. Анализ безопасности и предварительных результатов лечения
Автор: Шуринов А.Ю., Крылов В.В., Хвостунов И.К., Сигов М.А., Сидоренко Е.А., Бородавина Е.В., Степаненко В.Ф., Петухов А.Д., Северская Н.В., Тищенко В.К., Иванов С.А., Каприн А.Д.
Рубрика: Научные статьи
Статья в выпуске: 1 т.35, 2026 года.
Бесплатный доступ
Метод пептидрецепторной радионуклидной терапии 177LuDOTATATE активно применяется в зарубежной практике с 2017 г. для лечения метастатических гастроэнтеропанкреатических нейроэндокринных опухолей (ГЭПНЭО) и внесён в клинические рекомендации международных профильных научномедицинских сообществ. В Медицинском радиологическом научном центре им. А.Ф. Цыба 13 марта 2024 г., в рамках одноцентрового открытого нерандомизированного клинического исследования впервые в России был применён радиофармацевтический лекарственный препарат 177LuDOTATATE, синтезированный непосредственно в медицинском учреждении с использованием отечественного 177Lu [177LuCl3]. В данное клиническое исследование были включены пациенты с метастатическими нейроэндокринными опухолями; исследование проводилось в рамках внутреннего протокола клинического исследования. Были поставлены следующие задачи: оценка безопасности и клинической эффективности отечественного радиофармацевтического лекарственного препарата 177LuDOTATATE и анализ лучевой нагрузки на медицинский персонал, задействованный в процессе радиохимического синтеза и лечебных манипуляций. Всем пациентам проводился комплекс лабораторных и инструментальных исследований, необходимый для проведения данного вида радионуклидной терапии, в том числе динамическая нефросцинтиграфия, ПЭТ/КТ с 68GaDOTATATE, либо ОФЭКТ/КТ с 99mTcEDDA/HYNICTOC. Курс лечения состоял из 36 введений 177LuDOTATATE (от 3,7 до 7,4 ГБк) с применением нефропротективного протокола, включающего внутривенную коинфузию раствора аминокислот. В процессе проведённого лечения не было отмечено значимой гематологической токсичности и нефротоксичности, а также превышения показателей поглощённой дозы на организм пациентов выше 1,4 Гр. Улучшение качества в виду купирования болевого синдрома жизни отмечено в 100% наблюдений. Лучевая нагрузка на инженерный и медицинский персонал не превысила предельно допустимых показателей. В рамках предварительных результатов было сделано заключение, что применение отечественного 177LuDOTATATE при лечении метастатических ГЭПНЭО является безопасным и эффективным методом.
Ядерная медицина, радионуклидная терапия, пептидрецепторная радионуклидная терапия; радиофармацевтический лекарственный препарат, 177LuDOTATATE, нейроэндокринная опухоль, безопасность 177LuDOTATATE, поглощённая доза
Короткий адрес: https://sciup.org/170211681
IDR: 170211681 | УДК: 616-006.88-033.2:615.849.2:546.669.02.177 | DOI: 10.21870/0131-3878-2026-35-1-151-166
The first Russian experience in the use of peptide-receptor radionuclide therapy 177Lu-DOTA-TATE in metastatic neuroendocrine tumors. Analysis of safety and preliminary treatment results
The peptidereceptor radionuclide therapy method 177LuDOTATATE has been actively used in international practice since 2016 for the treatment of metastatic gastroenteropancreatic neuroendocrine tumors (GEPNETs) and is included in clinical guidelines of international specialized scientific and medical communities. On March 13, 2024, the A. Tsyb Medical Radiology Research Center used the radiopharmaceutical drug 177LuDOTATATE, synthesized directly at the medical facility using domestically produced 177Lu [177LuCl3], for the first time in Russia as part of a singlecenter, openlabel, nonrandomized clinical trial. This clinical trial included patients with metastatic neuroendocrine tumors; the study was conducted within the framework of an internal clinical trial protocol. The scientific objectives were to evaluate the safety and clinical efficacy of the domestic radiopharmaceutical 177LuDOTATATE and to analyze the radiation exposure of medical personnel involved in the radiochemical synthesis and treatment procedures. All patients underwent the full range of laboratory and instrumental studies required for this type of radionuclide therapy, including dynamic nephroscintigraphy, PET/CT with 68GaDOTATATE, or SPECT/CT with 99mTcEDDA/HYNICTOC. The treatment course consisted of 36 administrations of 177LuDOTATATE (from 3.7 to 7.4 GBq) using a nephroprotective protocol including intravenous coinfusion of an amino acid solution. During the treatment, no significant hematological or nephrotoxicity was observed, nor were patient absorbed doses exceeding 1.4 Gy. Improved quality of life due to pain relief was observed in 100% of cases. Radiation exposure to engineering and medical personnel did not exceed the maximum permissible limits. Preliminary results concluded that the use of domestically produced 177LuDOTATATE in the treatment of metastatic GEPNETs is a safe and effective treatment method.
Текст научной статьи Первый в России опыт применения пептид-рецепторной радионуклидной терапии 177Lu-DOTA-TATE при метастатических нейроэндокринных опухолях. Анализ безопасности и предварительных результатов лечения
Нейроэндокринные опухоли (НЭО) – это высокодифференцированные неоплазии, развивающиеся из клеток APUD-системы, представляют собой гетерогенную группу злокачественных новообразований с разнообразной морфологией и номенклатурой. Одной из проблем современной онкологии является полное отсутствие объективной мировой статистики, в том числе в России, по заболеваемости НЭО в целом. Такая ситуация может быть связана с рядом пересмотров
Шуринов А.Ю.* – зам. директора Института ядерной медицины, к.м.н.; Крылов В.В. – директор Института ядерной медицины, д.м.н.; Хвостунов И.К. – гл. науч. сотр., д.б.н.; Сигов М.А. – зав. отд., врач-радиолог; Сидоренко Е.А. – врач-радиолог; Бородавина Е.В. – ст. науч. сотр., к.м.н.; Степаненко В.Ф. – зав. лаб., д.б.н., проф.; Петухов А.Д. – ст. науч. сотр., к.б.н.; Северская Н.В. – зав. отд., к.м.н.; Тищенко В.К. – зав. лаб., д.б.н.; Иванов С.А. – директор, чл.-корр. РАН, д.м.н., проф. каф. РУДН. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России. Каприн А.Д. – ген. директор, директор МНИОИ им. П.А. Герцена, зав. каф. РУДН, акад. РАН, д.м.н., проф. ФГБУ «НМИЦ радиологии» Минздрава России.
патоморфологических классификаций данной группы заболеваний, включающей не менее 25 локализаций согласно МКБ-10. По данным ряда авторов, заболеваемость НЭО может находиться в пределах 1-8 случаев на 100000 населения в год [1, 2], что относит эту группу злокачественных заболеваний к категории орфанных [3].
Как радиофармацевтический лекарственный препарат (РФЛП) – 177Lu-[DOTA(о), Tyr3] ок-треотат (177Lu-DOTA-TATE) представляет собой циклический пептид, аналог соматостатина, меченный 177Lu ковалентно-связанным хелатором: 1,4,7,10-тетраазациклододекан-1,4,7,10-тетраук-сусной кислотой с молекулярной массой 1609,6 Da [4]. Механизм действия препарата напрямую связан с его структурой: агонист соматостатина (октреотат) избирательно связывается с опухолевыми клетками, экспрессирующими соматостатиновые рецепторы второго типа (ССТР2), проникает внутрь опухолевой клетки вместе с хелатированным бета-излучающим изотопом 177Lu, где излучение вызывает одноцепочечные и двухцепочечные (одиночные и двойные) разрывы ДНК, из которых последние вносят основной вклад в индукцию гибели опухолевых клеток посредством запуска механизма апоптоза [5]. Метод пептид-рецепторной радионуклидной терапии (ПРРТ) 177Lu-DOTA-TATE активно применяется в зарубежной практике с 2018 г. для лечения метастатических гастроэнтеропанкреатических нейроэндокринных опухолей (ГЭП-НЭО) в первой и последующих линиях терапии, внесён в клинические рекомендации профильных зарубежных научно-медицинских сообществ по результатам опубликованных многоцентровых рандомизированных исследований NETTER-I, NETTER-II [6, 7]. По данным результатов многоцентрового исследования NETTER-P (NCT04711135) 23 апреля 2024 г. FDA одобрено применение 177Lu-DOTA-TATE также пациентам в возрасте от 12 до 17 лет при ГЭП-НЕО, феохромацитоме и параганглиоме. Эффективность применения данного РФЛП в неадъювантном режиме у пациентов с НЭО поджелудочной железы было доказано в исследовании NEOLUPANET [8]. В настоящий момент проводятся пилотные одноцентровые исследования эффективности 177Lu-DOTA-TATE при раках с нейроэндокринной дифференцировкой: молочная железа, предстательная железа, щитовидная железа и т.д. [9, 10].
Внедрение методики ПРРТ 177Lu-DOTA-TATE в российскую клиническую практику является значимым шагом для обеспечения доступа пациентов к современным и эффективным методам лечения НЭО. Впервые на территории Российской Федерации терапевтическое применение РФЛП 177Lu-DOTA-TATE было проведено 13 марта 2024 г. в Медицинском радиологическом научном центре им. А.Ф. Цыба (г. Обнинск) пациенту с метастатическим поражением печени при ГЭП-НЭО. В течение первых 8 мес. ПРРТ 177Lu-DOTA-TATE проводилась пациентам в рамках протокола клинического исследования, утверждённого на Учёном совете Центра 8 февраля 2024 г. В дальнейшем, на основании клинических данных о эффективности и безопасности ПРРТ, полученных от ФГБУ «НМИЦ радиологии» Минздрава России и ФГБУ «НМИЦ онкологии» Минздрава России, руководством Минздрава России было принято решение о внесении данного вида лечения в перечень методов высокотехнологичной медицинской помощи, что стало целевым результатом проведённой научно-исследовательской работы и позволило применять ПРРТ в рутинной клинической практике. Этот подход обеспечил независимость от импортных поставок и способствовал развитию отечественной ядерной медицины.
Целью настоящего исследования было изучение безопасности и эффективности 177Lu-DOTA-TATE у пациентов с метастатическими НЭО, экспрессирующими рецепторы к соматостатину, оценка воздействия на здоровые органы и ткани, а также радиологической безопас- ности медицинского персонала, участвующего в синтезе и введении РФЛП. Первичной конечной точкой было определено – оценить эффективность ПРРТ по завершению курса лечения, вторичной – оценка выживаемости без прогрессирования. В рамках целей научного исследования были сформированы задачи: 1) оценить эффективность и безопасность ПРРТ 177Lu-DOTA-TATE; 2) установить частоту объективного ответа на лечение по данным посттерапевтической ОФЭКТ/КТ, к моменту завершения циклов ПРРТ; 3) определить частоту и тяжесть нежелательных явлений, включая гематологическую, почечную и печёночную токсичность, а также уровень хромосомных аберраций в процессе ПРРТ; 4) определить лучевую нагрузку на медицинский персонал в процессе лечения.
Материалы и методы
Для участия в клиническом исследовании допускались пациенты старше 18 лет, с верифицированным результатом иммуногистохимического исследования, диагнозом НЭО с метастатическим поражением печени, и экспрессирующей рецепторы к соматостатину, подтверждённым на этапе скрининга результатом исследования ПЭТ/КТ с 68Ga-DOTA-TATE или ОФЭКТ/КТ с 99mTc-EDDA/HYNIC-TOC: накопление в метастатических очагах по шкале Кренинга 3-4 балла. На догоспитальном этапе всем пациентам проводились общеклинические анализы крови и мочи, УЗИ брюшной полости и почек, динамическая нефросцинтиграфия, ЭКГ. Обследование МРТ брюшной полости и ПЭТ/КТ с 68Ga-DOTA-TATE и 18F-FDG осуществляли для сравнительного анализа последних по шкале NETPET: допустимым для ПРРТ являлись категории 1, 2a, 2b [11].
Для лечения были отобраны пациенты, у которых клиническая картина заболевания соответствовала показаниям к проведению ПРРТ. Такими показателями являются высокодифференцированные (Grade 1, Grade 2, Grade 3, при Ki67 не более 55%) неоперабельные и метастатические ГЭП-НЭО, включая НЭО, исходящие из верхних, средних и нижних отделов первичной эмбриональной кишечной трубки, в том числе опухоли тимуса и лёгких, прогрессирующих на фоне терапии АСС, химиотерапии и иных доступных методов лечения. Противопоказаниями к проведению ПРРТ, которые также определялись на этапе скрининга, являлись: беременность и лактация; ожидаемая продолжительность жизни менее 6 мес.; статус по шкале ECOG 3-4 балла; неуправляемая обструкция мочевых путей или гидронефроз; скорость клубочковой фильтрации (СКФ) выше двукратного верхнего предела нормы; повышение уровней аланинаминотрансферазы (АЛТ) и/или аспартатаминотрансферазы (АСТ) выше пятикратного верхнего предела нормы; миелосупрессия (i - общее количество лейкоцитов (L) менее 2,5 х 10 9 /л, ii - количество тромбоцитов (Tr) менее 75 х 10 9 /л, iii - количество эритроцитов (Er) менее 100 х 1012) [12]. Ограничивающими факторами для отбора пациентов, не относящимся к противопоказаниям для ПРРТ, являлись: метастатическое поражение паренхимы печени более 90% по данным КТ или МРТ, метаболическая активность метастатических очагов (ССТР-статус) по шкале Кренинга < 2 балла, категория NETPET > 3. В таких клинических ситуациях эффективность ПРРТ значимо снижается при высоких рисках общей радиологической токсичности [11].
После завершения скрининга в исследование включён 21 пациент преимущественно среднего возраста, из них 9 женщин и 12 мужчин, с метастатическим поражением печени, подтверждённым инструментальными и лабораторными диагностическими методами. По данным иммуногистохимического исследования у 10 пациентов степень дифференцировки опухоли определена как G1, у 8 – G2, у 3 – G3. При каждой госпитализации для проведения ПРРТ всем пациентам выполнялись общеклинические анализы крови и мочи, а также анализ на хромосомные аберрации для ретроспективной оценки уровня цитогенетических повреждений. РФЛП 177Lu-DOTA-TATE синтезировался в МРНЦ им. А.Ф. Цыба из двух компонентов 177Lu [177LuСl3] и оксодотреотида: DOTA-TATE отечественного производства (рис. 1) непосредственно перед терапевтическим применением в производственной аптеке с правом изготовления РФЛП с обязательным проведением контроля радиохимической чистоты каждой партии, достигающей средне-высоких показателей M=97,5% (ДИ 95% 97,5±1,1). Регламентирующим документом, позволяющим производство непосредственно в специализированных медицинских учреждениях, является Приказ Минздрава России № 249н от 22 мая 2023 г. «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, имеющими лицензию на фармацевтическую деятельность от 22 мая 2023 г. № 249н».

Рис. 1. Процесс радиохимического синтеза 177Lu-DOTA-TATE в производственной аптеке с правом изготовления РФЛП в условиях Института ядерной медицины МРНЦ им. А.Ф. Цыба (г. Обнинск).
Процедура введения РФЛП заключалась в коинфузии раствора аминокислот (Аминовен 5% – 1000 мл) со скоростью 250-350 мл/ч, которая начиналась за час до лечебной процедуры. Через час после начала инфузии аминокислот посредством инфузомата проводилось введение раствора 177Lu-DOTA-TATE (объём раствора M=12,6 мл) со скоростью 30 мл/ч. Данная методика унифицирована, но в различных медицинских учреждениях может отличаться [13].
Курс лечения состоял из 3-6 введений лечебной активности 177Lu-DOTA-TATE от 3,5 до 7,5 ГБк, с интервалом от 8 до 15 недель (табл. 1) и являлся персонализированным в большинстве случаев.
Всем пациентам проводился радиометрический контроль на 1 м от поверхности тела через 12, 24 и 48 ч ретроспективный радиометрический анализ мочи. Через 24, 48 и 72 ч выполнялась гибридная однофотонная эмиссионная компьютерная томография, совмещённая с рентгеновской компьютерной томографией (ОФЭКТ/КТ) всего тела на диагностическом сканере Discovery NM/CT 670 для оценки распределения РФЛП и последующего ретроспективного анализа поглощённых доз в критических органах и метастатических очагах, итоговой оценки объективного ответа на лечение в условиях отделения радионуклидной диагностики МРНЦ им. А.Ф. Цыба (табл. 2).
Таблица 1
|
№ |
Пол |
Анализ на хромосом-ные аберрации* |
Код МКБ-10 |
Год рождения |
T |
N |
M |
Grade (1/2/3) |
Ki67 (%) |
Предшествующее лечение |
Год установки диагноза |
Начало ПРРТ (дд.мм. гг) |
M±δ (дни) |
Асумм. 177Lu- DOTA-TATE (ГБк) |
Число курсов ПРРТ |
|
1 |
Ж |
Да (П1) |
C78.7 |
1972 |
x |
x |
1 |
1 |
н.д.** |
АСС |
2022 |
15.03. 2024 |
73±16 |
39,7 |
6 |
|
2 |
М |
Да (П2) |
C25.0 |
1971 |
3 |
N0 |
1 |
1 |
н.д. |
АСС |
2023 |
14.03. 2024 |
60±24 |
42 |
6 |
|
3 |
М |
Нет |
C25.2 |
1971 |
3 |
0 |
1 |
3 |
40 |
АСС |
2023 |
11.04. 2024 |
66±16 |
42,4 |
6 |
|
4 |
Ж |
Да (П3) |
C80.9 |
1968 |
x |
x |
1 |
1 |
н.д. |
Хир, АСС |
2023 |
15.05. 2024 |
94±21 |
39,7 |
6 |
|
5 |
Ж |
Да (П5) |
C25.2 |
1968 |
4 |
1 |
1 |
1 |
2 |
Хир, АСС |
2023 |
29.07. 2024 |
87±51 |
34,5 |
6 |
|
6 |
М |
Да (П6) |
C22.7 |
1974 |
3 |
0 |
1 |
2 |
5 |
Хир, ТАХЭ, АСС |
2022 |
19.08. 2024 |
58±14 |
29,5 |
4 |
|
7 |
Ж |
Нет |
C25.1 |
1981 |
4 |
1 |
1 |
1 |
2 |
АСС |
2024 |
26.12. 2024 |
95±12 |
26,5 |
4 |
|
8 |
М |
Да (П7) |
C25.2 |
1971 |
3 |
0 |
1 |
3 |
40 |
АСС |
2023 |
11.04. 2024 |
70±14 |
42,4 |
6 |
|
9 |
Ж |
Да (П8) |
C16.2 |
1980 |
1 |
0 |
1c |
2 |
9 |
Хир, АСС |
2015 |
26.12. 2024 |
66±13 |
34,2 |
5 |
|
10 |
М |
Да (П9) |
C25.2 |
1961 |
2 |
1 |
1 |
2 |
4 |
АСС |
2024 |
11.03. 2025 |
77±24 |
29 |
4 |
|
11 |
Ж |
Нет |
C17.8 |
1959 |
4 |
1c |
1 |
2 |
40 |
Хир, АСС |
2019 |
20.11. 2024 |
60±13 |
27,5 |
4 |
|
12 |
М |
Нет |
C17.1 |
1956 |
3 |
1 |
1 |
1 |
2 |
Хир, АСС |
2012 |
24.03. 2025 |
75±27 |
25 |
4 |
|
13 |
М |
Нет |
C97 |
1954 |
3 |
0 |
1 |
2 |
н.д. |
Хир, АСС |
2019 |
11.03. 2025 |
77±24 |
26,5 |
4 |
|
14 |
М |
Нет |
C25.2 |
1969 |
4 |
1 |
1c |
2 |
7 |
Хир, АСС |
2021 |
07.05. 2025 |
65±8 |
30,5 |
4 |
|
15 |
М |
Нет |
C25.1 |
1987 |
2 |
1 |
1 |
2 |
20 |
Хир, АСС |
2024 |
24.04. 2025 |
70±14 |
27,6 |
4 |
|
16 |
М |
Нет |
C34.1 |
1968 |
1 |
0 |
1c |
1 |
3 |
АСС |
2020 |
26.12. 2024 |
73±26 |
36,8 |
5 |
|
17 |
Ж |
Да (П10) |
C17.2 |
1952 |
2 |
1 |
1 |
3 |
н.д. |
РЧА, АСС |
2022 |
19.02. 2025 |
68±8 |
26,5 |
4 |
|
18 |
М |
Да (П12) |
C17.0 |
1958 |
3 |
1 |
1a |
2 |
18 |
Хир, АСС |
2016 |
19.02. 2025 |
64±8 |
31,6 |
5 |
|
19 |
Ж |
Нет |
C25.1 |
1953 |
3 |
1b |
M0 |
1 |
4 |
АСС |
2015 |
14.04. 2025 |
72±5 |
29,5 |
4 |
|
20 |
Ж |
Да (П13) |
C25.2 |
1964 |
2 |
0 |
1 |
1 |
н.д. |
Хир, АСС |
2019 |
29.07. 2024 |
59±4 |
25 |
4 |
|
21 |
М |
Да (П15) |
C17.2 |
1962 |
3 |
2 |
1b |
1 |
1 |
Хир, АСС |
2014 |
15.05. 2024 |
74 и 56 |
15,7 |
3 |
Характеристика группы пациентов, включённых в исследование
Примечание: * – Да (П. № в табл. 3)/Нет; П – пациент; ** н.д. – нет данных; Ki67 (%) – индекс пролиферативной активности; M±δ – интервал между курсами ПРРТ; ПРРТ – пептид-рецепторная радионуклидная терапия; Асумм. – суммарная лечебная активность 177Lu-DOTA-TATE; Хир – хирургическое лечение; АСС – агонисты соматостатиновых рецепторов; ТАХЭ – трансартериальная химиоэмболизация; РЧА – радиочастотная абляция.
Все пациенты получали терапию парэнтеральными пролонгированными формами агонистов соматостатиновых рецепторов (АСС): Октреотид-депо, Ланреотид и т.д. Данная терапия отменялась за 21 день до ПРРТ. Иное лечение (ингибиторы сигнальных путей, химиотерапия, тирозинкиназные ингибиторы и т.п.) отменялось за 2 мес. до начала ПРРТ с целью снижения риска кумулятивной токсичности.
С целью оценки побочного действия РФЛП на здоровые органы и ткани пациентов был использован метод биологической дозиметрии на основе анализа аберраций хромосом в лимфоцитах крови [14, 15]. Для цитогенетического анализа использовали образцы периферической крови, взятые из локтевой вены до начала терапии и повторно через 2-3 дня после введения РФЛП. Образцы крови у всех обследованных лиц брались в соответствии с действующим законодательством Российской Федерации и нормами медицинской этики после получения информированного согласия. Хромосомные аберрации изучались метафазным методом в клетках первого митоза стандартным методом. Приготовление препаратов и фиксацию выполняли по стандартной методике в соответствии с международными рекомендациями МАГАТЭ. Анализировали аберрации хромосомного типа: ацентрики (ace: парные фрагменты и точки), центрические кольца (rc) и дицентрики (dic).
Таблица 2
Основные лабораторные показатели и данные объективного ответа на лечение в зависимости от Grade метастатических очагов в печени и категории NETPET
|
№ |
Показатели анализов крови до начала ПРРТ 177Lu-DOTA-TATE |
Показатели анализов крови через 1 мес. после завершения циклов ПРРТ 177Lu-DOTA-TATE |
5 3 ф 2 0 |
со 1— 2 ш 03 ^ о ш о Z 2 ё О 03 > X Й а о £ |
ф 5 i Л ф СО ф х аз Ф X н Ю ф О “ о |
||||||||||||
|
ш |
т |
о ь |
1 _1 |
5 ш 5 |
Й ГО 2 ф v &2 |
11 О х о < X |
ш |
т |
о ь |
i _1 |
5 ш 5 |
Й ГО 2 ф X &2 |
11 О х о < X |
||||
|
1 |
4,28 |
127 |
120 |
6,44 |
17,7 |
73 |
962 |
3,2 |
97 |
146 |
3,88 |
15,4 |
72 |
601 |
1 |
2a |
ЧО |
|
2 |
5,26 |
170 |
285 |
6,63 |
20,7 |
88 |
79 |
4,3 |
151 |
211 |
3,6 |
55,6 |
86 |
38,2 |
1 |
2b |
ЧО |
|
3 |
4,15 |
128 |
266 |
7,36 |
33,4 |
96 |
811 |
3,6 |
115 |
153 |
3,37 |
22,1 |
97 |
335 |
3 |
1 |
ЧO |
|
4 |
4,69 |
139 |
242 |
7,16 |
18,6 |
81 |
104 |
3,7 |
110 |
175 |
4,99 |
11,6 |
83 |
46,7 |
1 |
1 |
ПО |
|
5 |
4,38 |
130 |
305 |
4,47 |
25,9 |
71 |
43 |
3,4 |
105 |
371 |
4,24 |
34,7 |
67 |
38,3 |
1 |
2b |
ЧО |
|
6 |
4,15 |
125 |
286 |
7,42 |
9,8 |
85 |
14 |
3,5 |
113 |
167 |
3,81 |
11,8 |
90 |
21,6 |
2 |
1 |
ПО |
|
7 |
4,15 |
132 |
145 |
7,28 |
14,4 |
77 |
61 |
3,4 |
118 |
149 |
5,31 |
12,5 |
83 |
н.д. |
1 |
1 |
ЧО |
|
8 |
4,02 |
124 |
273 |
8,09 |
33,5 |
108 |
811 |
3,6 |
115 |
153 |
3,37 |
22,1 |
97 |
335 |
3 |
2a |
ЧО |
|
9 |
4,08 |
129 |
188 |
4,52 |
67,7 |
44 |
849 |
3,4 |
105 |
194 |
3,96 |
65,2 |
49 |
314 |
2 |
1 |
ЧО |
|
10 |
4,27 |
129 |
278 |
7,46 |
56,4 |
70 |
948 |
3,6 |
119 |
163 |
3,97 |
48,8 |
68 |
565 |
2 |
2а |
ЧО |
|
11 |
4,33 |
123 |
316 |
6,62 |
11,8 |
70 |
123 |
4,7 |
137 |
283 |
6,28 |
15,2 |
85 |
168 |
2 |
2b |
ЧО |
|
12 |
4,47 |
148 |
245 |
7,87 |
14,4 |
146 |
н.д. |
3,7 |
121 |
136 |
5,59 |
16,2 |
176 |
178 |
1 |
2a |
ЧО |
|
13 |
4,62 |
143 |
297 |
6,65 |
18,3 |
106 |
323 |
4,6 |
141 |
272 |
7,6 |
18,7 |
107 |
н.д. |
2 |
1 |
ЧО |
|
14 |
5,21 |
159 |
161 |
12 |
10 |
81 |
200 |
4,9 |
151 |
344 |
7,95 |
25,7 |
92 |
34 |
2 |
1 |
ЧО |
|
15 |
4,59 |
110 |
404 |
9,26 |
74,5 |
77 |
н.д. |
4,9 |
134 |
624 |
13,2 |
22,9 |
87 |
67,8 |
2 |
1 |
ЧО |
|
16 |
5,51 |
160 |
228 |
4,75 |
19,2 |
81 |
428 |
4,7 |
143 |
228 |
3,9 |
15,9 |
83 |
350 |
1 |
2a |
ЧО |
|
17 |
4,73 |
147 |
216 |
6,39 |
18,4 |
101 |
н.д. |
4,4 |
141 |
161 |
4,72 |
16 |
93 |
898 |
3 |
2а |
ЧО |
|
18 |
4,47 |
136 |
149 |
5,69 |
17,5 |
119 |
49 |
3,7 |
118 |
153 |
4,34 |
18,6 |
125 |
39,3 |
2 |
1 |
ПО |
|
19 |
5,36 |
157 |
337 |
8,15 |
12 |
84 |
20 |
4,3 |
135 |
152 |
4,48 |
18,4 |
93,4 |
129 |
1 |
2a |
ЧО |
|
20 |
4,14 |
137 |
278 |
5,5 |
16,2 |
71 |
39 |
3,7 |
123 |
347 |
4,31 |
21,4 |
66 |
35,2 |
1 |
2b |
СТ |
|
21 |
3,96 |
126 |
213 |
5,71 |
13,6 |
80 |
140 |
3,4 |
116 |
249 |
3,18 |
12 |
79 |
101 |
1 |
2a |
ЧО |
Примечание: ПРРТ – пептид-рецепторная радионуклидная терапия; н.д. – нет данных; СТ – стабилизация; ЧО – частичный ответ; ПО – полный ответ.
Для расчёта дозы при пролонгированном внутреннем облучении в течение периода T с зависящей от времени мощностью дозы частота аберраций Y , как функция дозы D , вычислялась в рамках линейно-квадратичной модели по формуле:
Y = c+ a D + G(T)eD 2 , (1)
где c , а , в - коэффициенты дозовой зависимости при остром облучении; G(T) - обобщенный временной фактор эффекта мощности дозы Lea-Catcheside, который вычислялся с учётом снижения мощности дозы и репарации разрывов хромосом в рамках модели неполной репарации [14].
Используя экспериментально оценённую константу репарации разрывов хромосом в лимфоцитах крови человека ^=0,438 ч-1 и эффективный период полувыведения 177Lu-DOTA-TATE Teff=4,7 ч [16], в настоящей работе была рассчитана величина G(T=48 ч)=0,251. На текущий момент проведено цитогенетическое обследование 12 пациентов (6 мужчин и 6 женщин, возраст от 50 до 74 лет на дату первого введения РФЛП). Результаты представлены в табл. 1. Из 12 паци- ентов (дважды за курс ПРРТ) было обследовано 11 человек за I курс (в течение 0-3 дней), 9 человек за II курс (в течение 58-78 дней), 7 человек за III курс (в течение 114-134 дней) и 2 человека за IV курс (в течение 195-197 дней от начала ПРРТ). На рис. 2 представлены хромосомные аберрации в форме суммы ace+rc+dic на 100 клеток за I-IV курсы радионуклидной терапии (РНТ) в сравнении со спонтанным уровнем у здоровых лиц [17]. Средняя частота аберраций у пациентов до начала ПРРТ составила 2,14±0,24 абер./100 клет., что существенно выше спонтанного уровня, который равняется 0,25 абер./100 клет. Данный факт свидетельствует о значительном радиационном воздействии на пациентов до начала ПРРТ в форме диагностических процедур.
35 I 1 1 до РНТ
. в после РНТ
30 спонтанный уровень
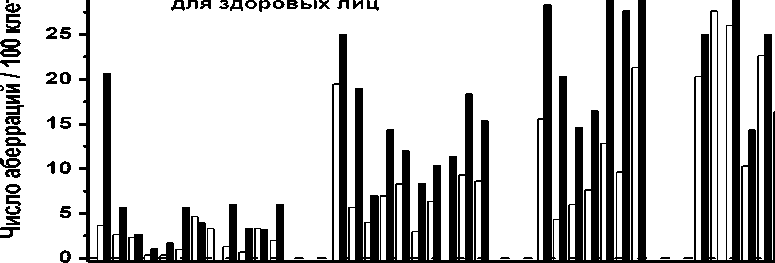
Курс II Курс III Курс IV
Курс I, день 0 - 3 день 56 - 78 день 114-134 день 178-227
Рис. 2. Хромосомные аберрации в форме суммы ace+rc+dic на 100 клеток за I-IV курсы РНТ в сравнении со спонтанным уровнем у здоровых лиц.
В табл. 3 представлены персональные дозы для обследованных пациентов, рассчитанные по биодозиметрической модели с учётом эффекта мощности дозы, используя индукцию радиационных маркерных аберраций в виде суммы ace+rc+dic.
В результате средняя доза от первого к четвёртому курсу постоянно возрастала: I – 0,55 Гр; II – 0,76 Гр; III – 1,63 Гр; IV – 1,38 Гр. Следует отметить, что оценка дозы за IV курс является скорее всего заниженной в силу недостаточной статистики. Начиная с III курса у отдельных пациентов ожидается достижение дозы облучения здоровых органов и тканей установленного безопасного предела 2 Гр (П7, П13).
Таблица 3
Частота хромосомных аберраций и биодозиметрическая оценка дозы общего облучения обследованных пациентов
|
Код – № курса |
Период дней |
До введения РФЛП |
T, ч |
После введения РФЛП |
Прирост ∆M±SE* |
G (T) |
Доза, Гр (ДИ**) |
||
|
клетки |
M 1 ±SE* |
клетки |
M 2 ±SE* |
||||||
|
П1-1 |
0-3 |
300 |
1,67±0,75 |
72 |
300 |
9,0±1,73 |
7,33±2,48 |
0,2518 |
1,65 (0,76-2,32) |
|
П2-1 |
0-2 |
300 |
0,67±0,47 |
48 |
300 |
3,67±1,11 |
3,0±1,58 |
0,2522 |
0,95 (0,0-1,55) |
|
П3-1 |
0-2 |
300 |
0,67±0,47 |
48 |
300 |
1,33±0,67 |
0,67±1,14 |
0,2522 |
0,33 (0-1,00) |
|
П5-1 |
0-2 |
300 |
0,33±0,33 |
48 |
285 |
0,70±0,50 |
0,37±0,83 |
0,2522 |
0,20 (0-0,81) |
|
П6-1 |
0-3 |
300 |
0,33±0,33 |
72 |
300 |
0,33±0,33 |
0,0±0,66 |
0,2518 |
0,0 (0-0,64) |
|
П7-1 |
0-2 |
300 |
0,33±0,33 |
48 |
300 |
2,33±0,88 |
2,0±1,22 |
0,2522 |
0,73 (0-1,28) |
|
П8-1 |
0-2 |
300 |
0,67±0,47 |
48 |
300 |
2,33±0,88 |
1,67±1,35 |
0,2522 |
0,64 (0-1,27) |
|
П9-1 |
0 |
300 |
0,33±0,33 |
– |
– |
– |
– |
– |
н.д.*** |
|
П10-1 |
0-2 |
300 |
0,0±0,46 |
48 |
300 |
2,67±0,94 |
2,67±1,40 |
0,2522 |
0,88 (0-1,45) |
|
П12-1 |
0-3 |
300 |
0,0±0,46 |
72 |
300 |
2,00±0,82 |
2,00±1,28 |
0,2518 |
0,73 (0-1,30) |
|
П13-1 |
0-2 |
300 |
0,33±0,33 |
48 |
254 |
1,18±0,68 |
0,85±1,02 |
0,2522 |
0,39 (0-0,99) |
|
П15-1 |
0-2 |
300 |
0,67±0,47 |
48 |
300 |
0,67±0,47 |
0,0±0,94 |
0,2522 |
0,0 (0-0,78) |
|
Все № 1 |
0-2,3 |
3600 |
0,50±0,12 |
54,5 |
3239 |
2,41±0,27 |
1,91±0,39 |
0,2520 |
0,70 (0,36-0,96) |
Продолжение таблицы 3
|
Код – № курса |
Период дней |
До введения РФЛП |
T, ч |
После введения РФЛП |
Прирост ∆M±SE* |
G (T) |
Доза, Гр (ДИ**) |
||
|
клетки |
M 1 ±SE* |
клетки |
M 2 ±SE* |
||||||
|
П1-2 |
65-67 |
298 |
12,08±2,01 |
48 |
156 |
14,10±3,01 |
2,02±5,02 |
0,2522 |
0,73 (0-2,28) |
|
П2-2 |
75-78 |
300 |
3,67±1,11 |
72 |
342 |
8,48±1,57 |
4,81±2,68 |
0,2518 |
1,28 (0-2,08) |
|
П3-2 |
74-76 |
300 |
1,67±0,75 |
48 |
600 |
3,67±0,78 |
2,00±1,53 |
0,2522 |
0,73 (0-1,38) |
|
П5-2 |
75-78 |
300 |
3,67±1,11 |
72 |
300 |
8,33±1,67 |
4,67±2,78 |
0,2518 |
1,26 (0-2,08) |
|
П6-2 |
56-59 |
300 |
3,00±1,00 |
72 |
100 |
5,00±2,24 |
2,00±3,24 |
0,2518 |
0,73 (0-1,86) |
|
П7-2 |
75-78 |
300 |
2,33±0,88 |
72 |
300 |
5,00±1,29 |
2,67±2,17 |
0,2518 |
0,88 (0-1,67) |
|
П9-2 |
74-76 |
300 |
1,67±0,75 |
48 |
299 |
4,68±1,25 |
3,02±2,00 |
0,2522 |
0,95 (0-1,67) |
|
П12-2 |
56-59 |
10 |
10,0±10,0 |
72 |
229 |
5,24±1,51 |
< 0 |
0,2518 |
0,0 (0-2,88) |
|
П13-2 |
74-76 |
300 |
5,00±1,29 |
48 |
300 |
9,00±1,73 |
4,00±3,02 |
0,2522 |
1,14 (0-2,06) |
|
П15-2 |
74-76 |
300 |
5,67±1,37 |
48 |
300 |
5,67±1,37 |
0,0±2,74 |
0,2522 |
0,0 (0-1,44) |
|
Все № 2 |
56-78 |
2708 |
4,32±0,40 |
60 |
2906 |
6,43±0,47 |
2,10±0,87 |
0,2519 |
0,75 (0,0-1,18) |
|
П2-3 |
131-134 |
77 |
6,49±2,90 |
72 |
300 |
19,33±2,54 |
12,84±5,44 |
0,2518 |
2,29 (0,68-3,36) |
|
П3-3 |
130-133 |
300 |
0,67±0,47 |
72 |
300 |
7,00±1,53 |
6,33±2,00 |
0,2518 |
1,51 (0,74-2,10) |
|
П5-3 |
131-134 |
300 |
2,00±0,82 |
72 |
137 |
5,84±2,06 |
3,84±2,88 |
0,2518 |
1,11 (0,0-2,01) |
|
П6-3 |
114-116 |
300 |
3,33±1,05 |
48 |
170 |
4,71±1,66 |
1,37±2,72 |
0,2522 |
0,56 (0,0-1,64) |
|
П7-3 |
131-134 |
109 |
4,59±2,05 |
72 |
130 |
16,92±3,61 |
12,34±5,66 |
0,2518 |
2,24 (0,40-3,36) |
|
П13-3 |
130-133 |
300 |
5,67±1,37 |
72 |
300 |
19,67±2,56 |
14,00±3,93 |
0,2518 |
2,41 (1,44-3,22) |
|
П15-3 |
130-133 |
300 |
12,33±2,03 |
72 |
300 |
17,33±2,40 |
5,00±4,43 |
0,2518 |
1,31 (0,0-2,48) |
|
Все № 3 |
114-134 |
1686 |
4,86±0,54 |
68,6 |
1637 |
13,93±0,92 |
9,06±1,46 |
0,2518 |
1,87 (1,43-2,29) |
|
П2-4 |
225-227 |
300 |
11,67±1,97 |
48 |
300 |
16,67±2,36 |
5,00±4,43 |
0,2522 |
1,31 (0,0-2,45) |
|
П3-4 |
195-197 |
300 |
8,33±1,97 |
48 |
8 |
12,50±12,50 |
4,17±14,17 |
0,2522 |
1,17 (0,0-3,98) |
|
П6-4 |
178-182 |
300 |
4,67±1,25 |
96 |
307 |
7,17±1,53 |
2,50±2,78 |
0,2517 |
0,84 (0,0-1,81) |
|
П7-4 |
189-191 |
300 |
16,67±2,36 |
48 |
12 |
0,0 |
< 0 |
0,2522 |
н.д. |
|
П13-4 |
195-197 |
300 |
17,0±2,38 |
48 |
0 |
– |
< 0 |
0,2522 |
н.д. |
|
П15-4 |
195-197 |
296 |
15,54±2,29 |
48 |
300 |
21,0±2,65 |
5,46±4,94 |
0,2522 |
1,38 (0,0-2,62) |
|
Все № 4 |
178-227 |
1796 |
12,31±0,83 |
56 |
927 |
14,67±1,26 |
2,37±2,02 |
0,2520 |
0,81 (0,0-1,60) |
Примечание: * – стандартная ошибка среднего; ** ДИ – 95% доверительный интервал; ***н.д. – нет данных.
В рамках проспективного анализа поглощённых доз у медицинского персонала, участвующего в синтезе и введении РФЛП, проводилось размещение сборки ТЛ-дозиметров « а -А1 2 0 з :С» на всех пальцах обеих рук, а также вблизи глаз. Дозиметры помещали в светонепроницаемые оболочки, в каждой из которых в условиях электронного равновесия в виде сборки размещали по три дозиметра. В соответствии с условиями ОСПОРБ-99/2010 площадь сборки дозиметров равна 2,7 см2, толщина слоя оболочки в сборках составляет 40 мг/см2 (для кожи рук) и 300 мг/см2 для глаз [18]. Сборки стандартно применяются при аналогичных дозиметрических исследованиях [19].
Статистический анализ проводился c использованием программных пакетов Excel Office 365 Microsoft и SPSS Statistics 26 IBM.
Результаты и обсуждение
На основании проведённого анализа установлено, что все пациенты к моменту проведения терапии 177Lu-DOTA-TATE имели удовлетворительные общеклинические и биохимические показатели (табл. 2). В процессе лечения имелась тенденция к снижению уровня как Er х1012/л до 4,9-3,2 (95% ДИ 3,93±0,56) относительно показателей до лечения 5,51-4,14 (95% ДИ 4,51±0,46), так и уровня L х109/л 12,0-4,47 (95% ДИ 6,92±1,70) до лечения и 13,2-3,18 (95% ДИ 5,05±2,27) при завершении курсов ПРРТ. При этом у 7 пациентов (33%) отмечалась лейкопения 1 степени на фоне стабильно нормальных показателей уровней Tr х109/л как до 404-120 (95% ДИ 249±70,2), так и после лечения 624-136 (95% ДИ 233±114). Уровень корреляции данных по вышеописанным показателям p<0,05. Показатели АЛТ (Ед/л) продемонстрировали стабильные уровни: до лечения 74,5-9,8 (95 ДИ 24,9±18,5) и после лечения достоверно не отличались 65,2-11,6 (95% ДИ 23,8±14,9), несмотря на наличие у всех пациентов метастатического поражения паренхимы печени. Значения уровней креатинина (мкмоль/л) значимо не изменились в процессе проведения ПРРТ. Так, до лечения показатели были на уровнях 146-44 (95% ДИ 86,1±21,3), после лечения – в пределах 176-49 (95% ДИ 89,4±25,3). У одного из пациентов, с ранее установленным диагнозом хронической почечной недостаточности 1 степени, данный показатель в процессе лечения увеличился на 12%. Уровень относительно специфического для НЭО биохимического маркера хромогранина А (нг/мл) при не Гауссовском распределении показателей достоверно (p<0,05) снизился относительно значений в начале лечения: с 104 (61; 428), до 101 (39,3; 335) в 48% клинических наблюдений (табл. 2).
Переносимость процедур у всех пациентов была удовлетворительной, острых нежелательных явлений не зарегистрировано. Это свидетельствует о хорошем профиле безопасности отечественного 177Lu-DOTA-TATE. В процессе лечения у 3-х пациентов отмечалась транзиторная лейкопения 1 степени без изменения уровня нейтрофилов, у 4-х пациентов – транзиторная тромбоцитопения 1 степени тяжести (3 пациента) и у одного пациента – 2 степень. Эти нежелательные явления были временными и купировались самостоятельно, но требовали увеличения межкурсовых интервалов.
В течение первых суток от момента введения РФЛП регистрировалась максимальная экскреция свободного 177Lu-DOTA-TATE с мочой, что указывает на эффективное выведение несвязанного препарата и снижение лучевой нагрузки на организм. Через 24 ч от момента введения РФЛП мощность экспозиционной дозы на расстоянии 1 м от пациента не превышала M=9,63 мкЗв/ч во всех наблюдениях (N=98), что подтверждает соответствие нормам радиационной безопасности для персонала и окружения. Данный вид анализа продолжается и его подробные результаты будут представлены в следующих публикациях.
Через 2 мес. по завершении циклов ПРРТ у 1 одной пациентки (G3) отмечалась стабилизация метастатического процесса в печени при исходном градировании по шкале NETPET – 2b, у 17 пациентов (G1 – 8, G2 – 8, G –1) регистрировалась картина частичного ответа (рис. 3, 4) при показателях NETPET 1-2a, а у 3 пациентов (G1 – 1 и G2 – 2) – полный структурный ответ на ПРРТ при исходном градировании по шкале NETPET равном 1. Ни у одного из пациентов не зарегистрировано нарушения функции почек, проанализированное по уровню креатинина к моменту завершения терапии 177Lu-DOTA-TATE, что говорит об отсутствии значимой подострой нефротоксичности (табл. 2).
Средняя поглощённая доза на красный костный мозг, согласно проведённому анализу хромосомных аберраций лимфоцитов, от первого к четвёртому курсу возрастала: I – 0,55 Гр; II – 0,76 Гр; III – 1,63 Гр; IV – 1,38 Гр. Лучевая нагрузка на персонал, задействованный в синтезе или введении РФЛП, рассчитана в следующих показателях. Сотрудник, работая с суммарной активностью 177Lu-DOTA-TATE до 42 ГБк при времени контакта с РФЛП от 3 до 17 мин однократно может получить максимальные величины измеренных локальных доз облучения за один рабочий день: пальцы правой руки – от 3,2 ± 0,08 мГр (мизинец) до 21 ± 1 мГр (указательный палец); оправа очков вблизи глаз – 0,1 ± 0,004 мГр. Эти дозы значительно ниже годовых пределов доз для персонала, установленных ОСПОРБ-99/2010 (кожа – 500 мЗв, хрусталики глаз – 150 мЗв), что подтверждает эффективность стандартных мер радиационной защиты персонала [18].
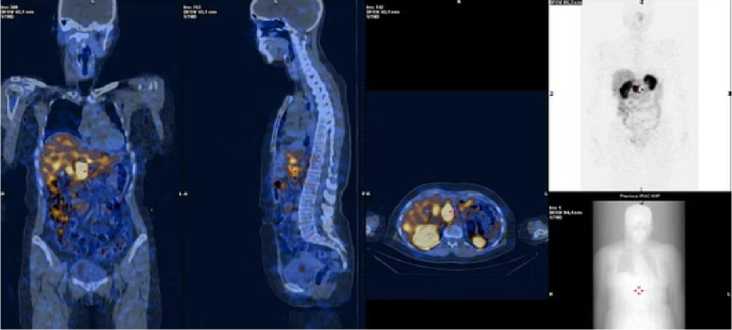
Рис. 3. ОФЭКТ/КТ пациентки Б., с метастатическим поражением печени при НЭО после первого введения 177Lu-DOTA-TATE: множественные мтс-очаги в печени.
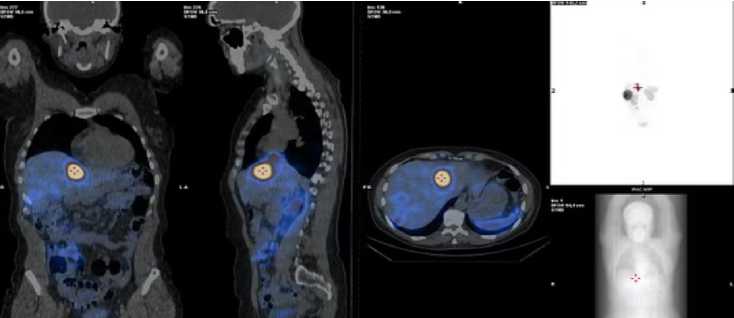
Рис. 4. ОФЭКТ/КТ пациентки Б., с метастатическим поражением печени при НЭО после
6 введений 177Lu-DOTA-TATE (Асумм.=39,7 ГБк): исчезновение множественных мтс-очагов в печени, единичный мтс-очаг в левой доле. Картина частичного ответа на лечение.
На основании анализа полученных результатов в соответствии с поставленными задачами научного исследования были сделаны выводы:
-
1) метод ПРРТ 177Lu-DOTA-TATE, синтезированным из отечественных фармакологических субстанций в условиях производственной аптеки с правом изготовления РФЛП и его применение в МРНЦ им. А.Ф. Цыба, является безопасным при терапии метастатических ГЭП-НЭО;
-
2) в рамках предварительного анализа результатов лечения по данным ОФЭКТ/КТ всего тела после проведённых по индивидуальным программам курсов ПРРТ установлено: в 4,8% наблюдений отмечена стабилизация метастатического процесса, в 14,3% – полный и в 80,9% – частичный ответ на лечение;
-
3) к моменту завершения терапии 177Lu-DOTA-TATE гематологическая токсичность в виде лейкопении 1 степени выявлена у 9 пациентов (43%); непрерывное систематическое накопление повреждений в лимфоцитах крови пациентов в форме аберраций хромосом наблюдается со средним интервалом в 2 мес., при этом ожидается увеличение поглощённой дозы на кровь (на костный мозг) за курс, вплоть до безопасного предела 2 Гр, что требует дальнейшего мониторинга и оптимизации режимов подбора лечебных активностей РФЛП;
-
4) проведение процедур синтеза РФЛП и ПРРТ 177Lu-DOTA-TATE при соблюдении норм радиационной безопасности не представляет опасности для персонала.
Заключение
Отсутствие серьёзных нежелательных явлений, особенно нефротоксичности, подтверждает адекватность нефропротективного протокола и выбранных значений лечебной активности 177Lu-DOTA-TATE [20]. Первичная конечная точка исследования в виде оценки объективного ответа на лечение была достигнута; вторичная конечная точка не достигнута, т.к. наблюдение за данной группой пациентов в настоящее время продолжается. Использование метода биологической дозиметрии позволило детально оценить кумулятивную лучевую нагрузку на пациентов и подчеркнуть влияние предшествующих диагностических процедур. Контроль доз облучения персонала свидетельствует о возможности безопасного внедрения методики в рутинную практику при соблюдении регламентов радиационной безопасности. Высокий процент (ЧО+ПО=95,2%) объективных ответов на проведённое лечение у пациентов с метастатическими ГЭП-НЭО подчёркивает клиническую значимость ПРРТ, а проведённое исследование в целом закладывает основу для дальнейшего развития данного вида радиотаргетной терапии в России и расширения показаний к её применению при различных формах НЭО, а также при раках с нейроэндокринной дифференцировкой и нейроэндокринных раках.


