ПЭТ/КТ и радиогенный риск: особенности влияния факторов риска на прогноз дожития среди населения Озёрского городского округа
Автор: Осипов М.В., Сокольников М.Э., Новикова Т.С.
Рубрика: Научные статьи
Статья в выпуске: 3 т.33, 2024 года.
Бесплатный доступ
В статье представлены результаты анализа факторов риска, влияющих на смертность от злокачественных новообразований (ЗНО) среди жителей Озёрского городского округа, обследованных методом позитронно-эмиссионной компьютерной томографии (ПЭТ/КТ) в Челябинском областном клиническом центре онкологии и ядерной медицины. Исследование выполнено ретроспективно когортным методом. Данные о диагностическом облучении пациентов при проведении ПЭТ/КТ собраны за период с 2010 по 2018 гг. Проанализирована информация о половозрастном распределении обследованных, количестве выполненных исследований, суммарной активности введённого радиофармпрепарата и дозах облучения пациентов при проведении ПЭТ/КТ, а также наличии контакта с производственным радиационным воздействием для работников ПО «Маяк». Выполнен расчёт количества сопутствующих компьютерно-томографических исследований и суммарной эффективной дозы облучения пациента за счёт КТ. Для онкологических пациентов получена информация о стадии ЗНО, назначении химио- и лучевой терапии, жизненном статусе и причинах смерти на дату 31 декабря 2021 г. Оценка влияния повторных ПЭТ/КТ с учётом других факторов риска радиационной и нерадиационной природы выполнена при помощи регрессионного анализа в многофакторной математической модели, основанной на дискретном распределении зависимой переменной. Установлено, что проведение неоднократных ПЭТ/КТ-исследований онкологическим пациентам в краткосрочный период средней длительностью 3,5 года, сопряжённое с воздействием дозы диагностического облучения до 400 мЗв, не связано с ухудшением прогноза дожития пациентов. Основными факторами риска нерадиационной природы, влияющими на смертность от ЗНО, является достигнутый возраст пациента на дату проведения исследования и стадия ЗНО.
Пэт/кт, компьютерная томография, производственное облучение, диагностическое облучение, лучевая терапия, химиотерапия, радиогенный риск
Короткий адрес: https://sciup.org/170206287
IDR: 170206287 | УДК: 614.876:616-073.75 | DOI: 10.21870/0131-3878-2024-33-3-108-122
The role of repeated PET/CT scans and additional risk factors in predicting cancer mortality among Ozyorsk residents
The article aims at assessing the impact of diagnostic radiation exposure from positron-emission computed tomography (PET/CT) examinations and other risk factors on cancer mortality among residents of the nuclear city of Ozyorsk, examined at the Chelyabinsk Regional Clinical Center of Oncology and Nuclear Medicine. Data on gender and age at exposure, the number of PET/CT examinations, total activity of the administered radiopharmaceuticals and radiation doses delivered to patients during PET/CT examinations, were retrospectively collected. Information on potential contact with occupational radiation exposure for Mayak PA workers was included in the study. The number of additional routine computed tomography examinations, performed outside the Center of Nuclear Medicine, and the related effective dose of diagnostic radiation were calculated. For cancer patients, information on the stage of malignancy, chemotherapy, and radiotherapy administered were collected. Information on vital status and cause of death was updated as of December 31, 2022. The impact of repeated PET/CT, taking into account other radiation and non-radiation risk factors, was assessed using multivariate regression analysis. It was found that repeated PET/CT examinations of cancer patients, resulting in a total cumulative radiation dose up to 400 mSv, were not associated with a negative survival prognosis over an average follow-up period of 3.5 years. The main non-radiation risk factors contributing to cancer mortality among the study cohort were age at exposure and the stage of malignancy.
Текст научной статьи ПЭТ/КТ и радиогенный риск: особенности влияния факторов риска на прогноз дожития среди населения Озёрского городского округа
Позитронно-эмиссионная томография (ПЭТ) – современный радиоизотопный метод диагностической визуализации, получивший широкое распространение в онкологии и позволяющий проводить неинвазивные исследования на ранних стадиях онкологических заболеваний. Данный метод исследования основан на использовании радиофармацевтических препаратов (РФП), содержащих короткоживущие радионуклиды. Наиболее часто применяемым РФП является 18-фтор-2-дезокси-D-глюкоза (18-ФДГ), в состав которого входит в - активный изотоп 18F. Поскольку глюкоза является основным источником энергии для клеток, метаболизм 18-ФДГ в организме пациента позволяет визуализировать активность тех областей, которые используют больше глюкозы, по сравнению с нормальными тканями, такими как воспалительные очаги и неопластические процессы [1].
В зависимости от вида исследования и антропометрических данных пациента, при средней введённой активности изотопа 18F 350-500 МБк, ожидаемая величина эффективной дозы (ЭД) за одно исследование ПЭТ составляет порядка 5-10 мЗв [2]. Для получения изображения анатоми-
ческих границ органов и тканей, окружающих очаги накопления 18-ФДГ, ПЭТ сочетают с компьютерной томографией (ПЭТ/КТ) [3], что позволяет повысить информативность исследования, однако, вместе с этим повышается и уровень облучения пациента за счёт воздействия рентгеновского излучения компьютерного томографа.
Типовым сценарием облучения пациента при выполнении большинства ПЭТ/КТ является проведение сканирований по протоколу «whole-body» («всё тело»), в отличие от рутинных КТ, при которых воздействие рентгеновского излучения является, как правило, локальным. С учётом дозы от РФП, средняя ожидаемая величина суммарной ЭД за одно исследование ПЭТ/КТ составляет порядка 15-25 мЗв. Оценка динамики опухолевого процесса [4] является причиной назначения повторных ПЭТ/КТ, что приводит к увеличению суммарной дозы диагностического облучения. Дополнительным фактором увеличения дозы диагностического облучения онкологических пациентов является проведение рутинных КТ-исследований [5].
Население городов атомной промышленности относится к категории лиц, связанной с потенциально повышенным риском развития радиационно-индуцированных эффектов, как вследствие воздействия производственного излучения на персонал предприятий ядерно-промышлен-ного комплекса, так и у потомков людей, получивших облучение при выполнении профессиональных обязанностей [6]. Таким образом, сочетанное влияние нескольких различных радиационных факторов требует особого внимания при оценке потенциального радиационного риска от диагностического облучения с учётом наличия профессионального радиационного анамнеза. Необходимо отметить, что в некоторых случаях при проведении одного исследования ПЭТ/КТ уровни облучения пациентов могут превышать годовые уровни, регламентированные для персонала радиационно-опасных предприятий (20 мЗв).
По данным литературы дополнительными факторами риска, влияющими на прогноз дожития онкологических пациентов, могут являться радиационное воздействие при лучевой терапии [7], токсическое воздействие на организм пациента химиотерапии [8, 9] при лечении как единственной опухоли, так и первично-множественных злокачественных новообразований (ЗНО) [10]. Совокупное воздействие нескольких факторов риска радиационной и нерадиационной природы требует дифференцированной оценки их влияния на прогноз дожития пациентов с целью корректного обоснования проведения процедур ПЭТ/КТ и оптимизации уровней лучевой нагрузки при проведении диагностических исследований.
Исходя из вышеизложенного, целью работы является оценка влияния диагностического облучения при ПЭТ/КТ на смертность от ЗНО среди онкологических пациентов, подвергающихся сочетанному воздействию нескольких факторов риска радиационной и нерадиационной природы, включая воздействие производственного и диагностического излучения.
Материалы и методы
Исследование проведено ретроспективно когортным методом. Данные для исследования предоставлены центром позитронно-эмиссионной томографии (ПЭТ-центр) Челябинского областного клинического центра онкологии и ядерной медицины (ЧОКЦО и ЯМ). Информация о жителях Озёрского городского округа, обследованных в ПЭТ-центре, была собрана за период с момента внедрения ПЭТ в клиническую практику в ЧОКЦО и ЯМ в 2010 г.
Критериями включения в когорту являлись наличие постоянной регистрации по месту жительства пациента в пределах Озёрского городского округа и прохождение обследования в ПЭТ-центре ЧОКЦО и ЯМ Челябинска в период с 1 января 2010 г. по 31 декабря 2018 г. Критерии исключения из когорты – отсутствие информации о жизненном статусе на дату окончания наблюдения и/или обследование пациента по поводу неонкологического заболевания.
Датой входа под наблюдение считалась дата проведения первого обследования пациента в ПЭТ-центре ЧОКЦО и ЯМ с помощью ПЭТ/КТ сканера Siemens Biograph-64 или Biograph-40. Дата выхода из-под наблюдения – 31 декабря 2021 г., либо дата смерти пациента, если данное событие наступало раньше.
Оценка ЭД облучения пациента за счёт введения РФП выполнялась по методике, предложенной МКРЗ [11], оценка ЭД за счёт компьютерной томографии – согласно методическим указаниям МУ 2.6.1.2944-11 «Контроль эффективных доз пациентов при рентгенологических исследованиях». Данные о предшествующих КТ-исследованиях пациентов получены из базы данных медико-дозиметрического регистра населения Озёрского городского округа, обследованных при помощи КТ в лечебных учреждениях города Озёрск и Челябинской области за период с 1993 по 2019 гг. («Регистр КТ») [12].
Информация о диагнозе заболевания ЗНО, стадии заболевания, и назначении лучевой и химиотерапии была получена из базы данных противоракового регистра ЧОКЦО и ЯМ. Для удобства статистической обработки оценка распространённости опухолевого процесса проводилась с помощью 4-стадийной клинической классификации, отражающей размер опухоли и взаимоотношение её с окружающими тканями, при которой I стадия соответствовала наименьшей распространённости, IV стадия – наибольшей распространённости с наличием метастазов.
Методы статистического анализа
Для характеристики распределения параметра использовалось среднее значение и его стандартная ошибка. Для характеристики дозиметрических величин, распределение которых отличалось от нормального, использовалось медианное значение, минимальное и максимальное значение параметра. Уровни воздействия диагностического излучения на пациента при проведении ПЭТ/КТ определялись дискретной переменной, характеризующейся количеством выполненных исследований, а также непрерывной переменной, характеризующейся величиной суммарной ЭД, накопленной за период наблюдения.
Реализация наблюдаемого исхода (смерти от ЗНО) количественно описывалась бинарной переменной, принимающей значение 1 в случае, если в течение периода наблюдения основной причиной смерти пациента являлось ЗНО, и 0 в случае, если на дату окончания наблюдения пациент был жив, либо умер от причин, не связанных с ЗНО. Для оценки частот реализации изучаемого исхода использовался показатель смертности, равный отношению количества случаев смерти от ЗНО к общему количеству наблюдений за период, равный одному году.
Математическое моделирование выполнялось с использованием программного пакета для статистической обработки и анализа данных Stata [13]. Основной гипотезой исследования, тестируемой в модели, являлось различие в частоте смертности от ЗНО среди лиц, неоднократно подвергавшихся воздействию диагностического излучения при ПЭТ/КТ, по сравнению с обследованными однократно, с учётом других факторов риска радиационной и нерадиационной природы.
Для оценки взаимосвязи показателя смертности с различными уровнями радиационного воздействия в результате проведения повторных ПЭТ/КТ применялась регрессия Пуассона [14] при предположении, что распределение вероятности изучаемого исхода подчинено пуассоновскому закону (1):
P(nlA,h)= -(^ e -A-h , (1)
где P(nlA,h) - распределение вероятности исхода; n - количество случаев наблюдаемого исхода; А - количество человеко-лет наблюдения; h - показатель смертности.
Сравнительная оценка частот наступления изучаемого эффекта выполнялась при помощи многофакторной регрессии с учётом взаимодействия между регрессорами. Для описания зависимости влияния факторов риска на величину годового показателя смертности h использовалась обобщённая линейная модель вида у = Po + Pt + е , вычисляемая при помощи преобразующей функции, в качестве которой использован натуральный логарифм (2):
ln-hlA)=fl0 + fli + E , (2)
где в о - константа регрессии; e i - факторы риска, s - ошибка модели.
Для вычисления относительной частоты наступления смерти от ЗНО (IRR), связанной с воздействием нескольких факторов риска e i , включая воздействие дозы облучения ( d ) при ПЭТ/КТ, использовалось следующее соотношение (3):
exp -ln(A)+Po+Pi +P-l+d))
IRR -d) = exp -i-nW+Po+Pi+ Pd) ’ (3)
где IRR (d) - отношение частот наступления смерти от ЗНО в экспонированной и неэкспонированной группах; e d - коэффициент при дозе; e i - коэффициенты регрессии при других факторах риска.
Параметры, характер влияния которых на зависимую переменную был нелинейным, перед включением в модель подвергались линеаризации. Подгонка модели осуществлялась путём последовательного включения линеаризованных параметров в модель. Оценка качества подгонки модели регрессии с различным количеством параметров e i выполнялось при помощи теста отношения правдоподобия (LRT). Оценка дисперсии зависимой переменной, описанной при помощи модели, проводилась при помощи критерия «псевдо-R2». Расчёт доверительных интервалов для заданного 95% уровня значимости выполнялся при помощи дельта-метода, различия считались статистически значимыми при p<0,05 [14].
Результаты и обсуждение
Проанализирована информация из 651 протокола исследования 347 пациентов, проживавших в Озёрском городском округе и обследованных по клиническим показаниям в ПЭТ-центре за период с 2010 по 2019 гг. В исследуемой когорте 43,1% мужчин и 56,9% женщин, на момент проведения исследования лиц, достигших возраста от 19 до 91 года. Половозрастное распределение исследуемой когорты и его приближение функцией нормального распределения представлено на рис. 1.
Средний возраст обследованных составил 57 лет, стандартная ошибка (с.о.) - 0,7, распределение пациентов по возрасту на дату исследования отличалось от нормального и имело смещение в область старших возрастов (р=0,0003, медиана возраста - 59 лет). Среднее значение и медиана возрастного распределения для мужчин составили 56 и 58 лет, для женщин - 58 и 60 лет соответственно.
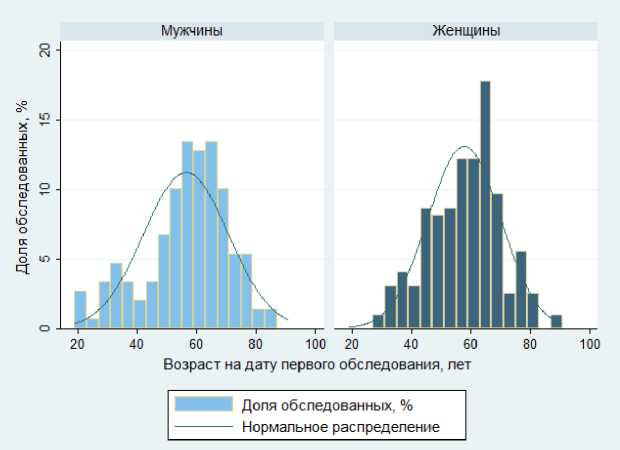
Рис. 1. Характеристика наблюдаемой когорты по возрасту на дату проведения исследования и полу.
У 95,9% пациентов исследуемой группы на момент проведения исследования был установлен диагноз ЗНО. Характеристика исследуемой когорты в зависимости от локализации ЗНО и пола обследованных представлена в табл. 1.
Таблица 1
Характеристика заболеваемости ЗНО в исследуемой когорте в распределении по локализации ЗНО и полу
|
Локализация ЗНО |
n |
% |
Мужчины, (%) |
Женщины, (%) |
|
Губа, полость рта и глотка |
4 |
1,2 |
4 (2,8) |
0 (0,0) |
|
Органы пищеварения |
66 |
19,9 |
36 (25,4) |
30 (15,9) |
|
Органы дыхания |
45 |
13,6 |
38 (26,8) |
7 (3,7) |
|
Кожа, кости, соединительная ткань и молочная железа |
77 |
23,3 |
10 (7,0) |
67 (35,4) |
|
Выделительная и репродуктивная системы |
67 |
20,2 |
18 (12,7) |
49 (25,9) |
|
Головной мозг и ЦНС |
19 |
5,7 |
8 (5,6) |
11 (5,8) |
|
Кроветворная система |
53 |
16,0 |
28 (19,7) |
25 (13,2) |
|
Всего |
331 |
100,0 |
142 (100,0) |
189 (100,0) |
Наиболее часто встречающимся диагнозом при обследовании ПЭТ/КТ у мужчин являлся рак лёгкого (34 случая, 23,9%), среди женщин – ЗНО молочной железы (52 случая, 27,5%). В 53 случаях (16,0%) причиной обследования у мужчин и женщин являлось заболевание кроветворной и лимфоидной тканей. Из них лимфомы – 14 случаев, болезнь Ходжкина – 16 случаев, другие ЗНО лимфоидной ткани – 20 случаев, множественная миелома – 1 случай, острый миелоидный лейкоз – 1 случай. Количество лиц, которым назначалась химиотерапия (в том числе в виде адъювантной терапии), оставило 204 человека (59,0%), среди них 85 мужчин (41,7%) и 119 женщин (58,3%).
Стадия ЗНО была установлена для 315 пациентов (94,3%), из которых 12,1% диагнозов относились к 1 стадии, 26,3% – 2 стадии, 32,1% – 3 стадии, 29,2% – 4 стадии развития ЗНО. Между количеством выполненных ПЭТ/КТ и стадией ЗНО наблюдалась слабая корреляционная связь (R2=0,12).
Характеристика радиационного воздействия
Исследуемая группа включает 64,8% однократно обследованных и 35,2% пациентов, проходивших повторные ПЭТ/КТ. Максимальное количество повторных исследований одного пациента в течение периода наблюдения составило 11. Медиана распределения количества исследований для мужчин составила 1,9, для женщин – 1,7. Характеристика изучаемой когорты по количеству выполненных обследований (n), введённой активности ФДГ (Афдг) и средней суммарной эффективной дозе (ЭД) за все исследования ПЭТ/КТ представлена в табл. 2.
Таблица 2
Количество и доля выполненных ПЭТ/КТ, средняя суммарная активность введённого РФП (A Фдг ) и средняя суммарная ЭД за все исследования
|
ПЭТ/КТ |
n |
ПЭТ/КТ, % |
Афдг (с.о.) |
ЭД (с.о.) |
|
1 |
225 |
64,8 |
391,2 (5,6) |
22,1 (0,5) |
|
2 |
66 |
19,1 |
806,8 (14,9) |
47,4 (1,3) |
|
3 |
19 |
5,5 |
1185,8 (36,9) |
74,8 (3,9) |
|
4-5 |
22 |
6,3 |
1682,2 (63,7) |
110,2 (10,3) |
|
6-8 |
11 |
3,2 |
2599,8 (130,2) |
192,6 (23,3) |
|
9> |
4 |
1,2 |
5678,0 (н/о) |
327,6 (93,2) |
|
Всего |
347 |
100,0 |
- |
- |
Среднее значение суммарной введённой активности РФП в изучаемой когорте с учётом повторных исследований составило 660,6 МБк (медиана – 420 МБк, минимум – 200 МБк, максимум – 5678,0 МБк), что соответствовало средней ЭД 7,3 (с.о. – 0,1) мЗв (медиана – 5,9 мЗв).
Средняя суммарная величина накопленной ЭД с учётом повторных ПЭТ/КТ-исследований для мужчин и женщин составила 41,2 мЗв. Распределение величины накопленной суммарной ЭД за счёт всех ПЭТ/КТ-исследований в зависимости от пола представлено на рис. 2.
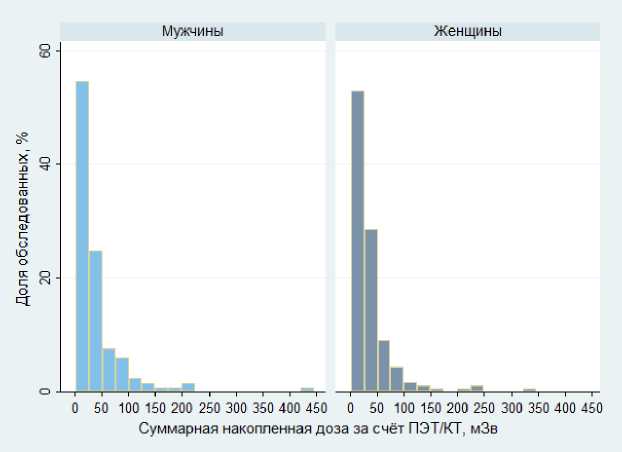
Рис. 2. Распределение величины накопленной суммарной эффективной дозы облучения пациентов за счёт всех исследований ПЭТ/КТ, мЗв.
Среднее значение суммарной ЭД за все ПЭТ/КТ-исследования составило для мужчин 42,8 мЗв (минимум – 10,4 мЗв, медиана – 26,4 мЗв, максимум – 420,8 мЗв), для женщин – 40,1 мЗв (минимум – 10,5 мЗв, медиана – 26,3 мЗв, максимум – 328,8 мЗв). Наименьшая величина суммарной ЭД при проведении повторных исследований для мужчин составила 30,7 мЗв, среднее значение – 83,9 мЗв (медиана – 58,1 мЗв, максимум – 420,8 мЗв), для женщин соответственно 33,0 мЗв и 73,8 мЗв (медиана – 52,7 мЗв, максимум – 328,8 мЗв).
Распределение количества проведённых обследований по анатомической области исследования и полу представлено в табл. 3.
Таблица 3
Количество и доля обследований ПЭТ/КТ в зависимости от анатомической области исследования и пола
|
Область исследования |
n |
% |
Мужчины (%) |
Женщины (%) |
|
Головной мозг |
5 |
0,8 |
4 (1,4) |
1 (0,3) |
|
Грудная клетка |
16 |
2,5 |
11 (3,7) |
5 (1,4) |
|
ГК и БП |
22 |
3,4 |
17 (5,7) |
5 (1,4) |
|
ГК, БП и МТ |
43 |
6,6 |
24 (8,1) |
19 (5,4) |
|
БП и МТ |
26 |
4,0 |
15 (5,1) |
11 (3,1) |
|
Всё тело |
539 |
82,8 |
225 (76,0) |
314 (88,5) |
|
Всего |
651 |
100,0 |
100,0 |
100,0 |
ГК – грудная клетка; БП – брюшная полость; МТ – малый таз.
Большинство проведённых ПЭТ/КТ-исследований (82,8%) выполнялось с использованием протокола “whole body” («всё тело»). В остальных случаях (при использовании ПЭТ только в режиме КТ) область исследования была ограничена зоной интереса.
Количественная характеристика исследуемой когорты по наличию воздействия других факторов риска радиационной и нерадиационной природы в распределении по полу представлена в табл. 4.
Таблица 4
Количественная характеристика других факторов риска в распределении по полу
|
Фактор риска |
n |
% |
Мужчины,% |
Женщины,% |
|
ПО «Маяк» |
73 |
21,1 |
53 (72,6 %) |
20 (27,4 %) |
|
КТ, кроме ПЭТ/КТ |
243 |
69,9 |
110 (45,5 %) |
133 (54,5 %) |
|
Лучевая терапия |
90 |
25,9 |
36 (40 %) |
54 (60 %) |
|
Химиотерапия |
204 |
59,0 |
85 (41,7 %) |
119 (58,3 %) |
|
ЛТ и ХТ |
63 |
18,2 |
22 (34,9 %) |
41 (65,1 %) |
ЛТ – лучевая терапия; ХТ – химиотерапия; КТ – компьютерная томография.
Доля работников, нанятых на ПО «Маяк» в период с 1948 по 2008 гг., составила 21,1%. Средний возраст обследованных работников составил 62,2 года (с.о. – 1,2), медиана – 63 года. Количество работников основных производств (реакторное, радиохимическое и/или плутониевое) ПО «Маяк» составило 59 человек (80,8%), вспомогательных производств (ремонтно-механический завод и завод водоподготовки) – 14 человек (19,2%). Количество работников, которые по данным дозиметрической системы «Доза-2013» [15] имели информацию об учтённых дозах профессионального облучения, составило 49 человек (67,1%).
Более 2/3 изучаемой когорты (69,6%) подвергались воздействию диагностического облучения за счёт компьютерной томографии, проведённой в Клинической больнице № 71 Озёрска и других медицинских учреждениях Челябинской области за период с 1993 по 2019 гг. Суммарное количество всех КТ-исследований пациентов изучаемой группы, выполненных вне ПЭТ-центра, составило 866, с максимальным количеством исследований одного пациента, равным 27. Среднее суммарное количество КТ-исследований в изучаемой когорте составило 3,3 (с.о. – 0,23), медиана – 2,0. Распределение суммарной величины накопленной ЭД за счёт КТ-исследований представлено на рис. 3.
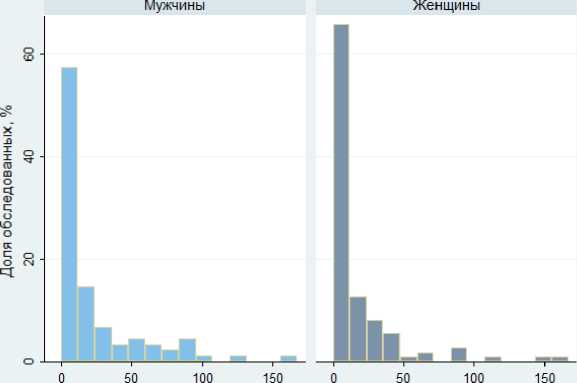
Суммарная накопленная величина ЭД от всех КТ, кроме ПЭТ/КТ, мЗв
Рис. 3. Распределение суммарной величины накопленной ЭД за счёт КТ-исследований, выполненных вне ПЭТ-центра.
Медиана суммарной ЭД для мужчин составила 8,2 мЗв, максимальное значение – 174 мЗв, для женщин – 6,3 мЗв и 167,4 мЗв соответственно. Таким образом, максимальная величина суммарной накопленной ЭД диагностического облучения пациентов, включая ПЭТ/КТ и КТ, выполненные вне ПЭТ-центра, составила для мужчин 461,5 мЗв (медиана – 40,1 мЗв), для женщин – 391,1 мЗв (медиана – 40,7 мЗв).
Доля пациентов, которым назначалась лучевая терапия, составила 25,9%. Доза облучения пациента за счёт проведения лучевой терапии рассчитывалась согласно рекомендациям [16]. Среднее значение суммарной дозы облучения очага ЗНО, накопленной за счёт нескольких сеансов фракционированного лечения, составило 38,96 Гр (с.о. – 1,85), медиана – 36 Гр, минимальное значение – 8 Гр, максимальное значение – 94 Гр. Для мужчин среднее значение и медиана составили 35,1 Гр (с.о. – 2,5), медиана – 32 Гр, максимальное значение – 70 Гр, для женщин – 41,8 Гр (с.о. – 2,6), медиана – 42 Гр, максимальное значение – 94 Гр).
Жизненный статус и функция дожития
По состоянию на 31.12.2022 г. количество умерших в исследуемой группе составило 238 (68,9%), из них 110 мужчин (46,2%) и 128 женщин (53,8%). Количество онкологических пациентов, основной причиной смерти которых являлся диагноз ЗНО, составило 221 (92,9% от общего числа умерших), среди них 101 мужчина (45,7%) и 120 женщин (54,3%). Доля злокачественных опухолей, подтверждённых на аутопсии, составила 94%.
Средняя продолжительность периода наблюдения за каждым пациентом исследуемой группы составила 3,5 года (с.о. – 0,17), максимум – 11 лет. 5-летняя выживаемость среди лиц изучаемой когорты составила 30,5%. Распределение доли умерших от всех причин в зависимости от достигнутого возраста на дату смерти и пола представлено на рис. 4.
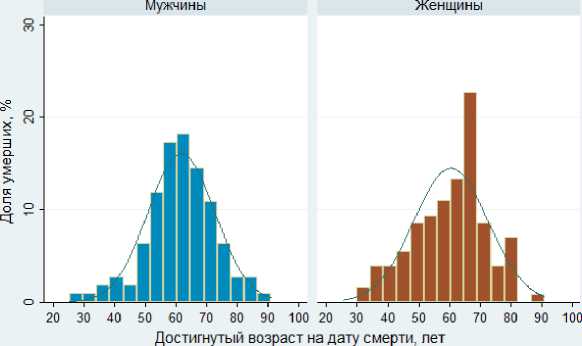
^^Н Доля умерших ------ Нормальное распределение
Рис. 4. Доля умерших от всех причин в распределении по возрасту и полу.
Распределение по достигнутому возрасту на момент смерти среди мужчин и женщин было близко к нормальному (р=0,08), среднее значение составляет 61,1 год (с.о. – 0,75). Среднее значение достигнутого возраста на момент смерти для мужчин – 61,2 года, медиана – 61,9 лет, для женщин – 60,5 лет, медиана – 63,1 года. На дату окончания наблюдения 50% мужчин и женщин исследуемой когорты пробыли под наблюдением более 908 дней (t 50 =2,5 года). Функция дожития для пациентов исследуемой когорты приведена на рис. 5.
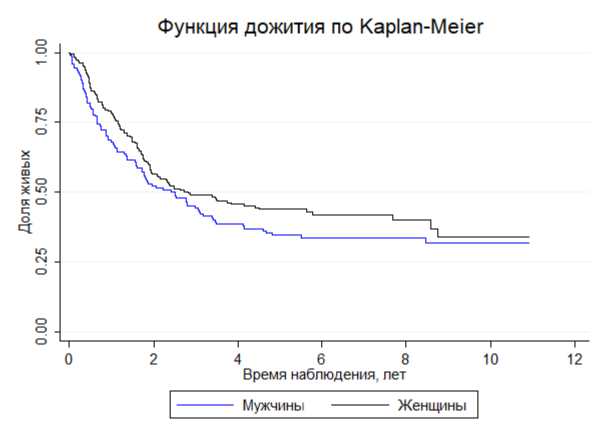
Рис. 5. Кривая выживаемости в изучаемой когорте.
Исследуемая когорта характеризуется высокой интенсивностью вымирания, более выраженной среди мужчин. Количество пациентов, умерших в течение первого года наблюдения, составило 38,2% от общего количества умерших, 5-летняя выживаемость составила 29,5% (для мужчин – 26,9%, для женщин – 31,3%). Доля выживших на дату окончания наблюдения составила 29,2% при среднем возрасте на момент первого обследования 59,6 лет и средней длительности периода наблюдения 7,0 лет.
Анализ риска
Среди населения Озёрского городского округа, обследованного методом ПЭТ/КТ в Челябинском областном клиническом центре онкологии и ядерной медицины, доля лиц, умерших от ЗНО на дату окончания наблюдения составляет 61,3% (64,8% для мужчин и 58,1% для женщин). Оценка влияния факторов риска на смертность от ЗНО, и от всех причин среди лиц изучаемой когорты представлена в табл. 5.
Таблица 5
Оценка влияния факторов риска радиационной и нерадиационной природы на смертность от ЗНО и от всех причин
|
Параметр |
Смертность от ЗНО |
Смертность от всех причин |
||||
|
IRR |
р |
ДИ 95% |
IRR |
р |
ДИ 95% |
|
|
Пол (мужчины) |
1,15 |
0,35 |
0,86-1,55 |
1,18 |
0,26 |
0,89-1,58 |
|
Возраст* |
1,25 |
0,0001 |
1,11-1,40 |
1,25 |
0,0001 |
1,11-1,40 |
|
Стадия ЗНО |
1,42 |
0,0001 |
1,22-1,66 |
1,43 |
0,0001 |
1,23-1,66 |
|
ПО «Маяк» |
1,16 |
0,42 |
0,82-1,63 |
1,13 |
0,47 |
0,81-1,58 |
|
Количество ПЭТ/КТ |
0,88 |
0,011 |
0,80-0,97 |
0,88 |
0,009 |
0,81-0,97 |
|
КТ, кроме ПЭТ |
0,99 |
0,54 |
0,95-1,03 |
0,98 |
0,31 |
0,94-1,02 |
|
ЛТ |
0,98 |
0,02 |
0,98-1,0 |
0,99 |
0,02 |
0,98-1,00 |
|
ХТ |
1,24 |
0,23 |
0,87-1,75 |
1,24 |
0,21 |
0,88-1,74 |
|
ЛТ и ХТ |
1,81 |
0,021 |
1,09-2,96 |
1,77 |
0,02 |
1,09-2,88 |
* возраст на дату первого исследования по категориям с интервалом в 10 лет; ЛТ – лучевая терапия; ХТ – химиотерапия; КТ – компьютерная томография.
Статистически значимое влияние на частоту реализации летальных исходов по причине ЗНО среди пациентов исследуемой когорты оказывают возраст на момент обследования (95% ДИ 1,11-1,40) и стадия ЗНО (95% ДИ 1,22-1,66). Частота смертности от ЗНО у онкологических пациентов, проходивших повторные ПЭТ/КТ, была ниже (95% ДИ 0,80-0,97) по сравнению с однократно обследованными. Модификация количества выполненных ПЭТ/КТ стадией ЗНО статистически незначимо изменяла эффект от воздействия повторных диагностических процедур на частоту смерти от ЗНО (ОР=0,99; р=0,97).
Включение в модель переменной, содержащей значение накопленной суммарной ЭД за счёт всех ПЭТ/КТ-обследований, выполненных в течение периода наблюдения, показало статистически незначимое повышение показателя смертности как от ЗНО, так и от всех причин (ОР=1,0014; 95% ДИ 0,99-1,005; р=0,45). Модификация эффекта дозы стадией ЗНО незначимо изменяла результаты оценки ОР (95% ДИ 0,99-1,024; р=0,26). Количество КТ-исследований, выполненных вне ПЭТ-центра, сопряжённых с воздействием средней дозы облучения 17,5 мЗв (максимум – 174 мЗв), незначимо влияло на частоту смерти от ЗНО (ОР=0,99; 95% ДИ 0,95-1,03).
Статистическая значимость наличия контакта с профессиональным радиационным воздействием у пациентов, нанятых на основные и вспомогательные производства ПО «Маяк», не была достигнута на уровне 95% ДИ (0,82-1,63). Полученный результат может быть следствием неопределённости, связанной с различиями в накопленной дозе профессионального облучения, а также отсутствием среди лиц, включённых в изучаемую когорту, информации о статусе курения, влияние которого значимо повышает риск смерти от ЗНО среди персонала [17].
Влияние дозы облучения, полученной пациентами вследствие проведения лучевой терапии, статистически значимо не влияло на увеличение частоты реализации летальных исходов (95% ДИ 0,98-1,0). Данный факт свидетельствует о правильном подборе дозы лучевого лечения и режима её фракционирования. В то же время, в подгруппе пациентов, получавших химиолучевое лечение, было обнаружено статистически значимое повышение риска смерти (95% ДИ 1,09-2,96) при отсутствии различий в стадии ЗНО для сравниваемых подгрупп (p>0,5). При этом, данное повышение риска было значимо выражено лишь для подгруппы населения (ОР=2,21; 95% ДИ 1,3-3,7). Полученные различия свидетельствуют о необходимости дальнейшего, более детального, изучения вопроса о влиянии сочетанного воздействия данных факторов лечения на прогноз дожития пациентов.
Величина суммарной дозы облучения при повторных ПЭТ/КТ, достигающая значений порядка 0,3-0,4 Зв, свидетельствует о наличии потенциального радиационного фактора риска развития последующих ЗНО [10]. Особенностью наблюдаемой когорты является относительно небольшая средняя длительность периода наблюдения – 3,5 года (t 50 =2,5 года), не достигающая минимальной величины лаг-периода (5 лет), рекомендованной МКРЗ для оценки канцерогенных рисков. С учётом того, что 5-летняя выживаемость в изучаемой когорте составила 30,5%, а доля лиц, живых на дату окончания исследования, составляет 31,2%, дальнейшее наблюдение за когортой может дать дополнительные данные для оценки реализации радиационно-индуцированных первично-множественных ЗНО.
По данным литературы [18] прогнозируемая величина пожизненного атрибутивного риска смерти от ЗНО (LAR) среди пациентов, обследованных на ПЭТ/КТ в возрасте 40 лет в средней ЭД 20,6 мЗв, сопоставимой с уровнем однократного облучения в изучаемой когорте, составляет 0,169% для мужчин и 0,126% для женщин. Согласно данным настоящего исследования фактическая величина верхнего предела возраста дожития онкологических пациентов составляет 61 год, что существенно ниже используемого возрастного предела при оценке LAR для обследованных методом ПЭТ/КТ (85-120 лет) [19]. При этом, частота развития первично-множественных ЗНО, для которых указанные оценки LAR могут быть действительно применимы, в 1,3 раза ниже, чем частота заболеваемости первыми ЗНО [7, 10], что является источником неопределённости при прогнозировании ожидаемой величины риска смертности среди онкологических пациентов, обследованных на ПЭТ/КТ.
Заключение
Обследования пациентов методом ПЭТ/КТ сопряжены с воздействием ионизирующего излучения в диапазоне малых и средних доз. Суммарная величина эффективной дозы при повторных ПЭТ/КТ в зависимости от количества проведённых исследований находилась в интервале от 31,2 до 420,8 мЗв. Воздействие диагностического облучения при проведении повторных ПЭТ/КТ-исследований в краткосрочном периоде средней длительностью 3,5 года не ухудшало прогноз выживаемости онкологических пациентов. Основными факторами риска, связанными с увеличением частоты смертности среди онкологических пациентов в ближайший период после проведения исследований ПЭТ/КТ, являлись возраст пациента на дату первого исследования и стадия злокачественного новообразования.
Результаты проведённого исследования свидетельствуют о необходимости более детального изучения в исследуемой когорте фактора профессионального радиационного воздействия у персонала ПО «Маяк» с учётом анализа дозовых историй работников и фактора курения, а также сочетанного воздействия химиолучевой терапии. Расширение периода наблюдения за изучаемой когортой позволит выполнить оценку канцерогенного риска первично-множественных злокачественных новообразований, потенциально связанного с воздействием диагностического облучения при ПЭТ/КТ с учётом необходимого лаг-периода.
Понимание взаимосвязи между дозой диагностического облучения и радиогенным риском является ключевым аспектом для дальнейшего улучшения стратегий лечения и мониторинга онкологических пациентов.
Список литературы ПЭТ/КТ и радиогенный риск: особенности влияния факторов риска на прогноз дожития среди населения Озёрского городского округа
- Национальное руководство по радионуклидной диагностике /под ред. Ю.Б. Лишманова, В.И. Чернова. Т. 2. Томск: STT, 2010. 418 с.
- ICRP, 2015. Radiation dose to patients from radiopharmaceuticals: a compendium of current information related to frequently used substances. ICRP Publication 128 //Ann. ICRP. 2015. V. 44, N 2S. Р. 1-321.
- Beyer T., Townsend D.W., Brun T., Kinahan P.E., Charron M., Roddy R., Jerin J., Young J., Byars L., Nutt R. A combined PET/CT scanner for clinical oncology //J. Nucl. Med. 2000. V. 41, N 8. P. 1369-1379.
- Brix G., Nekolla E.A., Borowski M., Noßke D. Radiation risk and protection of patients in clinical SPECT/CT //Eur. J. Nucl. Med. Mol. Imaging. 2014. V. 41 (Suppl.). P. S125-S136.
- Осипов М.В. Компьютерная томография как фактор риска злокачественных новообразований среди населения города атомной промышленности Озёрск //Радиация и риск. 2023. Т. 32, № 3. C. 109-121.
- Соснина С.Ф., Окатенко П.В., Сокольников М.Э. Риск перинатальных потерь среди потомков персонала радиационно опасного производства //Анализ риска здоровью. 2023. № 3. С. 123-137.
- Dracham C.B, Shankar A., Madan R. Radiation induced secondary malignancies: a review article //Radiat. Oncol. J. 2018. V. 36, N 2. P. 85-94.
- Boffetta P., Kaldor J.M. Secondary malignancies following cancer chemotherapy //Acta Oncol. 1994. V. 33, N 6. P. 591-598.
- Soubeyran P., Fonck M., Blanc-Bisson C., Blanc J.F., Ceccaldi J., Mertens C., Imbert Y., Cany L., Vogt L., Dauba J., Andriamampionona F., Houédé N., Floquet A., Chomy F., Brouste V., Ravaud A., Bellera C., Rainfray M. Predictors of early death risk in older patients treated with first-line chemotherapy for cancer //J. Clin. Oncol. 2012. V. 30, N 15. P. 1829-1834.
- Жунтова Г.В., Азизова Т.В., Банникова М.В. Характеристика первично-множественных злокачественных новообразований у работников, подвергшихся хроническому облучению //Медицинская радиология и радиационная безопасность. 2024. Т. 69, № 1. С. 67-72.
- ICRP, 1998. Radiation dose to patients from radiopharmaceuticals (Addendum to ICRP Publication 53). ICRP Publication 80 //Ann. ICRP. 1998. V. 28, N 3. P. 1-143.
- Осипов М.В., Сокольников М.Э., Фомин Е.П. Свидетельство о государственной регистрации базы данных № 2020622807 Российская Федерация. База данных компьютерной томографии населения г. Озёрск («Регистр КТ»). [Электронный ресурс]. URL: https://new.fips.ru/registers-doc-view/fips_servlet?DB=DB&DocNumber=2020622807&TypeFile=html (дата обращения 1.07.2024).
- Stata statistical software: Release 7.0. Stata Corporation, College Station, 2001.
- Chatterjee S., Hadi A.S. Regression analysis by example. 4th ed. New York: Wiley, 2006.
- Napier B.A. The Mayak Worker Dosimetry System (MWDS-2013): an introduction to the documentation //Radiat. Prot. Dosim. 2017. V. 176, N 1-2. P. 6-9.
- Determination of absorbed dose in a patient irradiated by beams of X or gamma rays in radiotherapy proce-dures. ICRU Report 24. Bethesda, MD: ICRU, 1976.
- Sokolnikov M., Preston D., Gilbert E., Schonfeld S., Koshurnikova N. Radiation effects on mortality from solid cancers other than lung, liver, and bone cancer in the Mayak worker cohort: 1948-2008 //PLoS One. 2015. V. 10, N 2. P. e0117784. DOI: 10.1371/journal.pone.0117784.
- Kessara A., Buyukcizmeci N., Gedik G.K. Cancer risk estimation for patients undergoing whole-body PET/CT scans //Radiat. Prot. Dosim. 2023. V. 199, N 6. P. 509-518.
- Пряхин Е.А., Кащеев В.В., Меняйло А.Н., Иванов В.К. Оценка радиационных рисков при однократном прохождении ПЭТ/КТ-сканирования //Радиация и риск. 2017. Т. 26, № 2. С. 41-48.


